元素周期表中的递变规律
- 格式:doc
- 大小:40.50 KB
- 文档页数:3
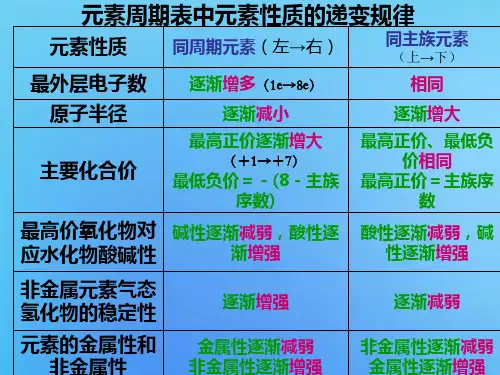




同周期的元素从左到右原子半径依次减小,金属性减弱,非金属性增强。
同主族的元素从上到下原子半径依次增大,金属性增强,非金属性减弱。
氧化性对应非金属性,还原性对应金属性。
同周期的元素从左到右,还原性减弱,氧化性增强。
同主族的元素从上到下原子半径依次增大,还原性增强,氧化性减弱。
化学元素(Chemical element)就是具有相同的核电荷数(核内质子数)的一类原子的总称。
从哲学角度解析,元素是原子的电子数目发生量变而导致质变的结果。
化学元素(英语:Chemical element),指自然界中一百多种基本的金属和非金属物质,只由一种原子组成,其原子核具有同样数量的质子,用一般的化学方法不能使之分解,并且能构成一切物质。
一些常见元素的例子有氢,氮和碳。
2012年为止,共有118种元素被发现,其中94种存在于地球上。
拥有原子序数≧83(铋元素及其后)的元素的原子核都不稳定,会放射衰变。
第43和第61种元素(锝和钷)没有稳定的同位素,会进行衰变。
自然界现存最重的元素是93号镎,可是,即使是原子序数高达95,没有稳定原子核的元素都一样能在自然中找到,这就是铀和钍的自然衰变。
自然界理论上能合成的最大原子序数的元素是98号元素锎;但是更重的元素不断地被合成,现在已经合成到了118号Og。
元素周期表的尽头在哪还没有明确的答案,现在最被广泛支持的是173号。

第一章物质结构元素周期表第一节 元素周期表一、周期表原子序数 = 核电荷数 = 质子数 = 核外电子数1、依据横行:电子层数相同元素按原子序数递增从左到右排列纵行:最外层电子数相同的元素按电子层数递增从上向下排列2、结构周期序数=核外电子层数主族序数=最外层电子数短周期(第 1、2、3 周期)周期:7 个(共七个横行)周期表长周期(第 4、5、6、7 周期)主族 7 个:ⅠA -ⅦA族:16 个(共 18 个纵行)副族 7 个:IB-ⅦB第Ⅷ族 1 个(3 个纵行)过渡元素零族(1 个)稀有气体元素二.元素的性质和原子结构(一)碱金属元素:1、原子结构 相似性:最外层电子数相同,都为 1 个递变性:从上到下,随着核电核数的增大,电子层数增多,原子半径增大2、物理性质的相似性和递变性:(1)相似性:银白色固体、硬度小、密度小(轻金属) 熔点低、易导热、导电、有展性。
(2)递变性(从锂到铯):①密度逐渐增大(K 反常)②熔点、沸点逐渐降低结论:碱金属原子结构的相似性和递变性,导致物理性质同样存在相似性和递变性。
3、化学性质(1)相似性:(金属锂只有一种氧化物)4Li + O 2 点燃 Li 2O2Na + O 2 点燃 Na 2O 22 Na + 2H 2O = 2NaOH + H 2↑2K + 2H 2O = 2KOH + H 2↑2R + 2 H 2O = 2 ROH + H 2 ↑产物中,碱金属元素的化合价都为+1价。
结论:碱金属元素原子的最外层上都只有 1 个电子,因此,它们的化学性质相似。
(2)递变性:①与氧气反应越来越容易②与水反应越来越剧烈结论:①金属性逐渐增强②原子结构的递变性导致化学性质的递变性。
总结:递变性:从上到下(从Li到Cs),随着核电核数的增加,碱金属原子的电子层数逐渐增多,原子核对最外层电子的引力逐渐减弱,原子失去电子的能力增强,即金属性逐渐增强。
所以从Li到Cs的金属性逐渐增强。


元素周期表中的规律一、最外层电子数规律1. 最外层电子数为1的元素:主族(IA族)、副族(IB、VIII族部分等)。
2. 最外层电子数为2的元素:主族(IIA族)、副族(IIB、IIIB、IVB、VIIB 族)、0族(He)、VIII族(26Fe、27Co等)。
3. 最外层电子数在3~7之间的元素一定是主族元素。
4. 最外层电子数为8的元素:0族(He除外)。
二、数目规律1. 元素种类最多的是第IIIB族(32种)。
2. 同周期第IIA族与第IIIA族元素的原子序数之差有以下三种情况:(1)第2、3周期(短周期)相差1;(2)第4、5周期相差11;(3)第6、7周期相差25。
4. 同主族相邻元素的原子序数:第IA、IIA族,下一周期元素的原子序数=上一周期元素的原子序数+上一周期元素的数目;第IIIA~VIIA族,下一周期元素的原子序数=上一周期元素的原子序数+下一周期元素的数目。
三、化合价规律1. 同周期元素主要化合价:最高正价由+1 +7(稀有气体为0价)递变、最低负价由-4 -1递变。
2. 关系式:(1)最高正化合价+|最低负化合价|=8;(2)最高正化合价=主族族序数=最外层电子数=主族价电子数。
3. 除第VIII族元素外,原子序数为奇(偶)数的元素,元素所在族的序数及主要化合价也为奇(偶)数。
四、对角线规律金属与非金属分界线对角(左上角与右下角)的两主族元素性质相似,主要表现在第2、3周期(如Li和Mg、Be和Al、B和Si)。
五、分界线规律位于金属与非金属之间的分界线,右上方的元素为非金属(周期表中的颜色为深绿色),在此可以找到制造农药的元素(如Cl、P等),左下角为金属元素(H除外),分界线两边的元素一般既有金属性,又有非金属性;能与酸和碱反应(如Be、Al等),还可找到制造半导体材料的元素(如Si、Ge等)。
六、金属性、非金属性变化规律1. 同一周期,从左到右(0族除外)金属性减弱,非金属性增强;同一主族,从上到下金属性增强,非金属性减弱。

元素周期表中元素及其化合物的递变性规律1.1原子半径(1)除第1周期外,其他周期元素(惰性气体元素除外)的原子半径随原子序数的递增而减小;(2)同一族的元素从上到下,随电子层数增多,原子半径增大。
1.2元素化合价(1)除第1周期外,同周期从左到右,元素最高正价由碱金属+1递增到+7,非金属元素负价由碳族-4递增到-1(氟无正价,氧无+6价,除外);(2)同一主族的元素的最高正价、负价均相同1.3单质的熔点(1)同一周期元素随原子序数的递增,元素组成的金属单质的熔点递增,非金属单质的熔点递减;(2)同一族元素从上到下,元素组成的金属单质的熔点递减,非金属单质的熔点递增1.4元素的金属性与非金属性(1)同一周期的元素从左到右金属性递减,非金属性递增;(2)同一主族元素从上到下金属性递增,非金属性递减。
1.5最高价氧化物和水化物的酸碱性元素的金属性越强,其最高价氧化物的水化物的碱性越强;元素的非金属性越强,最高价氧化物的水化物的酸性越强。
1.6非金属气态氢化物元素非金属性越强,气态氢化物越稳定。
同周期非金属元素的非金属性越强,其气态氢化物水溶液一般酸性越强;同主族非金属元素的非金属性越强,其气态氢化物水溶液的酸性越弱。
1.7单质的氧化性、还原性一般元素的金属性越强,其单质的还原性越强,其氧化物的氧离子氧化性越弱;元素的非金属性越强,其单质的氧化性越强,其简单阴离子的还原性越弱。
2.推断元素位置的规律判断元素在周期表中位置应牢记的规律:(1)元素周期数等于核外电子层数;(2)主族元素的序数等于最外层电子数;(3)确定族数应先确定是主族还是副族,其方法是采用原子序数逐步减去各周期的元素种数,即可由最后的差数来确定。
最后的差数就是族序数,差为8、9、10时为VIII族,差数大于10时,则再减去10,最后结果为族序数。
非金属氧性化渐性强渐氢化物渐稳定强还原熔氢原子沸化性半点物渐径渐渐熔强渐大稳沸金大定点属最高价氧化物的水合物的酸性渐强渐性最高价氧化物的水合物的碱性渐强大渐强原子半径渐大化合价+1 +2 +3 +4 +5 +6 +7 +6 +6 +6 +2 +2 +3 +4 +5 +6 +7+3 +4 +3 +3 +3 +1 +2 +4 +4 +5 化合价最高正价渐高+3 +2 +2 +2 +3 +4+2 +3+1 +1-4 -3 -2 -11. 元素周期表中元素性质的递变规律2.3.几个规律:①.金属性强弱:单质与水或非氧化性酸反应难易;单质的还原性(或离子的氧化性);M(OH)n的碱性;金属单质间的置换反应;原电池中正负极判断,金属腐蚀难易;非金属性强弱:与氢气反应生成气态氢化物难易;单质的氧化性(或离子的还原性);最高价氧化物的水化物(H n RO m)的酸性强弱;非金属单质间的置换反应。
② .半径比较三规律:阴离子与同周期稀有气体电子层结构相同;阳离子与上周期稀有气体电子层结构相同。
(1)电子层数越多,半径越大(2)电子层数相同,核电荷数越多,半径越小(3)电子层数和核电荷数相同,最外层电子数越多,半径越大③ .元素化合价规律主族最高正价 == 最外层电子数,非金属的负化合价 == 最外层电子数-8,最高正价数和负化合价绝对值之和为8;其代数和分别为:0、2、4、6。
化合物氟元素、氧元素只有负价(-1、-2),但HFO中0为+1价;金属元素只有正价;④. 熔沸点高低的比较:原子晶体>离子晶体>分子晶体⑤. 1-20号元素符号、名称、原子结构、特殊化学性质。
⑥ .电子式的书写原子的电子式离子的电子式:分子或共价化合物电子式离子化合价电子式同周期元素性质的递变规律:同一周期元素(稀有气体元素除外)的原子,从左往右,最外层电子数逐渐增加,原子半径逐渐减小,元素的原子失电子能力逐渐减弱,得电子能力逐渐增强,即元素的金属性逐渐减弱,非金属性逐渐增强第3周期:元素原子失电子能力(元素的金属性、元素单质的还原性)Na > Mg > Al氧化性:Na+< Mg2+< Al3+(相反)与水或酸反应置换出氢的难易程度:Na > Mg > Al易难剧烈不剧烈最高价氧化物对应的水化物的碱性NaOH > Mg(OH)2> Al(OH)3元素原子得电子能力(元素的非金属性)Si < P < S < Cl还原性:P3->S2->Cl-(Si4-不存在) (相反)元素单质的氧化性Si < P < S < Cl2单质与氢气化合的难易程度Si < P < S < Cl2难易气态氢化物的稳定性SiH4< PH3< H2S < HCl最高价氧化物对应的水化物的酸性H4SiO4(或H2SiO3) < H3PO4< H2SO4< HClO4第2周期:元素原子失电子能力(元素的金属性、元素单质的还原性)Li > Be氧化性:Li+< Be2+(相反)与水或酸反应置换出氢的难易程度:Li > Be易较难剧烈较不剧烈最高价氧化物对应的水化物的碱性LiOH > Be(OH)2元素原子得电子能力(元素的非金属性)C < N < O < F还原性:N3->O2->F-(C4-不存在) (相反)元素单质的氧化性C < N2< O2< F2单质与氢气化合的难易程度C < N2< O2< F2难易气态氢化物的稳定性CH4< NH3< H2O < HF最高价氧化物对应的水化物的酸性H2CO3< HNO3同主族元素性质的递变规律:同主族元素从上到下,电子层数依次增多,原子半径逐渐增大,元素的原子失电子能力逐渐增强,得电子能力逐渐减弱即元素的金属性逐渐增强,非金属性逐渐减弱ⅦA族ⅠA族(除氢H外,即碱金属元素)ⅤA族。

第二单元元素性质的递变规律【学海导航】元素的性质随着核电荷数的递增而呈现周期性的变化,这个规律叫做元素周期律。
一、原子核外电子排布的周期性元素按原子序数递增的顺序依次排列时,原子的最外层上的电子数,由1(s1)到8(s2p6),呈现出周期性变化。
相应于这种周期性变化,每周期以碱金属开始,以稀有气体结束。
元素的化学性质,主要取决于元素原子的电子结构,特别是最外层电子结构。
所以元素性质的周期性,来源于原子电子层结构的周期性。
根据元素原子的外围电子排布的特征,可将元素周期表分成五个区域:s区、p区、d 区、ds区、f区。
二、元素第一电离能的周期性变化1、定义:从气态的基态原子中移去一个电子变成+1价气态阳离子所需的最低能量,称为第Ⅰ电离能。
常用符号I1表示。
M(g)→ M+(g)+ e-,+1价气态阳离子移去一个电子变成+2价气态阳离子所需的最低能量,称为第Ⅱ电离能。
依次类推。
元素的第一电离能越小,表示它越容易失去电子,即该元素的金属性越强。
2、影响电离能的因素电离能的大小主要取决于原子的核电荷、原子半径及原子的电子构型。
一般说来,核电荷数越大,原子半径越小,电离能越大。
另外,电子构型越稳定,电离能也越大。
3. 电离能的周期性变化同周期中, 从左向右,核电荷数增大,原子半径减小, 核对电子的吸引增强, 愈来愈不易失去电子, 所以 I 总的趋势是逐渐增大。
但有些元素(如Be、Mg、N、P等)的电离能比相邻元素的电离能高些,这主要是这些元素的最外层电子构型达到了全充满或半充满的稳定构型。
同主族元素自上而下电离能依次减小。
但在同一副族中,自上而下电离能变化幅度不大,且不甚规则。
4.电离能与价态之间的关系失去电子后, 半径减小, 核对电子引力大, 更不易失去电子, 所以有: I1 < I2 < I3 < I4…., 即电离能逐级加大.三、元素电负性的周期性变化1、定义:电负性: 表示一个元素的原子在分子中吸引电子的能力. 元素的电负性越大,表示原子吸引成键电子的能力越强,该元素的非金属性也就越强;电负性越小,该元素的金属性越强。
元素周期表中的规律一、最外层电子数规律1.最外层电子数为1的元素:主族(IA族)、副族(IB、VIII族部分等)。
2.最外层电子数为2的元素:主族(IIA族)、副族(IIB、IIIB、IVB、VIIB 族)、0 族(He)、VIII 族(26Fe、27C0 等)。
3.最外层电子数在3~7之间的元素一定是主族元素。
4.最外层电子数为8的元素:0族(He除外)。
二、数目规律1.元素种类最多的是第IIIB族(32种)。
2.同周期第IIA族与第IIIA族元素的原子序数之差有以下三种情况:(1)第2、3周期二短周期)相差1;(2)第4、5周期相差11;(3)第6、7周期相差25。
(加+ »仗士2)'1设氏澜期序妆.扭一周期槿阳元書的散目为,诗曹周閉対2主帰酸周期为 2 .如第3周鞘丸2沖卜第4周期为2种.*4.同主族相邻元素的原子序数:第IA、IIA族,下一周期元素的原子序数=上一周期元素的原子序数+上一周期元素的数目;第IIIA~VIIA 族,下一周期元素的原子序数=上一周期元素的原子序数+下一周期元素的数目。
三、化合价规律1.同周期元素主要化合价:最高正价由+1 +7 (稀有气体为0价)递变、最低负价由-4 -1递变。
2.关系式:(1)最高正化合价+|最低负化合价|=8 ;(2)最高正化合价=主族族序数=最外层电子数=主族价电子数。
3.除第VIII族元素外,原子序数为奇(偶)数的元素,元素所在族的序数及主要化合价也为奇(偶)数。
四、对角线规律金属与非金属分界线对角(左上角与右下角)的两主族元素性质相似,主要表现在第2、3周期(如Li和Mg Be和Al、B和Si )。
五、分界线规律位于金属与非金属之间的分界线,右上方的元素为非金属(周期表中的颜色为深绿色),在此可以找到制造农药的元素(如 Cl、P等),左下角为金属元素(H除外),分界线两边的元素一般既有金属性,又有非金属性;能与酸和碱反应(如Be Al 等),还可找到制造半导体材料的元素(如 Si、Ge等)。
元素周期律知识点总结元素周期律学问点总结 1一.元素周期表的结构周期序数=核外电子层数主族序数=最外层电子数原子序数=核电荷数=质子数=核外电子数二.元素的性质和原子结构(一)碱金属元素:2.碱金属化学性质的递变性:递变性:从上到下(从Li到Cs),随着核电核数的增加,碱金属原子的电子层数渐渐增多,原子核对最外层电子的引力渐渐减弱,原子失去电子的力量增加,即金属性渐渐增加。
所以从Li到Cs的金属性渐渐增加。
结论:1)原子结构的递变性导致化学性质的递变性。
2)金属性强弱的推断依据:与水或酸反应越简单,金属性越强;最高价氧化物对应的水化物(氢氧化物)碱性越强,金属性越强。
3.碱金属物理性质的相像性和递变性:1)相像性:银白色固体、硬度小、密度小(轻金属)、熔点低、易导热、导电、有展性。
2)递变性(从锂到铯):①密度渐渐增大(反常) ②熔点、沸点渐渐降低3)碱金属原子结构的相像性和递变性,导致物理性质同样存在相像性和递变性(二)卤族元素:2.卤素单质物理性质的递变性:从F2到I21)卤素单质的颜色渐渐加深;2)密度渐渐增大;3)单质的熔、沸点上升3.卤素单质与氢气的反应: X2 + H2 = 2 HX卤素单质与H2 的猛烈程度:依次减弱;生成的氢化物的稳定性:依次减弱4. 非金属性的强弱的推断依:1. 从最高价氧化物的水化物的酸性强弱,或与H2反应的难易程度以及氢化物的稳定性来推断。
2. 同主族从上到下,金属性和非金属性的递变:同主族从上到下,随着核电核数的增加,电子层数渐渐增多,原子核对最外层电子的引力渐渐减弱,原子得电子的力量减弱,失电子的力量增加,即非金属性渐渐减弱,金属性渐渐增加。
3. 原子结构和元素性质的关系:原子结构打算元素性质,元素性质反应原子结构。
同主族原子结构的相像性和递变性打算了同主族元素性质的相像性和递变性。
三.核素(一)原子的构成:(1)原子的质量主要集中在原子核上。
(2)质子和中子的相对质量都近似为1,电子的质量可忽视。
Al3+/Al,-1.66V)。
②铍和铝经浓硝酸处理都表现钝化,而其它碱土金属均易与硝酸反应。
③铍和铝都是两性金属,既能溶于酸也能溶于碱。
④氢氧化物均为两性,而其它碱土金属氢氧化物均为碱性。
⑤BeO和Al2O3都有高熔点和高硬度。
⑥铝和铍的氯化物是共价分子,能通过氯桥键形成双聚分子,易升华、易聚合,易溶于有机溶剂。
3、硼和硅的相似性。
B和Si虽是不同族元素,在周期表中处于相邻族的对角位置,由于离子极化作用相近(Si4+电荷高一些,但半径大;B3+电荷低一些,但半径小),性质上有许多相似之处。
①单质晶体都是高熔点原子晶体;与键强度相关。
②在自然界均以含氧化合物存在。
③卤化物都彻底水解,生成含B─O,Si─O键的化合物(硅酸、硼酸)④都有一系列氢化物,氢化物均有挥发性,不稳定。
⑤含氧酸都是弱酸,含氧酸盐都易水解对角线规则是从有关元素及其化合物的许多性质中总结出来的经验规律;对此可以用离子极化的观点加以粗略的说明。
同一周期最外层电子构型相同的金属离子,从左至右随离子电荷的增加而引起极化作用的增强;同一族电荷相同的金属离子,自上而下随离子半径的增大而使得极化作用减弱。
因此,处于周期表中左上右下对角线位置上的邻近两个元素,由于电荷和半径的影响恰好相反,它们的离子极化作用比较相近,从而使它们的化学性质比较相似。
由此反映出物质的结构与性质之间的内在联系。
三. 周期表中的变化规律(一) 同一元素:r -离子>r原子>r+离子>r2+离子(二) 同一周期1. 短周期:每一个短周期从左到右,有效核电荷依次增大,所以原子半径依次递减.2. 长周期:过渡元素自左至右,电子逐一填入(n-1)d层,而它对核的屏蔽作用较小,所以自左向右半径减小的幅度不如主族元素那么大.3. 内过渡元素:电子填入再次外层的(n-2)f层,由于f电子对核的屏蔽作用更小,使得原子半径由左至右收缩的平均幅度更小.比较短周期和长周期,相邻元素原子半径减小的平均幅度大致是非过渡元素>过渡元素>内过渡元素(~10pm)(~5pm)(<1pm)(三) 同一族1. 主族:同一主族由上而下,原子半径一般是增大的.因为同族元素原子由上而下电子层数增多,所以半径由上至下依次增大.2. 副族:副族元素由上至下,原子半径增大的幅度较小,特别是五,六周期的同族元素原子半径非常接近,这是由于后面要提到的镧系收缩效应所造成的结果.特殊元素集锦1、最活泼的金属元素、最高价氧化物对应的水化物碱性最强的元素、阳离子氧化性最弱的元素是铯(Cs)。
元素周期表的非金属性变化规律
元素周期表非金属性变化规律是:
1、同一周期的元素从左到右金属性递减,非金属性呈现递增。
2、同一主族元素从上到下金属性递增,非金属性呈现递减。
元素周期表是元素周期律用表格表达的具体形式,它反映元素原子的内部结构和它们之间相互联系的规律。
元素周期表简称周期表。
元素周期表有很多种表达形式,目前最常用的是维尔纳长式周期表。
元素周期表有7个周期,有16个族和4个区。
元素在周期表中的位置能反映该元素的原子结构。
周期表中同一横列元素构成一个周期。
同周期元素原子的电子层数等于该周期的序数。
同一纵行(第Ⅷ族包括3个纵行)的元素称“族”。
族是原子内部外电子层构型的反映。
元素周期表中的递变规律
同周期(左右)同主族(上下)
结构电子层结
构
电子层数相同递增
最外层电子数递增(18或2)相同(族序数)原子核内的质子数递增递增
性质原子半径
递减(除稀有气体元
素)
递增主要化合价
+1+7
—4—1
相似
元素原子失电子能力减弱增强元素原子得电子能力增强减弱
性质应用最高价氧
化物对应
水化物
酸性增强减弱
碱性减弱增强
非金属气
态氢化物
形成难易难易易难
稳定性增强减弱
金属单质与水或酸置换出氢气的难易
程度
变难变容易
短周期元素推断题记忆常见“题眼”
(1)位置与结构
a.周期序数等于族序数两倍的短周期的元素是Li。
b.最高正价数等于最低负价绝对值三倍的短周期元素是S。
c.次外层电子数等于最外层电子数四倍的短周期元素是Mg。
d.次外层电子数等于最外层电子数八倍的短周期元素是Na。
e.族序数与周期数相等的短周期元素是H、Be、Al;族序数是周期数两倍的短周期元素是C、S;族序数是周期数三倍的短周期元素是O。
f.只由质子和电子构成的元素原子是H()。
(2)含量与物理性质
a.地壳中质量分数最大的元素是O,其次是Si。
b.地壳中质量分数最大的金属元素是Al。
c.氢化物中氢元素百分含量最高的元素是C。
d.其单质为天然物质中硬度最大的元素是C。
e.其气态氢化物最易溶于水的元素是N。
在常温、常压下,1体积水溶解700体积NH3。
f.其气态氢化物沸点最高的非金属元素是O。
g.常温下,其单质是有色气体的元素是F、Cl。
h.所形成的化合物种类最多的元素是C。
i.在空气中,其最高价氧化物的含量增加会导致“温室效应”的元素是C。
j.其单质是最易液化的气体的元素是Cl。
k.其单质是最轻的金属元素的是Li。
l.其最高价氧化物的水化物酸性最强的元素是Cl。
m.常温下其单质呈液态的非金属元素是Br。
(3)化学性质与用途
a.单质与水反应最剧烈的非金属元素是F。
b.其气态氢化物与最高价氧化物对应水化物能起化合反应的是N。
NH3+HNO3=NH4NO3。
c.常温下其气态氢化物与其最低价氧化物能反应生成该元素的单质的元素是S。
2H2S+SO2=3S+2H2O。
d.在空气中,其一种同素异形体易在空气中自燃的元素是P。
e.其气态氢化物水溶液可雕刻玻璃的元素是F。
f.其两种同素异形体对人类生存都非常重要的元素是O。
臭氧(O3)层被称为人类和生物的保护伞。
g.能与强碱溶液作用的单质有:Al、Cl2、Si、S等。
常见元素化合价的一般规律
(1)金属元素无负价。
因为金属元素最外层电子数目少,易失去电子变为稳定结构,故金属元素无负价,除零价外,在反应中只显正价。
(2)氟无正价,氧有正价但无最高正价。
氟、氧得电子能力特别强,尤其是氟元素,只能夺取电子而成为稳定结构,除零价外,只显负价。
氧只跟氟结合时,才显正价,如在OF2中氧呈+2价。
(3)在1~20号元素中,除O、F外,元素的最高正价等于最外层电子数;元素的最低负价与最高正价的关系为:最高正价+∣最低负价∣=8。
既有正价又有负价的元素一定是非金属元素;所有元素都有零价。
(4)除个别元素外(如氮元素),原子序数为奇数的元素,其化合价也常呈奇数价,原子序数为偶数的元素,其化合价也常呈偶数价,即序奇价奇,序偶价偶。
若原子的最外层电子数为奇数(m),则元素的正常化合价为一系列连续的奇数,从+1到+m,若出现偶数则为非正常化合价,其氧化物是不成盐氧化物,例如NO2、NO;若原子的最外层电子数为偶数,从—2价到+m。
例如:Na2S、SO2、H2SO4。
离子化合物与共价化合物的判断
(1)根据化合物类别判断
①强碱、盐、大多数碱性氧化物属离子化合物;
②非金属氧化物、非金属氢化物、含氧酸、有机化合物属共价化合物。
(2)根据化合物性质判断
①熔化状态下导电的化合物是离子化合物;
②熔、沸点较低的化合物(SiO2、SiC等除外)一般为共价化合物;溶于水和熔化状态下不导电的化合物为共价化合物。
(3)根据组成物质的微粒间的成键类型判断
①离子化合物中一定有离子键,也可能有共价键,如NH4Cl、Na2SO4。
②共价化合物只有共价键,一定没有离子键。
③稀有气体是单原子分子,不含化学键;非金属单质中一定只含共价键。
③离子化合物中一般既含金属元素又含非金属元素(铵盐除外);共价化合物中一般只含非金属元素,但只含非金属元素的化合物不一定是共价化合物,如(NH4)2SO4。