分裂能:中心离子的d轨道的简并能级因配位场
的影响而分裂成不同组能级之间的能量差。 分裂能的大小与下列因素有关:
1 配位场 亦即几何构型类型 如△t=(4/9)△o
2 金属离子
(1) 金属离子的电荷
中心金属离子电荷增加,△值增加。这是由于随着金 属离子的电荷的增加,金属离子的半径减小,因而配体更 靠近金属离子,从而对 d 轨道产生的影响增大之故,三价 离子的分裂能 比二价离子要大40~60%。
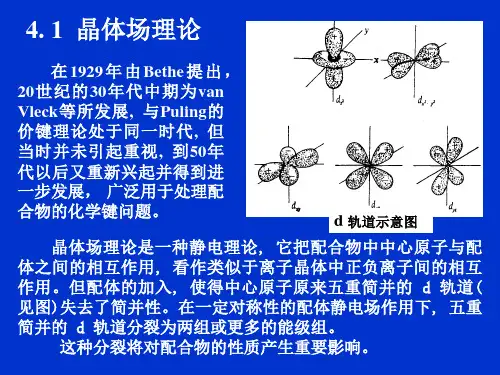
八面体场中的d轨道
若改变负电荷在球壳上的分布,
把它们集中在球的内接正八面体的 六个顶点上, 且这六个顶点均在x、 y、z轴上, 每个顶点的电量为1个单 位的负电荷, 由于球壳上的总电量 仍为6个单位的负电荷, 因而不会改 变对d电子的总排斥力, 即不会改变 d轨道的总能量, 但是那个单电子处 在不同的d轨道上时所受到的排斥 作用不再完全相同。
3 配体的本性
将一些常见配体按光谱实验测得的分裂能从小到大次
序排列起来,便得光谱化学序:
这个化学序代表了配位场的强度顺序。由此顺序可见 ,对同一金属离子,造成△值最大的是CN-离子,最小的
是I-离子,通常把CN-、NO2-等离子称作强场配位体, I-、Br-、F-离子称为弱场配位体。
须指出的是, 上述配体场强度顺序是纯静电理 论所不能解释的。例如OH-比H2O分子场强度弱, 按 静电的观点OH-带了一个负电荷, H2O不带电荷, 因 而OH-应该对中心金属离子的d轨道中的电子产生较 大的影响作用, 但实际上是OH-的场强度反而低, 显 然这就很难纯粹用静电效应进行解释。这说明了
t2
e
由于在四面体场中,这两组轨道都在一定程度下避 开了配体、没有像八面体中d轨道与配体迎头相撞的情 况,可以预料分裂能△t将小于△o,计算表明


![[课件]第四章 休克尔(Hückel) 分子轨道理论PPT](https://uimg.taocdn.com/1cf29dc819e8b8f67c1cb992.webp)