锂电池基础知识
- 格式:ppt
- 大小:1.15 MB
- 文档页数:52

电池基础知识培训资料一、锂离子电池工作原理与性能简介:1、电池的定义:电池是一种能量转化与储存的装置,它通过反应将化学能或物理能转化为电能,电池即是一种化学电源,它由两种不同成分的电化学活性电极分别组成正负极,两电极浸泡在能提供媒体传导作用的电解质中,当连接在某一外部载体上时,通过转换其内部的化学能来提供能源.2、锂离子电池的工作原理:即充放电原理。
Li-ion的正极材料是氧化钴锂,负极是碳。
当对电池进行充电时,电池的正极上有锂离子生成,生成的锂离子经过电解液运动到负极.而作为负极的碳呈层状结构,它有很多微孔,达到负极的锂离子就嵌入到碳层的微孔中,嵌入的锂离子越多,充电容量越高。
同样,当对电池进行放电时(即我们使用电池的过程),嵌在负极碳层中的锂离子脱出,又运动回正极。
回正极的锂离子越多,放电容量越高。
我们通常所说的电池容量指的就是放电容量。
在Li-ion的充放电过程中,锂离子处于从正极→负极→正极的运动状态。
Li—ion就象一把摇椅,摇椅的两端为电池的两极,而锂离子就象运动员一样在摇椅两端来回奔跑。
所以,Li—ion又叫摇椅式电池。
通俗来说电池在放电过程中,负极发生氧化反应,向外提供电子;在正极上进行还原反应,从外电路接收电子,电子从负极流到正极,而电流方向正好与电子流动方向相反,故电流经外电路从正极流向负极。
电解质是离子导体,离子在电池内部的正负极之间定向移动而导电,阳离子流向正极,阴离子流向负极。
整个电池形成了一个由外电路的电子体系和电解质的离子体系构成的完整放电体系,从而产生电能。
正极反应:LiCoO2==== Li1-xCoO2+ xLi+ + xe负极反应:6C + xLi+ + xe—=== Lix C6电池总反应:LiCoO2 + 6C ==== Li1-xCoO2 + LixC63、电池的连接:根据电池的电压与容量的需求,可以把电池做串联、并联及混连连接。
a、串联:电压升高,容量基本不变;b、并联:电压基本不变,容量升高;c、混联:电压与容量都会升高;4、化学电池的种类:锂离子电池按电池外形来分类,可分为圆柱形、方形、钮扣形和片状形等。

(一)锂电池的构成锂电池主要由两大块构成,电芯和保护板PCM(动力电池一般称为电池管理系统BMS),电芯相当于锂电池的心脏,管理系统相当于锂电池的大脑。
电芯主要由正极材料、负极材料、电解液、隔膜和外壳构成,而保护板主要由保护芯片(或管理芯片)、MOS管、电阻、电容和PCB板等构成。
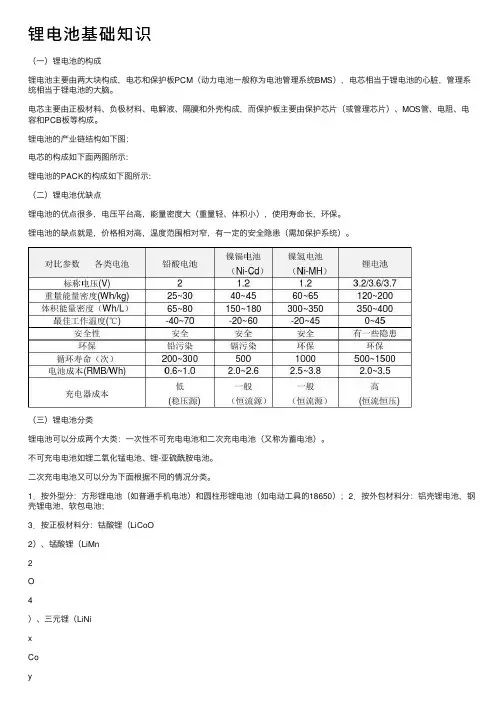
锂电池的产业链结构如下图:电芯的构成如下面两图所示:锂电池的PACK的构成如下图所示:(二)锂电池优缺点锂电池的优点很多,电压平台高,能量密度大(重量轻、体积小),使用寿命长,环保。
锂电池的缺点就是,价格相对高,温度范围相对窄,有一定的安全隐患(需加保护系统)。
(三)锂电池分类锂电池可以分成两个大类:一次性不可充电电池和二次充电电池(又称为蓄电池)。
不可充电电池如锂二氧化锰电池、锂-亚硫酰胺电池。
二次充电电池又可以分为下面根据不同的情况分类。
1.按外型分:方形锂电池(如普通手机电池)和圆柱形锂电池(如电动工具的18650);2.按外包材料分:铝壳锂电池,钢壳锂电池,软包电池;3.按正极材料分:钴酸锂(LiCoO2)、锰酸锂(LiMn2O4)、三元锂(LiNi x Co y Mn z O2)、磷酸铁锂(LiFePO4);4.按电解液状态分:锂离子电池(LIB)和聚合物电池(PLB);5.按用途分:普通电池和动力电池。
6.按性能特性分:高容量电池、高倍率电池、高温电池、低温电池等。
(四)常用术语解释1. 容量(Capacity)指一定的放电条件下可以从电池锂获得的电量。
我们在高中学物理是知道,电量的公式为Q=I*t,单位为库伦,电池的容量单位规定为Ah (安时)或mAh(毫安时)。
意思是1AH的电池在充满电的情况下用1A的电流放电可以放1个小时。
以前的NOKIA的老手机的电池(像BL-5C)一般是500mAh,现在的智能手机电池800~1900mAh,电动自行车一般都是10~20Ah,电动汽车一般都是20~200Ah等。
2. 充放电倍率(Charge-Rate/Discharge-Rate)表示以多大的电流充电、放电,一般以电池的标称容量的倍数为计算,一般称为几C。

锂电池基础知识培训锂电池是一种常见的电池类型,广泛应用于移动设备、电动车辆和可再生能源存储等领域。
本文将为大家介绍锂电池的基础知识,包括锂电池的结构、工作原理、充放电特性、安全性等方面。
一、锂电池结构锂电池通常由正极、负极、电解质和隔膜组成。
正极材料一般使用氧化物,如钴酸锂(LiCoO2)、磷酸铁锂(LiFePO4)等。
这些正极材料能够释放或吸收锂离子,实现电池的充放电过程。
负极材料通常采用石墨,能够嵌著锂离子形成锂插层化合物。
电解质是锂离子的传导介质,一般采用液态或聚合物电解质。
液态电解质具有高离子传导性和低内阻,而聚合物电解质则具有良好的安全性能。
隔膜用于隔离正负极,防止短路。
二、锂电池工作原理锂电池的工作原理是基于锂离子在正负极材料之间的嵌脱插过程。
充电时,外部电源提供电流,使得正极材料氧化,负极材料脱锂。
锂离子在电解液中移动,通过隔膜到达负极,嵌入到负极材料中。
放电时,锂离子从负极材料脱出,通过隔膜到达正极,嵌入到正极材料中。
同时,电子通过外部电路流动,产生电流,为外部设备供电。
锂电池的充放电过程是可逆的,可以循环多次使用。
三、锂电池充放电特性锂电池的充放电特性与其正负极材料有关。
充电时,锂电池通常采取恒流充电和恒压充电两个阶段。
恒流充电阶段中,电流保持不变,直到电池电压达到设定的峰值电压;恒压充电阶段中,电流逐渐减小,直到电池容量充满,电压保持恒定。
放电时,锂电池的电压会随着放电过程逐渐下降,当电压达到一定程度时需要停止放电,以避免过放。
锂电池的容量可以通过充放电循环实验来测试,常用的容量单位是安时(Ah)。
四、锂电池的安全性锂电池具有较高的能量密度,因此在不正确使用或存储时存在一定的安全风险。
首先,要注意避免过充和过放。
过充会造成电池内部压力过高,甚至发生爆炸;而过放会导致电池无法再次充电,损坏电池。
其次,在存储和携带锂电池时,应注意避免与金属物品短路,避免受到外力撞击。
此外,锂电池在高温环境下的使用会降低其寿命和安全性能,因此要避免长时间暴露在高温环境中。



锂电池安全知识教育手册锂电池作为一种高效、环保的能源存储方式,在众多领域得到了广泛应用。
然而,由于锂电池具有较高的能量密度和化学活性,其安全性问题也不容忽视。
为了确保锂电池的安全使用,提高大家的锂电池安全意识,我们特编制本手册,供大家研究和参考。
一、锂电池基础知识1.1 锂电池的定义与分类锂电池是一种以锂为主要活性物质的原子电池。
根据电池的正极材料的不同,锂电池可分为锂离子电池、锂聚合物电池、锂铁磷酸电池等。
1.2 锂电池的工作原理锂电池在放电过程中,正极材料发生氧化反应,释放出电子;负极材料发生还原反应,吸收电子。
电子通过外电路流动,形成电流。
在充电过程中,反应方向相反。
1.3 锂电池的主要性能参数- 能量密度:单位体积或单位质量的电池所能储存的能量。
- 循环寿命:电池可重复充电和放电的次数。
- 工作温度范围:电池能正常工作的环境温度。
- 充放电速率:电池在单位时间内所能充电或放电的容量。
二、锂电池的安全使用与维护2.1 锂电池的存放- 避免高温、高湿环境存放。
- 避免与金属、尖锐物品等接触,以免短路。
- 存放时应保持电池电量在20%-80%之间。
- 存放环境应通风、干燥。
2.2 锂电池的充电- 使用符合国家标准的充电器和电池。
- 充电时避免电池受到撞击、振动。
- 充电过程中,注意电池的温度变化,避免过热。
- 充满后及时拔掉电源,避免过充。
2.3 锂电池的使用- 避免电池受到强烈撞击、震动。
- 避免电池长时间处于高温、高湿环境。
- 避免电池过充、过放。
- 定期检查电池外观,如有异常应及时处理。
2.4 锂电池的维护- 定期对电池进行充放电,以保持其活性。
- 避免电池长时间不用,导致性能下降。
- 如电池出现鼓包、漏液等异常现象,应立即停止使用,并妥善处理。
三、锂电池的安全事故处理3.1 锂电池安全事故的类型- 过充、过放导致的热失控。
- 电池短路导致的火灾、爆炸。
- 电池受到撞击、振动导致的破损、泄漏。


一、电池的化学知识物质发生化学反应的种类有多种,其中一种是氧化还原反应,在这种反应中,实际是电子在反应物中的转移过程。
通常把提供电子的物质叫还原剂,接受电子的物质叫氧化剂。
在电池体系里,一般把这些还原剂或氧化剂统一称作活性物质,活性物质在电池体系中发生的氧化还原反应就是电池反应。
原剂或氧化剂和导电骨架加工在一起,便成了电极,其中,还原剂电极发生电池反应时是失去电子,叫负极,而由氧化剂组成的电极在反应中则得到电子,叫正极,对于可充电的电池,正极又叫阴极,负极又叫阳极。
当电极插入到相关的溶液时,便获得了一电势,一般称为电极电位.正极,负极处于一相同溶液体系之下是否有电位差,是能否发生电池反应的必要条件。
1.1. 电池的工作原理和分类电池是将物质的化学能转变成电能的一种装置。
电池工作时,负极(阳极)发生化学反应,给出电子,电子通过外部电子通道传到正极(阴极)并被其消耗,就这样,电池工作时,电子会源源不断的从负极(阳极)跑出来,通过外部电路到达正极(阴极),直到两电极中某一方被消耗完,电子才会停止转移。
电子的定向流动便成为电流,最终获得电能。
1.2. 电池的组成要使电池能连续工作,必需包含以下部分:电极,电解质,隔离物以及电池外壳。
1.2.1 电极一般由活性物质和导电骨架组成,如前所述,又分为正(阴)极和负(阳)极,是电池的核心部分,是电池产生电能的源泉,通过两极上活性物质和化学变化使化学能转变为电能,导电骨架主要起着传导电子和支撑活性物质的作用,又叫集流体。
1.2.2 电解质的一般作用是完成电池放电时的离子导电过程。
电池工作时,负极提供的电子通过电池体系的外部电路到达正极从而提供电能,要实现这个能量转换过程,还必需要有一个内部离子导电过程以完成电流回路。
离子的正向移动产生电流,电解质的导电就是通过其内部体系的离子迁移从而实施离子导电。
1.2.3 隔离物能常是指置于电池正负极之间的材料,其作用是阻止正、负极活性材料的直接接触,防止电池的内部短路,并能阻挡两极粉状物质的透过。
锂电池基础知识(⼀)锂电池的构成锂电池主要由两⼤块构成,电芯和保护板PCM(动⼒电池⼀般称为电池管理系统BMS),电芯相当于锂电池的⼼脏,管理系统相当于锂电池的⼤脑。
电芯主要由正极材料、负极材料、电解液、隔膜和外壳构成,⽽保护板主要由保护芯⽚(或管理芯⽚)、MOS管、电阻、电容和PCB板等构成。
锂电池的产业链结构如下图:电芯的构成如下⾯两图所⽰:锂电池的PACK的构成如下图所⽰:(⼆)锂电池优缺点锂电池的优点很多,电压平台⾼,能量密度⼤(重量轻、体积⼩),使⽤寿命长,环保。
锂电池的缺点就是,价格相对⾼,温度范围相对窄,有⼀定的安全隐患(需加保护系统)。
(三)锂电池分类锂电池可以分成两个⼤类:⼀次性不可充电电池和⼆次充电电池(⼜称为蓄电池)。
不可充电电池如锂⼆氧化锰电池、锂-亚硫酰胺电池。
⼆次充电电池⼜可以分为下⾯根据不同的情况分类。
1.按外型分:⽅形锂电池(如普通⼿机电池)和圆柱形锂电池(如电动⼯具的18650);2.按外包材料分:铝壳锂电池,钢壳锂电池,软包电池;3.按正极材料分:钴酸锂(LiCoO2)、锰酸锂(LiMn2O4)、三元锂(LiNixCoyMnzO2)、磷酸铁锂(LiFePO4);4.按电解液状态分:锂离⼦电池(LIB)和聚合物电池(PLB);5.按⽤途分:普通电池和动⼒电池。
6.按性能特性分:⾼容量电池、⾼倍率电池、⾼温电池、低温电池等。
(四)常⽤术语解释1.容量(Capacity)指⼀定的放电条件下可以从电池锂获得的电量。
我们在⾼中学物理是知道,电量的公式为Q=I*t,单位为库伦,电池的容量单位规定为Ah (安时)或mAh(毫安时)。
意思是1AH的电池在充满电的情况下⽤1A的电流放电可以放1个⼩时。
以前的NOKIA的⽼⼿机的电池(像BL-5C)⼀般是500mAh,现在的智能⼿机电池800~1900mAh,电动⾃⾏车⼀般都是10~20Ah,电动汽车⼀般都是20~200Ah等。
2.充放电倍率(Charge-Rate/Discharge-Rate)表⽰以多⼤的电流充电、放电,⼀般以电池的标称容量的倍数为计算,⼀般称为⼏C。

锂电池基础知识三篇篇一:锂电池基础知识配料基础知识一、电极的组成:1、正极组成:a、钴酸锂:正极活性物质,锂离子源,为电池提高锂源。
b、导电剂:提高正极片的导电性,补偿正极活性物质的电子导电性。
提高正极片的电解液的吸液量,增加反应界面,减少极化。
c、PVDF粘合剂:将钴酸锂、导电剂和铝箔或铝网粘合在一起。
d、正极引线:由铝箔或铝带制成。
2、负极组成:a、石墨:负极活性物质,构成负极反应的主要物质;主要分为天然石墨和人造石墨两大类。
b、导电剂:提高负极片的导电性,补偿负极活性物质的电子导电性。
提高反应深度及利用率。
防止枝晶的产生。
利用导电材料的吸液能力,提高反应界面,减少极化。
(可根据石墨粒度分布选择加或不加)。
c、添加剂:降低不可逆反应,提高粘附力,提高浆料黏度,防止浆料沉淀。
d、水性粘合剂:将石墨、导电剂、添加剂和铜箔或铜网粘合在一起。
e、负极引线:由铜箔或镍带制成。
二、配料目的:配料过程实际上是将浆料中的各种组成按标准比例混合在一起,调制成浆料,以利于均匀涂布,保证极片的一致性。
配料大致包括五个过程,即:原料的预处理、掺和、浸湿、分散和絮凝。
三、配料原理:(一)、正极配料原理1、原料的理化性能。
(1)钴酸锂:非极性物质,不规则形状,粒径D50一般为6-8μm,含水量≤0.2%,通常为碱性,PH值为10-11左右。
锰酸锂:非极性物质,不规则形状,粒径D50一般为5-7μm,含水量≤0.2%,通常为弱碱性,PH值为8左右。
(2)导电剂:非极性物质,葡萄链状物,含水量3-6%,吸油值~300,粒径一般为2-5μm;主要有普通碳黑、超导碳黑、石墨乳等,在大批量应用时一般选择超导碳黑和石墨乳复配;通常为中性。
(3)PVDF粘合剂:非极性物质,链状物,分子量从300,000到3,000,000不等;吸水后分子量下降,粘性变差。
(4)NMP:弱极性液体,用来溶解/溶胀PVDF,同时用来稀释浆料。
2、原料的预处理(1)钴酸锂:脱水。