实验室配制溶液标签
- 格式:doc
- 大小:42.00 KB
- 文档页数:1

手把手教你填写实验室溶液标签!
实验室溶液标签一般需要写明五项内容:名称、浓度、配制人、配制日期、有效期。
以下举例说明:
一、标准溶液
例1、氟化物标准储备液[P(F-)]=1mg∕1]
不规范写法:
正确写法:
名称:氟化物标准储备液
浓度:P(E)=1OmgZ1
配置F1期:年月日
有效日期:年月日
配制人: *** (全名)
例2、草酸钠标准使用液[C(1∕2Na2C204)=0.01OOmoI/1]
不规范写法:
正确写法:
例3、混标
不规范写法:
正确写法:
对于所含物质较多的混标,建议在一旁多贴一个标签说明
:P(A§,Se)=O.O1mg∕1浓度:P(Cd,Pb)=O.O2mg∕i7
二、辅助溶液
例1、酚Bk指示剂:由50mg酚ft+50m1乙醇+50m1纯水配制而成
例2、酚红指示剂:由50mgKtt+50m1乙醇+50In1纯水配制而成
名称:酚红指示剂一
浓度:适用PH范围:6.8∙8.4配置口期:年月日一
有效口期:年月—一
配制人: *** (全名)
例3、按体积比配制的酸液:1份盐酸+2份纯水配制的盐酸不规范写法:
正确写法:
名称:盐酸溶液
浓度:~Ha(I+2)
或:Ha+%0(1+2)
配一日期:年月曰
有效日期:年月曰
配制人: ***(全名)
份硝酸+5份纯水配制的盐酸溶液。

实验室溶液的配制一.蛋白试验(1)4%的硼酸吸收液:分析纯硼酸,4g溶于50ml水,加热使其溶解,冷却,再用蒸馏水标至100ml。
(2)40%的氢氧化钠:分析纯氢氧化钠,40g溶于100ml水。
(4)0.1mol/L盐酸标准溶液:量取9ml盐酸(GB622,分析纯),用蒸馏水定容到1000ml,摇匀。
标定:在电子天平上准确称取5份烘干至恒重的基准无水碳酸钠,每份0.2g左右,记下所称的基准无水碳酸钠的质量m,将5份基准无水碳酸钠分别置于5个250ml锥形瓶中(提前标号),加入50ml水,加2~3滴甲基红指示剂,然后用待标定的0.1mol/L的HCL标准溶液滴定至溶液由黄色变为灰红色,记下消耗的盐酸标准液的体积Vo,然后将滴定完的锥形瓶在电炉上烧至沸腾,然后转小火保持沸腾2分钟,溶液中的二氧化碳被赶出后溶液又变为蓝绿色,冷却,再用盐酸标准溶液滴定至溶液变为灰红色,记下消耗的盐酸标准液体积Vi,两次滴定之和即为消耗的盐酸标准液体积。
平行滴定5份基准无水碳酸钠,记录好每份的数据。
计算公式:C(Hcl)=m/(V o+Vi)×0.05299,五次结果的平均值即为盐酸标准液的浓度,将盐酸标准液转入1000ml容量瓶保存即可。
贴上标签标明配制时间,配制人,溶液浓度。
注:测凯氏定氮仪漏气不漏气的方法——取分析纯硫酸铵0.2g左右做蛋白试验,测其氮含量,作3个平行试验,测得硫酸铵含氮量为21.19%±0.2%,否则应检查加减,蒸馏,滴定各步骤是否正确。
二.钙的测定(1)10%o淀粉溶液的配制:10g淀粉溶于水,加热使其溶解,冷却后转移到1000ml容量瓶,用蒸馏水定容到1000ml。
(2)1/1三乙醇胺溶液(即50%溶液):取100ml三乙醇胺溶于100ml蒸馏水中,摇匀,贴上保存于磨口瓶中。
(3)1/1乙二胺溶液:取100ml乙二胺溶于100ml水中,摇匀,贴上标签保存于磨口瓶中。
(4)200g/LKOH溶液:用电子天平称取40g分析纯氢氧化钾,溶于1000ml蒸馏水中(通风橱中进行),搅拌后放置,溶解完全后转移至磨口瓶中,贴上标签保存。

实验室常见配制试剂的标签颜色及分级一、前言实验室是科学研究的重要场所,为了保证实验的准确性和安全性,需要使用各种试剂。
为了方便使用和管理,实验室会对试剂进行标注和分类。
本文将介绍实验室常见配制试剂的标签颜色及分级。
二、试剂标签颜色1. 红色标签红色标签通常用于警示危险试剂,如有毒、易燃、腐蚀等。
这些试剂需要特别注意安全操作,并且在存储时需要单独放置,并且远离其他试剂。
2. 橙色标签橙色标签用于表示有刺激性或者过敏原性的试剂。
这些试剂容易引起皮肤或者黏膜刺激,需要特别小心操作,并且在使用时需要佩戴防护手套等防护措施。
3. 黄色标签黄色标签通常用于表示化学品的危险性较低,但仍需注意安全操作。
这些化学品可能会对人体造成轻微伤害或者引起火灾等事故。
4. 蓝色标签蓝色标签通常用于表示试剂为生物危险品,如细菌、病毒等。
这些试剂需要特别小心操作,并且在使用时需要佩戴防护面罩等防护措施。
5. 绿色标签绿色标签通常用于表示试剂为环保型或者无害的化学品。
这些化学品对人体没有危害,也不会对环境造成污染。
三、试剂分级1. 一级试剂一级试剂是指对人体和环境危害较小的化学品,如食盐、葡萄糖等。
这些化学品可以在实验室中自由使用,不需要特别注意安全操作。
2. 二级试剂二级试剂是指对人体和环境有一定危害的化学品,如硫酸、氢氧化钠等。
这些化学品需要特别注意安全操作,并且在使用时需要佩戴防护手套等防护措施。
3. 三级试剂三级试剂是指对人体和环境危害较大的化学品,如氰化物、致癌物质等。
这些化学品需要特别小心操作,并且在使用时需要佩戴全面防护装备。
四、总结实验室常见配制试剂的标签颜色及分级是保证实验室安全操作的重要手段。
在使用试剂时,需要仔细阅读标签上的信息,并且根据试剂的危险级别进行相应的防护措施。
只有这样才能保证实验室的安全和顺利进行。

实验室常用溶液的配制1.30%丙烯酰胺溶液【配制方法】将29g丙烯酰胺和1g N,N’-亚甲双丙烯酰胺溶于总体积为60ml的水中。
加热至37℃溶解之,补加水至终体积为100ml。
用Nalgen e滤器(0.45μm孔径)过滤除菌,查证该溶液的p H值应不大于7.0,置棕色瓶中保存于室温。
【注意】丙烯酰胺具有很强的神经毒性并可以通过皮肤吸收,其作用具累积性。
称量丙烯酰胺和亚甲双丙烯酰胺时应戴手套和面具。
可认为聚丙烯酰胺无毒,但也应谨慎操作,因为它还可能会含有少量未聚合材料。
一些价格较低的丙烯酰胺和双丙烯酰胺通常含有一些金属离子,在丙烯酰胺贮存液中加入大约0.2体积的单床混合树脂(MB-1Mallin ckrodt),搅拌过夜,然后用What man 1号滤纸过滤以纯化之。
在贮存期间,丙烯酰胺和双丙烯酰胺会缓慢转化成丙烯酰和双丙烯酸。
2.40%丙烯酰胺【配制方法】把380g丙烯酰胺(DNA测序级)和20g N,N’-亚甲双丙烯酰胺溶于总体积为600ml的蒸馏水中。
继续按上述配制30%丙烯酰胺溶液的方法处理,但加热溶解后应以蒸馏水补足至终体积为1L。
【注意】见上述配制30%丙烯酰胺的说明,40%丙烯酰胺溶液用于DNA序列测定。
3.放线菌素D溶液【配制方法】把20mg放线菌素D溶解于4ml 100%乙醇中,1:10稀释贮存液,用100%乙醇作空白对照读取OD440值。
放线菌素D(分子量为1255)纯品在水溶液中的摩尔消化系数为21,900,故而1mg/ml的放线菌素D溶液在440nm处的吸光值为0.182,放线菌素D的贮存液应放在包有箔片的试管中,保存于-20℃。
【注意】放线菌素D是致畸剂和致癌剂,配制该溶液时必须戴手套并在通风橱内操作,而不能在开放在实验桌面上进行,谨防吸入药粉或让其接触到眼睛或皮肤。

20种实验室常用溶液配制与标定方法乙二胺四醋酸二钠滴定液(0.05mol/L)C10H14N2Na2O8•2H2O=372.2418.61g→1000mL 【配制】取乙二胺四醋酸二钠19g,加适量的水使溶解成1000mL,摇匀。
【标定】取于约800℃灼烧至恒重的基准氧化锌0.12g,精密称定,加稀盐酸3mL使溶解,加水25mL,加0.025%甲基红的乙醇溶液1滴,滴加氨试液至溶液显微黄色,加水25mL与氨-氯化铵缓冲液(pH10.0)10mL,再加铬黑T指示剂少量,用本液滴定至溶液由紫色变为纯蓝色,并将滴定的结果用空白试验校正。
每1mL乙二胺四醋酸二钠滴定液(0.05mol/L)相当于4.069mg的氧化锌。
根据本液的消耗量与氧化锌的取用量,算出本液的浓度,即得。
【贮藏】置玻璃塞瓶中,避免与橡皮塞、橡皮管等接触。
乙醇制氢氧化钾滴定液(0.5mol/L)KOH=56.1128.06g→1000mL【配制】取氢氧化钾35g,置锥形瓶中,加无醛乙醇适量使溶解并稀释成1000mL,用橡皮塞密塞,静置24小时后,迅速倾取上清液,置具橡皮塞的棕色玻瓶中。
【标定】精密量取盐酸滴定液(0.5mol/L)25mL,加水50mL稀释后,加酚酞指示液数滴,用本液滴定。
根据本液的消耗量,算出本液的浓度,即得。
本液临用前应标定浓度。
【贮藏】置橡皮塞的棕色玻瓶中,密闭保存。
四苯硼钠滴定液(0.02mol/L)(C6H5)4BNa=342.22 6.845g→1000mL【配制】取四苯硼钠7.0g,加水50ml振摇使溶解,加入新配制的氢氧化铝凝胶(取三氯化铝1.0g,溶于25mL水中,在不断搅拌下缓缓滴加氢氧化钠试液至pH8~9),加氯化钠16.6g,充分搅匀,加水250mL,振摇15分钟,静置10分钟,滤过,滤液中滴加氢氧化钠试液至pH8~9,再加水稀释至1000mL,摇匀。
【标定】精密量取本液10mL,加醋酸-醋酸钠缓冲液(pH3.7)10mL与溴酚蓝指示液0.5mL,用烃铵盐滴定液(0.01mol/L)滴定至蓝色,并将滴定的结果用空白试验校正。

实验室常用溶液的配制1.30%丙烯酰胺溶液(100ml)【配制方法】将29g丙烯酰胺和1g N,N'-亚甲双丙烯酰胺溶于总体积为60ml的蒸馏水中。
加热至37℃溶解之,补加水至终体积为100ml。
用Nalgene滤器(0.45μm孔径)过滤除菌,查证该溶液的pH值应不大于7.0,置棕色瓶中保存于4℃温度。
【注意】丙烯酰胺具有很强的神经毒性并可以通过皮肤吸收,其作用具累积性。
称量丙烯酰胺和亚甲双丙烯酰胺时应戴手套和面具。
可认为聚丙烯酰胺无毒,但也应谨慎操作,因为它还可能会含有少量未聚合材料。
一些价格较低的丙烯酰胺和双丙烯酰胺通常含有一些金属离子,在丙烯酰胺贮存液中加入大约0.2体积的单床混合树脂(MB-1Mallinckrodt),搅拌过夜,然后用Whatman 1号滤纸过滤以纯化之。
在贮存期间,丙烯酰胺和双丙烯酰胺会缓慢转化成丙烯酰和双丙烯酸,因此大于1年的溶液应该被丢弃。
2.40%丙烯酰胺(用于DNA测序,1L)【配制方法】把380g丙烯酰胺(DNA测序级)和20g N,N'-亚甲双丙烯酰胺溶于总体积为600ml 的蒸馏水中。
继续按上述配制30%丙烯酰胺溶液的方法处理,但加热溶解后应以蒸馏水补足至终体积为1L。
置棕色瓶中保存于室温。
【注意】见上述配制30%丙烯酰胺的说明,40%丙烯酰胺溶液用于DNA序列测定。
3.0.1mol/L腺苷三磷酸(ATP)溶液(1ml)【配制方法】在0.8ml蒸馏水中溶解60mg ATP,用0.1mol/L NaOH调至pH值至7.0,用蒸馏水稀释1ml【注意】分装成小份保存于-70℃4.10mol/L乙酸铵溶液(1L)【配制方法】把770g乙酸铵溶解于800ml蒸馏水中,加水稀释至1L后过滤除菌。
在4°C 储存。
【注意】乙酸铵是热不稳定的。
不要高压灭菌。
5.10%过硫酸铵溶液(10ml)【配制方法】把1g过硫酸铵溶于8ml蒸馏水中,用蒸馏水补足体积至10ml。
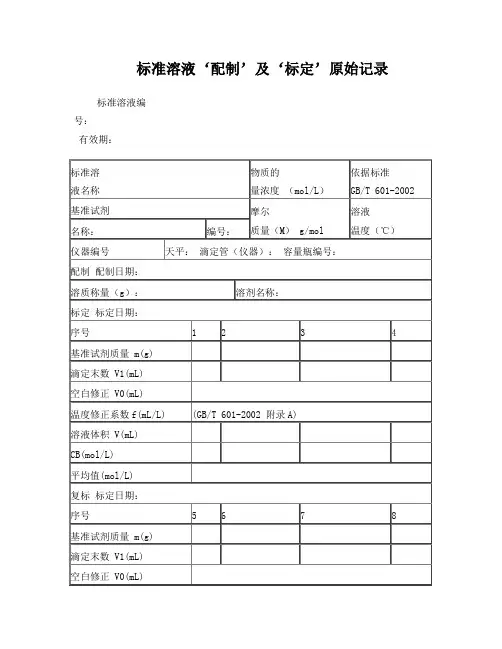
标准溶液‘配制’及‘标定’原始记录标准溶液编号:有效期:温度修正系数f(mL/L) (GB/T 601-2002 附录A)溶液体积 V(mL)CB(mol/L)平均值(mol/L)计算式:V=(V1-V0)×(1+f/1000)CB=1000m/(M×V)说明:每次滴定必须从“0”开始备注:配制人:标定:复标:审核:标准物质配制(标定)记录编号: CHEC/QBG-075名称:、配制方法:使用天平型号编号室温℃、湿度 %RH配制:取定溶 mL标定:取份:⑴⑵⑶⑷用溶液滴定,滴定消耗量(mL)V1= 、V2= 、V3= 、V4= 、V0= 。
标准溶液浓度计算公式:C=计算结果():C1= C2= C3= C4= C =相对偏差(%):S1= S2= S3= S4=备注:。
配制人:复核人:配制日期:年月日有效期年月日标准溶液配制记录编号: CHEC/QBG-147标准溶液名称:规格:配制方法:仪器名称:溯源标准:温度:℃ 、湿度: %RH 标准溶液拟配浓度:配制或稀释过程:配制日期:年月日有效期:年月日配制人:复核人:0.1mol/L盐酸标准滴定溶液的标定编号:JL/LJ-001-01一、标定方法:GB/T5009.1-2003二、使用仪器:AEL-200电子天平(仪器编号:JYB001)马弗炉(仪器编号:JYC009)三、操作1、量取9ml盐酸,加适量水并稀释至1000ml。
混匀,待标定。
2、标定:精密称取约0.15g在270~300℃干燥至恒量的基准无水碳酸钠,加50ml水使之溶解,加10滴溴甲酚绿-甲基红混合指示液,用本溶液滴定至溶液由绿色转变为紫红色,煮沸2min,冷却至室温,继续滴定至溶液由绿色变为暗紫色。
四、记录和结果1、计算公式:c(HCl)=m/[(V1-V2)×0.0530]0.0530……与1.00ml盐酸标准滴定溶液[c(HCl)=1mol/L]相当的基准无水碳酸钠的质量,g2、数据配制人:复核人:配制日期:复核日期:稀释记录表标准溶液(滴定液)管理工作的基本要求关键词(必填项目):标准溶液、滴定液目的(必填项目):对标准溶液的使用等制定统一的要求,便于统一的管理。

大学化学实验实验一酸碱标准溶液的配制和标定实验目的1.掌握标准溶液的配制方法。
2.掌握滴定法定量测定溶液浓度的原理,熟悉滴定管、移液管的准备、使用及滴定操作。
3.熟悉甲基橙和酚酞指示剂的使用和终点的确定。
实验原理酸碱滴定法是化学定量分析中最基本的分析方法。
一般能与酸或碱直接(或间接)发生酸碱反应的物质大多可用酸碱滴定法测定他们的浓度。
按酸碱反应方程式中的化学计量系数之比,酸与碱完全中和时的pH 值称为化学计量点,达到化学计量点时,应满足如下基本关系:c A V A c B V BA B式中, c A、V A、A 分别为酸的“物质的量”浓度、体积、化学计量系数;c B、V B、 B 分别为碱的“物质的量”浓度、体积、化学计量系数。
其中,酸、碱的化学计量系数由酸碱反应方程式决定。
由于酸、碱的强弱程度不同,因此酸碱滴定的化学计量点不一定在pH=7 处。
通常,酸碱溶液为无色,酸碱中和是否完全,需用指示剂的变色来判断。
指示剂往往是一些有机的弱酸或弱碱,它们在不同pH 值条件下颜色不同。
用作指示剂时,其变色点(在化学计量点附近)的 pH 值称为滴定终点。
选用指示剂要注意:①变色点与化学计量点尽量一致;②颜色变化明显;③指示剂用量适当。
酸碱滴定中常用 HCl 和 NaOH 溶液作为标准溶液,但由于浓 HCl 容易挥发,NaOH 固体容易吸收空气中的 H2O 和 CO2,直接配成的溶液其浓度不能达到标准溶液的精度,只能用标定法加以标定。
基准物质H2C2O4的分子式确定,化学性质稳定,不易脱水或吸水,可以准确称量,所以,本实验采用(H2C2O4·2H2O,摩尔质量为 126.07g· mol-1)为基准物质,配成 H2C2O4标准溶液。
以酚酞为指示剂,用 H2C2O4标准溶液标定 NaOH 溶液;再以甲基橙为指示剂,用标定后的NaOH 标准溶液滴定 HCl 溶液,从而得到 HCl 标准溶液。
仪器与试剂电子天平,酸式滴定管(50 mL),碱式滴定管( 50 mL),容量瓶(250 mL),移液管( 25 mL),吸耳球,锥形瓶( 250 mL),试剂瓶,量筒,洗瓶,滴定台,蝴蝶夹,烧杯,玻棒,滴瓶,滴管。

常见实验用溶液的配制方法默认分类2008-07-04 14:10:54 阅读4 评论0 字号:大中小一、常用溶液1mol/L亚精胺(Spermidine):溶解2.55g亚精胺于足量的水中,使终体积为10ml。
分装成小份,贮存于-20℃。
1mol/L精胺(Spermine):溶解3.48g精胺于足量的水中,使终体积为10ml。
分装成小份,贮存于-20℃。
10mol/L乙酸胺(ammonium acetate):将77.1g乙酸胺溶解于水中,加水定容至1L后,用0.22um孔径的滤膜过滤除菌。
10mg/ml牛血清蛋白(BSA):加100mg的牛血清蛋白(组分V或分子生物学试剂级,无DNA酶)于9.5ml水中(为减少变性,须将蛋白加入水中,而不是将水加入蛋白),盖好盖后,轻轻摇动,直至牛血清蛋白完全溶解为止。
不要涡旋混合。
加水定容到10ml,然后分装成小份,贮存于-20℃。
1mol/L二硫苏糖醇(DTT):在二硫苏糖醇5g的原装瓶中加32.4ml水,分成小份贮存于-20℃。
或转移100mg的二硫苏糖醇至微量离心管,加0.65ml的水配制成1mol/L二硫苏糖醇溶液。
8mol/L乙酸钾(potassium acetate):溶解78.5g乙酸钾于足量的水中,加水定容到100ml。
1mol/L氯化钾(KCl):溶解7.46g氯化钾于足量的水中,加水定容到100ml。
3mol/L乙酸钠(sodium acetate):溶解40.8g的三水乙酸钠于约90ml水中,用冰乙酸调溶液的pH至5.2,再加水定容到100ml。
0.5mol/L EDTA:配制等摩尔的Na2EDTA和NaOH溶液(0.5mol/L),混合后形成EDTA的三钠盐。
或称取186.1g的Na2EDTA·2H2O和20g的NaOH,并溶于水中,定容至1L。
1mol/L HEPES:将23.8gHEPES溶于约90ml的水中,用NaOH调pH(6.8-8.2),然后用水定容至100ml。

实验室常用溶液配制(希望对大家有帮助)一. 常用贮液与溶液1mol/L亚精胺(Spermidine): 溶解2.55g亚精胺于足量的水中,使终体积为10ml。
分装成小份贮存于-20℃。
1mol/L精胺(Spermine):溶解3.48g精胺于足量的水中,使终体积为10ml。
分装成小份贮存于-20℃。
10mol/L乙酸胺(ammonium acetate):将77.1g乙酸胺溶解于水中,加水定容至1L后,用0.22um孔径的滤膜过滤除菌。
10mg/ml牛血清蛋白(BSA):加100mg的牛血清蛋白(组分V或分子生物学试剂级,无DNA酶)于9.5ml水中(为减少变性,须将蛋白加入水中,而不是将水加入蛋白),盖好盖后,轻轻摇动,直至牛血清蛋白完全溶解为止。
不要涡旋混合。
加水定容到10ml,然后分装成小份贮存于-20℃。
1mol/L二硫苏糖醇(DTT):在二硫苏糖醇5g的原装瓶中加32.4ml水,分成小份贮存于-20℃。
或转移100mg的二硫苏糖醇至微量离心管,加0.65ml的水配制成1mol/L二硫苏糖醇溶液。
8mol/L乙酸钾(potassium acetate):溶解78.5g乙酸钾于足量的水中,加水定容到100ml。
1mol/L氯化钾(KCl):溶解7.46g氯化钾于足量的水中,加水定容到100ml。
3mol/L乙酸钠(sodium acetate):溶解40.8g的三水乙酸钠于约90ml水中,用冰乙酸调溶液的pH至5.2,再加水定容到100ml。
0.5mol/L EDTA:配制等摩尔的Na2EDTA和NaOH溶液(0.5mol/L),混合后形成EDTA的三钠盐。
或称取186.1g的Na2EDTA•2H2O和20g的NaOH,并溶于水中,定容至1L。
1mol/L HEPES:将23.8gHEPES溶于约90ml的水中,用NaOH调pH(6.8-8.2),然后用水定容至100ml。

实验室常用溶液的配制1.30%丙烯酰胺溶液(100ml)【配制方法】将29g丙烯酰胺和1g N,N’—亚甲双丙烯酰胺溶于总体积为60ml的蒸馏水中.加热至37℃溶解之,补加水至终体积为100ml。
用Nalgene滤器(0。
45μm孔径)过滤除菌,查证该溶液的pH值应不大于7.0,置棕色瓶中保存于4℃温度。
【注意】丙烯酰胺具有很强的神经毒性并可以通过皮肤吸收,其作用具累积性.称量丙烯酰胺和亚甲双丙烯酰胺时应戴手套和面具.可认为聚丙烯酰胺无毒,但也应谨慎操作,因为它还可能会含有少量未聚合材料。
一些价格较低的丙烯酰胺和双丙烯酰胺通常含有一些金属离子,在丙烯酰胺贮存液中加入大约0.2体积的单床混合树脂(MB-1Mallinckrodt),搅拌过夜,然后用Whatman 1号滤纸过滤以纯化之。
在贮存期间,丙烯酰胺和双丙烯酰胺会缓慢转化成丙烯酰和双丙烯酸,因此大于1年的溶液应该被丢弃。
2.40%丙烯酰胺(用于DNA测序,1L)【配制方法】把380g丙烯酰胺(DNA测序级)和20g N,N'-亚甲双丙烯酰胺溶于总体积为600ml 的蒸馏水中。
继续按上述配制30%丙烯酰胺溶液的方法处理,但加热溶解后应以蒸馏水补足至终体积为1L。
置棕色瓶中保存于室温。
【注意】见上述配制30%丙烯酰胺的说明,40%丙烯酰胺溶液用于DNA序列测定.3.0。
1mol/L腺苷三磷酸(ATP)溶液(1ml)【配制方法】在0。
8ml蒸馏水中溶解60mg ATP,用0。
1mol/L NaOH调至pH值至7。
0,用蒸馏水稀释1ml【注意】分装成小份保存于—70℃4.10mol/L乙酸铵溶液(1L)【配制方法】把770g乙酸铵溶解于800ml蒸馏水中,加水稀释至1L后过滤除菌.在4°C储存。
【注意】乙酸铵是热不稳定的.不要高压灭菌.5.10%过硫酸铵溶液(10ml)【配制方法】把1g过硫酸铵溶于8ml蒸馏水中,用蒸馏水补足体积至10ml.该溶液可在4℃保存数周。
标准溶液制备和标定一、标准溶液的种类:1. 滴定分析用标准溶液:也称为标准滴定溶液,主要用于:测定样品的主体成分或常量成分。
其浓度要求准确到4位有效数字,常用的浓度表示方法是物质的量浓度和滴定度。
2. 杂质测定用标准溶液:包括元素标准溶液、标准比对溶液(如标准比色溶液、标准比浊溶液等)。
主要用于对样品中微量成分(元素、分子、离子等)进行定量、半定量或限量分析,其浓度通常经质量浓度来表示,常用的单位是mg/mL,mg/L,μg/mL等。
3. pH测量用标准缓冲液:具有准确的pH数值,由pH基准试剂进行配制。
用于对pH计的校准,亦称定位。
一般溶液是指非标准溶液,它在食品检验中常作为溶解样品、调节pH值、分离或掩蔽离子、显色等使用。
一般溶液配制的浓度要求不高,只需保留1~2位有效数字。
试剂的质量由架盘天平称量,体积用量筒量取即可。
二、滴定分析用标准溶液的制备1. 一般规定:标准溶液的浓度准确程度直接影响分析结果的准确度。
因此,制备标准溶液在方法、使用仪器、量具和试剂等方面都有严格的要求。
国家标准GB/T601-2016《滴定分析用标准溶液的制备》中对上述各个方面的要求作了一般规定,即在制备滴定分析(容量分析)用标准溶液时,应达到下列要求:①配制标准溶液用水,至少应符合GB/T 6682-2008中三级水的规格。
②所用试剂纯度应在分析纯以上,标定所用的基准试剂应为容量分析工作中使用的基准试剂。
③所用分析天平及砝码应定期检定。
④所用滴定管、容量瓶及移液管均需定期校正,校正方法按JJG196-2006《常用玻璃量器检定规程》中规定进行。
⑤制备标准溶液的温度系指20℃时的浓度,在标定的使用时,如温度有差异,应按GB/T 601-2016中附录A进行补正。
⑥标定标准溶液时,平行试验不得少于8次,两人各作4次平行测定,检测结果在按GB/T 601-2016规定的方法进行数据的取舍后取平均值,浓度值取4位有效数字。
实验室常用溶液的配制标准程序3 、适用范围XXXX研发部常用溶液:3M 醋酸钠、2N NaOH 、5M NaCL、Solution Ⅰ、Solution ⅡSolution 、Solution Ⅲ、LB培养基、1M Tris-HCl 、10 ×TE Buffer 、10 ×PBS Buffer 、苯酚/ 氯仿/ 异戊醇、10%(W/V )SDS 、0.5M EDTA(pH 8.0) 、50 ×TAEBUffer 、20 ×SSC 、封闭缓冲液(Wester杂交)。
4 、配制4.1 、用具干燥洁净的200ml量桶一只,三角烧瓶两只,天平一架,250ml、1000ml广口瓶各一只。
4.2 、配制步骤4.2.1 、配制NaAC溶液⑴用天平称取40.8克分析纯的NaOAC固体,置于250ml三角烧瓶中。
⑵用100ml量桶准确取40ml去离子水,摇荡三角烧瓶使NaOH固体充分溶解⑶加去离子水将溶液定容到100ml⑷高压灭菌后,室温保存。
4.2.2 、配制NaOH溶液⑴用100ml量桶准确取80ml去离子水,置于250ml三角烧瓶中。
⑵用天平称取8克NaOH固体缓缓加入三角烧瓶中。
⑶摇荡混匀溶液。
用去离子水将溶液体积定容到100ml。
⑷将混匀的溶液转移入玻璃瓶中,室温保存。
4.2.3 、配制NaCL溶液⑴用天平称取292.2克NaCL固体置于1L烧杯中,加入800ml的去离子水后搅拌溶解。
⑵加去离子水将溶液定容至1L,适量分成小份。
⑶高压灭菌后,4 0 C 保存。
4.2.4 、配制Solution Ⅰ溶液(1)量取1M Tris-HCL(ph8.0) 25ml ,1.5M EDTA(ph8.0) 20ml , 20 %Glucose(1.11M) 45ml, dH 2 O 910ml , 置于1L烧杯中。
(2)高温高压灭菌后,4 0 C 保存。
(3)使用前每50 ml的Solution Ⅰ加入2 ml 的RNaseA(20mg / ml).4.2.5 、配制Solution Ⅱ溶液(1) 量取10 %SDS 50 ml, 2N NAOH 50 ml, 置于500 ml 烧杯中。
溶液配置标签格式溶液浓度是指在一定质量或一定体积的溶液中所含溶质的量.化学分析所用的溶液不仅种类繁多,而且要求的浓度也千差万别.正确表示各种溶液浓度及正确书写标签内容是搞好检测工作的基本规范要求之一.国际标准化组织ISO,国际理论化学与应用化学联合会IUPAC和我国国家标准GB都作出相关规定.现结合日常工作实践,就化学分析用各种溶液的浓度表示方法和标签内容格式作一介绍,以满足实验室认可对化学分析用各种溶液的浓度表示方法和标签内容书写格式的要求.1 标准滴定溶液 standard volumetric solution1.1 定义已知准确浓度的用于滴定分析用的溶液.1.2 浓度表示方法1.2.1 物质的量浓度a. 定义:单位体积中所含溶质B的物质的量.b. 物质的量浓度符号:cB.c. 物质的量浓度单位:计量单位为"mol/m3"及其倍数,实验室中常用的单位是"mol/L"或1mol/dm3.d. 说明:物质的量的SI基本单位是摩尔 (单位符号为"mol"),其定义如下:摩尔是一系统的物质的量,该系统中所包含的基本单元数与0.012kg碳-12。
在使用摩尔时,基本单元应予指明,可以是原子,分子,离子,电子及其他粒子,或是这些粒子的特定组合.因此,在使用物质的量浓度时也必须指明基本单元.e. 实例c(NaOH)=0.1015mol/L氢氧化钠溶液,小括号内的NaOH是指溶液中溶质的基本单元,c(NaOH)是表示基本单元为NaOH的物质的量浓度.等号右边的0.1015mol/L表示物质的量浓度数数值为0.1015摩尔每升,即每升含氢氧化钠1×氢氧化钠分子量×0.1015克.c(1/2H2SO4)=0.2042mol/L硫酸溶液,表示基本单元为1/2H2SO4的物质的量浓度为0.2042摩尔每升.即每升含硫酸1/2×硫酸分子量×0.2042克.c(1/5KMnO4)=0.1000mol/L高锰酸钾溶液,表示基本单元为1/5KMnO4的物质的量浓度为0.1000摩尔每升.即每升含高锰酸钾1/5×高锰酸钾分子量×0.1000克.c(1/6K2Cr2O7)=1.0042mol/L重铬酸钾溶液,表示基本单元为1/6 K2Cr2O7的物质的量浓度为1.0042摩尔每升.即每升含重铬酸钾1/6×重铬酸钾分子量×1.0042克.c(1/2Ca2+)=1.0035mol/L钙阳离子溶液,表示基本单元为1/2 Ca2+的物质的量浓度为1.0035摩尔每升.即每升含钙阳离子1/2×钙原子量×1.0035克.1.2.2 质量浓度a. 质量浓度定义:作为溶质的物质的质量除以混合物(即溶液)体积.b. 质量浓度符号:ρB B代表作为溶质的物质.c. 质量浓度单位:计量单位为"kg/m3","kg/L"(1kg/L=103kg/ m3=1kg/d实验室常用"g/L","mg/L","mg/mL","μg/mL"等.d. 质量浓度表示法实例: ρB表示法:ρ(Na2CO3)=0.5021mg/mL碳酸钠标准滴定溶液,表示碳酸钠标准滴定溶液的质量浓度为0.5021毫克每毫升.ρA/B表示法: A代表被测物质;B代表滴定溶液中有效物质分子式.ρ(Cl-/AgNO3)=0.5000mg/mL硝酸银标准滴定溶液表示1mL硝酸银标准滴定溶液相当于0.5000mg的氯离子.1.3 标准滴定溶液标签的书写内容及格式用物质的量浓度表示浓度的标准滴定溶液的标签的书写内容包括以下几项:配制,标定,校验及稀释等都要有详细的记录,应当与检测原始记录一样要求. 标签上应有溶液名称,浓度类型,浓度值,介质,配制日期,配制温度(指配制时恒温室室温),校核周期(或有效期),配制者和配制的同一溶液的瓶编号,注意事项及其他需要注明事项等.介质是水时,可不必标出,介质是其他物质时应予标明.标签格式举例说明.溶液名称重铬酸钾标准滴定溶液浓度 C(1/6K2Cr2O7)=0.6022mol/L介质配制温度配制日期 2003-03-20校核周期半年配制者×××,×××瓶编号 1#2 基准溶液2.1 定义用于标定其他溶液的作为基准的溶液.2.2 浓度表示方法基准溶液的浓度,按1.1.2中标准滴定溶液的浓度表示方法同样表示.2.3 基准溶液的标签书写内容及格式基准溶液的标签书写内容及格式与1.1.3中标准滴定溶液的标签书写内容及格式基本相同,仅将标签中溶液名称一栏中的"标准滴定溶液"换为"基准溶液"即可.3 标准溶液 standard solution3.1 定义由用于制备该溶液的物质而准确知道某种元素,离子,化合物或基团浓度的溶液. 这类溶液也被称为元素标准溶液或组份标准溶液.3.2 浓度表示方法a. 这类溶液的浓度一般均采用质量浓度表示.即作为溶液的物质的质量除以混合物(即溶液)的体积b. 符号:ρB B代表作为溶质的物质.c. 单位:计量单位为"kg/m3","kg/L"(1kg/L=103kg/ m3=1kg/d m3)及其倍数.实验中常用"g/L","mg/L","μg/mL"单位.d. 表示实例ρ(Zn2+)=2μg/mL,在一般情况下,用ρB表示元素标准溶液的浓度时,只写整数及小数点后的非零数字.这种表示法不考虑有效数字的规定.如:ρ(Zn2+)=2μg/mL不写成ρ(Zn2+)=2.000μg/mL;(Ag)=1.5μg/mL不写成ρ(Ag)=1.500μg/mL.3.3 标准溶液标签书写内容及格式标准溶液标签书写内容及格式与1.1.3基本相同,仅将溶液名称栏内的"标准滴定溶液"改为"标准溶液".标签格式举例:溶液名称铅标准溶液浓度ρ(Pb)=1μg/mL介质 1% HNO3配制温度 17 ℃配制日期 2005-02-10 校核周期配制者××× 瓶编号 2#介质栏内1%HNO3是作为非水介质,介质的溶质是液体时,不特别注明则为体积分数φB,作为介质,不带量符号.若介质的溶质为固体时,则用ρB表示介质的质量浓度,不带量符号.如下述例子中介质栏40g/L NaOH溶液就是指ρB(质量浓度).4 标准比对溶液 standard matching solution此术语仅用于此类溶液的统称,其每个溶液通常用适当的形容词更加具体的命名.如"标准比色溶液","标准比浊溶液"等.4.1定义已知或已确定有关特性(如色度,浊度)的并用来评定试验溶液各该特性的溶液。
试剂配制注意事项
1、分析实验所用的溶液应用纯水配制,容器应用纯水洗三次以上。
特殊要求的溶液应事先作纯水的空白值检验。
如配制A g NO3溶液,应检验水中无C1,配制用于EDTA络合滴定溶液应检验水中无阳离子。
2、溶液要用带塞的试剂瓶盛装,见光易分解的溶液要装于棕色瓶中,挥发性试剂例如用有机溶剂配制的溶液,瓶塞要严密,见空气易变质及放出腐蚀性气体的溶液也要盖紧,不能用玻璃磨口塞。
3、每瓶试剂溶液必须有标明名称、规格、浓度和配制日期的标签。
4、配制硫酸、硝酸、盐酸等溶液时,都应把酸倒入水中,对于溶解时放热较多的试剂,不可在试剂瓶中配制,以免破裂。
配制硫酸溶液时,应将浓硫酸分为小份慢慢倒入水中,边加边搅,必要时冷却烧杯外壁。
5、要熟悉一些常用溶液的配制方法。
如碘溶液应将于较浓的碘化钾水溶液中,才可稀释。
配制易水解的盐类的水溶液应先加酸溶解后,再以一定浓度稀酸稀释。
如配制SnC12溶液时,如果操作不当已发生水解,加相当多的酸仍难溶解沉淀。
6、不能用手接触腐蚀性及有剧毒的溶液。
剧毒废液应作解毒处理,不可直接倒入下水道。
7、溶液贮存时可能发生变质现象,应予注意,对于酸、碱、氧化性、还原标准溶液等应经常标定,以免给分析结果带来误差。
磷标准溶液标签全文共四篇示例,供读者参考第一篇示例:磷标准溶液是实验室常用的一种化学试剂,在科研、教学和工业生产中都有着重要的应用。
为了确保磷标准溶液的使用安全和准确性,通常会在瓶子上贴上相应的标签,以便对其成分、规格、有效期等信息进行标示和识别。
本文将就磷标准溶液标签的制作相关知识进行介绍。
一、标签内容磷标准溶液标签上通常会包含以下内容:1. 产品名称:明确标识出瓶中溶液的成分,即磷标准溶液。
2. 规格浓度:标明溶液的浓度,如mg/L或mol/L。
3. 生产日期:记录制造磷标准溶液的具体日期,以便对其有效期做出准确的评估。
4. 有效期:注明磷标准溶液的有效期限,建议在此期限内使用,超过有效期限制时间后建议丢弃。
5. 保存条件:指明磷标准溶液的最佳存放条件,如避光、防潮、低温保存等。
6. 生产厂家:注明生产磷标准溶液的厂家名称和联系方式,以方便用户在需要时进行咨询和反馈。
7. 警示标语:如有对该溶液的特殊警示要求,如“易燃”、“腐蚀”等,应在标签上进行明确标示,以确保使用者的安全。
以上是磷标准溶液标签上常见的内容,可以根据实际需要进行适当调整和扩充。
二、标签材质制作磷标准溶液标签时,需要选用合适的标签材质,以确保其质量和耐久性。
常见的标签材质有:1. 纸质标签:适用于一次性使用的标签,成本较低。
2. PVC标签:适用于在潮湿环境下使用的标签,具有一定的防水性能。
3. PET标签:具有较好的耐腐蚀性和耐高温性能,适用于高要求的使用环境。
根据磷标准溶液的使用场景和特点,选择合适的标签材质非常重要。
三、制作方法制作磷标准溶液标签可以通过专业的标签打印机进行,也可以通过手工制作的方式进行。
下面介绍一种简单的手工制作方法:1. 准备标签材料:选择合适的标签材质,如纸质标签、PVC标签或PET标签,按照磷标准溶液瓶子的大小和形状进行裁剪。
2. 设计标签内容:根据磷标准溶液的需要,设计标签内容,选择合适的字体和颜色,确保标签清晰易读。
实验室常用溶液及试剂配制实验室常用溶液、试剂的配制表一普通酸碱溶液的配制名称(分子式)比重(d)含量(w/w%)近似摩尔浓度(mol/L)欲配溶液的摩尔浓度(mol/L)6 3 2 1配制1L溶液所用的ml数(或g)盐酸(HcL) 1.18~1.19 36~38 12 500 250 167 83硝酸(HNO3) 1.39~1.40 65~68 15 381 191 128 64硫酸(H2SO4) 1.83~1.84 95~98 18 84 42 28 14冰醋酸(Hac) 1.05 99.9 17 253 177 118 59磷酸(H3PO4) 1.69 85 15 39 19 12 6氨水(NH3•H2O) 0.90~0.91 28 15 400 200 134 77氢氧化钠(NaOH)(240)(120)(80)(40)氢氧化钾(KOH)(339)(170)(113)(56.5)表二常用酸碱指示剂指示剂 PKHIn 变色范围pH 酸色碱色配制方法百里酚蓝(麝香草酚蓝) 1.65 12.~2.8 红黄 0.1%的20%乙醇溶液甲基橙 3.4 3.1~4.4 红橙黄 0.05%水溶液溴甲酚绿 4.9 3.8~5.4 黄蓝 0.1%的20%乙醇溶液或0.1g指示剂溶于2.9ml 0.05mol/L NaOH加水稀释至100ml甲基红 5.0 4.4~6.2 红黄 0.1%的60%乙醇溶液溴百里酚蓝(麝香草酚蓝) 7.3 6.2~7.3 黄蓝 0.1%的20%乙醇溶液中性红 7.4 6.8~8.0 红黄橙 0.1%的60%乙醇溶液百里酚蓝(第二变色范围) 9.2 8.0~9.6 黄蓝 0.1%的20%乙醇溶液酚酞 9.4 8.0~10.0 无色红 0.5%的90%乙醇溶液百里酚酞 10.0 9.4~10.6 无色蓝 0.1%的90%乙醇溶液表三混合酸碱指示剂指示剂组成(体积比)变色点pH 酸色碱色备注一份0.1%甲基橙水溶液一份0.25%靛蓝二磺酸钠水溶液 4.1 紫绿灯光下可滴定一份0.02%甲基橙水溶液一份0.1溴甲酚绿钠盐水溶液 4.3 橙蓝绿 PH3.5黄色PH4.05绿黄PH4.3浅绿三份0.1%溴甲酚绿20%乙醇溶液一份0.2%甲基红60%乙醇溶液 5.1 酒红绿颜色变化极鲜明一份0.2%甲基红乙醇溶液一份0.1%次甲基蓝乙醇溶液 5.4 红紫绿 PH5.2红紫PH5.4暗蓝PH5.6绿色一份0.1%溴甲酚绿钠盐水溶液一份0.1%绿酚红钠盐水溶液 6.1 黄绿蓝紫 PH5.6蓝绿PH5.8蓝色PH6.0浅紫PH6.2蓝紫一份0.1%溴甲酚紫钠盐水溶液一份0.1溴百里酚蓝钠盐水溶液 6.7 黄紫蓝 PH6.2黄紫PH6.6紫PH6.8蓝紫一份0.1中性红乙醇溶液一份0.1次甲基蓝乙醇溶液 7.0 蓝紫绿 PH7.0为蓝绿必须保存在棕色瓶中一份0.1甲酚红钠盐水溶液三份0.1%百里酚蓝钠盐水溶液 8.3 黄紫 PH8.2玫瑰色PH8.4紫色一份0.1%百里酚蓝50%乙醇溶液三份0.1酚酞50%乙醇溶液 9.0 黄紫 PH9.0绿色表四容量分析基准物质的干燥基准物质干燥温度和时间基准物质干燥温度和时间碳酸钠(NaCO3) 500~650℃,40-50min 氯化物(NaCl) 500-650℃,干燥40-50min草酸钠(H2C2O4) 150-200℃,1-1.5h 硝酸银(AgNO3)室温,硫酸干燥器中至恒温草酸(H2C2•2H2O)室温,空气干燥2-4h 碳酸钙(CaCO3)120℃,干燥至恒重硼砂(Na2B2O•10H2O)室温,在NaCl和蔗糖饱和液的干燥器中,4h 氧化锌(ZnO)800℃灼烧至恒重邻苯二甲酸氢钾(KHC6H4O4) 100-120℃,干燥至恒重锌(Zn)室温,干燥器24h以上重铬酸钾(K2Cr2O7) 100-110℃,干燥3-4h 氧化镁(MgO)800℃灼烧至恒重表五缓冲溶液的配制1、氯化钾-盐酸缓冲溶液0.2mol/LKCl(ml) 50 50 50 50 50 50 500.2mol/LHCl(ml) 97.0 64.3 41.5 26.3 16.6 10.6 6.7 水(ml) 53.0 85.5 108.5 123.7 133.4 139.4 143.3PH(20℃) 1.0 1.2 1.4 1.6 1.8 2.0 2.22、邻苯二甲酸氢钾-氢氧化钾缓冲溶液0.2mol/LKHC6H4O4(ml) 50 50 50 50 500.2mol/LHCl(ml) 46.70 32.95 20.32 9.90 2.63水(ml) 103.30 117.05 129.68 140.10 147.37PH(20℃) 2.2 2.6 3.0 3.4 3.83、邻苯二甲酸氢钾-氢氧化钾缓冲溶液0.2mol/LKHC6H4O4(ml) 50 50 50 50 500.2mol/LHCl(ml) 0.40 7.50 17.70 29.95 39.85水(ml) 149.60 142.50 132.20 120.05 110.15PH(20℃) 4.0 4.4 4.8 5.2 5.64、乙酸-乙酸钠缓冲溶液0.2mol/LHAc(ml) 185 164 126 80 42 190.2mol/LNaAc(ml) 15 36 74 120 158 181PH(20℃) 3.6 4.0 4.4 4.8 5.2 5.65、磷酸二氢钾-氢氧化钠缓冲溶液0.2mol/LKH2PO4(ml) 50 50 50 50 50 500.2mol/LNaOH(ml) 3.72 8.60 17.80 29.63 39.50 45.20 水(ml) 146.26 141.20 132.20 120.37 110.50 104.80 PH(20℃) 5.8 6.2 6.6 7.0 7.4 7.86、硼砂-氢氧化钠缓冲溶液0.2mol/L硼砂(ml) 90 80 70 60 50 400.2mol/LNaOH(ml) 10 20 30 40 50 60PH(20℃) 9.35 9.48 9.66 9.94 11.04 12.327、氨水-氯化铵缓冲溶液0.2mol/LNH3•H2O(ml) 1 1 1 2 8 320.2mol/LNH4Cl(ml) 32 8 2 1 1 1PH(20℃) 8.0 8.58 9.1 9.8 10.4 11.08、常用缓冲溶液的配制PH 配制方法3.6 NaAc•3H2O 8g,溶于适量水中,加6mol/LHAc 134ml,稀释至500ml4.0 NaAc•3H2O 20g溶于适量水中,加6mol/LHAc 134ml,稀释至500ml4.5 NaAc•3H2O 32g溶于适量水中,加6mol/LHAc 68ml,稀释至500ml5.0 NaAc•3H2O 50g溶于适量水中,加6mol/LHAc 34ml,稀释至500ml8.0 NH4Cl 50g 溶于适量水中,加15mol/LNH3•H2O 3.5ml,稀释至500ml8.5 NH4Cl 40g 溶于适量水中,加15mol/LNH3•H2O 8.8ml,稀释至500ml9.0 NH4Cl 35g 溶于适量水中,加15mol/LNH3•H2O 24ml,稀释至500ml9.5 NH4Cl 30g 溶于适量水中,加15mol/LNH3•H2O 65ml,稀释至500ml10 NH4Cl 27g 溶于适量水中,加15mol/LNH3•H2O 197ml,稀释至500ml实验室常用试验方法2九、柠檬酸(C6H8O7•H2O)称取试样1.5g(精确到0.0002g)于三角瓶内,加入水50ml溶解,加酚酞指示剂3滴,用1mol/L氢氧化钠标准溶液滴定至粉红色为终点,同时做空白试验。