Q_JBSW 045-2019混合型饲料添加剂 液态溶菌酶
- 格式:pdf
- 大小:698.37 KB
- 文档页数:7

溶菌酶----新型免疫抗菌抗病毒药物、饲料添加剂溶菌酶研发背景:抗生素是人类应用最广泛的抗菌药物,不仅用于临床,也广泛用于畜禽饲养和农业方面。
在过去的50多年中,由于饲用抗生素在养殖中的长期使用导致大量耐药菌株的产生,且病原菌抗药性逐年增强,致使疗效下降,剂量提高,造成动物疾病越防越难防,越治越难治,给养殖业造成很大的损失和危害。
同时也给全人类的健康造成严重的影响。
因此,世界卫生组织于1994年就细菌耐药性的监测结果给全世界提出了警示:细菌对抗生素产生的耐药性正在以惊人的速度增加,而现在的抗生素药物正在失去原来的疗效。
因此寻求广谱、高效的新一代饲用抗菌药物已成为迫在眉睫的摆在人类面前的课题。
澳大利亚昆士兰大学医学系博士生导师、高级研究员王雯禾博士(1993年毕业于英国剑桥大学达尔文学院获微生物营养学博士学位),一直致力于生命科学的研究和发展,历经十多年的研究发现:酶广泛存在于生物体内,参与新陈代谢等多种生理功能,其中对微生物细胞壁具有水解功能的抗菌酶,如溶菌酶lysozyme能够溶解微生物细胞壁而使微生物死亡,而且溶菌酶lysozyme在人和动物的唾液、眼泪、乳汁以及肌体组织中大量存在,是人和动物自身重要的免疫因子,与人和动物的健康息息相关。
溶菌酶lysozyme的溶菌(杀菌)作用与传统的抗生素药物相比,具有对某一病原菌所有血清型都有效的优点,克服了一种抗生素只能预防一种或其中一种血清型病原菌的不足,更不存在药物残留和耐药性的问题。
王雯禾博士认为,溶菌酶lysozyme作为畜禽、水产饲料添加剂在替代抗生素,控制耐药菌,生产绿色肉蛋奶食品方面是最佳的选择。
并多次鼓励和支持国内年轻的科学家、学者,致力于这一伟大的、划时代的、对全人类的健康有杰出贡献的产品的开发和研究。
并于2003年10月推出最早用于防治动物疾病的产品--溶菌酶系列,由于它不但能溶解(杀死)细菌,增强动物的免疫能力,而且还能和病毒结合使病毒失活,所以它作为预防动物疾病的新型饲料添加剂,正在动物疾病防治的许多领域被广泛应用。

ICS65.120B 46 Q/JHSW 金河生物科技股份有限公司企业标准Q/JHSW 006—2019 混合型饲料添加剂 L-赖氨酸(报批稿)2019-11-26发布2019-12-26实施前言本标准依据GB/T1.1-2009给出的规则起草。
本标准由金河生物科技股份有限公司提出。
本标准由金河生物科技股份有限公司起草。
本标准由金河生物科技股份有限公司批准。
本标准主要起草人:张兴明、张明明。
本标准为首次发布。
混合型饲料添加剂 L-赖氨酸1 范围本标准规定了混合型饲料添加剂L-赖氨酸产品的技术要求、试验方法、检验规则、标识、包装、运输、贮存和保质期。
本标准适用于以L-赖氨酸盐酸盐为原料,以单硬脂酸甘油酯为载体加工而成的混合型饲料添加剂L-赖氨酸。
2 规范性引用文件下列文件对于本文件的应用是必不可少的。
凡是注日期的引用文件,仅所注日期的版本适用于本文件。
凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
GB/T 5917.1 饲料粉碎粒度测定 两层筛筛分法GB/T 6435 饲料中水分和其他挥发性物质含量的测定GB 10648 饲料标签GB 12904 商品条码 零售商品编码与条码表示GB 13078 饲料卫生标准GB/T 14699.1 饲料 采样GB/T 18823 饲料检测结果判定的允许误差GB 34466 饲料添加剂 L-赖氨酸盐酸盐《定量包装商品计量监督管理办法》(2005)中华人民共和国农业部公告 第1773号《饲料原料目录》中华人民共和国农业部公告 第2045号《饲料添加剂品种目录(2013)》3 要求3.1 感官本品为类白色至微黄色颗粒状物。
3.2 加工质量指标3.2.1 水分水分不大于10%。
3.2.2 粒度95%通过孔径为850μm的试验筛。
3.3 产品成分分析保证值产品L型L-赖氨酸(以盐酸盐计)含量不低于35.0%;产品M型L-赖氨酸(以盐酸盐计)含量不低于40.0%;产品H型L-赖氨酸(以盐酸盐计)含量不低于45.0%。

溶菌酶在饲料中的应用李鑫1 ,谭志坚1 ,凌欣华2,李巧贤3(1 佛山市正典生物技术有限公司,广东佛山 528138;2 梅州市畜牧兽医技术推广站,广东梅州 514021;3 广东现代农业集团研究院,广东广州 510630)溶菌酶(Lysozyme)又称胞壁质酶或N-乙酰胞质聚糖水解酶,是动物体内一种非特异性免疫因子,具有抗菌消炎、抗病毒、增强免疫力、促进双歧杆菌等有益菌增殖的作用。
本文介绍了溶菌酶的特性、分类和作用机理,重点综述了溶菌酶作为饲料添加剂在猪、鸡、鸭、反刍动物以及水产动物等饲料中的应用。
溶菌酶广泛存在于鸟类和家禽的蛋清中,亦存在于哺乳动物的泪液、唾液、血浆、乳汁、胎盘、体液及组织细胞内,其中以蛋清中含量最丰富。
溶菌酶对革兰氏阳性菌有抗菌作用,而对没有细胞壁的动物体细胞不会产生不利影响,因而安全性很高。
口服溶菌酶,可阻止流感和腺病毒繁殖。
作为抗生素的替代品,溶菌酶被WHO和许多国家认定为无毒、无害、安全的应用于食品和饲料添加剂领域,2010年被我国卫生部批准为食品添加剂。
1 溶菌酶的特性溶菌酶,又称胞壁质酶或N-乙酰胞壁质聚糖水解酶,能水解肽聚糖中的N-乙酰葡萄糖和N-乙酰胞壁酸之间的β-1,4糖苷键,以此破坏细菌的细胞壁,具有较强的抑菌抗菌活性。
溶菌酶是一种白色、微白色结晶型或无定型粉末,无臭、味甜且易溶于水,不溶于丙酮和乙醚等有机溶剂,在干燥室温可长期保存。
化学性质非常稳定,对热也极为稳定。
当pH在1.2-11.3范围内剧烈变化时,其结构几乎不变。
在酸性环境中,溶菌酶对热的稳定性很强,在pH4-7范围内,100℃处理1 min仍能保持原酶活性,pH3时能耐100℃加热处理45 min,但在碱性环境中溶菌酶对热稳定性较差。
最适pH为6.6,作用的最适温度为45~50℃,等电点pH10.5-11。
2 溶菌酶的分类2.1 c型溶菌酶, 主要分布在脊椎动物和昆虫中, 大部分虾溶菌酶属于c型,如凡纳滨对虾、日本囊对虾、斑节对虾、罗氏沼虾、日本沼虾的溶菌酶。

摘要:在畜牧养殖中,抗生素不仅作为动物发病时治疗的药物进行使用,还会作为促生长剂添加到动物的饲料中使用,目前全球75%的抗生素都用到了动物的生产养殖中。
持续广泛的滥用抗生素,不仅导致了细菌耐药性的产生,也使得肉食品中抗生素残留加大,威胁到了人类的健康。
因此,为了减少抗生素的过度使用、维护环境的安全性,寻找合适的抗生素替代品变得尤为紧迫和重要。
关键词:溶菌酶;猪;禽;应用溶菌酶在猪、禽上的应用顾振宏1,赵子惠2,蒋东平1(1.甘肃省白银市平川区畜牧兽医技术服务中心甘肃白银730900;2.甘肃省畜牧兽医研究所甘肃平凉744000)收稿日期:2023-03-08基金项目:猪IFN-λ1基因克隆、原核表达及抗PoRV 活性研究(项目编号:21JR7RA718)作者简介:顾振宏(1987.9—),男,本科,兽医师,主要从事动物防疫、检疫工作。
1溶菌酶的概述1.1溶菌酶的渊源溶菌酶是1922年由Fleming 从人的唾液和泪水中发现的一种具有溶解有些细菌作用的物质,因此将其命名为溶菌酶。
溶菌酶是一种单体碱性球蛋白,它的相对分子量为14.4ku ,溶菌酶的肽链包括129个氨基酸残基,其中包含18种氨基酸。
溶菌酶肽链N 末端由第40~88位氨基酸残基构成β-反平行折叠结构,含有4对由含硫氨基酸Cys 构成的二硫键,而C 末端由第1~39位和第89~129位氨基酸残基折叠形成α-螺旋结构。
肽链之间的活性位点是溶菌酶的功能核心,能够识别和水解细菌细胞壁的聚糖,从而发挥溶菌作用[1]。
溶菌酶是一种具有杀菌作用的天然抗感染物质,具有序列保守性和无毒副作用的碱性蛋白。
它广泛存在于人体各种组织、禽类和鸟类蛋清中,以及哺乳动物的泪液、血浆、唾液和乳液等液体中。
此外,微生物中同样含有溶菌酶[2]。
据来源不同可分为以下四类:微生物溶菌酶、植物溶菌酶、动物溶菌酶和蛋清溶菌酶[3]。
目前绝大多数的溶菌酶是从蛋清中提取而来的,经常采用的提取方法是:亲和层析法、离子交换树脂法、聚丙烯酸沉淀法和直接结晶法等。

术语和定义溶菌酶酶活性单位:在25℃、pH值为6.2的条件下,于450nm处每分钟引起溶酶小球菌体(Micrococcus Lysodeiktidus)溶液吸光度下降0.001所需要的酶量为一个酶活性单位U。
本定义适合“比浊法”。
溶菌酶效价:溶菌酶在一定浓度范围内,其对数计量与抑菌圈直径(面积)呈对数关系,通过检测其对微生物的抑制作用,比较标准品与样品产生抑菌圈的大小,计算出样品的效价,单位为u。
本定义适合“管碟法”。
技术要求外观和性状要求粉酶为白色或微黄色的结晶或无定形粉末。
技术指标粉酶水分含量:≤12%。
粉酶粒度:420μm孔径分析筛筛上物≤4%。
粉酶炽灼残渣:≤10.0%。
酶活(效价)指标表1 产品成分分析保证值项目指标粉状50型溶菌酶酶活性(效价),≥U/g(u)500000卫生指标符合GB 13078和NY/T 722的有关规定。
试验方法本标准所用试剂和水,在没有注明其他要求时,均指分析纯试剂和GB/T 6682中规定的三级水,所用试液中的标准溶液,在没有注明其他要求时均要求按GB/T 601,GB/T 602制备。
外观的测定取样品少许放入烧杯,下衬白纸进行目测。
粉酶水分的测定按GB/T 6435 规定进行检测。
粉酶粒度的测定按GB/T 5917 规定进行检测。
粉酶炽灼残渣的测定按《中国兽药典》规定进行检测。
卫生指标的测定按饲料卫生标准GB13078和NY/T 722规定的方法进行。
溶菌酶酶活性(效价)的测定溶菌酶微生物测定法系在适宜条件下,通过检测溶菌酶对微生物的抑制作用,计算出溶菌酶活性(效价)的方法。
依据试验设计原理不同,可分为比浊法和琼脂扩散法(即管碟法)。
试剂和溶液溶酶小球菌(Micrococcus Lysodeiktidus)将溶酶小球菌接种于固体培养基上,置37℃培养48小时,用无菌水将菌体洗下,用纱布滤过,滤液离心后,倾去上层清液,用水洗涤菌体数次,然后用少量水悬浮,冰冻干燥,得淡黄色粉末,供测定用,保存一年。

B46天津奥特奇生物制品有限公司企业产品标准Q/12ATQ 013—2019代替Q/12ATQ 013-2017 混合型饲料添加剂酶制剂2019-03-06发布2019-03-07 实施前言本标准根据GB/T 1.1—2009《标准化工作导则第1部分:标准的结构和编写》的要求进行编写。
本标准的附录A、B、C、D、E为规范性附录。
本标准由天津奥特奇生物制品有限公司提出并起草。
本标准主要起草人:徐素惠、张旭。
本标准所代替标准的历次版本发布情况为:——Q/12ATQ 013-2017。
混合型饲料添加剂酶制剂1 范围本标准规定了混合型饲料添加剂酶制剂的要求、试验方法、检验规则、标签、包装、运输、贮存。
本标准适用于以淀粉酶(产自枯草芽孢杆菌)、β -葡聚糖酶(产自长柄木霉)、纤维素酶(产自长柄木霉)、蛋白酶(产自米曲霉)为主要原料,以轻质碳酸钙、硫酸钙、二氧化硅和啤酒酵母粉为载体经混合、搅拌而成的混合型饲料添加剂酶制剂。
2 规范性引用文件下列文件对于本文件的应用是必不可少的。
凡是注日期的引用文件,仅所注日期的版本适用于本文件。
凡是不注明日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
GB/T 5917.1—2008 饲料粉碎粒度测定两层筛筛分法GB/T 6435—2014 饲料中水分的测定GB 10648 饲料标签GB/T 13079—2006 饲料中总砷的测定GB/T 13080—2004 饲料中铅的测定原子吸收光谱法GB/T 14699.1—2005 饲料采样JJF 1070—2005 定量包装商品净含量计量检验规则国家质量监督检验检疫总局令(2005)第75号《定量包装商品计量监督管理办法》3 要求3.1 感官色泽均匀,无发霉变质、无结块、无异味、无异嗅。
3.2 加工质量指标3.2.1 粉碎粒度产品应全部通过2 mm分析筛,0.6 mm筛上物应不大于10%。
3.2.2 混合均匀度产品应混合均匀,其混合均匀度之变异系数(CV)应不大于5%。
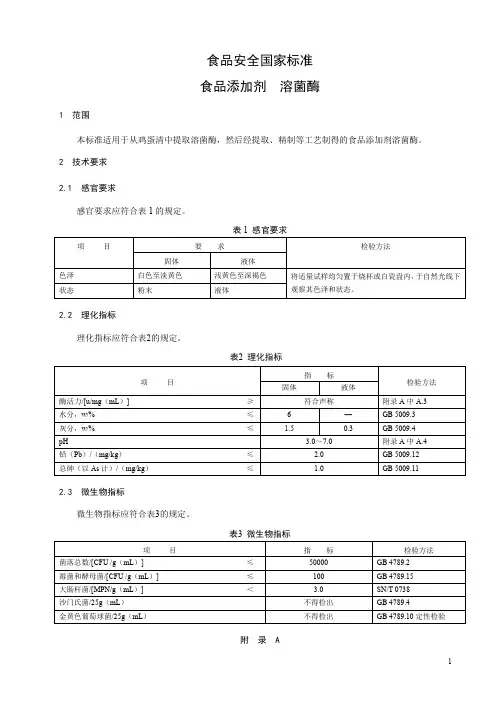
食品安全国家标准 食品添加剂 溶菌酶1 范围本标准适用于从鸡蛋清中提取溶菌酶,然后经提取、精制等工艺制得的食品添加剂溶菌酶。
2 技术要求 2.1 感官要求感官要求应符合表1的规定。
表1 感官要求项 目要 求检验方法固体液体色泽 白色至淡黄色 浅黄色至深褐色 将适量试样均匀置于烧杯或白瓷盘内,于自然光线下观察其色泽和状态。
状态粉末液体2.2 理化指标理化指标应符合表2的规定。
表2 理化指标2.3 微生物指标微生物指标应符合表3的规定。
表3 微生物指标项 目指 标 检验方法菌落总数/[CFU /g (mL )] ≤ 50000 GB 4789.2 霉菌和酵母菌/[CFU /g (mL )] ≤ 100 GB 4789.15 大肠杆菌/[MPN/g (mL )] < 3.0 SN/T 0738 沙门氏菌/25g (mL ) 不得检出 GB 4789.4金黄色葡萄球菌/25g (mL )不得检出GB 4789.10定性检验附 录 A项 目指 标 检验方法固体液体酶活力/[u/mg (mL )] ≥ 符合声称附录A 中A.3 水分,w /% ≤ 6 — GB 5009.3 灰分,w /% ≤ 1.50.3 GB 5009.4 pH3.0~7.0 附录A 中A.4 铅(Pb )/(mg/kg ) ≤ 2.0 GB 5009.12 总砷(以As 计)/(mg/kg )≤1.0 GB 5009.11检验方法A.1 一般规定本标准除另有规定外,所用试剂的纯度应在分析纯以上,所用标准滴定溶液、杂质测定用标准溶液、制剂及制品,应按GB/T 601、GB/T 602、GB/T 603的规定制备,实验用水应符合GB/T 6682中三级水的规定。
试验中所用溶液在未注明用何种溶剂配制时,均指水溶液。
A.2 鉴别试验0.01%醋酸盐缓冲溶液(pH 5.4)于279 nm~281 nm处有最大吸收。
A.3 酶活力的测定A.3.1 方法原理溶菌酶可水解细菌的细胞壁,造成溶壁微球菌的溶解而引起溶液吸光度值的降低。
Q/JBSW 江西嘉博生物工程有限公司企业标准
Q/JBSW045-2019混合型饲料添加剂液态溶菌酶
2019-09-01发布2019-09-10实施
Q/JBSW045-2019
前言
本标准起草单位:江西嘉博生物工程有限公司。
本标准主要起草人:周志、李成龙。
本标准为首次发布。
混合型饲料添加剂液态溶菌酶
1范围
本标准规定了混合型饲料添加剂液态溶菌酶的原料要求、技术要求、试验方法、检验规则、标签、包装、运输和贮存。
本标准适用于以饲料添加剂溶菌酶按一定比例溶于纯化水中,制成的混合型饲料添加剂液态溶菌酶。
2规范性引用文件
下列文件对于本文件的应用是必不可少的。
凡是注日期的引用文件,仅注日期的版本适用于本文件。
凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
GB/T9724化学试剂pH值测定通则
GB10648饲料标签
GB/T13079饲料中总砷的测定
GB/T13080饲料中铅的测定原子吸收光谱法
GB/T13091饲料中沙门氏菌的检测方法
GB/T13092饲料中霉菌总数测定方法
GB/T17480饲料中黄曲霉毒素B1的测定酶联免疫吸附法
GB/T18823饲料检测结果判定的允许误差
GB/T14699.1饲料采样
GB/T20195动物饲料试样的制备
中华人民共和国国家质量监督检验检疫总局令(2005)第75号《定量包装商品计量监督管理办法》中华人民共和国农业部公告第1773号《饲料原料目录》
中华人民共和国农业部公告第1849号《混合型饲料添加剂生产企业许可条件》
中华人民共和国农业部公告第2045号《饲料添加剂品种目录(2013)》
3原料要求
生产产品所用原料应符合《饲料原料目录》的规定,所用添加物应符合《饲料添加剂品种目录(2013)》的规定,严禁使用国家明令禁止的添加物和化学制品。
4技术要求
4.1感官
液态,色泽一致,久置有少量沉淀,无发霉变质及异味、异嗅。
4.2pH值
pH值应为3.0~7.0。
4.3卫生指标
总砷不大于10mg/L,铅不大于20mg/L,霉菌总数不大于4.0×104cfu/ml,黄曲霉毒素B1不大于10ug/L,沙门氏菌不得检出。
4.4主要营养成分
表1
产品名称
混合型饲料添加剂液态溶菌酶
Ⅰ型Ⅱ型Ⅲ型Ⅳ型
溶菌酶,u/ml≥100≥500≥1000≥2000 5试验方法
5.1感官
取适量样品,在非阳光直射条件下,观其色泽、形态,嗅其气味。
5.2pH值
pH值的测定按GB/T9724执行。
5.3溶菌酶
溶菌酶的测定按附录A执行。
5.4总砷
总砷的测定按GB/T13079执行。
5.5铅
铅的测定按GB/T13080执行。
5.6霉菌总数
霉菌总数的测定按GB/T13092执行。
5.7沙门氏菌
沙门氏菌的测定按GB/T13091执行。
5.8黄曲霉毒素B1
黄曲霉毒素B1的测定按GB/T17480执行。
6检验规则
6.1批次
以同批原料、同一配方、相同设备的每日生产量为一个批次。
6.2采样
按GB/T14699.1执行。
6.3检验
6.3.1出厂检验
出厂产品由本公司质检部门负责检验,检验项目为感官、pH值和溶菌酶。
产品检验合格后方可出厂,每批出厂产品应附有质量检验合格证(章)和使用说明。
6.3.2型式检验
型式检验为全项目检验,每年不得少于一次。
如有下列情况之一时,应进行型式检验:
a)主要原、辅材料,配方,生产工艺或设备发生较大改变时;
b)停产半年以上再恢复生产时;
c)出厂检验结果与上次型式检验结果有较大差异时;
d)国家有关部门监督检验与抽查时。
6.4判定规则
检测结果判定的允许误差按GB/T18823执行。
6.5复检规则
产品在检验中如有一项指标不符合本标准时,应重新加倍抽样进行复检。
复检结果中仍有一项指标不符合本标准时,则该批产品判为不合格品。
7标签、包装、运输和贮存
7.1标签
按GB10648执行。
7.2包装
包装物采用无毒、无害,对产品质量无影响的材料。
包装规格(净含量)为:100ml、200ml、500ml、1L、2L、5L、10L,也可根据用户提出的净含量要求进行包装。
包装净含量允许误差应符合《定量包装商品计量监督管理办法》的规定。
7.3运输
产品在运输过程中应防止日晒雨淋、包装破损,严禁与有毒、有害物质混运。
7.4贮存
产品应贮存于阴凉、通风、干燥处,严禁与有毒、有害物质混贮。
在上述条件下,自生产之日起,产品保质期为8个月。
附录A
(规范性附录)
溶菌酶活力的测定
A.1原理
在一定浓度的浑浊溶液中,溶菌酶可以水解细菌细胞壁上的肽聚糖,从而使细菌裂解而浓度降低,透光度增强,因此可以根据其透光度的变化来测定溶菌酶的含量。
A.2试剂和材料
除非另有说明,在分析中仅使用确认为分析纯的试剂;蒸馏水或去离子水或符合GB/T6682中规定的三级水或相当纯度的水。
试验中所用试剂、制品,均按GB/T603的规定制备。
A.3仪器和设备
A.3.1移液枪:精度为5ul,量程为50~1000ul。
A.3.2分析天平:感量0.0001g
A.3.3酸度计
A.3.4匀浆器
A.3.5紫外可见分光光度
A.3.6恒温水浴锅
A.3.7涡旋混合器
A.4分析步骤
A.4.1底物的制备
菌种为溶菌小球菌,将其接种与营养琼脂培养基上,置35℃±2℃培养48小时,用生理盐水将菌体洗下,用纱布滤过,滤液离心后,倾去上层清夜,再加生理盐水适量,如此反复洗涤菌体数次,取下层沉淀,供测定用;或者将洗涤后的菌体用少量水悬浮,冰冻干燥,得淡黄色粉末,供测定用,可保存一年。
或直接购买成品。
A.4.2试样溶液的制备
精密称取式样适量(约相当于溶菌酶活力125000IU),置100ml量瓶中,加磷酸盐缓冲液溶解并稀释至刻度,摇匀;精密量取5ml置25ml量瓶中,用磷酸盐缓冲液稀释至刻度,摇匀,即得。
A.4.3底物悬浮液的制备
另外称取底物(即菌体)5-15mg,加磷酸盐缓冲液4-5ml,在匀浆器内研磨5分钟,倾出,用磷酸盐缓冲液稀释到适当体积,使悬浮液在25℃±0.1℃时,用磷酸盐缓冲液调零,用分光光度法,在450nm 波长处测定吸收度为0.65-0.75时(临用前配制),进行酶活力测定。
A.4.4测定
精密量取25℃±0.1℃底物悬浮液3ml,放入比色皿中,用分光光度法,在450nm 波长处测定吸收度,作为零时读数,然后量取25℃±0.1℃时的试样0.15ml 溶液,加入上述比色皿中,迅速混合,用秒表计算时间,至60秒时在测定吸收度;同时精密量取磷酸盐缓冲液0.15ml,同法操作,作为空白试验,测得零秒的读数及60秒的读数。
A.4.5结果计算
用于酶解反应的稀释酶液中溶菌酶活力按(A.1)计算;
(A 0-A)-(a 0-a)
X=
————-—--—×103
M
式中:
X:式样中的溶菌酶的活力的,单位为每毫克(u/mg)
A 0:试样零时吸收度;A:试样60秒时吸收度;a 0:空白零时吸收度;a :空白60秒时吸收度;
M :测定液中试样的重量,单位为毫克(mg)
103:转化因子。
每个试样取两个平行样进行测定,以其算平均值为结果,结果保留整数。
A.4.6重复性
同一试样两个平行测定值的相对偏差,不超过10%。