乙烯的性质及加成反应
- 格式:ppt
- 大小:439.00 KB
- 文档页数:10

乙烯(不饱和烃)⑴ 分子结构特点分子式:C 2H 4 结构简式:CH 2=CH 2 结构式:⑵ 物理性质:无色、稍有气味的气体,标准状况下密度为1.25g·L -1,比空气略轻,难溶于水。
⑶ 化学性质:易氧化、易加成(加聚)、易分解 ① 氧化反应ⅰ与酸性高锰酸钾反应(特征反应)现象:酸性高锰酸钾溶液褪色。
(乙烯被酸性高锰酸钾氧化成CO 2)ⅱ 可燃性:现象:火焰明亮,伴有黑烟。
② 加成反应:CH 2=CH 2+Br 2CH 2Br ―CH 2Br (1,2—二溴乙烷)加成反应:有机物分子中双键(或三键)两端的碳原子与其他原子或原子团直接结合生成新的化合物的反应叫做加成反应。
被加成的试剂如:H 2、X 2(X 为Cl 、Br 或I)、H 2O 、HX 、HCN 等能离解成一价原子或原子团的物质。
通过有机物发生加成反应时反应物之间的量关系,还可定量判断该有机物分子结构中不饱和键的情况:是C =C 键,还是C≡C 键,或是苯环结构,以及它们的个数。
能与Cl 2、H 2 、HX 、H 2O 的加成:CH 2=CH 2+Cl 2CH 2Cl ―CH 2Cl③ 加聚反应CH 2=CH 2+CH 2=CH 2+CH 2=CH 2+···催化剂[―CH 2―CH 2―+―CH 2―CH 2―+―CH 2―CH 2―+···]→[―CH 2―CH 2―CH 2―CH 2―CH 2―CH 2―···]→ⅰ 加聚反应:在聚合反应中,由不饱和(即含碳碳双键或三键)的相对分子质量小的化合物分子通过加成聚合的形式结合成相对分子质量很大的高分子化合物的反应。
ⅱ 聚合反应:相对分子质量小的化合物分子互相结合成相对分子质量很大的高分子化合物的反应。
ⅲ 高分子化合物:相对分子质量很大(1万以上)的物质,简称高分子或高聚物。
聚乙烯,塑料,分子量达几万到几十万,性质坚韧,化学性质稳定,难降解。

乙烯和氢气加成反应条件乙烯和氢气加成反应是一种重要的化学反应,用于生产乙烯的重要原料乙烷。
下面将介绍乙烯和氢气加成反应的条件。
1. 反应物:乙烯(化学式C2H4)和氢气(化学式H2)是乙烯和氢气加成反应的两种重要反应物。
乙烯是一种带有双键的不饱和碳氢化合物,是乙烷的同分异构体。
氢气是一种常见的气体,在化学反应中常用作还原剂。
2. 催化剂:在乙烯和氢气加成反应中,通常需要使用催化剂来促进反应的进行。
常用的催化剂包括铂(Pt)、钯(Pd)、镍(Ni)等。
这些催化剂能够降低乙烯和氢气之间的活化能,提高反应速率。
3. 温度:温度是乙烯和氢气加成反应的一个重要条件。
一般来说,较高的反应温度可以提高反应速率,但是过高的温度可能导致副反应的发生。
乙烯和氢气加成反应的适宜温度范围一般在100-200摄氏度之间。
4. 压力:压力是乙烯和氢气加成反应的另一个关键条件。
在反应过程中,较高的压力可以增加气相的反应物的浓度,从而促进反应的进行。
一般来说,在反应开始时,可以使用较高的压力,然后随着反应的进行逐渐减小压力。
5. 反应时间:乙烯和氢气加成反应的反应时间取决于反应条件和所需的产物。
一般来说,较高的温度和压力可以缩短反应时间,但需要控制反应时间,以获得所需的产物。
6. 反应器:乙烯和氢气加成反应可以在不同类型的反应器中进行,包括批量反应器、连续流动反应器等。
反应器的选择取决于反应条件和需求。
综上所述,乙烯和氢气加成反应的条件包括乙烯和氢气作为反应物、适当的催化剂、适宜的温度和压力、适当的反应时间和适当的反应器。
这些条件的选择将直接影响到乙烯和氢气加成反应的效率和产物的选择。
因此,在实际生产过程中,需要仔细控制这些条件,以获得理想的反应结果。

从乙烯的结构式可以看出,乙烯分子里含有C=C双键,链烃分子里含有碳碳双键的不饱和烃叫做烯烃。
乙烯是分子组成最简单的烯烃。
乙烯分子的空间构型为了更简单形象地描述乙烯分子的结构,我们常用分子模型来表示(如下图)。
在下图中,I 的球棍模型里,两个碳原子间用两根可以弯曲的弹性短棍来连接,用它们来表示双键。
在下图中,II 是乙烯分子的比例模型。
乙烯分子的模型实验表明,乙烯分子里的C=C双键的键长是 1.33×10-10m,乙烯分子里的两个碳原子和四个氢原子都处在同一平面上。
它们彼此之间的键角约为120°。
乙烯双键的键能是615kJ/mol,实验测得乙烷C-C单键的键长是1.54×10-10m,键能是348kJ/mol。
这表明C=C双键的键能并不是C-C单键键能的两倍,而是比两倍略少。
因此,只需要较少的能量,就能使双键里的一个键断裂。
这从下面介绍的乙烯的化学性质是可以得到证实。
制取乙烯的原理工业上所用的乙烯,主要是从石油炼制工厂和石油化工厂所生产的气体里分离出来的。
实验室里是把酒精和浓硫酸混合加热,使酒精分解制得。
浓硫酸在反应过程里起催化剂和脱水剂的作用。
制取乙烯的反应属于液——液加热型乙烯能使酸性KMnO4溶液很快褪色,这是乙烯被高锰酸钾氧化的结果,而甲烷等烷烃却没有这种性质。
乙烯的化学性质——加成反应把乙烯通入盛溴水的试管里,可以观察到溴水的红棕色很快消失。
乙烯能跟溴水里的溴起反应,生成无色的1,2-二溴乙烷(CH2Br-CH2Br)液体。
这个反应的实质是乙烯分子里的双键里的一个键易于断裂,两个溴原子分别加在两个价键不饱和的碳原子上,生成了二溴乙烷。
这种有机物分子里不饱和碳原子跟其它原子或原子团直接结合生成别的物质的反应叫做加成反应。
乙烯还能跟氢气、氯气、卤化氢以及水等在适宜的反应条件下起加成反应。
乙烯的化学性质——氧化反应点燃纯净的乙烯,它能在空气里燃烧,有明亮的火焰,同时发出黑烟。

乙烯的性质一、物理性质通常情况下,乙烯是一种无色稍有气味的气体,密度为1.25g/L,比空气的密度略小,难溶于水,易溶于四氯化碳等有机溶剂。
世界上已将乙烯产量作为衡量一个国家石油化工发展水平的重要标志之一。
二、化学性质①常温下极易被氧化剂氧化。
如将乙烯通入酸性KMnO4溶液,溶液的紫色褪去,乙烯被氧化为二氧化碳,由此可用鉴别乙烯。
②易燃烧,并放出热量,燃烧时火焰明亮,并产生黑烟。
CH2═CH2+3O2→2CO2+2H2O③烯烃臭氧化:CH2=CH2+O3,在锌保护下水解→2HCHO2CH2=CH2+O2—Ag、加热,酸性水解→2CH3—CHO加成反应:CH2═CH2+Br2→CH2Br—CH2Br(常温下使溴水褪色)CH2═CH2+HCl—催化剂、加热→CH3—CH2Cl(制氯乙烷)CH2═CH2+水—催化剂、170℃→CH3CH2OH(制酒精)CH2═CH2+H2—Ni或Pd,加热→CH3CH3CH2═CH2+Cl2→CH2Cl—CH2Cl加成反应:有机物分子中双键(或三键)两端的碳原子与其他原子或原子团直接结合生成新的化合物的反应。
加聚反应:nCH2═CH2→-(CH2—CH2)- n (制聚乙烯)三、制取酒精硫酸一比三,催化脱水是硫酸。
温度速至一百七,不生乙醚生乙烯。
反应液体呈黑色,酒精炭化硫酸致。
为防暴沸加碎瓷,排水方法集乙烯。
苯的性质一、物理性质常温下为一种无色、有甜味的透明液体,并具有强烈的芳香气味。
苯可燃,有毒,也是一种致癌物质。
苯是一种碳氢化合物也是最简单的芳烃。
它难溶于水,易溶于有机溶剂,本身也可作为有机溶剂。
苯是一种石油化工基本原料。
结构平面正六边形。
溶解性:不溶于水,可与乙醇、乙醚、乙酸、汽油、丙酮、四氯化碳和二硫化碳等有机溶剂互溶。
二、化学性质苯参加的化学反应大致有3种:一种是其他基团和苯环上的氢原子之间发生的取代反应;一种是发生在苯环上的加成反应(注:苯环无碳碳双键,而是一种介于单键与双键的独特的键);一种是普遍的燃烧(氧化反应)(不能使酸性高锰酸钾褪色)。

第二节 乙烯与有机高分子材料人非圣贤,孰能无过?过而能改,善莫大焉。
《左传》大地二中 张清泉第1课时 乙烯[核心素养发展目标] 1.掌握乙烯的组成及结构特点,体会结构决定性质的观念,增强“宏观辨识与微观探析”的能力。
2.掌握乙烯的化学性质,认识加成反应的特点,培养“证据推理与模型认知”能力。
3.了解乙烯在生产及生活中的应用,培养“科学态度与社会责任”。
(一)乙烯的分子组成与结构(二)乙烯的性质1.乙烯的物理性质2.乙烯的化学性质(1)氧化反应①燃烧:现象:火焰明亮,伴有黑烟。
化学方程式:C2H4+3O2――→点燃2CO2+2H2O 。
②和酸性KMnO4溶液反应现象:酸性KMnO4溶液褪色。
结论:乙烯能被酸性KMnO4溶液氧化。
(2)加成反应①将乙烯通入溴的四氯化碳溶液中现象:溴的四氯化碳溶液褪色。
化学方程式:。
②加成反应定义:有机物分子中的不饱和碳原子与其他原子或原子团直接结合生新的化合物的反应。
书写下列加成反应的化学方程式:(3)聚合反应①定义:由相对分子质量小的化合物分子互相结合成相对分子质量大的聚合物的反应。
②乙烯自身加成生成聚乙烯的方程式:该反应是聚合反应,同时也是加成反应,这样的反应又被称为加成聚合反应,简称加反应。
其中,—CH2—CH2—称为链节,n称为聚合度,小分子乙烯称为聚乙烯的单体。
(三)乙烯的用途1.乙烯是重要的化工原料,在一定条件下用来制聚乙烯塑料、聚乙烯纤维、乙醇等。
乙烯的产量可以用来衡量一个国家的石油化工发展水平。
2.在业生产中用作植物生长调节剂。
(1)乙烯的结构简式可书写为CH2CH2( ×)提示乙烯分子中含有,在书写时,官能团不能省略,应为CH2==CH2。
(2)乙烯是一种无色无味,易溶于水的气体( ×)提示乙是一种稍有气味,难溶水的气体。
(3)乙的化学性质比乙烷活泼( √)(4)乙烯能使酸性KMnO4溶液和溴水褪色,反应原理相同( × )提示 乙烯使酸性KMnO4溶液褪色发生的是氧化反应,乙烯使溴水褪色发生的为加成反应。

乙烯加成反应的教案篇一:乙烯的教案第二节乙烯一、教学设计1、知道乙烯分子的组成和结构特点2、掌握乙烯的典型化学性质,掌握加成反应3、了解乙烯的用途二、教学重、难点重点:乙烯的化学性质难点:乙烯的分子结构和加成反应三、教学过程【导入新课】我们常说煤是工业的粮食,石油是工业的血液,从煤和石油不仅可以得到多种常用燃料,而且可以从中获取大量的基本化工原料。
那么从煤和石油中都能获得哪些重要的化工原料呢?【板书】第二节来自石油和煤的两种基本化工原料――乙烯【过渡】到底乙烯是怎样的物质呢?能否从石油中得到乙烯?从石油分馏中得到的石蜡油进一步加热会得到什么呢?【探究实验】投影教材P67石蜡油的分解实验,将分解产生的气体通入溴水、高锰酸钾溶液、并点燃气体,分别观察现象。
【观察与思考】观看视频并思考:1、实验中看到哪些现象?2、石蜡油分解实验中生成的物质与甲烷的性质比较有什么异同?3、由以上实验我们可以得出什么结论?【归纳】石蜡油分解得到的产物中含有与烷烃性质不同的烃——烯烃【学与问】投影乙烯的球棍模型和比例模型,写出乙烯分子的电子式和结构式和结构简式。
【板书】一、乙烯的分子组成和结构分子式:C2H4,电子式:结构式:结构简式:CH2=CH2【思考与交流】乙烯分子的空间结构有什么特点?学生讨论后回答,由教师补充【归纳】乙烯分子的空间结构的特点:1、碳原子之间以双键结合,其中一根键不稳定。
2、原子之间的夹角均为120°。
3、乙烯分子为平面型结构,所有原子都在同一平面内。
【板书】乙烯分子的空间结构的特点:平面型结构,所有原子都在同一平面内。
【教师】乙烯有哪些物理性质呢?【投影】乙烯的物理性质:无色,稍有气味的气体,难溶于水(排水法收集)【板书】二、乙烯的物理性质【过渡】由于乙烯分子中存在碳碳双键,所以乙烯表现出较活泼的化学性质。
那么乙烯都能发生哪些反应呢?【讲解】在探究实验中体现了乙烯的氧化反应【板书】三、化学性质1、氧化反应:(1)乙烯使酸性高锰酸钾溶液褪色(2)燃烧:C2H4+3O22CO2+2H2O现象:明亮的火焰并伴有黑烟,同时放出大量的热。
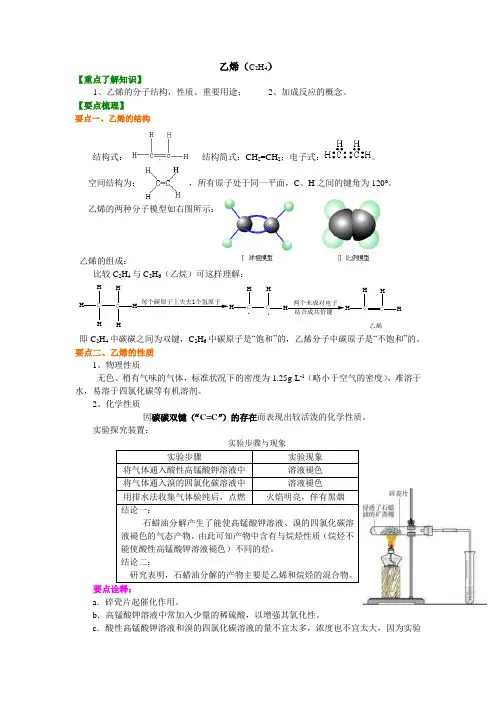
乙烯(C 2H 4)【重点了解知识】1、乙烯的分子结构,性质、重要用途;2、加成反应的概念。
【要点梳理】要点一、乙烯的结构结构式: , 结构简式:CH 2=CH 2;电子式:。
空间结构为: ,所有原子处于同一平面,C 、H 之间的键角为120°。
乙烯的两种分子模型如右图所示:乙烯的组成:比较C 2H 4与C 2H 6(乙烷)可这样理解:C HH HC HH H每个碳原子上失去1个氢原子HH CH .两个未成对电子CHHC HH 乙烯.即C 2H 4中碳碳之间为双键,C 2H 6中碳原子是“饱和”的,乙烯分子中碳原子是“不饱和”的。
要点二、乙烯的性质 1、物理性质无色、稍有气味的气体,标准状况下的密度为1.25g·L -1(略小于空气的密度),难溶于水,易溶于四氯化碳等有机溶剂。
2、化学性质因碳碳双键(“C=C ”)的存在而表现出较活泼的化学性质。
实验探究装置:实验步骤与现象要点诠释:a .碎瓷片起催化作用。
b .高锰酸钾溶液中常加入少量的稀硫酸,以增强其氧化性。
c .酸性高锰酸钾溶液和溴的四氯化碳溶液的量不宜太多,浓度也不宜太大,因为实验中乙烯量不大。
d .酸性高锰酸钾、溴的四氯化碳溶液能检验乙烯等不饱和烃。
(1)氧化反应①乙烯被酸性高锰酸钾溶液氧化——使酸性高锰酸钾溶液褪色启示:利用此性质可鉴别CH 4和C 2H 4,但不能除去CH 4中的C 2H 4,原因是:5CH 2=CH 2+12KMnO 4+18H 2SO 410CO 2↑+6K 2SO 4+12MnSO 4+28H 2O 产物中有CO 2↑,仍混在甲烷中,达不到除杂的目的。
②乙烯的燃烧在空气中燃烧,现象:火焰明亮并伴有黑烟,同时放出大量的热。
C 2H 4 + 3O22CO 2 +2H 2O重点提示:a . 产生黑烟:乙烯分子中含碳量较高,燃烧时部分碳并没有完全被氧化,而导致多余的碳析出。
以黑烟的形式冒出。
碳粒本身被烧成炽热的状态,所以乙烯的火焰很明亮,没有被氧化的碳呈游离态 b .乙烯属于易燃易爆的气体,点燃前一定要先验纯。


乙烯中碳原子的空间构型乙烯是一种重要的有机化合物,其分子式为C2H4。
乙烯分子由两个碳原子和四个氢原子组成,碳原子的空间构型对于乙烯的性质和反应起着重要的影响。
乙烯中的碳原子呈现出一种特殊的空间构型,被称为sp2杂化。
这种杂化形式使得碳原子的电子云排列成平面三角形的形状。
乙烯中的两个碳原子之间通过一个共用电子对形成了一个σ键,而每个碳原子上还有一个未配对的p轨道上的电子,它们垂直于乙烯分子的平面。
乙烯中碳原子的空间构型决定了乙烯的性质。
首先,由于碳原子的sp2杂化形态,乙烯分子具有平面结构,这使得乙烯具有比较高的平面刚性。
这种刚性使得乙烯的π键能够更容易地形成和破裂,从而参与各种化学反应。
乙烯中碳原子的空间构型使得乙烯分子呈现出共轭结构。
共轭结构导致乙烯分子中的π电子云得到了扩展,使得乙烯具有较低的能量。
这也是乙烯具有稳定性较高的原因之一。
乙烯中碳原子的空间构型还决定了乙烯的立体异构体。
由于碳原子的sp2杂化形态,乙烯分子中两个碳原子之间的π键可以自由旋转。
这导致乙烯存在两种立体异构体,分别称为顺式乙烯和反式乙烯。
顺式乙烯中两个氢原子位于同一侧,而反式乙烯中两个氢原子位于相对的侧面。
乙烯的空间构型对于其反应也具有重要影响。
由于乙烯中碳原子的sp2杂化形态,使得乙烯分子具有较高的反应性。
乙烯可以进行加成反应、聚合反应等多种反应。
在加成反应中,乙烯的π键可以被其他物质攻击,形成新的化学键。
在聚合反应中,乙烯分子可以通过π键进行连接,形成高分子化合物。
乙烯中碳原子的空间构型对于乙烯的性质、反应和立体异构体具有重要影响。
通过了解乙烯分子中碳原子的空间构型,我们可以更好地理解乙烯的化学性质和反应机理,为乙烯的应用和研究提供更多的理论基础。

乙烯的制取和性质实验乙烯在石油化工等行业是一个极为重要的试剂。
它可以进行多种类型的反应,从而制出化工产品。
例如生活中塑料类物品:盛放食品的保鲜膜,有机玻璃,快餐盒等等都是以乙烯为原料制成的。
乙烯还是一种植物激素,可以用作水果和蔬菜的催熟剂。
【目的】那么在实验室里该怎样制取乙烯呢?好,下面,我们来看一下今天的实验目的,主要有两点:第一,掌握乙烯的实验室制法和性质实验操作技能;第二,联系上次甲烷的实验,了解饱和烃和不饱和烃的共性和特性。
【内容】1、乙烯的制取2、乙烯的性质:加成反应——直接将乙烯气体通入溴水里,观察溴水颜色变化。
氧化反应——直接通入被酸化的高锰酸钾溶液中,观察溶液颜色变化;直接点燃【原理】实验室制取乙烯是实验室里是将无水乙醇和浓硫酸按1:3混合迅速加热到170℃,乙醇发生分子内脱水生成乙烯。
乙醇与浓硫酸反应,首先生成硫酸氢乙酯。
硫酸氢乙酯在170℃分解,放出乙烯。
生成硫酸氢乙酯的反应是一个可逆反应,为了使反应向生成酯的方向移动,并使乙醇的利用率有所提高,常增加硫酸的用量,一般硫酸与乙醇的用量酯1:3。
在140度以下乙醇会大量挥发,140到160度之间乙醇会发生分子间脱水生成醚。
超过180度,会因温度过高,导致浓硫酸使酒精迅速脱水碳化,并将碳氧化生成二氧化碳,同时浓硫酸被还原成二氧化硫气体,不利于乙烯的生成。
发生很多副反应,生成的乙烯中含有乙醇、乙醚、二氧化碳、一氧化碳、二氧化硫、水蒸气等杂质气体。
我们知道二氧化硫和乙醚等回污染环境,并且二氧化硫具有还原性,能使溴水褪色。
【装置】从上面的实验原理可以看出,制取乙烯的反应属于液液加热型,我们会用到一种新的仪器—带支管的蒸馏烧瓶,大家要注意了,不能直接对烧瓶加热,所以在加热过程中要使用石棉网,下面我们来看一下实验装置图。
必须立即升温到170度,由于我们没有电热套,公共台上有脱脂棉,大家可以用脱脂棉沾一点酒精,放在酒精灯上加热,使温度立即上升到170度,不过大家要小心点。

乙烯相关知识点总结一、乙烯的化学性质1. 物理性质乙烯是一种无色、有刺激性气味的气体,在常温常压下,密度比空气小,易燃易爆。
它可以溶解于乙腈、乙酮、四氯化碳等有机溶剂中,但不溶于水。
此外,乙烯在高温下可以被氧气氧化,生成二氧化碳和水。
乙烯是一种具有较活泼化学性质的烃类物质,它可以和卤素、水、酸等发生化学反应。
2. 化学性质(1)乙烯的卤素化反应乙烯和氯气、溴气或碘气反应,可以生成相应的卤代乙烷。
例如,乙烯和氯气反应可以生成氯乙烷:C2H4 + Cl2 → C2H5Cl(2)乙烯的加成反应乙烯可以和卤素化合物、酸化合物等进行加成反应,生成相应的饱和化合物。
例如,乙烯和溴水反应可以生成1,2-二溴乙烷:C2H4 + Br2 → C2H4Br2(3)乙烯的氧化反应乙烯在空气中或氧气中高温燃烧,会生成二氧化碳和水:C2H4 + 3O2 → 2CO2 + 2H2O(4)乙烯的聚合反应在特定的催化剂存在下,乙烯可以进行聚合反应,生成聚乙烯。
这种反应是乙烯应用最广泛的领域之一,也是乙烯化工产业的重要部分。
二、乙烯的生产工艺乙烯的生产工艺主要有以下几种:1. 石油裂化石油裂化是乙烯的主要生产方式之一。
它通过在高温、高压等条件下,将石油馏分或液化气体经裂化反应产生乙烯。
这种方法可以获得较高纯度的乙烯,但成本较高。
2. 乙烷蒸汽裂解在乙烷蒸汽裂解反应中,利用高温和催化剂的作用,将乙烷分解成乙烯和氢气。
这种生产方式操作简单,且成本较低,因此被广泛应用。
3. 轻质烃催化裂化轻质烃(如原油污泥油气等)催化裂化方法也是一种常见的乙烯生产方式。
通过在催化剂存在下,将轻质烃进行裂解反应,生成乙烯等产品。
4. 乙醇水热裂解利用高温、高压和催化剂的作用,将乙醇进行水热裂解反应,也可以获得乙烯。
这种方法产物中有少量未反应的乙醇存在。
5. 天然气液化工艺将天然气中的乙烷分选出来,并通过乙烷蒸汽裂解的方式,生产乙烯。
三、乙烯的应用领域乙烯作为一种重要的化工原料,应用领域非常广泛。
乙烯的性质和用途乙烯是一种无色、无味的气体,化学式为C2H4,相对分子质量为28.05、以下是关于乙烯的性质和用途的详细介绍:乙烯的物理性质:1.熔点和沸点:乙烯的熔点为-169.4°C,沸点为-103.9°C。
2. 密度:乙烯的密度为0.879 g/cm33.溶解性:乙烯在水中几乎不溶,但可以溶于有机溶剂如醚、醇、酮等。
4.稳定性:乙烯具有较高的化学稳定性,不易燃烧,但在高温和高压条件下会发生自发性聚合反应。
乙烯的化学性质:1.氧化反应:乙烯可以与氧气发生燃烧反应,生成二氧化碳和水。
2.加成反应:乙烯是一种典型的亲电试剂,在反应中与其他化合物发生加成反应,如和卤代烷反应生成烷烃,和水反应生成乙醇等。
3.聚合反应:乙烯是一种重要的单体,可以发生聚合反应生成聚乙烯,这是一种常用的塑料材料。
乙烯的用途:1.聚乙烯的制备:乙烯是聚乙烯的主要原料。
通过高温、高压催化剂的作用,乙烯通过聚合反应可以制备聚乙烯。
聚乙烯是一种重要的塑料材料,具有良好的化学稳定性、电绝缘性能和低温耐性,广泛用于包装、建筑、电子、汽车等行业。
2.乙烯的制醇:乙烯可以通过加水反应生成乙醇。
乙醇是一种重要的有机溶剂,广泛用于化工、制药、冶金等领域。
3.乙烯的制醛:乙烯通过氧化反应可以生成乙醛。
乙醛是一种常用的有机合成原料,广泛用于制造树脂、染料、药品等。
4.乙烯的制酯:乙烯可以与酸酐反应生成相应的酯。
乙烯酯是一种重要的溶剂和涂料原料,在化工、油漆、印刷等领域中有广泛的应用。
5.乙烯的制橡胶:乙烯可以通过聚合反应制备乙烯橡胶。
乙烯橡胶具有高强度、耐磨性好等特点,广泛用于轮胎、密封件、管道等领域。
6.乙烯的催化裂化:乙烯可以通过催化裂化反应在高温下分解成其他有机化合物,如乙苯、丙烯等。
这些有机化合物是许多化工产品的重要原料。
7.乙烯的用于水果成熟:乙烯可以作为植物生长激素,促进水果的成熟和脱落。
总结:乙烯是一种重要的化工原料,具有广泛的用途。
乙烯知识点归纳总结一、乙烯的分子结构乙烯是一种无色、易燃、具有强烈气味的有机化合物,分子式为C2H4。
其结构式为H2C=CH2,乙烯分子是由两个碳原子和四个氢原子组成的,其中碳原子以双键连接,这是乙烯最重要的结构特征。
二、乙烯的物理性质乙烯是一种透明、无味的气体,具有强烈的刺激性。
其密度为0.925g/L,比空气轻。
在标准压力下,乙烯的沸点为-103.7℃,熔点为-100.6℃。
乙烯的溶解性较好,可以溶解在有机溶剂中。
三、乙烯的化学性质1、氧化反应:乙烯与氧气反应,生成环氧乙烷和水。
2、加成反应:乙烯与氢气反应,生成乙烷;与卤素单质反应,生成卤代烷;与水反应,生成乙醇。
3、聚合反应:乙烯在一定条件下可以聚合成高分子化合物。
4、裂解反应:在热和催化剂的作用下,乙烯发生裂解反应,生成小分子烯烃。
四、乙烯的制备主要通过石油裂解和天然气转化两种方法制备乙烯。
石油裂解是将石油中的长链烃断裂成乙烯的过程;天然气转化是将天然气转化为合成气,再进一步转化为乙烯的过程。
五、乙烯的应用1、制造聚合物:乙烯在聚合反应中生成高分子化合物,广泛用于制造塑料、纤维、橡胶等产品。
2、制造有机溶剂:乙烯与水反应生成乙醇,乙醇是一种良好的有机溶剂,可用于制造涂料、油漆等产品。
3、农业用途:乙烯是一种植物生长调节剂,可以促进植物生长和开花。
4、其他用途:乙烯还可用于制造乙醛、乙基胺等化学物质,以及用作制冷剂等。
六、乙烯的安全措施由于乙烯易燃、易爆,因此在处理和储存时应采取以下安全措施:1、储存于阴凉、通风的库房中,远离火源和热源。
2、避免与氧化剂、酸类物质混存。
3、使用防爆电气设备,并定期检查电线绝缘层是否完好。
4、使用前必须对设备进行彻底清洗和干燥,避免产生静电火花。
因式分解知识点归纳总结因式分解是数学中的一种重要技巧,它可以帮助我们简化计算,解决实际问题,并且还在数学竞赛中占有重要的地位。
因式分解就是把一个多项式分解为几个整式乘积的形式,它是一种重要的数学思维方法。
乙烯,也称乙烯烷、乙烯基,是一种重要的有机化学品和工业原料,广泛应用于塑料、橡胶、涂料、溶剂、纤维等领域。
本文将从多个角度来介绍乙烯的工业生产流程原理和应用趋势。
一、乙烯的化学性质乙烯的化学式为C2H4,为无色、无臭、易燃、难溶于水的气体。
乙烯分子是一条双键链,具有高度稳定的环境中相对较高的反应活性。
乙烯分子在高温下可以与其他分子发生加成反应,并可以与空气中的氧气发生燃烧反应。
乙烯还可以发生聚合反应,生成聚乙烯等大分子化合物。
二、乙烯的生产流程原理乙烯的生产工艺主要有三种方法:石油法、煤炭法和天然气法。
其中,石油法是目前最为常用的乙烯生产方法。
1.石油法石油法是利用石油裂化产生的裂解气体(轻烃)来生产乙烯的方法。
具体流程如下:(1)原料准备:将石油经过加热蒸馏分离得到裂解气体。
(2)分离净化:将裂解气体通过冷凝器和吸收塔进行分离、净化,得到高纯度的乙烯。
(3)加压储存:将得到的乙烯通过压缩机加压至30-40MPa,存储在储罐内。
2.煤炭法煤炭法是使用煤为原料来生产乙烯的方法。
该方法主要有两种工艺路线:煤焦油法和气相氧化法。
(1)煤焦油法:煤焦油是一种裂解煤后得到的液体产物,其中含有大量的芳香烃和不饱和烃。
将煤焦油通过加热、分离等工艺处理,可制得高纯度的乙烯。
(2)气相氧化法:将煤通过气化反应转化为一氧化碳和氢气,然后进一步与空气进行氧化反应得到乙烯。
3.天然气法天然气法是利用天然气裂解产生的裂解气体来制取乙烯。
与石油法类似,天然气法也需要通过分离、净化和加压储存等步骤得到最终产品。
三、乙烯的应用趋势1.塑料制品乙烯是制造塑料制品的主要原料之一。
随着人们对环保材料需求的增加,新型可降解塑料、生物塑料等新型塑料正在逐渐崛起,并开始在日常生活中得到广泛应用。
2.纤维制品乙烯还可以作为纤维制品的原料。
近年来,新型功能性纤维材料的研究不断深入,如碳纤维、芳纶纤维等,这些纤维具有重量轻、强度高、耐高温等优点,在航天、航空、汽车制造等领域的应用前景广阔。
乙烯的加成反应实验知识点乙烯的加成反应实验,那可是化学世界里很有趣的一个小角落。
乙烯这东西啊,就像个热情的交友达人。
在加成反应里,它特别乐意跟其他分子结合。
就说乙烯和溴的加成反应吧。
乙烯分子里有那碳碳双键,这双键就像是它身上特别吸引人的闪光点。
溴分子呢,就像个好奇的小访客,看到乙烯的双键就忍不住凑上去。
在做这个实验的时候,你会看到现象特别明显。
那乙烯通入溴水或者溴的四氯化碳溶液中,溶液的颜色会迅速变浅。
这就好比一群彩色的小珠子(代表溴分子),原本满满当当在溶液里,乙烯这个交友达人一来,就拉走了好多彩色小珠子,那溶液里彩色小珠子少了,颜色可不就变浅了嘛。
而且这反应速度还挺快的,就像两个很合拍的人,一见面就迅速熟络起来。
乙烯加成反应的本质呢,是它的碳碳双键断裂。
这就好比是乙烯打开了自己的一扇大门,欢迎其他分子进来。
以和溴的反应为例,断裂后的双键分别和溴原子结合,就形成了1,2 - 二溴乙烷。
这新生成的分子啊,就像是乙烯和溴结合后的小家庭,有着全新的结构和性质。
再说说反应条件。
有些加成反应在常温常压下就能顺利进行,就像乙烯和溴的反应,不需要什么特别复杂的外部助力,自己就能完成这个结合的过程。
但也有些加成反应可能需要稍微给点外力,比如加热或者催化剂。
这就好比有的人交朋友很容易,自然就成了,而有的人可能需要别人在中间撮合一下(催化剂)或者有个合适的环境(加热等条件)才能顺利成为朋友。
从反应类型来看,加成反应和取代反应可不一样。
取代反应就像是交换座位,一个原子或者原子团替换掉另一个。
而加成反应是直接加进去,不是替换。
这就好比在一个屋子里,取代反应是一个人把另一个人从座位上赶走自己坐上去,加成反应则是直接搬个新椅子进来坐。
在实际操作这个实验的时候,装置要密封好。
要是漏气了,乙烯跑出去了,就像你邀请的客人中途跑了,那这个反应可就不完整了。
而且要注意乙烯的制取和收集过程中的安全问题。
乙烯是可燃性气体,就像个小炸弹一样,要是不小心泄露多了,遇到明火那可就麻烦了。