第八章 金属和金属材料要点
- 格式:ppt
- 大小:6.33 MB
- 文档页数:10

考点一、金属材料(一)、纯金属材料:纯金属(90多种)纯金属:有色金属:通常是指除黑色金属以外的其他金属。
黑色金属:通常指铁、锰、铬及它们的合金。
有色金属:重金属:如铜、锌、铅等轻金属:如钠、镁、铝等(二)、合金(几千种):由一种金属跟其他一种或几种金属(或金属与非金属)一起熔合而成的具有金属特性的物质。
1.金属材料包括纯金属和合金两类。
金属属于金属材料,但金属材料不一定是纯金属,也可能是合金。
2.合金可能是金属与金属组成,也可能是金属与非金属组成。
金属材料中使用比较广泛的是合金。
合金的优点:(1)熔点高、密度小;(2)可塑性好、易于加工、机械性能好;(3)抗腐蚀性能好;下面是黄铜和铜片,焊锡和锡,铝合金和铝线的有关性质比较:钛和钛合金:被认为是21世纪的重要金属材料,钛合金与人体有很好的“相容性”,因此可用来制造人造骨等。
钛合金的优点:①熔点高、密度小;②可塑性好、易于加工、机械性能好;③抗腐蚀性能好钛镍合金具有“记忆”能力,可记住某个特定温度下的形状,只要复回这个温度,就会恢复到这个温度下的形状,又被称为“记忆金属”。
此外,钛还可制取超导材料,美国生产的超导材料中的90%是用钛铌合金制造的。
3.注意:(1)合金是金属与金属或金属与非金属的混合物。
(2)合金的很多性能与组成它们的纯金属不同,使合金更容易适于不同的用途。
(3)日常使用的金属材料,大多数为合金。
(4)金属在熔合了其它金属和非金属后,不仅组成上发生了变化,其内部组成结构也发生了改变,从而引起性质的变化。
(5)合金的形成条件:其中任一金属的熔点不能高于另一金属的沸点(当两种金属形成合金时)。
(6)青铜是人类历史上使用最早的合金;生铁和钢是人类利用最广泛的合金.(7)合金都属于混合物。
考点2金属的物理性质(1)常温下一般为固态(汞为液态),有金属光泽。
(2)大多数呈银白色(铜为紫红色,金为黄色)(3)有良好的导热性、导电性、延展性(4)密度和硬度较大,熔沸点较高。


初三下册化学第8单元知识点:课题1金属材料(实用版)编制人:______审核人:______审批人:______编制单位:______编制时间:__年__月__日序言下载提示:该文档是本店铺精心编制而成的,希望大家下载后,能够帮助大家解决实际问题。
文档下载后可定制修改,请根据实际需要进行调整和使用,谢谢!并且,本店铺为大家提供各种类型的实用资料,如工作总结、述职报告、心得体会、工作计划、演讲稿、教案大全、作文大全、合同范文、活动方案、其他资料等等,想了解不同资料格式和写法,敬请关注!Download tips: This document is carefully compiled by this editor.I hope that after you download it, it can help you solve practical problems. The document can be customized and modified after downloading, please adjust and use it according to actual needs, thank you!And, this store provides various types of practical materials for everyone, such as work summaries, job reports, insights, work plans, speeches, lesson plans, essays, contract samples, activity plans, and other materials. If you want to learn about different data formats and writing methods, please pay attention!第1页共2页初三下册化学第8单元知识点:课题1金属材料尽快地掌握科学知识,迅速提高学习能力,由化学网为您提供的初三下册化学第8单元知识点:课题1金属材料,希望给您带来启发!一、金属和合金1、金属的物理性质:常温下都是固体(汞除外),大多数为银白色,有金属光泽、优良的导电导热性、有延展性,密度、硬度较大,熔点较高。

1.物理性质:①金属光泽②机械强度大(Hg)③延展性(Au)④导电(Ag、Cu)⑤导热(Ag)2.性质越稳定的金属越早被人类利用,活泼金属近几百年才被利用:自然界除Au、Bt、Ag外,多数金属都以化合态形式存在,商周时期青铜器、春秋战国时期铁器,近代才出现铝合金。
活泼性:Cu<Fe<Al,因为要将金属从化合态中提炼出来是需要技术成本的,越活泼的金属越难提取。
3.合金:在金属中加热熔合其他金属或非金属,例:生铁和钢(钢含C量少,更硬)、黄铜(铜锌合金)、硬铝(铝合金)等合金硬度、强度、抗腐蚀性一般都要优于组成他们的纯金属,故生活中合金用途更广。
4.化学性质①:+O2→金属氧化物(可通过与氧气反应条件判断金属活动性,越活泼越容易反应)②:Mg、Al、Zn、Fe + HCl、H2SO4→盐+H2↑③:“救大哥”请写出Fe“救”CuSO4的方程式并描述现象,溶液质量变化?反应前后物质总质量变化?Fe+CuSO4=FeSO4+Cu现象:铁丝表面有一层红色物质析出,溶液由蓝色渐变为浅绿色。
溶液中溶质由CuSO4变为FeSO4,(Cu相对原子质量64,Fe:56),故溶液质量减小。
但反应前后物质总质量不变。
▲5.可通过哪些方法来比较Al、Fe、Cu的活动性顺序:①与酸反应看冒气泡速率②与其对应盐反应,例:Al和FeSO4反应说明Al比Fe活泼③与氧气反应的条件,例:Mg可与空气中点燃,Fe只能在纯氧中点燃6.金属冶炼:以铁矿石(主要成分是Fe2O3)炼铁为例实验室:原理:Fe2O3+3CO=2Fe+3CO2装置:现象:A处:红色粉末变黑B处:澄清石灰水变浑浊发生的反应方程式:Ca(OH)2 +CO2=CaCO3↓+H2O C处酒精灯作用是除去多余CO防止污染空气,发生反应方程式C + O2点燃CO2实验前先同一段时间CO再点燃酒精喷灯,结束后先熄灭酒精喷灯再停止通CO,原因是防止生成的Fe又在高温环境下与空气中氧气反应生成Fe3O4生产:高炉炼铁原料:铁矿石、焦炭、石灰石(作用?)涉及方程式:①C+O2②CO2+C③Fe2O3+CO、C+Fe2O37.防腐Fe锈蚀条件:①空气(O2)②水蒸气措施:①刷漆涂油镀铬(隔绝空气和水蒸气)②加入其他金或非金制成合金(改变自身内部结构)③回收利用、有计划开采、寻找替代品。



知1 金属材料(1)金属材料种类:金属材料是指金属元素或以金属元素为主构成的具有金属特性的材料的总称,包括纯金属和合金两大类。
如生铁中主要是铁,炭的含量很少。
注:①金属属于金属材料,金属材料不一定是纯金属,也可能是合金。
②某些物质中虽含金属元素,但不是金属材料,如Fe2O3、MgO、MnO2等,因为它们不具有金属的物理性质,如导热、导电。
③金属材料中至少含一种金属单质。
(2)金属材料的发展史:人类最早使用的金属是铜,然后是铁,在然后是钢。
目前使用最多的金属是铁,铝位居第二。
知2金属的物理性质(1)金属的共性:有金属光泽、导电、导热、延展、密度大、熔点高、固体(汞除外)等。
(2)金属的特性:指不同的金属有各自的特征。
如,金是黄色的,铜是红色的。
金属之最:导电导热性最好的金属是银Ag;硬度最大的金属是铬Cr;常温时是液态(熔点最低)的金属是汞Hg;地壳中含量最多的金属是铝Al;人体中含量最高的金属是钙Ca;熔点最高的金属是钨W;密度最大的金属是锇Os;密度最小的金属是锂Li;延展性最好的金属是金Au;最轻的合金是铝锂合金。
金属在日常生活中的应用:暖气片上刷的“银粉”是铝;包装香烟、巧克力等的金属箔是铝;保温瓶内胆上镀的金属是银;干电池外壳金属是锌;普通干电池负极材料的金属是锌;体温计、血压计中的金属是汞。
知3合金(1)合金定义:在金属中加热熔合某些金属或非金属制得的具有金属特征的物质。
注:①合金中至少含有一种金属,可以由金属与金属熔合而成,也可以由金属与非金属熔合而成。
②合金具有金属特性,如导热、导电、延展、金属光泽等。
③合金一定是混合物。
从这个角度也可以说明金属氧化物是纯净物,不是合金。
(2)不同物质熔合成合金的条件:任一物质的熔点低于另一物质的沸点。
①合金与组成它的纯金属性质比较:合金的硬度一般比组成它的纯金属硬度大,熔点比组成它的纯金属熔点低。
②生铁也叫铸铁,碳含量2%-4.3%;钢的碳含量0.03%-2%。
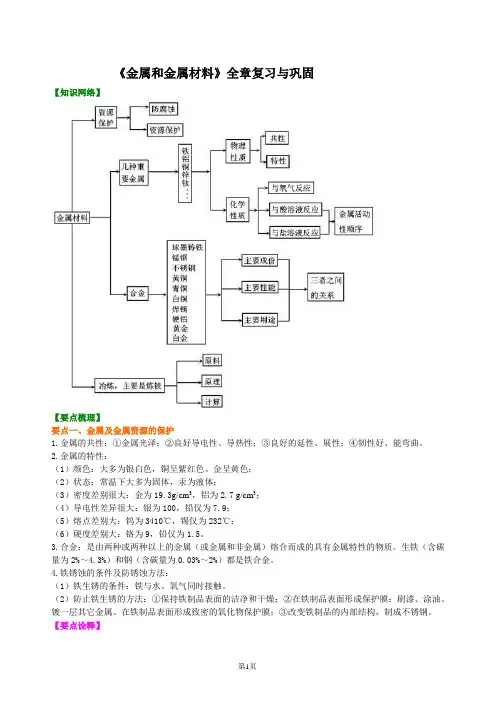
《金属和金属材料》全章复习与巩固【知识网络】【要点梳理】要点一、金属及金属资源的保护1.金属的共性:①金属光泽;②良好导电性、导热性;③良好的延性、展性;④韧性好、能弯曲。
2.金属的特性:(1)颜色:大多为银白色,铜呈紫红色、金呈黄色;(2)状态:常温下大多为固体,汞为液体;(3)密度差别很大:金为19.3g/cm3,铝为2.7 g/cm3;(4)导电性差异很大:银为100,铅仅为7.9;(5)熔点差别大:钨为3410℃,锡仅为232℃;(6)硬度差别大:铬为9,铅仅为1.5。
3.合金:是由两种或两种以上的金属(或金属和非金属)熔合而成的具有金属特性的物质。
生铁(含碳量为2%~4.3%)和钢(含碳量为0.03%~2%)都是铁合金。
4.铁锈蚀的条件及防锈蚀方法:(1)铁生锈的条件:铁与水、氧气同时接触。
(2)防止铁生锈的方法:①保持铁制品表面的洁净和干燥;②在铁制品表面形成保护膜:刷漆、涂油、镀一层其它金属、在铁制品表面形成致密的氧化物保护膜;③改变铁制品的内部结构,制成不锈钢。
【要点诠释】1.金属材料包括纯金属和它们的合金。
合金的硬度、强度、抗腐蚀性等一般都好于组成它们的纯金属。
2.保护金属资源的有效途径:①防止金属锈蚀;②废旧金属的回收利用;③合理有效的开采矿物;④寻找金属的替代品等。
要点二、金属活动性顺序、金属的化学性质1.在金属活动性顺序里,金属的位置越靠前,它的活动性就越强;位于氢前面金属可以置换出盐酸、稀硫酸中的氢;位于前面的金属能把位于后面的金属从它们化合物的溶液里置换出来(K 、Ca 、Na 除外)。
2.置换反应是由一种单质与一种化合物反应,生成另一种单质和另一种化合物的反应。
3.金属能与氧气、酸等发生反应。
【要点诠释】1.只有较活泼的金属才能把不太活泼的金属从它的化合物溶液里置换出来。
2.铁与酸或金属化合物发生置换反应时生成的铁的化合物中铁均显+2价。
要点三、金属冶炼及有关计算1.工业上把能用来提炼金属的矿物叫做矿石。

初三化学金属和金属材料知识点总结一、金属材料:金属材料包括纯金属以及它们的合金。
二、金属的物理性质1、在常温下一般为固态(汞为液态),有金属光泽(大多数金属呈银白色,铜呈紫红色,金呈黄色);2、导电性、导热性、熔点较高、延展性、能弯曲、硬度较大、密度较大。
三、金属之最1、地壳中含量最多的金属元素——铝2、人体中含量最多的金属元素——钙3、目前世界年产量最多的金属——铁(铁>铝>铜)4、导电、导热性最好的金属——银(银>铜>金>铝)5、熔点最高的金属——钨6、熔点最低的金属——汞7、硬度最大的金属——铬8、密度最大的金属——锇9、密度最小的金属——锂四、金属的分类五、金属的应用物质的性质在很大程度上决定了物质的用途,但这不是唯一的决定因素。
在考虑物质的用途时,还需要考虑价格、资源、是否美观、使用是否便利,以及废料是否易于回收和对环境的影响等多种因素。
1、铜、铝——电线——导电性好、价格低廉2、钨——灯丝——熔点高3、铬——电镀——耐腐蚀性4、铁——菜刀、镰刀、锤子等5、汞——体温计液柱6、银——保温瓶内胆7、铝——“银粉”、锡箔纸六、合金1、合金:由两种或两种以上的金属或金属与非金属经一定方法所合成的具有金属特性的物质。
合金是混合物。
目前已制得的纯金属只有90多种,而合金已达几千种。
2、合金的硬度一般比组成它的纯金属的硬度大,抗腐蚀性强。
3、合金的熔点一般比组成它的纯金属的熔点低。
4、常见的合金:5、钛和钛合金:被认为是21世纪的重要金属材料,钛合金与人体具有良好的“相容性”,可用来造人造骨。
钛和钛合金的优点:①熔点高、密度小;②可塑性好、易于加工、机械性能好;③抗腐蚀性能好。
6、生铁和钢性能不同的原因:含碳量不同。
3模块二金属的化学性质一、金属与氧气的反应1、镁、铝:(1)在常温下能与空气中的氧气反应:2Mg+O2=2MgO ;4Al+3O2=2Al2O3(2)铝的抗腐蚀性能好的原因:铝在空气中与氧气反应,其表面生成一层致密的氧化铝薄膜,从而阻止铝进一步氧化。


第八章 金属和金属材料知识点一、金属材料姓名:1. 金属材料包括纯金属和合金两类。
金属属于金属材料,但金属材料不一定是纯金属,也可能是合金。
2. 金属制品是由金属材料制成的,铁、铜、铝及其合金是人类使用最多的金属材料。
金属材料的发展史商朝,人们开始使用青铜器;春秋时期开始冶铁;战国时期开始炼钢;铜和铁一直是人类广泛应用的金属材料。
在100多年前,又开始了铝的使用,因铝具有密度小和抗腐蚀等许多优良性能, 铝的产量已超过了铜, 位于第二位。
(1) 常见金属的物理性质① 共性:大多数金属都具有金属光泽,密度和硬度较大,熔沸点较高,具有良好的延展性和导电、 温下除汞为液体,其余金属均为固体。
② 特性:颜色:铁、铝等大多数金属都呈银白色,铜呈紫红色,金呈黄色 密度:大多数金属的密度大于水,锂、钠、钾等金属的密度小于水 导电性:银、铜的导电性较好,铝的导电性较差延展性:金的延展性较好,锰的延展性很差 注意:颜色和光泽一般是指金属在整块时表现出来的外观特性, (2) 常见金属的物理性质比较:导电性 Ag Cu Au Al Zn Fe Pb由优到良 密度 Au Pb Ag Cu Fe Zn Al由大到小 熔点 WFeCu Au Ag Al Sn 由高到低 硬度Cr FeAgCuAuAlPb由大到小物质的性质与物质的用途之间的关系:1. 物质的性质决定物质的用途,而物质的用途又反映出物质的性质。
2. 物质的性质很大程度上决定了物质的用途。
但这不是唯一的决定因素,在考虑物质的用途时,还需要考虑价格、资源、是否美观、使用是否便利,以及废料是否易于回收和对环紧的影响 等多种因素。
合金1.合金:在金属中加热熔合某些金属和非金属,形成具有金属特性的物质。
注意:(1)合金是金属与金属或金属与非金属的混合物。
(2) 合金的很多性能与组成它们的纯金属不同,使合金更容易适于不同的用途。
(3) 日常使用的金属材料,大多数为合金。
九年级化学第八单元金属和金属材料一、金属的性质1. 导电性金属具有良好的导电性,是因为金属内部存在大量自由电子,这些自由电子可以在金属中自由移动,从而形成电流。
2. 导热性金属的导热性也非常好,当金属受热时,热量可以通过金属内部的自由电子传递,使整个金属均匀受热。
3. 延展性和韧性金属具有很好的延展性和韧性,可以被拉成细丝或者锻造成薄片,这也是金属在制作各种工艺品和建筑材料中的重要性。
4. 金属性金属的一般性质包括金属性,例如光泽、导电性和导热性,这些性质是金属材料在日常生活和工业生产中得以广泛应用的重要原因。
二、金属的化学性质1. 金属的化学性质通常表现为金属的氧化反应。
绝大多数金属在空气中与氧气反应,形成金属氧化物,这一过程称为金属的氧化。
2. 金属的活泼性金属的活泼性是指金属发生氧化反应的能力,一般来说,活泼性大的金属更容易与氧气反应,如钠、钾等,而活泼性小的金属则不容易与氧气反应。
3. 金属的腐蚀由于金属的化学性质,金属材料易受腐蚀的影响,一些金属在特定条件下会发生腐蚀现象,降低金属材料的耐久性和使用寿命。
三、金属材料的应用1. 金属材料在建筑领域的应用金属材料广泛应用于建筑领域,例如钢结构、铝合金和镁合金等,这些材料具有较高的强度和耐腐蚀性,可以用于建筑结构和装饰材料。
2. 金属材料在电子领域的应用金属材料在电子领域具有重要应用,例如铜、铝等金属作为导电材料广泛用于电路、电缆等,而金属的导热性也使其成为散热器、导热片等散热材料。
3. 金属材料在工艺品制作领域的应用金属材料被用于制作工艺品,例如黄铜、铜等金属可以制作成各种器皿、雕塑等工艺品,展现出金属的艺术魅力。
四、金属材料的保护和利用1. 金属材料的防腐蚀为了延长金属材料的使用寿命,防止其受到腐蚀的影响,可以采取一些防护措施,例如电镀、镀锌、喷涂防腐漆等方法,有效保护金属材料不受腐蚀。
2. 金属材料的再利用金属材料可以进行再生利用,例如废旧金属可以进行回收再加工,成为新的金属制品,减少对自然资源的消耗,实现资源的循环利用。
九年级化学金属及其合金材料知识点
金属元素
- 金属元素是化学中的一类物质,具有良好的导热性和导电性。
- 典型的金属元素包括铁、铜、铝等。
- 金属元素的外层电子较少,容易失去电子形成阳离子。
金属的性质
- 金属在常温下大多数是固体,具有良好的延展性和可塑性。
- 金属的熔点较高,可以在高温下熔化成液态。
- 金属的热导率和电导率较高,可以快速传递热量和电流。
- 金属的密度较大,具有一定的重量。
金属合金
- 金属合金是由两种或两种以上的金属元素组成的材料。
- 金属合金具有比纯金属更好的性能和特点。
- 金属合金可以根据需要调整合金元素的比例,改变合金的性质。
- 金属合金具有硬度高、强度大、抗腐蚀性能好等优点。
常见的金属合金
- 不锈钢:由铁、铬、镍等元素组成,具有较强的耐腐蚀性能。
- 铝合金:由铝、镁、锌等元素组成,具有较轻的重量和良好
的强度。
- 铜合金:由铜、锌、锡等元素组成,具有良好的导电性和导
热性。
金属及其合金的应用
- 铁用于建筑、制造机械等领域。
- 铝用于制造飞机、汽车等领域。
- 铜用于制造电线、电器等领域。
- 不锈钢用于制造厨具、建筑材料等领域。
以上是九年级化学金属及其合金材料的基本知识点,希望对你
有所帮助。
化学金属和金属材料知识点总结一、金属的基本概念1. 定义:金属是元素周期表中的一类元素,通常具有良好的导电性、导热性、延展性和可锻性。
2. 分类:- 根据电子结构:过渡金属、主族金属和镧系元素。
- 根据性质:铁磁性金属、非铁磁性金属、贵金属等。
3. 物理性质:- 高密度- 光泽(金属光泽)- 可锻性和延展性- 熔点和沸点范围广泛二、金属的化学性质1. 氧化还原反应:- 金属倾向于失去电子,形成阳离子。
- 金属氧化反应常见于金属的腐蚀过程。
2. 酸碱反应:- 金属与酸反应生成氢气和相应的金属盐。
- 金属与碱反应较少,但某些金属如铝可以与强碱反应。
3. 配位化学:- 金属离子能与配体形成配合物。
- 配合物在催化、生物化学和材料科学中有广泛应用。
三、金属材料的类型1. 纯金属:- 单一金属元素,如铁、铜、铝等。
2. 合金:- 由两种或两种以上金属元素组成的混合物。
- 合金通常具有比纯金属更优异的物理和化学性质。
3. 金属间化合物:- 具有特定化学计量比的金属化合物。
- 通常具有高硬度和高熔点。
四、金属的提取与加工1. 提取方法:- 矿石开采- 冶炼(火法和湿法)- 电解精炼2. 加工技术:- 铸造- 锻造- 轧制- 焊接五、金属材料的应用1. 建筑和结构:- 钢筋混凝土- 钢结构建筑2. 电子和电气:- 导线和电缆- 电子元件和芯片3. 交通运输:- 汽车和飞机的框架和发动机部件 - 船舶和火车的制造4. 医疗和生物技术:- 医疗器械- 生物相容性植入物六、金属的环境影响1. 金属污染:- 重金属污染- 金属的生物积累和放大2. 回收和再利用:- 金属的回收减少对环境的影响 - 再生金属的生产和应用七、未来趋势和挑战1. 新材料的开发:- 高性能合金- 轻质高强度材料2. 可持续发展:- 绿色冶金技术- 金属的生命周期评估结论金属和金属材料是现代社会不可或缺的基础材料。
了解它们的化学性质、加工技术和应用领域对于材料科学、工程学和环境科学等领域至关重要。
8第八单元金属和金属材料单元知识点总结金属和金属材料是化学中的一个重要单元,涵盖了金属的性质、结构、合金、金属材料的制备和应用等方面的知识。
以下是对这一单元的知识点进行总结。
1.金属的性质:-密度大:金属的密度通常较大,是固体中最大的。
-导电性好:金属是电子云流动的自由电子,因此具有良好的导电性。
-热导性好:金属内部电子的热运动使得热能得以迅速传导。
-延展性和塑性好:金属可以被拉长成线,也可以被锤打成薄片。
-光泽:金属具有光泽,可以反射光线。
-高熔点和沸点:金属的熔点和沸点通常较高。
2.金属的结构:-金属晶格:金属的晶格由金属原子通过金属键连接而成,具有规则的排列结构。
-金属原子的排列方式:金属原子通常呈现紧密堆积或者面心立方堆积的方式排列。
3.合金:-定义:合金是由两种或更多金属元素组成的固溶体。
-合金的作用:(1)提高材料的机械性能:合金可以通过调整金属元素的含量和种类,来提高材料的强度、硬度、耐磨性等机械性能。
(2)改善材料的耐腐蚀性:合金可以增加材料的抗腐蚀性能,提高材料在恶劣环境中的使用寿命。
(3)调整材料的物理性质:合金可以调整材料的热膨胀系数、导电性等物理性质。
-合金的分类:(1)置换型合金:合金中的金属原子替代了其他金属原子的位置。
(2)插入型合金:新原子插入到晶体间隙中,形成新的化合物。
(3)亚稳态合金:合金存在非平衡态结构,具有特殊的物理性质。
(4)反应性合金:含有活泼金属元素,能够与其他元素反应形成化合物。
4.金属材料的制备:-炼铁:从铁矿石中提取铁的过程,主要包括矿石的还原、炉渣的冶炼和铁的提纯等步骤。
-铸造:将熔化的金属倒入模具中,等待冷却凝固,得到所需形状的金属制品。
-锻造:将金属加热至高温后,在压力的作用下改变金属的形状和尺寸。
-淬火:将加热至高温的金属迅速冷却,使其获得较高的硬度。
-淬火方式:水淬、油淬、气淬、盐浴淬等。
5.金属材料的应用:-结构材料:金属广泛应用于建筑、桥梁、汽车、飞机等领域,用于承担结构载荷。
九年级化学第八单元金属和金属材料知识点归纳总结1.金属材料的种类:纯金属(90多种)合金(几千种)2.金属的物理性质:(1)常温下一般为固态(汞为液态),有金属光泽。
(2)大多数呈银白色(铜为紫红色,金为黄色)(3)有良好的导热性、导电性、延展性3.金属之最:(1)铝:地壳中含量最多的金属元素(2)钙:人体中含量最多的金属元素(3)铁:目前世界年产量最多的金属(铁>铝>铜)(4)银:导电、导热性最好的金属(银>铜>金>铝)(5)铬:硬度最高的金属(6)钨:熔点最高的金属(7)汞:熔点最低的金属(8)锇:密度最大的金属(9)锂:密度最小的金属4.金属分类:黑色金属:通常指铁、锰、铬及它们的合金。
有色金属:通常是指除黑色金属以外的其他金属。
重金属:如铜、锌、铅等轻金属:如钠、镁、铝等;5.合金:由一种金属跟其他一种或几种金属(或金属与非金属)一起熔合而成的具有金属特性的物质。
此可用来制造人造骨等。
优点:(1)熔点高、密度小;(2)可塑性好、易于加工、机械性能好;(3)抗腐蚀性能好二、金属的化学性质1.金属与氧气反应镁在空气(或氧气)中燃烧:2Mg + O2=2MgO铝在氧气中反应:4Al+ 3O2 =2Al2O3 (铝具有很好的抗腐蚀性能)铁在氧气中燃烧:3Fe + 2O2点燃Fe3O4铁在潮湿的空气中易生锈(铁锈的主要成分Fe2O3 ·xH2O)2.金属与酸反应由一种单质与一种化合物反应,生成另一种单质与另一种化合物的反应 A+BC→AC+B 3.金属与盐溶液反应实验1铝丝浸入硫酸铜溶液中 现象:铝丝表面覆盖一层紫红色的物质,溶液由蓝色变成无色 2Al+3CuSO 4== Al 2(SO 4)3+3Cu实验2铜丝浸入硝酸银溶液中 现象:铜丝表面覆盖一层银白色物质,溶液由无色逐渐变成蓝色 Cu+2AgNO 3= Cu(NO 3)2+2Ag实验3把锌片放入硫酸铜溶液中 现象:锌片表面有红色物质析出。