燃料电池综合特性研究
- 格式:docx
- 大小:216.07 KB
- 文档页数:13

竭诚为您提供优质文档/双击可除燃料电池实验报告篇一:燃料电池综合特性实验报告燃料电池综合特性实验【实验背景】燃料电池以氢和氧为燃料,通过电化学反应直接产生电力,能量转换效率高于燃烧燃料的热机。
燃料电池的反应生成物为水,对环境无污染,单位体积氢的储能密度远高于现有的其它电池。
因此它的应用从最早的宇航等特殊领域,到现在人们积极研究将其应用到电动汽车,手机电池等日常生活的各个方面,各国都投入巨资进行研发。
按燃料电池使用的电解质或燃料类型,可将现在和近期可行的燃料电池分为碱性燃料电池,质子交换膜燃料电池,直接甲醇燃料电池,磷酸燃料电池,熔融碳酸盐燃料电池,固体氧化物燃料电池6种主要类型,本实验研究其中的质子交换膜燃料电池。
能源为人类社会发展提供动力,长期依赖矿物能源使我们面临环境污染之害,资源枯竭之困。
为了人类社会的持续健康发展,各国都致力于研究开发新型能源。
未来的能源系统中,太阳能将作为主要的一次能源替代目前的煤,石油和天然气,而燃料电池将成为取代汽油,柴油和化学电池的清洁能源。
【摘要】燃料电池尤其是质子交换膜燃料电池(pem)以其高功率密度、高能量转换效率、可低温启动、环境友好等突出优点而受到瞩目。
本实验包含太阳能电池发电(光能—电能转换),电解水制取氢气(电能—氢能转换),燃料电池发电(氢能—电能转换)几个环节,形成了完整的能量转换,储存,使用的链条。
本实验通过研究燃料电池的工作原理,测量其输出特性,计算燃料电池的最大输出功率及效率并验证法拉第电解定律。
测量太阳能电池的特性,做出所测太阳能电池的伏安特性曲线,电池输出功率随输出电压的变化曲线。
获取太阳能电池的开路电压,短路电流,最大输出功率等。
【关键词】燃料电池,电解池,太阳能电池【正文】一、实验目的:1、了解燃料电池的工作原理。
2、观察仪器的能量转换过程:光能→太阳能电池→电能→电解池→氢能(能量储存)→燃料电池→电能3、测量燃料电池输出特性,做出所测燃料电池的伏安特性(极化)曲线,电池输出功率随输出电压的变化曲线。

燃料电池综合特性实验一、概述 1.新能源的定义新能源又称非常规能源。
是指传统能源之外的各种能源形式。
指刚开始开发利用或正在积极研究、有待推广的能源,如太阳能、地热能、风能、海洋能、氢能、生物质能和核聚变能等。
2.太阳能太阳能一般指太阳光的辐射能量。
太阳能的主要利用形式有太阳能的光热转换、光电转换以及光化学转换三种主要方式。
广义上的太阳能是地球上许多能量的来源,如风能,化学能,水的势能等由太阳能导致或转化成的能量形式。
利用太阳能的方法主要有:太阳电能池,通过光电转换把太阳光中包含的能量转化为电能;太阳能热水器,利用太阳光的热量加热水,并利用热水发电等。
本实验将测量太阳能电池下述特性:(1)测量太阳能电池在光照时的输出特性并求得它的短路电流(I SC )、开路电压(U OC )、最大输出功率及填充因子FF[(m P )(oc sc mU I P )]。
填充因子是代表太阳能电池性能优劣的一个重要参数。
(2)光照效应:a)测量短路电流I SC 和输出功率P 之间关系,画出I SC 与P 之间的关系图。
b)测量开路电压U OC 和输出功率P 之间的关系,画出U OC 与输出功率P 之间的关系图。
3.燃料电池燃料电池(Fuel Cell)是一种将存在于燃料与氧化剂中的化学能直接转化为电能的发电装置。
燃料和空气分别送进燃料电池,电就被奇妙地生产出来。
它从外表上看有正负极和电解质等,像一个蓄电池,但实质上它不能“储电”而是一个“发电厂”。
燃料电池十分复杂,涉及化学热力学、电化学、电催化、材料科学、电力系统及自动控制等学科的有关理论,具有发电效率高、环境污染少等优点。
总的来说,燃料电池具有以下特点:(1)能量转化效率高:它直接将燃料的化学能转化为电能,中间不经过燃烧过程,因而不受卡诺循环的限制。
目前燃料电池系统的燃料—电能转换效率在45%~60%,而火力发电和核电的效率大约在30%~40%。
(2)有害气体SOx、NOx及噪音排放都很低,CO2排放因能量转换效率高而大幅度降低,无机械振动。

燃料电池综合特性实验实验报告燃料电池综合特性实验实验报告燃料电池是一种利用化学能转化为电能的设备,其具有高效、清洁、可持续等特点,在能源领域具有广阔的应用前景。
为了深入了解燃料电池的综合特性,我们进行了一系列实验,并通过实验报告的形式进行总结和分析。
实验一:燃料电池的基本原理在这个实验中,我们首先了解了燃料电池的基本原理。
燃料电池通过氧化还原反应将燃料和氧气转化为电能和热能。
我们选择了常见的质子交换膜燃料电池(PEMFC)进行实验。
实验中,我们使用了氢气和氧气作为燃料和氧化剂,并通过电解质膜进行质子传导。
通过测量电流和电压的变化,我们得到了燃料电池的电流-电压曲线,从而了解了燃料电池的基本特性。
实验二:燃料电池的输出特性在这个实验中,我们研究了燃料电池的输出特性。
我们改变了燃料电池的负载电阻,测量了电流和电压的变化,并计算了燃料电池的输出功率。
通过绘制功率-电流曲线和功率-电压曲线,我们可以确定燃料电池的最大功率点。
实验结果表明,燃料电池的输出功率随着负载电阻的变化而变化,最大功率点的位置可以通过调整负载电阻来实现。
实验三:燃料电池的效率在这个实验中,我们研究了燃料电池的效率。
燃料电池的效率是指电能输出与燃料输入之间的比值。
我们通过测量燃料电池的输入功率和输出功率,计算了燃料电池的效率。
实验结果表明,燃料电池的效率受到多种因素的影响,包括燃料电池的工作温度、燃料的纯度等。
通过优化这些因素,可以提高燃料电池的效率。
实验四:燃料电池的稳定性在这个实验中,我们研究了燃料电池的稳定性。
燃料电池的稳定性是指燃料电池在长时间运行中的性能变化情况。
我们通过连续运行燃料电池,并测量电流和电压的变化,评估了燃料电池的稳定性。
实验结果表明,燃料电池的稳定性受到多种因素的影响,包括燃料电池的材料、温度和湿度等。
通过优化这些因素,可以提高燃料电池的稳定性。
实验五:燃料电池的寿命在这个实验中,我们研究了燃料电池的寿命。
燃料电池的寿命是指燃料电池在长时间运行中的使用寿命。

燃料电池综合特性实验一、实验目的:1、了解燃料电池的工作原理。
2、观察仪器的能量转换过程:光能→太阳能电池→电能→电解池→氢能(能量储存)→燃料电池→电能3、测量燃料电池输出特性,做出所测燃料电池的伏安特性(极化)曲线,电池输出功率随输出电压的变化曲线。
计算燃料电池的最大输出功率及效率。
4、测量质子交换膜电解池的特性,验证法拉第电解定律。
5、测量太阳能电池的特性,做出所测太阳能电池的伏安特性曲线,电池输出功率随输出电压的变化曲线。
获取太阳能电池的开路电压,短路电流,最大输出功率,填充因子等特性参数。
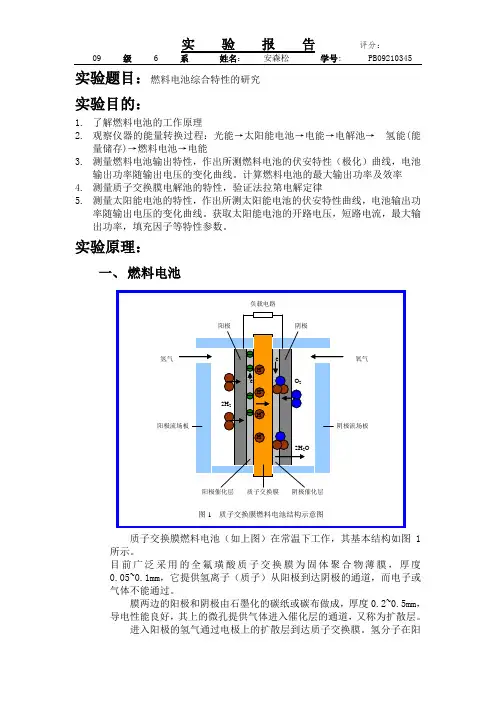
二、实验原理:1、燃料电池质子交换膜(PEM,Proton Exchange Membrane)燃料电池在常温下工作,具有启动快速,结构紧凑的优点,最适宜作汽车或其它可移动设备的电源,近年来发展很快,其基本结构如图l所示。
目前广泛采用的全氟璜酸质子交换膜为固体聚合物薄腆,厚度0.05~0.lmm,它提供氢离子(质子)从阳极到达阴极的通道,而电子或气体不能通过。
催化层是将纳米量级的铂粒子用化学或物理的方法附着在质子交换膜表面,厚度约0.03mm,对阳极氢的氧化和阴极氧的还原起催化作用。
膜两边的阳极和阴极由石墨化的碳纸或碳布做成,厚度0.2~0.5mm,导电性能良好,其上的微孔提供气体进入催化层的通道,又称为扩散层。
教学用燃料电池采用有机玻璃做流场板。
进入阳极的氢气通过电极上的扩散层到达质子交换膜。
氢分子在阳极催化剂的作用下解离为2个氢离子,即质子,并释放出2个电子,阳极反应为:H2=2H+2e (l)氢离子以水合质子H+(nH2O)的形式,在质子交换膜中从一个璜酸基转移到另一个璜酸基,最后到达阴极,实现质子导电,质子的这种转移导致阳极带负电。
在电池的另一端,氧气或空气通过阴极扩散层到达阴极催化层,在阴极催化层的作用下,氧与氢离子和电子反应生成水,阴极反应为:O2+4H+4e=2H2O (2)阴极反应使阴极缺少电子而带正电,结果在阴阳极间产生电压,在阴阳极间接通外电路,就可以向负载输出电能。

燃料电池综合特性的研究------------------------------------------作者xxxx------------------------------------------日期xxxx燃料电池综合特性的研究隋永德(中国海洋大学地信11级 050422011034)摘要:燃料电池是一种清洁能源,通过实验了解燃料电池的工作原理,测量质子交换膜电解池特性,验证法拉第电解定律,测量燃料电池的输出特性。
燃料电池通过电化学反应,直接将化学能转换成电能。
关键词:质子交换膜电解池、燃料电池、输出特性、极化特性曲线引言:燃料电池(Fuel Cell)是一种将存在与燃料与氧化剂中的化学能直接转化为电能的发电装置。
燃料和空气分别送进燃料电池,电就被奇妙地生产出来。
燃料电池由德国物理学及化学家尚班()于1838年提出,并刊登在当时著名的科学杂志。
英国物理学家威廉·葛洛夫()于1839年2月同样发现了燃料电池现象并做了设计草图。
燃料电池不污染环境,通过电化学反应,而不采用燃烧或储能方式。
燃料电池只产生水和热。
如果氢气通过可再生能源产生(光伏电池板、风能发电等),整个过程就不产生有害物质。
燃料电池无噪音。
按燃料电池使用的电解质或燃料类型,可将燃料电池分为以下六种:碱性燃料电池、质子交换膜燃料电池、直接甲醇燃料电池、磷酸燃料电池、熔融碳酸盐燃料电池、固体氧化物燃料电池。
本实验研究了质子交换膜燃料电池,氢气用电解水获得。
发展瓶颈:尽管燃料电池有诸多优势,但目前受燃料电池造价偏高、碳氢化合物燃料无法直接利用及氢气储存技术还不够发达,因此目前燃料电池还不能广泛应用。
1、实验原理质子交换膜(Proton exchange membrane,简称PEM)燃料电池,在原理上相当于水电解的“逆”装置,其单电池由阳极、阴极和质子交换膜组成,阳极为氢燃料发生氧化的场所,阴极为氧化剂还原的场所,两级都有加速电极化学反应的催化剂,质子交换膜作为电解质。
实验题目:燃料电池综合特性的研究实验目的:1.了解燃料电池的工作原理2.观察仪器的能量转换过程:光能→太阳能电池→电能→电解池→氢能(能量储存)→燃料电池→电能3.测量燃料电池输出特性,作出所测燃料电池的伏安特性(极化)曲线,电池输出功率随输出电压的变化曲线。
计算燃料电池的最大输出功率及效率4.测量质子交换膜电解池的特性,验证法拉第电解定律5.测量太阳能电池的特性,作出所测太阳能电池的伏安特性曲线,电池输出功率随输出电压的变化曲线。
获取太阳能电池的开路电压,短路电流,最大输出功率,填充因子等特性参数。
实验原理:一、燃料电池质子交换膜燃料电池(如上图)在常温下工作,其基本结构如图1所示。
目前广泛采用的全氟璜酸质子交换膜为固体聚合物薄膜,厚度0.05~0.1mm,它提供氢离子(质子)从阳极到达阴极的通道,而电子或气体不能通过。
膜两边的阳极和阴极由石墨化的碳纸或碳布做成,厚度0.2~0.5mm,导电性能良好,其上的微孔提供气体进入催化层的通道,又称为扩散层。
进入阳极的氢气通过电极上的扩散层到达质子交换膜。
氢分子在阳极催化剂的作用下解离为2个氢离子,即质子,并释放出2个电子,阳极反应为:H2= 2H++2e (1)氢离子以水合质子H+(nH2O)的形式,在质子交换膜中从一个璜酸基转移到另一个璜酸基,最后到达阴极,实现质子导电,质子的这种转移导致阳极带负电。
在电池的另一端,氧气或空气通过阴极扩散层到达阴极催化层,在阴极催化层的作用下,氧与氢离子和电子反应生成水,阴极反应为:O2+4H++4e = 2H2O (2)阴极反应使阴极缺少电子而带正电,结果在阴阳极间产生电压,在阴阳极间接通外电路,就可以向负载输出电能。
总的化学反应如下:2H2+O2= 2H2O (3)二、水的电解将水电解产生氢气和氧气,与燃料电池中氢气和氧气反应生成水互为逆过程。
水电解装置同样因电解质的不同而各异,碱性溶液和质子交换膜是最好的电解质。

燃料电池综合实验马新鑫 物基 2011301020001【实验目的】1.了解燃料电池的工作原理;2.观察仪器的能量转换过程;3.测量燃料电池输出特性,作出所测燃料电池的伏安特性(极化)曲线,电池输出功率随输出电压的变化曲线;4.测量质子交换膜电解池的特性,验证法拉第电解定律。
【实验原理】1、燃料电池主要包括三部分:质子交换膜、催化层、阳极和阴极。
质子交换膜,它提供氢离子(质子)从阳极到达阴极的通道,而电子或气体不能通过。
催化层是将纳米量级的的铂粒子用化学或物理的方法附着在质子交换膜表面,厚度约0.03mm ,对阳极氢的氧化和阴极氧的还原起催化作用。
膜两边的阳极和阴极由石墨化的碳纸或碳布做成,厚度0.2~0.5mm ,导电性能良好,其上的微孔提供气体进入催化层的通道,又称为扩散层。
进入阳极的氢气通过电极上的扩散层到达质子交换膜。
氢分子在阳极催化剂的作用下解离为2个氢离子,即质子,并释放出2个电子,阳极反应为:H 2 = 2H ++2e氢离子以水合质子H +(nH 2O )的形式,通过质子交换膜到达阴极,实现质子导电。
在电池的另一端,氧气或空气通过阴极扩散层到达阴极催化层,在阴极催化层的作用下,氧与氢离子和电子反应生成水,阴极反应为:O 2+4H ++4e = 2H 2O阴极反应使阴极缺少电子而带正电,结果在阴阳极间产生电压,在阴阳极间接通外电路,就可以向负载输出电能。
总的化学反应如下:2H 2+O 2 = 2H 2O理论分析表明,若不考虑电解器的能量损失,在电解器上加1.48伏电压就可使水分解为氢气和氧气,实际由于各种损失,输入电压高于1.6伏电解器才开始工作。
电解器的效率为:1.48100%U η=⨯电解输入根据法拉第电解定律,电解生成物的量与输入电量成正比。
在标准状态下(温度为零 ︒C ,电解器产生的氢气保持在1个大气压),设电解电流为I ,经过时间t 生产的氢气体积(氧气体积为氢气体积的一半)的理论值为:22.42ItV F=⨯氢气 式中F = e N = 9.65×104库仑/摩尔为法拉第常数,e = 1.602×10-19库仑为电子电量,N = 6.022×1023为阿伏伽德罗常数,It/2F 为产生的氢分子的摩尔(克分子)数,22.4升为标准状态下气体的摩尔体积。

燃料电池的特性测量实验燃料电池以氢和氧为燃料,通过电化学反应直接产生电力,能量转换效率高于燃烧燃料的热机。
燃料电池的反应生成物为水,对环境无污染,单位体积氢的储能密度远高于现有的其它电池。
因此它的应用从最早的宇航等特殊领域,到现在人们积极研究将其应用到电动汽车,手机电池等日常生活的各个方面,各国都投入巨资进行研发。
1839年,英国人格罗夫(W. R . Grove)发明了燃料电池,历经近两百年,在材料,结构,工艺不断改进之后,进入了实用阶段。
按燃料电池使用的电解质或燃料类型,可将现在和近期可行的燃料电池分为碱性燃料电池,质子交换膜燃料电池,直接甲醇燃料电池,磷酸燃料电池,熔融碳酸盐燃料电池,固体氧化物燃料电池6种主要类型,本实验研究其中的质子交换膜燃料电池。
燃料电池的燃料氢(反应所需的氧可从空气中获得)可电解水获得,也可由矿物或生物原料转化制成。
本实验包含太阳能电池发电(光能-电能转换),电解水制取氢气(电能-氢能转换),燃料电池发电(氢能-电能转换)几个环节,形成了完整的能量转换,储存,使用的链条。
实验内含物理内容丰富,实验内容紧密结合科技发展热点与实际应用,实验过程环保清洁。
能源为人类社会发展提供动力,长期依赖矿物能源使我们面临环境污染之害,资源枯竭之困。
为了人类社会的持续健康发展,各国都致力于研究开发新型能源。
未来的能源系统中,太阳能将作为主要的一次能源替代目前的煤,石油和天然气,而燃料电池将成为取代汽油,柴油和化学电池的清洁能源。
【实验目的】1.了解燃料电池的工作原理。
2.观察仪器的能量转换过程:光能—太阳能电池—电能—电解池—氢能(能量存储)—燃料电池—电能。
3.测量燃料电池的输出特性,作出燃料电池的伏安特性曲线,电池输出功率随输出电压的变化曲线,计算燃料电池的最大输出功率和效率。
4.测量质子交换膜电解池的特性,验证法拉第电解定律。
5.测量太阳能电池的特性,作太阳能电池的伏安特性曲线以及输出功率随输出电压的变化曲线,获取太阳能电池的开路电压、短路电流、最大输出功率、填充因子等特性参数。

燃料电池综合特性实验实验报告实验报告燃料电池综合特性实验实验报告实验目的:1、研究燃料电池的综合特性;2、探究不同条件下燃料电池的性能变化。
实验原理:燃料电池是一种利用化学能转化为电能的设备。
它通过电化学反应将氢气和氧气合成水的过程中释放出能量,并将能量转化为电能。
燃料电池的核心是电化学反应,在反应中产生的电能和功率取决于电化学反应的速率和电化学势。
电化学反应速率与温度、压力、反应物浓度等因素有关。
实验过程:1、将燃料电池与电子载流板连接,并调整电流控制器,为电池施加外电压;2、在恒定的温度和压力下,记录电池的电量输出、输出电压、输出电流、燃料消耗率等参数;3、调整温度和压力,重复实验;4、根据实验数据分析燃料电池的综合特性。
实验结果:在本次实验中,我们通过改变温度、压力等因素,研究了燃料电池的综合特性。
实验数据表明,在较低的温度和较高的压力下,燃料电池的性能最优。
同时,随着温度的升高和压力的降低,燃料电池的输出电量、电压和电流都会减少,燃料消耗率却会增加。
这些结果为燃料电池的应用和优化提供了实验依据。
结论:通过本次实验,我们得出了以下结论:1、低温和高压有利于燃料电池的性能提升;2、温度和压力的变化会对燃料电池的输出电量、电压、电流和燃料消耗率产生影响。
实验意义:燃料电池是一种具有广阔应用前景的新型能源设备,其性能的优化对于推广应用至关重要。
本次实验从实验数据的角度回答了一些关键问题,对未来的燃料电池研究和应用提供了参考和依据。
参考文献:1、《燃料电池基础及应用》;2、《燃料电池综合性能研究》。

燃料电池特性综合实验报告燃料电池特性综合实验报告燃料电池是一种将化学能直接转化为电能的装置,它具有高效、环保、低噪音等特点,被广泛应用于能源领域。
本次实验旨在研究燃料电池的特性,并探究其在不同条件下的性能表现。
1. 实验目的本次实验的主要目的是通过对燃料电池的特性进行综合实验,了解其工作原理和性能特点,为进一步研究和应用提供基础数据。
2. 实验器材本次实验所使用的器材包括燃料电池、电流电压源、电阻箱、数字万用表、数据采集卡等。
3. 实验步骤3.1 准备工作首先,我们需要检查实验器材的完好性,确保实验的顺利进行。
同时,还需准备好所需的燃料和氧气供应。
3.2 实验过程在实验开始前,我们首先将电流电压源和燃料电池进行连接,并通过电阻箱调节电流的大小。
然后,我们使用数字万用表测量电池的电压和电流,并将数据记录下来。
接下来,我们将改变电流的大小,观察燃料电池的电压变化情况。
最后,我们还可以改变燃料和氧气的供应量,探究其对燃料电池性能的影响。
4. 实验结果与分析通过实验数据的收集和分析,我们可以得出以下结论:4.1 燃料电池的电压-电流特性曲线呈现出非线性关系。
随着电流的增大,电压呈现出逐渐下降的趋势。
这是因为在高电流下,电池内部的电阻会导致电压损失。
4.2 燃料电池的性能受到温度的影响较大。
在较低温度下,电池的性能较差,电压下降明显。
而在较高温度下,电池的性能相对较好,电压下降较小。
4.3 燃料电池的性能也受到燃料和氧气供应量的影响。
当燃料供应量不足时,电池的电压下降明显;而当氧气供应量不足时,电压下降较小。
5. 实验结论通过本次实验,我们对燃料电池的特性有了更深入的了解。
我们发现燃料电池的电压-电流特性曲线呈现非线性关系,受到温度和燃料、氧气供应量的影响较大。
这些研究结果为燃料电池的进一步应用和优化提供了重要的参考。
6. 实验总结本次实验通过对燃料电池的特性进行综合实验,深入了解了其工作原理和性能特点。

燃料电池综合特性实验实验报告一、引言。
燃料电池是一种将化学能直接转换为电能的高效能源转换装置,具有高能量密度、低污染、无噪音等优点,因此受到了广泛关注。
燃料电池的综合特性实验旨在对燃料电池的性能进行全面评价,为其在实际应用中的推广提供参考。
二、实验目的。
本实验旨在通过对燃料电池的综合特性进行测试,掌握燃料电池的工作原理和性能特点,为燃料电池在能源领域的应用提供实验数据支持。
三、实验原理。
燃料电池是一种将氢气和氧气直接转化为电能和热能的装置,其工作原理是通过氢气在阳极催化剂表面的氧化反应产生电子和氢离子,电子通过外部电路流向阴极,氢离子通过电解质膜传递到阴极,与氧气发生还原反应产生水。
在这一过程中,电子流动形成电流,完成电能的转换。
四、实验步骤。
1. 准备工作,将燃料电池系统组装好,连接好氢气和氧气的供应管路,并进行密封检查。
2. 实验前检测,对燃料电池系统进行电压、电流、温度等参数的检测,确保系统处于正常工作状态。
3. 实验过程,通过控制氢气和氧气的流量,调节燃料电池系统的工作状态,记录电压、电流、温度等参数的变化。
4. 数据处理,对实验得到的数据进行整理和分析,得出燃料电池的综合特性参数。
五、实验结果与分析。
通过实验,我们得到了燃料电池在不同工作状态下的电压、电流、温度等参数。
经过数据处理和分析,我们得出了燃料电池的极化曲线、功率曲线等综合特性参数。
通过对这些参数的分析,我们可以评价燃料电池的性能表现,为其在实际应用中提供参考。
六、结论。
通过本次实验,我们对燃料电池的综合特性进行了全面评价,掌握了其工作原理和性能特点。
实验结果表明,燃料电池具有较高的能量转换效率和稳定性,具有广阔的应用前景。
然而,燃料电池在实际应用中还存在一些问题,如催化剂的稳定性、材料的成本等,需要进一步研究和改进。
七、参考文献。
1. 郑伟,李明. 燃料电池综合特性实验[M]. 北京,化学工业出版社,2015.2. Smith, John. Comprehensive characteristics of fuel cells. Journal of Power Sources, 2018, 392(1): 123-135.八、致谢。
燃料电池综合特性测量实验
燃料电池是通过将燃料与空气经过一系列反应产生电能的器件。
燃料电池的运行原理
是在阳极和阴极分别注入燃料和氧气,通过质子交换膜传递电导致产生电流。
燃料电池具
有高效、清洁、低噪音、低污染等特点,广泛应用于汽车、航空航天、能源等领域。
因此,对燃料电池的综合特性进行测试是非常重要的。
本实验旨在研究燃料电池的性能参数,其中包括开路电压、最大功率点、内电阻等指标,以及电池的稳定性和寿命等特性。
本实验采用市面上较为常见的质子交换膜燃料电池,利用多种测试方法对其进行测量。
在实验过程中,首先需要进行电化学测试。
通过分别在不同条件下测量出燃料电池的
开路电压和内电阻,并记录输出电流及其对应的电压值,计算出电池各项基本参数;同时,还需要在不同负载下,测试出燃料电池的最大功率点。
此外,为了研究电池的耐用性,需
要对其进行寿命测试,包括电化学循环测试和长时间运行测试。
在电化学循环测试中,通
过将电池循环充放电100次,并检测电池的状况,以评估电池的稳定性;在长时间运行测
试中,将电池长时间通电运行,并记录其输出的电流值和电压值,以测量电池的寿命。
通过上述测试,可以得出燃料电池的诸多性能参数,并对其稳定性和耐用性进行评估。
实验结果表明,该燃料电池的开路电压稳定在0.6V左右,最大功率点在4A左右,电池内
电阻较小,为0.1欧姆左右。
在100次循环测试中,电池的稳定性良好,且寿命也较长,
运行良好。
总之,本实验通过多种测试方法对燃料电池的特性进行了全面研究,为进一步完善燃
料电池技术提供了有益的参考。
燃料电池综合特性实验
一、准备
1.加水:打开气水塔连通管,加水至上、下限之间,关闭水连通管。
2. 电流源输出端串连电流表后接入电解池,将电压表并联到电解池两端。
3. 关闭气水塔输气管止水夹,调节恒流源输出到最大(顺时针到底)。
当气水塔下层的气体低于最低刻度线的时候,打开气水塔输气管止水夹,排出气水塔下层的空气。
如此反复2~3次。
二、电解池的特性测量
1. 调节输出电流分别为100mA,200m,A300mA,待电解池输出气体稳定后
三、燃料电池输出特性的测量
1. 电解池输入电流保持在300mA,关闭风扇。
2. 电压测量端口接到燃料电池输出端。
打开气水塔输气管止水夹,等待10分钟,电压稳定后记录开路电压值。
3. 电流量程切换到200mA,超量程切换到2A。
负载调至最大,电流测量端口与可变负载串联后接入燃料电池输出端,改变负载,稳定后记录电压、电流值。
每测量一个点需稳定约5分钟。
燃料电池的最大输出功率和最大输出功率时对应的效率是多少?
四、太阳能电池的特性测量
1. 电流测量端口与可变负载(调至最大)串联后接入太阳能电池的输出端,电压表并联到太阳能电池两端。
太阳能电池的开路电压U oc,短路电流I sc是多少?最大输出功率p m是多少?最大工作电压U m,最大工作电流I m是多少?填充因子FF是多少?。
燃料电池综合特性实验实验报告燃料电池是一种能够将化学能转化为电能的设备,具有高能量密度、零排放、低噪音等优点,因此在交通运输、能源存储等领域具有广阔的应用前景。
为了深入了解燃料电池的性能特点,我们进行了一系列的实验研究,旨在探究燃料电池的综合特性。
首先,我们对燃料电池进行了基本的特性测试。
实验结果显示,燃料电池具有较高的能量转化效率,能够将化学能转化为电能的效率高达90%以上。
同时,燃料电池的响应速度也较快,能够在短时间内输出稳定的电能。
这些特性使得燃料电池在需要高能量密度和快速响应的场合具有明显的优势。
其次,我们对燃料电池的耐久性进行了测试。
实验结果表明,燃料电池在长时间工作后并未出现明显的性能下降,稳定性较好。
这意味着燃料电池具有较长的使用寿命,能够在实际应用中保持稳定的性能表现。
此外,我们还对燃料电池的适应性进行了测试。
实验结果显示,燃料电池在不同工况下均能够保持较好的性能表现,无论是在高温、低温、高湿度、低湿度等环境条件下,燃料电池均能够正常工作,并输出稳定的电能。
这表明燃料电池具有较强的环境适应性,能够适应复杂多变的工作环境。
综合上述实验结果,我们可以得出结论,燃料电池具有较高的能量转化效率、较好的耐久性和较强的环境适应性,适用于多种应用场景。
然而,也需要注意到燃料电池在实际应用中仍面临着一些挑战,比如催化剂的稳定性、氢气的储存与输送等问题。
因此,未来的燃料电池研究仍需进一步深入,以提升其性能并推动其广泛应用。
总之,通过本次实验,我们对燃料电池的综合特性有了更深入的了解,这对于进一步推动燃料电池技术的发展具有重要意义。
希望通过我们的努力,能够为燃料电池技术的进步贡献一份力量。
燃料电池综合特性实验燃料电池是一种将氢气或可燃气体转化为电能的能源转换装置,其综合特性包括以下几个方面。
1. 燃料电池的能量效率燃料电池的能量效率是指其将燃料的化学能转化为电能的效率。
一般来说,燃料电池的能量效率较高,在理论上可达到60%以上。
而传统的热机发电的能量效率仅为30%左右。
因此,燃料电池的能量效率是其优良的特性之一。
2. 燃料电池的环保特性燃料电池所使用的燃料是氢气或可燃气体,而且其发电过程仅产生水和少量的氮氧化物等有害物质,对环境污染较小,所以燃料电池具有优良的环保特性。
燃料电池的稳定性是指其在长时间运行中能够保持其性能稳定。
燃料电池是由多种材料组成的复杂系统,其中任何一个环节出现故障都会影响整个系统的稳定性。
因此,燃料电池的稳定性是其应用价值的一个重要方面。
燃料电池的功率密度是指其单位面积或体积的发电能力。
燃料电池的功率密度越高,其发电能力就越大。
目前,燃料电池的功率密度已经能够达到现实应用的级别,比如汽车燃料电池的功率密度已经能够达到100W/cm2以上。
燃料电池的经济性是指其生产成本与使用效益之间的关系。
由于目前燃料电池的生产成本较高,其经济性还存在待提高的空间。
但是,随着燃料电池技术的不断进步,其生产成本将会逐步降低,经济性将会逐步提高。
燃料电池综合特性实验可以通过对燃料电池的性能指标进行测试,来评价其是否符合实际应用的要求,并探究其改善方式。
例如,可以对燃料电池的能量效率、环保特性、稳定性、功率密度等进行测试和比较,如测试其输出电压和稳定性,分析其原因并进行改进。
这样能够帮助我们更好地了解燃料电池的特性,推动其技术进步与应用发展。
一、实验目的1. 了解燃料电池的工作原理,观察仪器的能量转换过程。
2. 测量燃料电池输出特性,计算燃料电池的最大输出功率及效率。
3. 验证法拉第电解定律。
4. 研究太阳能电池的特性,绘制伏安特性曲线。
二、实验原理1. 燃料电池工作原理:燃料电池是一种将燃料的化学能通过电化学反应直接转换成电能的装置。
燃料通常是氢气、甲醇、乙醇、天然气或其它的碳氢化合物,氧化剂则可以用空气中的氧。
反应生成物为水,对环境无污染。
2. 质子交换膜燃料电池(PEMFC):在常温下工作,其基本结构如图1所示。
全氟磺酸质子交换膜为固体聚合物薄膜,厚度0.05~0.1mm,提供氢离子(质子)传输通道。
3. 法拉第电解定律:电解过程中,通过电解质溶液的电荷传递,电解质中的离子在电极上发生氧化还原反应,从而产生电能。
法拉第电解定律描述了电解过程中电荷与化学当量之间的关系。
4. 太阳能电池:将光能直接转换为电能的半导体器件。
太阳能电池的伏安特性曲线反映了太阳能电池在不同光照条件下的输出特性。
三、实验器材1. 燃料电池实验装置2. 电源3. 测量仪器(电压表、电流表、功率计)4. 太阳能电池5. 照度计6. 线路连接器材四、实验步骤1. 燃料电池实验(1)连接燃料电池实验装置,确保氢气和氧气供应正常。
(2)打开电源,调节电压和电流,观察燃料电池输出特性。
(3)记录燃料电池在不同电压和电流下的输出电压、电流和功率。
(4)计算燃料电池的最大输出功率及效率。
2. 太阳能电池实验(1)连接太阳能电池,确保光照条件良好。
(2)使用照度计测量光照强度。
(3)调节电压和电流,观察太阳能电池输出特性。
(4)记录太阳能电池在不同光照条件下的输出电压、电流和功率。
(5)绘制太阳能电池的伏安特性曲线。
五、实验结果与分析1. 燃料电池实验根据实验数据,绘制燃料电池的输出特性曲线,计算最大输出功率和效率。
分析燃料电池在不同电压和电流下的性能变化,探讨影响燃料电池输出特性的因素。
燃料电池综合特性研究
————————————————————————————————作者:————————————————————————————————日期:
燃料电池综合特性研究
2014级光电信息科学与工程李盼园摘要
燃料电池是基于氧化还原反应的能源产生装置,包括基于质子交换膜的水电解过程和燃料电池反应。
本实验利用电解、气水塔等试验装置对质子交换膜电解池特性及燃料电池输出特性进行验证。
实验目的:
1.了解燃料电池的工作原理;
2.测量质子交换膜电解池特性,验证法拉第电解定律;
3.测量燃料电池的输出特性。
实验原理:
1.燃料电池
质子交换膜(PEM)燃料电池,在原理上相当于电解水的逆装置,其单电池由阳极、阴极和质子交换膜组成,阳极为氢燃料发生氧化的场所,阴极为氧化剂还原的场所,两级都含有加速电极电化学反应的
催化剂,质子交换膜作为电解质。
工作时相当于直流电源,其阳极为电源正极,阴极为电源负极。
基本结构如图1-1.
阳极的化学反应:进入阳极的氢气通过电极上的扩散层到达质子交换膜。
氢分子在阳极催化剂的作用下解离成两个氢离子,即质子,并释放出两个电子,阳极反应式为:+=-H H 2e 22 (1-1)
氢离子以水合质子+H (nH 2O)的形式,通过质子交换膜到达阴极,实现质子导电,质子的转移使阳极带负电。
阴极化学反应:氧气或者空气通过阴极扩散层到达阴极催化层,在阴极催化层的作用下,氧和氢离子和电子反应生成水,阴极反应式为:O H e H O 22244=+++ (1-2).
阴极反应使氧气得到氢离子和电子变成水,由于阴极上缺少电子而带正电,在阴极和阳极之间产生电压,如果阴阳极接通外电路,就可以向负载输出电能。
总的化学反应式为:O H O H 22222=+ (1-3)
图1-1
质子交换膜的优点是:发电过程不涉及氢氧燃烧,因而不受卡诺循环限制,转化效率高;不产生污染,无噪声。
他是一种清洁高效的绿色环保能源。
2.水的电解
燃料电池和电解池在电极制造上通常有些差别,燃料电池的电极应该更有利于气体吸纳,而电解池应尽快排出气体。
燃料电池的水应该尽快排出,以免堵塞 气体通道,而电解池的阳极必须淹没。
电解水的化学反应式为:↑+↑−−→−22222O H O H 电解
(1-4)
图1-2
实验仪器
实验仪器由实验主板、测试仪、可变负载、太阳能电池组成。
如图1-3.
实验主板由气水塔、燃料电池、电解池、负载组成。
氢气和氧气的水塔为电解池提供纯水(二次蒸馏水),同时储存电解池产生的氧气和氢气,为燃料电池提供燃料。
测试仪可测量电流和电压,可以从供电输出端口向电解池供电。
可变负载的变化范围为0.1~999.9Ω,最小间隔为0.1Ω。
图1-3
实验内容
1.质子交换膜电解池的特性研究
根据法拉第电解定律,生物生成物的量和输入的电量成正比。
在标准状态下(温度为0,一个大气压),设电解电流为I ,经过时间t 产生的氢气的体积的理论值为 升氢气4.22*2F It V =
,经温度和气压的修正为:升氢气4.22*2**16.27316.2730F
It P P T V +=
(1-5) 。
其中1231910*022.610*062.1,--===mol N e eN F 库仑,。
测量不同的输入电流I (如100mA,200mA,300mA...)下,对应的输入电压及产生的一定体积的氢气(如53cm )所需的时间t 。
分析在时间t 内氢气的产生量与电量It 的关系,氢气产生的测量值与理论
值之间的关系。
若不管输入电压和电流的大小,氢气产生的测量值与理论值成正比,且相近,即可验证法拉第定律。
2.燃料电池输出特性研究
燃料电池的输出电压和输出电流的关系,在电化学上称为极化特性曲线。
如图1-4
图1-4
由于燃料电池的能量不能完全转换为电能,总有一部分转换为热能,燃料分子形成短路电流等原因,燃料的开路电压低于理想电动势。
燃料的极化特性曲线由电化学极化区、欧姆极化区,浓差极化区构成。
综合考虑燃料电池的利用率(恒流供应燃料时可表示为燃料电池电流和电解电流之比),及输出电压和理想电动势之间的差异,燃料
电池的效率定义为%100*48
.1*%100*48.1*电解输出输出电解电池电池I P U I I ==η (1-6)。
实验测量时,使电解池的输入电流保持在300mA ,关闭风扇。
将电压测量端口接到燃料电池的输出端,打开燃料电池和水汽塔之间的氢气、氧气连接阀,等待约10分钟,让电池中的燃料浓度达到平衡值,电压稳定后记录开路电压值。
将电流表量程切换到200MA ,可变负载调至最大,电流测量端口与可变负载串联后接入燃料电池输出端,改变负载电阻的大小,调整不同的电压值,读出相应的电流值,绘制极化特性曲线。
实验要求:作出所测燃料电池的极化曲线;作出该电池输出功率随输出电压变化曲线;测出该燃料电池最大输出功率为多少?最大输出功率对应的效率是多少?
实验数据记录及处理
1.电解池特性研究
实验数据及处理如下表
表1-1
说明:由公式
升
氢气
4.
22
*
2
*
*
16
.
273
16
.
273
F
It
P
P
T
V
+
=
计算氢气产生理论
值,取T=17K,P0=P,统一以mL为单位。
分析:对比氢气产生的测量值和理论值,可以看出氢气产生理论量与电量成正比,而测量值由于实验存在误差而无明显相关性;氢气产生量的理论值与测量值的最大误差为3.3%,平均误差为1.6%,测量值与理论值基本接近,可大致验证法拉定律。
2.燃料电池输出特性研究
极化曲线:
开路电压为1.0V。
输出功率随输出电压变化曲线
由曲线可得,燃料电池的最大输出功率为U=0.439V,P=65.3671W。
电
解电流为300mA,对应的效率由公式1-6计算得
%
7.
14
=
η。
思考讨论
1.误差分析
在电解池的测量中,测量氢气的产生量时由于主观因素的作用误差较大,实验可通过测量较多的氢气产生量来减小误差; 在燃料电池的实验中输出电流并不稳定,给读数带来了不便,实验时应在电流表示数相对稳定时进行读数。
2.电解池产生氢气量和氧气量是什么关系?关闭氧气水塔与燃料电池的输气管,让燃料电池是否还可以继续发电?
根据电解池的化学反应式可得产生的氢气和氧气量是2:1的关系。
关闭氧气水塔和输气管后,输气管中还存有未反应的氧气,可以继续与氢气发生反应,消耗完后将停止反应。
3.为什么实验系统需要用去离子水或二次蒸馏水?
H与氧减少杂质离子和气体对实验的干扰。
燃料电池的实质是+
H来自与氢气的分解,若水中含有较多离子,则会气发生反应,而+
对氢气的测定产生干扰,若水中含有气体,也会对实验中气体的测定产生干扰。
附录:
实验数据
燃料电池的综合特性
I(mA) U(V) P*10-3(W)1.3 1.01 1.313
3.3 0.93 3.069
4.9 0.893 4.3757
8.9 0.831 7.3959 12.5 0.8 10
17.4 0.764 13.2936 30.6 0.701 21.4506 34.7 0.687 23.8389
38 0.676 25.688
39 0.674 26.286
40.3 0.669 26.9607
42.1 0.665 27.9965
43 0.662 28.466
44.2 0.658 29.0836 46.8 0.65 30.42 49.9 0.643 32.0857 53.3 0.634 33.7922
57.2 0.624 35.6928
58 0.621 36.018 61.7 0.612 37.7604 63.7 0.606 38.6022 67.2 0.6 40.32 73.9 0.586 43.3054 82 0.569 46.658 92.3 0.548 50.5804 106 0.523 55.438 123.9 0.489 60.5871 148.9 0.439 65.3671 192.3 0.298 57.3054 198.4 0.188 37.2992。