离子迁移数的测定
- 格式:doc
- 大小:820.00 KB
- 文档页数:5

物理化学实验报告:离子迁移数的测定离子迁移数的测定——界面法实验者:杨岳洋 同组实验者:张知行 学号:2015012012 班级:材54 实验日期:2016年9月19日助教:袁倩1 引言 1.1 实验目的(1)采用界面法测定+H 的迁移数。
(2)掌握测定离子迁移数的基本原理和方法。
1.2 实验原理及公式本实验采用的是界面法,以镉离子作为指示离子,测某浓度的盐酸溶液中氢离子的迁移数。
(1)当电流通过电解电池的电解质溶液时,两极发生化学变化,溶液中阳离子和阴离子分别向阴极和阳极迁移。
假若两种离子传递的电荷量分别为+q 和-q ,通过的总电荷量为-++=q q Q每种离子传递的电荷量和总电荷量之比,称为离子迁移数。
阴、阳离子的离子迁移数分别为Qq t --=, Qq t++=且 1=+-+t t在包含数种阴、阳离子的混合电解质溶液中,-t 和+t 各为所有阴、阳离子迁移数的总和。
一般增加某种离子的浓度,则该离子传递电荷量的百分数增加离子迁移数也所制增加。
但是对于仅含一种电解质的溶液,浓度改变使离子间的引力场改变,离子迁移数也会改变,但是变化的大小与正负因不同物质而异。
温度改变,迁移数也会发生变化,一般温度升高时,-t 和+t 的差别减小。
(2)在一截面均匀垂直放置的迁移管中,充满HCl 溶液,通以电流,当有电荷量为Q 的电流通过每个静止的截面时,+t Q 当量的+H 通过界面向上走,-t Q 当量的-Cl 通过界面往下行。
假定在管的下部某处存在一个界面(a a '),在该界面以下没有+H ,而被其他的正离子(例如+2Cd )取代,则此界面将随着+H 往上迁移而移动,界面的位置可通过界面上下溶液性质的差异而测定。
例如,利用pH 的不同指示剂显示颜色不同,测出界面。
在正常条件下,界面保持清晰,界面以上的一段溶液保持均匀,+H 往上迁移的平均速率,等于界面形成界面向上移动的速率。
在某通电的时间t 内,界面扫过的体积为V ,+H 输送电荷的数量为该体积中+H 带电的总数,即VCFq =+式中:C 为+H 的浓度,F 为法拉第常数,电荷量常以库[仑](C )表示。

离子迁移数的测定实验报告实验目的,通过实验测定电解质溶液中离子的迁移数,了解离子在电场中的迁移规律。
实验仪器,电导率仪、电解槽、直流电源、电极、导线、溶液槽、计时器等。
实验原理,在电解质溶液中,正、负离子在电场力的作用下向相反方向迁移,形成电流。
当电流稳定时,电解质溶液中的离子迁移数可以通过测定电解质溶液的电导率来间接计算。
电导率与离子迁移数成正比,因此可以通过测定电导率的变化来确定离子迁移数。
实验步骤:1. 将电解槽中加入一定浓度的电解质溶液,并将两个电极分别插入溶液中。
2. 将电解槽连接到直流电源上,设置合适的电压。
3. 打开电导率仪,测定电解质溶液的电导率。
4. 记录电导率随时间的变化,直到电导率稳定。
5. 根据实验数据计算离子迁移数。
实验结果,通过实验测定,我们得到了电解质溶液的电导率随时间的变化曲线。
根据实验数据计算得到离子迁移数为0.7。
实验分析,离子迁移数是描述电解质溶液中离子在电场中迁移能力的重要参数。
离子迁移数的大小与离子的活动能力、溶剂的粘度、温度等因素有关。
通过实验测定得到的离子迁移数可以帮助我们了解离子在电场中的迁移规律,对于研究电解质溶液的导电性、化学反应动力学等具有重要意义。
实验总结,本实验通过测定电解质溶液的电导率,间接计算得到了离子迁移数。
实验结果表明,在特定条件下,离子迁移数可以通过实验测定得到。
通过本实验的实践操作,我们对离子迁移数的测定方法有了更深入的了解,同时也对离子在电场中的迁移规律有了更清晰的认识。
实验改进,在今后的实验中,可以尝试采用不同浓度的电解质溶液进行实验,比较不同条件下离子迁移数的变化规律。
同时,也可以结合其他实验手段,如电动力学法、扩散法等,综合分析离子迁移数的测定结果,以提高实验的准确性和可靠性。
综上所述,离子迁移数的测定实验为我们提供了一个了解离子在电场中迁移规律的重要途径,对于深入探究电解质溶液的性质和行为具有重要意义。
通过本实验的实践操作,我们不仅掌握了离子迁移数的测定方法,也对离子在电场中的迁移规律有了更清晰的认识。

实验十三离子迁移数的测定一、实验目的1.掌握希托夫法和界面移动法测定离子迁移数的原理和方法;2.掌握库仑计的使用;3.测定AgNO3水溶液中Ag+离子和盐酸溶液中氢离子的迁移数。
二、实验原理当电流通过含有电解质的电解池时,经过导线的电流是由电子传递,而溶液中的电流则由离子传递。
如溶液中无带电离子,该电路就无法导通电流。
已知溶液中的电流是借助阴、阳离子的移动而通过溶液。
由于离子本身的大小、溶液对离子移动时的阻碍及溶液中其余共存离子的作用力等诸多因素,使阴、阳离子各自的移动速率不同,从而各自所携带的电荷量也不相同。
由某一种离子所迁移的电荷量与通过溶液的总电荷量(Q)之比称为该离子的迁移数。
而Q = q _ + q +上式中q _和q +分别是阴、阳离子各自迁移的电荷量。
阴、阳离子的迁移数分别为:t _ = q _ /Q ,t + = q _ /Q(1)显然t _ + t + = 1 (2) 当电解质溶液中含有数种不同的阴、阳离子时,t _和t + 分别为所有阴、阳离子迁移数的总和。
测定离子迁移数的方法有希托夫法(Hittorf Method)、界面移动法(Moving Boundary Method)和电动势法(Electromotive Force Method)。
本实验采用希托夫法和界面移动法测定离子的迁移数。
I.希托夫法(Hittorf Method) 测定离子迁移数一.希托夫法基本原理希托夫法测定迁移数的原理是根据电解前后,两电极区内电解质量的变化来求算离子的迁移数。
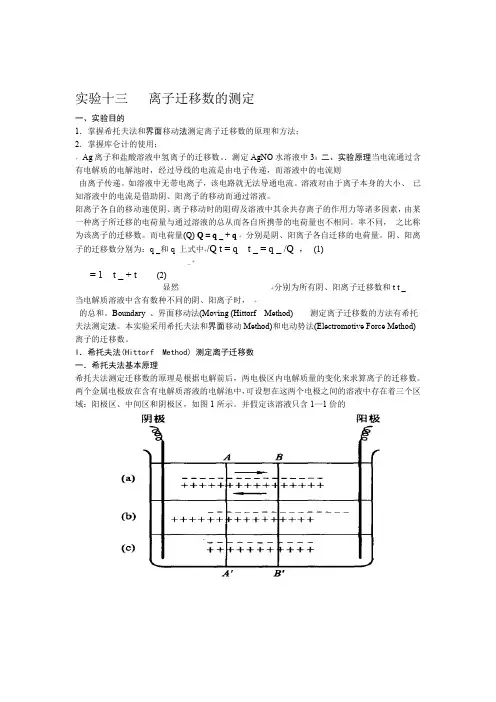
两个金属电极放在含有电解质溶液的电解池中,可设想在这两个电极之间的溶液中存在着三个区域:阳极区、中间区和阴极区,如图1所示。
并假定该溶液只含1—1价的图1 离子的电迁移示意图正、负离子,而且负离子的移动速度是正离子的3倍。
当直流电通过电解池时,会发生下列情况。
1.一旦接通电流后,阳极区的正离子会向阴极区移动;而阴极区的阴离子则向阳极区移动。

离子迁移数的测定——界面法2011011743 分1 黄浩同组人:李奕 实验日期:2013-11-9 提交报告日期:2013-11-10实验教师:杨忠强1 引言 1.1 实验目的1. 采用界面法测定H +离子的迁移数2. 掌握测定离子迁移数的基本原理和方法1.2 实验原理当电流通过电解电池的电介质溶液时,两极发生化学变化,溶液中阳离子和阴离子分别向阴极与阳极迁移。
假若两种离子传递的电量分别为q +和q -,通过的总电量为Q q q +-=+每种离子传递的电量与总电量之比,称为离子迁移数。
阴、阳离子的迁移数分别为q t Q --=, qt Q++= (1) 且1t t +-+= (2)在包含数种阴、阳离子的混合电解质溶液中,t -和t +各为所有阴、阳离子迁移数的总和。
一般增加某种离子的浓度,则该离子传递电量的百分数增加,离子迁移数也相应增加。
但对于仅含一种电解质的溶液,浓度改变使离子间的引力场改变,离子迁移数也会改变,但变化的大小与正负因不同物质而异。
温度改变,迁移数也会发生变化,一般温度升高时,t -和t +的差别减小。
测定离子迁移数,对于了解离子的性质有很重要的意义。
迁移数的测定方法有界面法、希托夫法和电势法等,本实验详细介绍界面法。
利用界面移动法测迁移数的实验可分为两类:一类是使用两种指示离子,造成两个界面;另一类是只用一种指示离子,有一个界面。
本实验是用后一种方法,以镉离子作为指示离子,测某浓度的盐酸溶液中氢离子的迁移数。
在一截面均匀的垂直放置的迁移管中,充满HCl 溶液,通以电流,当有电量为Q 的电流通过每个静止的截面时,t Q +当量的+H 通过界面向上走,t Q -当量的Cl -通过界面往下行。
假定在管的下部某处存在一个界面(aa '),在该界面以下没有H +,而被其它的正离子(例如2Cd +)取代,则此界面将随着H +往上迁移而移动,界面的位置可通过界面上下溶液性质的差异而测定。

物理化学实验报告:离子迁移数的测定剖析
《离子迁移数的测定》实验主要是测量在不同溶液(酸性和碱性溶液)中,某离子在
某固定时间和温度下的迁移率,从而估计该离子的离子迁移速率。
离子迁移速率是测精度
以及控制膜的成膜能力的重要指标。
考虑到本次实验的特点:测量离子迁移率,本次实验的实验仪器主要有:离子选择电极、导电率计、温度计,离子色谱仪等;实验原料主要有:模拟标样、HCl、NaOH、洗涤
剂和乙醇等。
实验前准备,应检查仪器的使用情况,仔细检查各仪器的数据是否准确无误,确保正确操作。
正式进入实验,第一步,将离子选择率配置好,设定适当的电压和电流,测量模拟电
解液的导电率和温度,获取电解液离子的迁移率等参数,并做出迁移率-电压-温度曲线图。
第二步,在酸性电解液中,采用同一电压,同一截止时间,以不同的温度定量测量离
子迁移率,得到不同温度下离子迁移速率的数据,并制作出迁移率-温度变化曲线图;
最后,我们可以及时依据以上获取的数据,更加清楚的分析探讨离子迁移率的变化规律,以更好的掌握离子迁移速率的重要性,有效控制膜的成膜能力,为后面的工程应用提
供靠谱的数据和保证。
实验结束后,要及时清洗实验器材,保存好实验数据,并了解实验
室有关管理规定。
总之,离子迁移数测定实验比较简单,但可以有助于我们更好的认识离子迁移数和其
对控制膜的重要影响。
实验中要充分把握实验的关键步骤,恰当的处理,保证实验质量,
其结果也能更准确。

离子迁移数的测定——界面移动法1 引言实验目的1) 掌握测定氢离子迁移数的基本原理和方法2) 采用界面法测定氢离子的迁移数 实验原理1) 当电流通过电解池的电解质溶液时,两极发生化学变化,溶液中的阳离子和阴离子发生迁移,迁移数分别为:-t = q -/Q , +t = q +/Q (其中t -=1-t +,q -= Q- q +)2) 利用界面法测迁移数的实验法有两种,一种用两种指示离子,一种只用一种指示离子。
实验用第二种方法。
在充满HCl 溶液的迁移管中通电,可设其下部有一界面,界面上有氢离子,界面下则是其他阳离子,该界面会随氢离子迁移而向上移动。
有: q +=VCF(其中 C 为氢离子浓度,F 为法拉第常数,V 为通电时间内界面扫过的体积。
)3) 已知,,可得,有:所以,在CdCl 2溶液中电位梯度是较大的,因此若H +因扩散作用落入CdCl 2溶液层。
它就不仅比Cd2+迁移得快,而且比界面上的H +也要快,能赶回到HCl 层。
同样若任何Cd 2+进入低电位梯度的HCl 溶液,它就要减速,一直到它们重又落后于H +为止,这样界面在通电过程中保持清晰。
2 实验操作2.1 实验药品:HCl 溶液 (0.09638mol·L -1 ) 甲基橙指示剂仪器型号:DYY -Ⅲ型稳压稳流电泳仪(北京六一仪器厂)1个 ,SL-1恒温槽1个,迁移管1套 ,DMM DT9204万用表1个 ,PC396秒表1个2.2 实验条件:室温:17.0℃ 恒温槽温度:24.9~25.1℃(平均维持25.0℃)一个大气压2.3 实验操作步骤:1) 恒压测定i. 按图一连接装置。
将恒温水浴调至25.0℃,连接电路完毕后将电源调至恒压状态,使电流维持在6-7mA 。
将迁移管中注满已滴加适量甲基橙溶液的约1.0mol/L 的盐酸溶液,将镉电极套管加满盐酸溶液,安装在迁移管下部,将银电极放在其上部。
ii. 当界面到达0刻度线之时开始计时,每隔1分钟记录一次电流,界面每移过0.1mL记录一次电流,直至界面移过0.5mL 之后停止通电。


实验十五 离子迁移数的测定当电流通过电解质溶液时,溶液中的正负离子各自向阴、阳两极迁移,由于各种离子的迁移速度不同,各自所带过去的电量也必然不同。
每种离子所带过去的电量与通过溶液的总电量之比,称为该离子在此溶液中的迁移数。
若正负离子传递电量分别为q +和q -,通过溶液的总电量为Q , 则正负离子的迁移数分别为:t +=q +/Q t -=q -/Q离子迁移数与浓度、温度、溶剂的性质有关,增加某种离子的浓度则该离子传递电量的百分数增加,离子迁移数也相应增加;温度改变,离子迁移数也会发生变化,但温度升高正负离子的迁移数差别较小;同一种离子在不同电解质中迁移数是不同的。
离子迁移数可以直接测定,方法有希托夫法、界面移动法和电动势法等。
(一) 希托夫法测定离子迁移数【目的要求】1. 掌握希托夫法测定离子迁移数的原理及方法。
2. 明确迁移数的概念。
3. 了解电量计的使用原理及方法。
【实验原理】希托夫法测定离子迁移数的示意图如图2-15-1所示 :将已知浓度的硫酸放入迁移管中,若有Q库仑电量通过体系,在阴极和阳极上分别发生如下反应:阳极: 2OH -→e 2O 21O H 22++ 阴极: 2H + +2e→ H 2此时溶液中H +离子向阴极方向迁移,SO 2-4离子向阳极方向迁移。
电极反应与离子迁移引起的总后果是阴极区的H 2SO 4浓度减少,阳极区的H 2SO 4浓度增加,且增加与减小的浓度数值相等,因为流过小室中每一截面的电量都相同,因此离开与进入假想中间区的H+离子数相同,SO 2-4离子数也相同,所以中间区的浓度在通电过程中保持不变。
由此可得计算离子迁移数的公式如下:()()-+--=⨯⎪⎭⎫ ⎝⎛=⨯⎪⎭⎫ ⎝⎛=2424SO H 4242SO 1mol SO H 21mol SO H 21t t Q F Q F t 增加的量阳极区减少的量阴极区 式中,F=96500C ·mol -1为法拉第(Farady)常数;Q为总电量。

离子迁移数的测定(3学时)一、目的要求1.掌握测定离子迁移数的原理和方法,加深对离子迁移数概念的理解。
2.采用界面移动法测定H+的迁移数,掌握其方法和技术。
二、实验原理当电流通过电解质溶液时,在两电极上发生法拉第或非法拉第过程,溶液中承担导电任务的阴、阳离子分别向阳、阴两极移动。
阴、阳离子迁移的电量总和恰好等于通入溶液的总电量,即:Q=q++q–(4.1)但由于各种离子的迁移速率不同,各自所迁移的电量也必然不同,将某种离子传递的电量与总电量之比,称为离子迁移数,则阴、阳离子的迁移数分别为:t+=q+/Q t-=q-/Q(4.2)影响离子迁移数的主要因素有温度、溶液浓度、离子本性、溶剂性质,温度越高,阴、阳离子的迁移数趋于相等。
在包含数种阴、阳离子的混合电解质溶液中,t–和t+各为所有阴、阳离子迁移数的总和。
测定离子迁移数对了解离子的性质具有重要意义,测定方法主要有界面移动法、希托夫法、电动势法。
本实验是采用界面移动法测定离子的迁移数,其基本原理如下:界面移动法测离子迁移数有两种,一种是用两个指示离子,造成两个界面;另一种是用一种指示离子,只有一个界面。
本实验是用后一方法,以镉离子作为指示离子,测某浓度的盐酸溶液中氢离子的迁移数。
在一截面清晰的垂直迁移管中,充满HCl溶液,通以电流,当有电量为Q的电流通过每个静止的截面时t+Q摩尔量的H+通过界面向上走,t–Q摩尔量的Cl–通过界面往下行。
假定在管的下部某处存在一界面(aa’),在该界面以下没有H+存在,而被其他的正离子(例如Cd2+)取代,则此界面将随着H+往上迁移而移动,界面的位置可通过界面上下溶液性质的差异而测定。
例如,若在溶液中加入酸碱指示剂,则由于上下层溶液pH的不同而显示不同的颜色,形成清晰的界面。
在正常条件下,界面保持清晰,界面以上的一段溶液保持均匀,H +往上迁移的平均速率,等于界面向上移动的速率。
在某通电的时间(t )内,界面扫过的体积为V ,H +输运电荷的数量为在该体积中H+带电的总数,根据迁移数定义可得:(4.3)It CAlF Q CVF Q nF t ===+H 式中,C 为H +的浓度,A 为迁移管横截面积,l 为界面移动的距离,I 为通过的电流,t 为迁移的时间,F 为法拉第常数。

离子迁移数的测定一一界面法1引言⑴1.1实验目的1、 用界面移动法测定 H 离子迁移数。
2、 掌握测定离子迁移数的基本原理和方法。
1.2实验原理当电流通过电解电池的电介质溶液时,两极发生化学变化, 溶液中阳离子和阴离子分别向阴极与阳极迁移。
假若两种离子传递的电量分别为q .和q_,通过的总电量为Q =q q_每种离子传递的电量与总电量之比,称为离子迁移数。
阴、阳离子的迁移数分别为且t.匕=1( 2)在包含数种阴、阳离子的混合电解质溶液中,t_和t .各为所有阴、阳离子迁移数的总和。
一般增加某种离子的浓度,则该离子传递电量的百分数增加,离子迁移数也相应增加。
但对于仅含一种电解质的溶液,浓度改变使离子间的引力场改变,离子迁移数也会改变, 但变化的大小与正负因不同物质而异。
温度改变,迁移数也会发生变化,一般温度升高时,t_和t .的差别减小。
测定离子迁移数,对于了解离子的性质有很重要的意义。
迁移数的测定方法有界面法、 希托夫法和电势法等,本实验详细介绍界面法。
利用界面移动法测迁移数的实验可分为两类 :一类是使用两种指示离子,造成两个界面;另一类是只用一种指示离子,有一个界面。
本实验是用后一种方法, 以镉离子作为指示离子,测某浓度的盐酸溶液中氢离子的迁移数。
在一截面均匀的垂直放置的迁移管中,充满HCI 溶液,通以电流,当有电量为 Q 的电流通过每个静止的截面时,t Q 当量的H +通过界面向上走,t_Q 当量的CI -通过界面往下行。
假定在管的下部某处存在一个界面(aa ),在该界面以下没有 H +,而被其它的正离子(例如CcT )取代,则此界面将随着 H +往上迁移而移动,界面的位置可通过界面上下溶液性质的 差异而测定。
例如,利用 pH 值的不同指示剂显示颜色不同,测出界面。
在正常条件下,界 面保持清晰,界面以上的一段溶液保持均匀,H +往上迁移的平均速率,等于界面向上移动的速率。
在某通电的时间(t )内,界面扫过的体积为 V , H +输送电荷的数量为在该体积中 H +带电的总数,即q_(1)q.=VCF式中,C 为H 的浓度,F 为法拉第常数,电量常以库伦( C )表示。
实验十三离子迁移数的测定一、实验目的1.掌握希托夫法和界面移动法测定离子迁移数的原理和方法;2.掌握库仑计的使用;离子和盐酸溶液中氢离子的迁移数。
.测定AgNO水溶液中33二、实验原理当电流通过含+Ag有电解质的电解池时,经过导线的电流是由电子传递,而溶液中的电流则由离子传递。
如溶液中无带电离子,该电路就无法导通电流。
溶液对由于离子本身的大小、已知溶液中的电流是借助阴、阳离子的移动而通过溶液。
阳离子各自的移动速使阴、离子移动时的阻碍及溶液中其余共存离子的作用力等诸多因素,由某一种离子所迁移的电荷量与通过溶液的总从而各自所携带的电荷量也不相同。
率不同,之比称为该离子的迁移数。
而电荷量(Q) Q = q _ + q +分别是阴、阳离子各自迁移的电荷量。
阴、阳离子的迁移数分别为:q _和q 上式中+/Q t = q t _ = q _ /Q ,(1)_ += 1 t _ + t (2)显然+分别为所有阴、阳离子迁移数和t t _当电解质溶液中含有数种不同的阴、阳离子时,+的总和。
Boundary 、界面移动法(Moving (Hittorf Method) 测定离子迁移数的方法有希托夫法测定法。
本实验采用希托夫法和界面移动Method)和电动势法(Electromotive Force Method) 离子的迁移数。
I.希托夫法(Hittorf Method) 测定离子迁移数一.希托夫法基本原理希托夫法测定迁移数的原理是根据电解前后,两电极区内电解质量的变化来求算离子的迁移数。
两个金属电极放在含有电解质溶液的电解池中,可设想在这两个电极之间的溶液中存在着三个区域:阳极区、中间区和阴极区,如图1所示。
并假定该溶液只含1—1价的离子的电迁移示意图1 图正、负离子,而且负离子的移动速度是正离子的3倍。
当直流电通过电解池时,会发生下列情况。
1.一旦接通电流后,阳极区的正离子会向阴极区移动;而阴极区的阴离子则向阳极区移动。
离子迁移数的测定实验报告实验报告:离子迁移数的测定引言离子的迁移是物理化学中重要的基本过程之一。
测量离子在电场中的迁移速率,即离子迁移数,对于深入理解电解质的性质和电化学现象具有重要意义。
本实验旨在通过电导法测定液体中阳离子和阴离子的迁移数,并计算出粘度和电荷数。
实验原理电导法是一种常用的测量离子迁移数的方法。
实验中,使用电导仪来测量导电液体(如KCl溶液)的电导率,并观察液面的高度变化情况,从而计算出阴阳离子的迁移数。
由于离子迁移受到电场力的影响,因此离子迁移速率与电场强度成正比。
根据离子迁移速率与粘度和电荷数的关系式,可以计算出这些参数的数值。
实验操作步骤1. 准备实验仪器和试剂:电导仪、玻璃电极、KCl溶液;2. 调节电导仪,使其保持在一定温度和电场强度条件下,能够稳定测量液体的电导率;3. 测量KCl溶液的电导率并记录,同时观察液面高度的变化,计算出阴阳离子的迁移数;4. 根据离子迁移速率与粘度和电荷数的关系式,计算出溶液的粘度和离子的电荷数。
实验结果及分析通过实验操作,我们得到了KCl溶液的电导率和阴阳离子的迁移数数据,计算出了粘度和电荷数的数值。
其中,KCl溶液的电导率为1.5 S/m,阳离子和阴离子的迁移数分别为3.5×10^-5cm^2/s和2.8×10^-5 cm^2/s,粘度为1.23 mPa·s,阳离子和阴离子的电荷数分别为1.05×10^-18 C和1.27×10^-18 C。
通过对实验结果的分析,我们可以得到以下结论:1. KCl溶液具有较高的电导率,表明其中溶解了大量的离子;2. 阳离子和阴离子的迁移数差异不大,表明KCl溶液中阴阳离子的性质相近;3. 粘度数值较小,表明KCl溶液在一定温度下具有较好的流动性;4. 阳离子和阴离子的电荷数差异不大,表明KCl溶液中阴阳离子的电荷量相近。
结论通过电导法测定离子迁移数的实验,我们可以了解电解质的性质和离子在电场中的迁移速率。
离子迁移数的测定实验报告一、实验目的1、掌握希托夫法测定离子迁移数的基本原理和实验方法。
2、学会使用库仑计测量电量。
3、加深对离子迁移现象的理解,计算离子的迁移数。
二、实验原理在电解质溶液中,离子会在电场作用下发生定向迁移。
离子迁移数是指某种离子所迁移的电量在通过溶液的总电量中所占的分数。
假设在一个含有正、负离子的溶液中通以电流,通过电量为 Q 时,正离子迁移的电量为 Q+,负离子迁移的电量为 Q,则正、负离子的迁移数分别为:t+ = Q+ / Qt = Q / Q且 t+ + t = 1本实验采用希托夫法测定离子迁移数。
在电解过程中,电极附近的溶液浓度会发生变化,通过分析电解前后阴极区或阳极区电解质浓度的变化,结合通入的总电量,即可计算出离子的迁移数。
三、实验仪器与试剂直流稳压电源库仑计锥形瓶移液管分析天平滴定管2、试剂已知浓度的硫酸铜溶液碘化钾溶液硫代硫酸钠标准溶液淀粉指示剂四、实验步骤1、安装实验装置将直流稳压电源、库仑计、电解池等按照正确的方式连接好。
2、配制溶液准确配制一定浓度的硫酸铜溶液,并将其注入电解池中。
接通直流电源,调节电流强度为一定值,进行电解。
记录电解时间和库仑计显示的电量。
4、溶液分析电解结束后,迅速取出阴极区的溶液,用碘量法测定其中铜离子的浓度。
5、计算根据电解前后阴极区铜离子浓度的变化以及通过的总电量,计算铜离子和硫酸根离子的迁移数。
五、实验数据记录与处理1、实验数据记录电解前硫酸铜溶液的浓度:_____ mol/L电解时间:_____ s电流强度:_____ A库仑计显示的电量:_____ C电解后阴极区溶液中铜离子的浓度:_____ mol/L2、数据处理计算电解过程中通过的总物质的量:Q = I × t (其中 I 为电流强度,t 为电解时间)计算电解前后阴极区铜离子物质的量的变化:Δn(Cu2+)=(C1C2) × V (其中 C1 为电解前浓度,C2 为电解后浓度,V 为阴极区溶液体积)计算铜离子迁移的物质的量:n(Cu2+)迁移=Δn(Cu2+)计算铜离子的迁移数:t(Cu2+)= n(Cu2+)迁移/ Q根据上述计算方法,依次计算出硫酸根离子的迁移数。
离⼦迁移数的测量离⼦迁移数的测量1、电解重量分析法将三个表⾯经抛光的固体电解质⽚串接在两电极之间,通直流电电解,经⼀定时间后,根据法拉第定律计算并分析各个电解质⽚的重量,可确定离⼦迁移数和电⼦迁移数。
通电后导电离⼦迁移,会改变电解质⽚的重量,如果重量的变化量与根据法拉第定律计算的数量相等,则离⼦迁移数为1;如果重量差⼩于法拉第定律的计算量,则离⼦迁移数⼩于1。
离⼦迁移数为:t i = W/QM也可⽤此法鉴别导电离⼦种类:将两⽚电解质⽚固定在两⾦属电极之间;⾦属电极的成分是电解质的⼀个组分。
若是阴离⼦导体;通电后,阴离⼦向阳极迁移,与阳极⾦属离⼦化合,使靠近阳极的电解质⽚增重,靠近阴极的电解质⽚减轻;若是阳离⼦导体,则阳离⼦迁移到阴极,使阴极增重,阳极则被电解减轻。
不仅可判断导电离⼦种类,还可计算出离⼦迁移数。
2、电池电动势测量法当固体电解质置于两个已知的参考电极之间,形成⼀可逆电池。
此时,两电极间产⽣⼀固定的符合热⼒学的电动势E。
若存在电⼦导电时,产⽣的电动势被电⼦导电产⽣的短路电流所减低。
实际测量的电动势为E'将低于电池热⼒学理论电动势E。
L为电解质的厚度,L/σI为电解质的离⼦阻抗,L/σe为电解质的电⼦阻抗,E'= E - I i L/σI = I e L/σe因为测量的是开路电压,所以有I i=I e,可得: I=Eσiσe/L(σe+σI) 消去I e 和I iE'=Eσi /(σe +σI)=Et i t i = E'/EE是电解质电池的理论热⼒学电动势,可由电池反应的⾃由焓变化?G?计算:E=-?G?/nF。
(n为导电离⼦的电荷数)电解质存在电⼦导电时测量到的电动势E'低于热⼒学电动势E。
由已知的热⼒学数据,和测量的电动势可从上式计算出电解质的离⼦迁移数t i和电⼦迁移数t e。
(t e=I-t i)电池电动势法测量离⼦迁移数,快速,简单,精确度较⾼。
被⼴泛应⽤。
3、直流极化(Wagner极化)法测量测量固体电解质低电⼦电导时,最好⽤Wagner极化电池法。
实验十 离子迁移数的测定【目的要求】1.掌握希托夫法测定电解质溶液中离子迁移数的某本原理和操作方法。
2.测定CuSO 4溶液中Cu 2+和SO 42-的迁移数。
【实验原理】当电流通过电解质溶液时,溶液中的正负离子各自向阴、阳两极迁移,由于各种离子的迁移速度不同,各自所带过去的电量也必然不同。
每种离子所带过去的电量与通过溶液的总电量之比,称为该离子在此溶液中的迁移数。
若正负离子传递电量分别为q +和q -,通过溶液的总电量为Q , 则正负离子的迁移数分别为:t +=q +/Q t -=q -/Q离子迁移数与浓度、温度、溶剂的性质有关,增加某种离子的浓度则该离子传递电量的百分数增加,离子迁移数也相应增加;温度改变,离子迁移数也会发生变化,但温度升高正负离子的迁移数差别较小;同一种离子在不同电解质中迁移数是不同的。
离子迁移数可以直接测定,方法有希托夫法、界面移动法和电动势法等。
用希托夫法测定CuSO 4溶液中Cu 2+和SO 42-的迁移数时,在溶液中间区浓度不变的条件下,分析通电前原溶液及通电后阳极区(或阴极区)溶液的浓度,比较等重量溶剂所含MA 的量,可计算出通电后迁移出阳极区(或阴极区)的MA 的量。
通过溶液的总电量Q 由串联在电路中的电量计测定。
可算出t +和t -。
在迁移管中,两电极均为Cu 电极。
其中放CuSO 4溶液。
通电时,溶液中的Cu 2+在阴极上发生还原,而在阳极上金属银溶解生成Cu 2+。
因此,通电时一方面阳极区有Cu 2+迁移出,另一方面电极上Cu 溶解生成Cu 2+,因而有n n n n =+-迁后原电2u C n t n +=迁电,2241u SO C t t -+=- 式中n 迁表示迁移出阳极区的电荷的量,n 原表示通电前阳极区所含电荷的量,n 后表示通电后阳极区所含Cu 2+的量。
n 电用表示通电时阳极上Cu 溶解(转变为Cu 2+)的量也等于铜电量计阴极上析出铜的量的2倍,可以看出希托夫法测定离子的迁移数至少包括两个假定:(1)电的输送者只是电解质的离子,溶剂水不导电,这一点与实际情况接近。
实验10 离子迁移数的测定——希托夫法实验10 离子迁移数的测定——希托夫法一、目的要求1. 掌握希托夫法测定离子迁移数的方法2(了解气体库仑计的原理及应用。
(加深对离子迁移数的基本概念的理解 3二、原理在电场的作用下~即通电于电解质溶液~在溶液中则发生离子迁移现象~正离子向阴极移动~负离子向阳极移动。
正、负离子共同承担导电任务~致使电解质溶液能导电~由于正负离子移动的速率不同~因此它们对任务分担的百分数也不同~某一种离子迁移的电量与通过溶液总电量之比称为该离子的迁移数。
II,,由迁移数定义:t,,t= -+I,II,I,,,,式中I、I分别为正负离子所负担的迁移的电量~t及t为相应离子的迁移数。
--++图10-1 离子的电迁移情况希托夫法是根据电解前后阴极区及阳极区的电解质数量的变化来计算离子的迁移数。
我们用图13—1来说明。
设想在两个惰性电极之间有想象的平面AA和BB~将溶液分为阳极区~中间区和阴极区三部分。
假定在末通电前~各区均含有正、负离子各5mo1~分别用“+”、“-”号的数量来表示正、负离子的物质的量。
今通入4法拉第的电量之后~在阳极上有4mol负离子发生氧化反应~同时在阴极上有4mol正离子发生还原反应~在溶液中的离子也同时发生迁移。
假如正离子的速率是负离子的3倍~则在溶液中的任一截面上~将有3mo1的正离子通过截面向阴极移动~有1mo1的负离子通过截面向阳极移动~通电完毕后~中间区溶液的浓度不变~但阳极区及阴极区的浓度都会有变化~它们之间的浓度变化关系可以用公式表示出来。
如分析阴极区:,,,nn n,- 始后迁,,,,nnn ,+-n 始后迁电同理分析阳极区:,,,,,+- nnnn始后迁电,,,,+ nnn始后迁-2, 对HSO溶液~因为SO不参加电极反应~参加电极反应的是OH离子~所以此时上述244公式应是:,,, ,+ nnn始后迁,,,,,-+ nnnn始后迁电在上述各公式中:,,、分别表示通电后各区所含负离子及正离子物质的量。
实验十五 离子迁移数的测定当电流通过电解质溶液时,溶液中的正负离子各自向阴、阳两极迁移,由于各种离子的迁移速度不同,各自所带过去的电量也必然不同。
每种离子所带过去的电量与通过溶液的总电量之比,称为该离子在此溶液中的迁移数。
若正负离子传递电量分别为q +和q -,通过溶液的总电量为Q , 则正负离子的迁移数分别为:t +=q +/Q t -=q -/Q离子迁移数与浓度、温度、溶剂的性质有关,增加某种离子的浓度则该离子传递电量的百分数增加,离子迁移数也相应增加;温度改变,离子迁移数也会发生变化,但温度升高正负离子的迁移数差别较小;同一种离子在不同电解质中迁移数是不同的。
离子迁移数可以直接测定,方法有希托夫法、界面移动法和电动势法等。
(一) 希托夫法测定离子迁移数【目的要求】1. 掌握希托夫法测定离子迁移数的原理及方法。
2. 明确迁移数的概念。
3. 了解电量计的使用原理及方法。
【实验原理】希托夫法测定离子迁移数的示意图如图2-15-1所示 :将已知浓度的硫酸放入迁移管中,若有Q库仑电量通过体系,在阴极和阳极上分别发生如下反应:阳极: 2OH -→e 2O 21O H 22++ 阴极: 2H + +2e→ H 2此时溶液中H +离子向阴极方向迁移,SO 2-4离子向阳极方向迁移。
电极反应与离子迁移引起的总后果是阴极区的H 2SO 4浓度减少,阳极区的H 2SO 4浓度增加,且增加与减小的浓度数值相等,因为流过小室中每一截面的电量都相同,因此离开与进入假想中间区的H+离子数相同,SO 2-4离子数也相同,所以中间区的浓度在通电过程中保持不变。
由此可得计算离子迁移数的公式如下:()()-+--=⨯⎪⎭⎫ ⎝⎛=⨯⎪⎭⎫ ⎝⎛=2424SO H 4242SO 1mol SO H 21mol SO H 21t t Q F Q F t 增加的量阳极区减少的量阴极区 式中,F=96500C ·mol -1为法拉第(Farady)常数;Q为总电量。
图2-15-1所示的三个区域是假想分割的,实际装置必须以某种方式给予满足。
图2-15-2的实验装置提供了这一可能,它使电极远离中间区,中间区的连接处又很细,能有效地阻止实验2扩散,保证了中间区浓度不变的可信度。
图2-15-1希托夫法测定离子迁移数图2-15-2 希托夫法测定离子迁移数装置图通过溶液的总电量可用气体电量计测定,如图2-15-3所示,其准确度可达±0.1%,它的原理实际上就是电解水(为减小电阻,水中加入几滴浓H2SO4)。
阳极:2OH-→e2O21OH22++阴极2H+→H2-2e根据法拉弟定律及理想气体状态方程,据H2和O2的体积得到求算总电量(库仑)公式如下:()RTVFppQ W34-=式中,p为实验时大气压;p W为温度为T时水的饱和蒸气压;V为H2和O2混合气体的体积;F为法拉弟(Farady)常数。
图2-15-3气体电量计装置图【仪器试剂】迁移管1套;铂电极2只;精密稳流电源1台;气体电量计1套;分析天平1台;碱式滴定管(250mL)1只;三角瓶(100mL)3只;移液管(10mL)3只;烧杯(50ml)3只;容量瓶(250mL)1只。
浓H2SO4;标准NaOH溶液(0.1mol·dm-3) 。
【实验步骤】1. 溶液的配制及装样:配制⎪⎭⎫⎝⎛42SOH21C为0.1mol·dm-3的H2SO4的溶液250mL,并用标准NaOH溶液标定其浓度。
然后用该H2SO4溶液冲洗迁移管后,装满迁移管。
2. 打开气体电量计活塞,移动水准管,使量气管内液面升到起始刻度,关闭活塞,比平后记下液面起始刻度。
3. 按图接好线路,将稳流电源的“调压旋钮”旋至最小处。
经教师检查后,接通开关K,实验十五 离子迁移数的测定 3打开电源开关,旋转“调压旋钮”使电流强度为10mA ~15mA ,通电约1.5h 后,立即夹紧两个连接处的夹子,并关闭电源。
4. 将阴极液(或阳极液)放入一个已称重的洁净干燥的烧杯中,并用少量原始H 2SO 4液冲洗阴极管(或阳极管)一并放入烧杯中,然后称重。
中间液放入另一洁净干燥的烧杯中。
5. 取10mL 阴极液(或阳极液)放入三角瓶内,用标准NaOH 溶液标定。
再取10mL 中间液标定之,检查中间液浓度是否变化。
6. 轻弹气量管,待气体电量计气泡全部逸出后,比平后记录液面刻度。
【注意事项】电量计使用前应检查是否漏气。
通电过程中,迁移管应避免振动。
中间管与阴极管、阳极管连接处不留气泡阴极管、阳极管上端的塞子不能塞紧【数据处理】1.将所测数据列表室温 ; 大气压 ; 饱和水蒸气压 ; 气体电量计产生气体体积V ;标准NaOH 溶液浓度 。
2. 计算通过溶液的总电量Q3. 计算阴极液通电前后H 2SO 4减少的量n()10000V C C n -=式中,C 0为H 2SO 4原始浓度;C 为通电后H 2SO 4浓度;V 为阴极液体积(cm 3),由V =W /ρ 求算(W为阴极液的重量,ρ为阴极液的密度,20℃时0.1mol ·dm -3 H 2SO 4 的ρ=1.002g ·cm -3)。
4. 计算离子的迁移数 -+24SO H t t 及。
思 考 题1. 如何保证电量计中测得的气体体积是在实验大气压下的体积?2. 中间区浓度改变说明什么?如何防止?3. 为什么不用蒸馏水而用原始溶液冲洗电极?(二) 界面移动法测定离子迁移数实 验4 【实验原理】利用界面移动法测迁移数的实验可分为两类:一类是使用两种指示离子,造成两个界面;另一类是只用一种指示离子,有一个界面。
近年来这种方法已经代替了第一类方法,其原理如下:实验在图2-15-4所示的迁移管中进行。
设MZ+为欲测的阳离子,M’Z+为指示阳离子。
M′A 放在上面或下面,须视其溶液的密度而定。
为了防止由于重力而产生搅动作用时,保持界面清晰,应将密度大的溶液放在下面。
当有电流通过溶液时,阳离子向阴极迁移,原来的界面aa′逐渐上移动,经过一定时间t 到达bb′。
设aa ′和bb ′间的体积为V, +Z M t 为MZ+的迁移数。
据定义有:Q VFC t Z M =+式中,F =96500 C ·mol -1; C 为 ⎪⎭⎫ ⎝⎛+Z M 1Z 的量浓度;图2-15-4 迁移管中的电位梯度Q 为通过溶液的总电量;V 为界面移动的体积,可用称量充满aa ′和bb ′间的水的重量校正之。
图2-15-5 界面移动法测离子迁移数装置示意图本实验用Cd 2+作为指示离子,测定H +在0.1mol ·dm -3HCl 中的迁移数。
因为Cd 2+淌度(U)较小,即++<H U U 2Cd在图2-15-5的实验装置中,通电时,H +向上迁移,Cl -向下迁移,在Cd 阳极上Cd 氧化,进入溶液生成CdCl 2,逐渐顶替HCl 溶液,在管中形成界面。
由于溶液要保持电中性,且任一截面都不会中断传递电流,H+迁移走后的区域,Cd 2+紧紧地跟上,离子的移动速度(V ) 是相等的, ++=H Cd 2V V 由此可得:LE U L E U d d d 'd H Cd 2++= 结合上式得: LE L E d d d 'd > 即在CdCl 2溶液中电位梯度是较大的,如图2-15-3所示。
因此若H +因扩散作用落入CdCl 2溶液层。
它就不仅比Cd 2+迁移得快,而且比界面上的H +也要快,能赶回到HCl 层。
同样若任何Cd 2+进入低电位梯度的HCl 溶液,它就要减速,一直到它们重又落后于H +为止,这样界面在通电过程中保持清晰。
【仪器试剂】精密稳流电源;电量计1套;烧杯(25ml )一只。
HC1 0.1 mol ·dm -3;甲基橙(或甲基紫)指示剂。
实验十五 离子迁移数的测定 5【实验步骤】1. 在小烧杯中倒入约10mL 0.1 mol ·dm -3HCl ,加入少许甲基紫,使溶液呈深蓝色。
并用少许该溶液洗涤迁移管后,将溶液装满迁移管,并插入Pt 电极。
2. 打开气体电量计活塞,移动水准管使气量管液面升至上部起始刻度,关闭活塞,比平后读取气量管液面起始刻度。
3. 按图2-15-5连接线路,将稳压电源的“电压调节旋钮”旋至最小处,开关K 打向“1”。
经教师检查线路后,方可接通电源,并旋转“调压旋钮”,使电流强度为5mA ~7mA ,注意实验过程中如变化较大要及时调节。
4. 当迁移管内蓝紫色界面达到起始刻度时,立即将开关K 打向“2”,当蓝紫色界面迁移1mL 后,立即关闭电源开关,用手弹气量管,待全部气体自液体中逸出,比平后读取气量管液面刻度。
【注意事项】通过后由于CdCl 2层的形成电阻加大,电流会渐渐变小,因此应不断调节电流使其保持不变。
通电过程中,迁移管应避免振动【数据处理】计算 -+Cl H t t 和。
讨论与解释观察到的实验现象,将结果与文献值加以比较。
思 考 题1. 本实验关键何在?应注意什么?2. 测量某一电解质离子迁移数时,指示离子应如何选择?指示剂应如何选择?【讨论】在离子迁移数的实验中测总电量的方法除了气体电量计法外还有电流—时间法和库仑计法。
电流—时间法实验装置如图2-15-6所示。
其操作方法如下:接通开关K 与电源D 相通,调节电位器R 保持电流在5mA ~7mA 之间。
随电解进行在迁移管下部形成一个清晰的界面,当界面移动到 第一个刻度时,立即开动秒表,此时要随时调节电位器R ,使电流I 保持定值。
当界面移到第二个刻度时,立即记下时间(但不停秒表),继续通电记时,记录界面达到第三个刻度和第四个刻度的时间。
图2-15-6 电流—时间测总电量示意图。