初中化学九年级下册思维导图
- 格式:docx
- 大小:1.09 MB
- 文档页数:2

第一单元走进化学世界思维导图物都,,富咨做.槽,’T二成三宣:目林,渣二■芥1T二成M:祯蹴*珀推茬尊跆c,标却]手廿••也秋再睡^* ;:袱部庠成神础既引定壁;重奇•眩建电闫方注应假点用,睇TK------------------------------ 雷牺■的邮壬理顼:型飘:整片驱.祖困,更习症-----------------------------暗"“店时'总菰:乎匕受址 /------------------------------<——(y也g中何jMhh% / ' ---------------------------------------;,{ 岗哽寸质'巧行瓦胃■典it*哽化就段毗旅印住伊_刁注.--\甘於( _- '------- [构手■巳专吉■■装受仕二耒毗隶跳忙NW的奇} 命麻的1用J»*〔佟匿菌,旋、菅S--------------------------- 略陶豹底1stm ----------------------- 括勤!睡阻也4M传,I干帝乔*,河唐Y四叶曹斯环陀能表泵心而瑚昕RD请麻n右虹E戋部WUMM 蚌H 琴*物- i L堂耍吐亚—亿学生卷出呵I砌4野£g第二单元 我们周围的空气 思维导图 jtifc, anHAggftftua ',童THg^ntr 萱祀璧M 是一斟E1、:A •.宰中•二-d.^~«+帝Hftfl 咛孑mvwn ::元*s* 睡通坎 口芯初;羿白完 :ij 丰布适 r-0^S<7Cn誓故* KT* ¥旧吱*异H —并ftfMfafa &裁%一:坝寮.k 野JL-族板4岂砂K¥^!££t 3Ftt3Dj£&tjOd钠Bf 邮鹿田懈&戒A&,:布计轼而待•:二*材.翦:,UH tHK 祉、础醐■申2_ ^―?>:h;0 - 0j1| ggisg=〜。

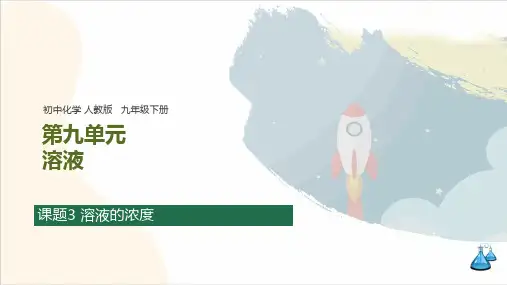
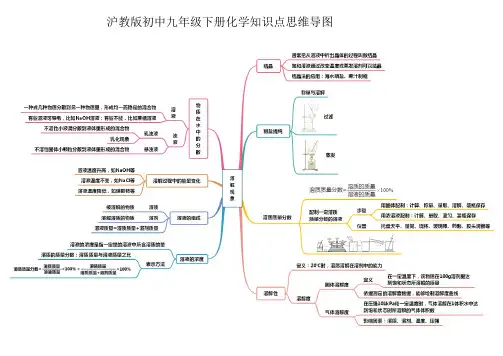
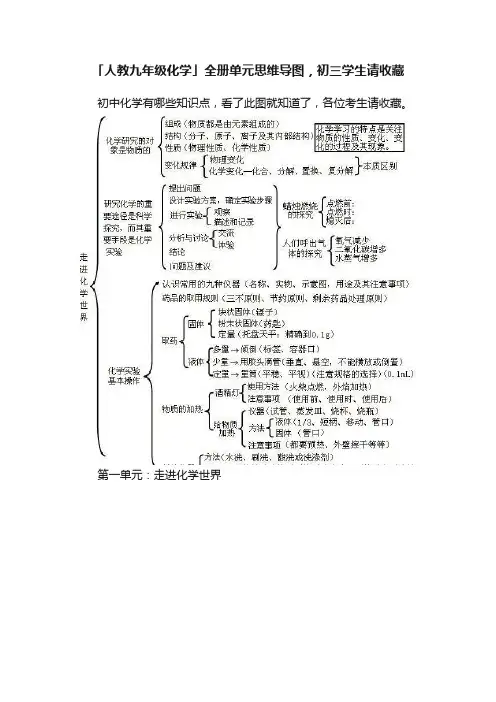



九年级下册化学思维导图
第一章:化学基本概念
- 原子、分子和离子的概念及区别
- 元素和化合物的特点和分类
- 常见的基本元素及其性质
第二章:物质的组成
- 液体、固体和气体的性质比较
- 纯净物和混合物的概念和区别
- 常见物质的组成和结构分析方法
第三章:化学反应
- 化学方程式的表示和平衡
- 不同类型的化学反应:合成、分解、置换、还原和氧化- 化学反应速率和反应速率相关的因素
第四章:酸碱及中和反应
- 酸和碱的定义和性质
- 酸碱中和反应的原理和应用
- pH值和酸碱指示剂的使用
第五章:氧化与还原反应
- 氧化和还原的概念与意义
- 金属和非金属在氧化还原反应中的特点- 氧化还原反应的应用及其环境意义
第六章:盐和金属
- 盐的性质和分类
- 盐的制备和应用
- 金属的性质和应用
第七章:碳的化学
- 碳的存在形态及其性质
- 有机化合物的基本概念
- 碳的循环与重要性
第八章:燃烧与火焰
- 燃烧的基本概念和条件
- 不同物质的燃烧特点和应用
- 火焰的结构和性质
第九章:化学能与化学反应的能量变化
- 化学能的概念和计算
- 化学反应的能量变化及其影响因素
- 能量守恒定律在化学反应中的应用
第十章:化学实验与化学技术
- 化学实验室的常规操作和安全注意事项
- 常见的化学实验和实验技术
- 化学技术及其在生活中的应用
以上是九年级下册化学思维导图的初步概述。
通过学习这些知识,同学们将能够更好地理解化学的基本概念和原理,提高化学思维能力,为更深入的学习打下基础。

目录思维导图绪论化学使世界变得更加绚丽多彩 (1)第一单元走进化学世界 (1)第二单元空气和氧气 (2)第三单元物质构成的奥秘 (3)第四单元自然界的水 (4)第五单元化学反应的定量关系 (5)第六单元碳和碳的氧化物 (6)第七单元能源的合理利用与开发 (7)第八单元金属和金属材料 (8)第九单元溶液 (9)第十单元常见的酸、碱、盐 (10)第十一单元化学与社会 (12)11绪论化学使世界变得更加绚丽多彩第一单元走进化学世界质量守恒定律 拉瓦锡(法国)化学史 原子论道尔顿(英国)分子学说阿伏加德罗(意大利 元素周期律门捷列夫(俄国)化学是研究物质的组成、结构、性质、转化及应用的一门基础学科绿色化学物质的变化和性质实验室规则物质的变化物质的性质化学变化 物理变化 化学性质 物理性质块状固体试剂的取用化学试剂的取用 粉末状固体试剂的取用量简的使用液体试剂的取用胶头滴管的使用酒精灯的使用方法物质的加热 固体物质的加热把玻璃导管插入带孔橡胶塞仪器装置的连接一连接玻璃导管和乳胶管检查装置的气密性玻璃仪器的洗涤 洗过的玻璃仪器内壁附着的水既不聚成水滴,也不成股流下点燃前顾色、状态、形状、气味、硬度、密度等)燃着时火焰的分层情况、燃烧产物的检验)熄后(白烟成分的检验)化学使世界变得 更加绚丽多彩 走进化学世界连接橡胶塞和容器2第二单元空气和氧气第三单元物质构成的奥秘3概念一由分子构成的物质,分子是保持其化学性质的最小拉子质量和体积通常都很小分子不断运动性质- 分子间有间隔同种分子构成的物质,化学性质相同,不同种分子 构成的物质.化学性质不同 在化学变化中可以再分在化学变化中,分子可以分为原子,原子又可以结合成新的分子概 念 原子是化学变化中的最小粒子原子核H[ 质子(+)结构 中子核外电子(一)核外电子的排布 相对原子质量4离子的形成离子与原子的区别 离子符号的写法与读法概 念H 质子数即校电荷数相同的一类原子的总称书 写微观表示一个该原子意 义宏现表示该元素组成:7个周阴、16个族 元素周期表每个小格表示的意义金属元素分类 非金属元素插有气体元素宏现组成H 元素物质构成的奥图元素符号微现构成离子原 子空气的组成主 氧气的用途支持燃烧中Si食品包装 制造低温制造电光源.Si制造低温(氢空气的保护、空气质量监测195变阳排纯净物 物理性质木炭燃烧氧气的性质化学性质蜡烛燃烧 红确燃烧刚烈氧化氧化反应级慢红化高锰酸钾分解实验室制取 改变化学反应速率催 化 剂工业制取化学反应类型质量不变热化学性质不变分肉液态空气法(物理变化)元单一美供给呼吸 化合反应(多变一 分解反应(一变多无色无臭的气体、密度比空气大、不易溶于水 硫的燃烧 铁丝燃烧 稀有气体的用途过氧化氢分解座航和氧气物质的分类氧气的制取氮气的用途 空气. 卫混合物: 年SI4第四单元 自然界的水第五单元化学反应的定量关系5化学反应反应物的质量总和=生成物的质量总和 原子的种类、数目、质量部不变以客观事实为基础书写原则遵守质量守恒定律概 念 用化学式来表示化学反应的式子化学方程式 书写原则化学反应的书写步骤写 写出反应物和生成物的化学式配 配平化学方程式书写步骤注 注明反应条件和生成物状态 等 画上等号。