药审中心主审审评员资格人员名单
- 格式:doc
- 大小:728.00 KB
- 文档页数:2

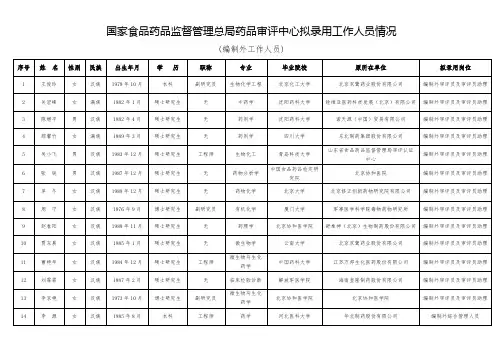
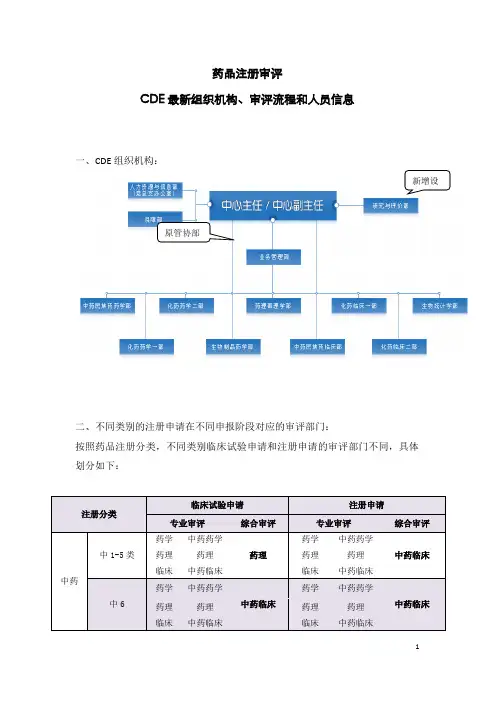
药品注册审评CDE最新组织机构、审评流程和人员信息一、CDE组织机构:原管协部二、不同类别的注册申请在不同申报阶段对应的审评部门:按照药品注册分类,不同类别临床试验申请和注册申请的审评部门不同,具体划分如下:注:1、所有的药品申请在各阶段的审评都有业务管理部的参与,表中略;2、表中的“临床”指的是化药临床一部或者二部,具体按品种适应症分。
三、化药相关审评部门人员如下:※:表示主持工作的负责人四、CDE 简易审评流程图:注意事项: (1)药品审评中心自2010年4月6日起在具体注册申请的技术审评过程中同步完成质量标准、说明书、包装标签等文件的修订审核工作,请注册申请人在注册申请到达我中心后及时通过CDE 网站电子提交系统提交相关电子文件。
(2)技术审评阶段如存在以下情况,有可能会影响审评进度,请您关注:请务必在我中心专业审评阶段结束前登陆我中心网站电子提交系统提交相关电子文档(注意根据注册申请的具体事项确定提交的具体内容)。
电子提交工作将有助于提高审评工作的效率。
(3)关注检验报告提示:注册申请如要求提交检验报告,请务必关注检验报告的寄交情况。
如专业审评时仍未收到检验报告,将暂停审评,同时暂停审评计时。
(4)业务管理部接收申报资料后,将对申报资料进行立卷审查:确认电子任务与物理资料是否同步到达、是否缴纳审评费、是否提交研制现场核查报告、仿制药是否提交生产现场检查报告及动态检验报告。
上述条件均满足后,将正式启动审评。
五、CDE 发布的《药品技术审评原则和程序》及审评流程图:详见:/regulat.do?method=view&id=2133专业审评中综合评价技术审核文件制作与中心审核签发业务管理部接受资料业务管理部分配任务审评部安排审评计划呈送SFDA等待执行其它业务药品技术审评简化程序示意图主审人部长部长分配任务主审人部长部长分配任务部长中心主任参审人参参审人单专业审评程序平行审评程序序贯审评程序。

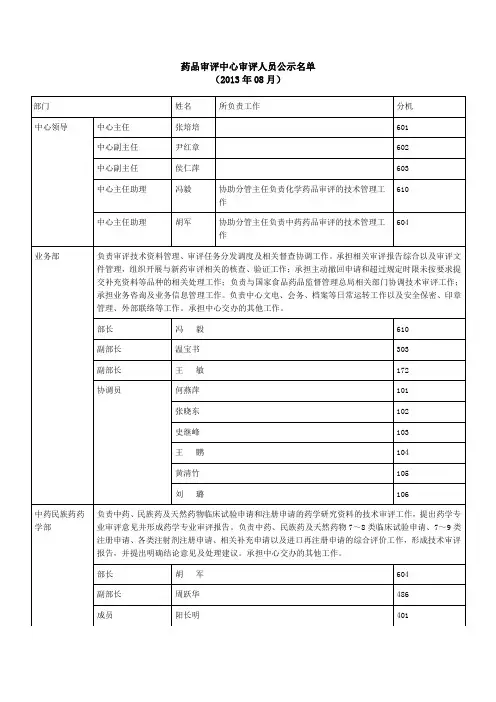
药品审评中心审评人员公示名单 (2015年4月)部门姓名 所负责工作分机中心主任许嘉齐611中心副主任尹红章602中心副主任侯仁萍603中心领导中心主任助理胡 军协助分管主任负责中药药品审评的技术管理工作604负责审评技术资料管理、审评任务分发调度及相关督查协调工作。
承担相关审评报告综合以及审评文件管理,组织开展与新药审评相关的核查、验证工作;承担主动撤回申请和超过规定时限未按要求提交补充资料等品种的相关处理工作;负责与国家食品药品监督管理局相关部门协调技术审评工作;承担业务咨询及业务信息管理工作。
负责中心文电、会务、档案等日常运转工作以及安全保密、印章管理、外部联络等工作。
承担中心交办的其他工作。
副部长温宝书303副部长王 敏172 何燕萍101张晓东102王 鹏104黄清竹105业务管理部协调员刘 璐106负责中药、民族药及天然药物临床试验申请和注册申请的药学研究资料的技术审评工作,提出药学专业审评意见并形成药学专业审评报告。
负责中药、民族药及天然药物7~8类临床试验申请、7~9类注册申请、各类注射剂注册申请、相关补充申请以及进口再注册申请的综合评价工作,形成技术审评报告,并提出明确结论意见及处理建议。
承担中心交办的其他工作。
部长胡 军604 副部长周跃华486阳长明401张永文402曲建博406金 芳407李计萍408周 刚409韩 炜412中药民族药药学部成员马秀璟413负责化学药物1~3类临床试验申请和注册申请、国际多中心临床试验申请的药学研究资料的技术审评工作,提出药学专业审评意见并形成药学专业审评报告。
负责化学药物3类临床试验申请的综合评价工作,形成技术审评报告,并提出明确结论意见及处理建议。
承担中心交办的其他工作。
副部长马玉楠577王 旸502任连杰505康建磊506王亚敏507于 红508王宏亮511马 磊512张 宁513霍秀敏514化药药学一部成员刘宗英515 负责化学药物4~5类临床试验申请、进口药注册申请、进口再注册申请、相关补充申请及其他申请的药学研究资料及生物等效性试验资料的技术审评工作,提出药学专业和相应生物等效性资料的审评意见并形成药学专业审评报告。


国家食品药品监督管理总局药品审评中心审评员管理暂行办法(试行)第一章总则第一条为推进药品审评审批制度改革,深化国家食品药品监督管理总局药品审评中心(以下简称“中心”)人事制度改革,规范药品审评人员管理,保障审评员的合法权益,根据《事业单位人事管理条例》、《人事部关于在事业单位试行人员聘用制度意见》以及药品医疗器械审评审批制度改革工作意见等法规政策,结合药品审评工作实际,制定本办法。
第二条本办法所称审评员,是指在规定的岗位范围内,按照聘用合同管理,从事药品审评工作的专业技术人员,包括事业编制内和事业编制外审评员。
第三条中心按照“招得到、用得好、留得住、退得出”的原则,建立科学、规范、有效的审评员管理制度。
第二章岗位设置第四条根据审评工作需要,科学合理设置审评岗位,坚持按需设岗、精简高效、按岗聘用、分级管理。
第五条根据药品审评职责任务和岗位任职条件,分级设置审评岗位。
审评岗位包括:首席审评员、高级审评员、主审审评员、审评员。
其中主审审评员岗位分为6档,审评员岗位分为4档。
药品审评实行首席审评员负责制,首席审评员对技术审评工作进行总把关,经中心授权签发技术审评意见。
第六条根据审评任务数量、审评任务结构、产业发展趋势等因素合理确定并调整各审评相关学科、各专业审评岗位职数和比例。
第七条各级审评岗位的主要职责如下:(一)首席审评员:负责药品安全、有效、质量可控方面的技术把关,并根据中心授权签发技术审评意见;制定并实施药品审评专业技术领域的学科建设规划,负责跟踪把握国内外本专业领域学科发展前沿趋势,构建药品审评专业技术领域的科学化审评体系;牵头开展药品审评规范、指导原则体系、审评共性问题的研究,组织审评团队解决疑难品种和评审疑难问题;指导和培养其他审评人员开展工作。
(二)高级审评员:负责建立或完善药品审评专业技术领域的科学化审评体系;负责组织开展本专业领域相关技术标准和指导原则的起草工作;负责对本专业领域的疑难问题提出处理意见;指导和培养主审审评员和审评员开展工作。
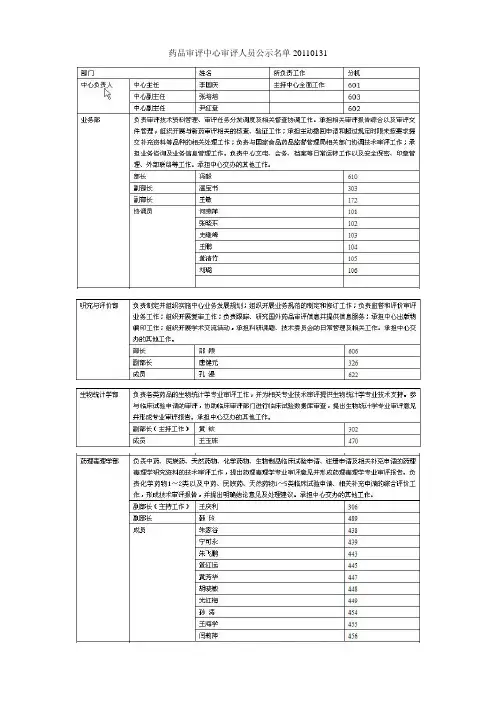
药品审评中心审评人员公示名单20110131关于国家食品药品监督管理局药品审评中心调整主要职责和内设机构的批复国食药监人函[2010]219号(一)业务管理部负责审评技术资料管理、审评任务分发调度及相关督查协调工作。
承担相关审评报告综合以及审评文件管理,组织开展与新药审评相关的核查、验证工作;承担主动撤回申请和超过规定时限未按要求提交补充资料等品种的相关处理工作;负责与国家食品药品监督管理局相关部门协调技术审评工作;承担业务咨询及业务信息管理工作。
负责中心文电、会务、档案等日常运转工作以及安全保密、印章管理、外部联络等工作。
承担中心交办的其他工作。
(二)中药民族药药学部负责中药、民族药及天然药物临床试验申请和注册申请的药学研究资料的技术审评工作,提出药学专业审评意见并形成药学专业审评报告。
负责中药、民族药及天然药物7~8类临床试验申请、7~9类注册申请、各类注射剂注册申请、相关补充申请以及进口再注册申请的综合评价工作,形成技术审评报告,并提出明确结论意见及处理建议。
承担中心交办的其他工作。
(三)化药药学一部负责化学药物1~3类临床试验申请和注册申请、国际多中心临床试验申请的药学研究资料的技术审评工作,提出药学专业审评意见并形成药学专业审评报告。
负责化学药物3类临床试验申请的综合评价工作,形成技术审评报告,并提出明确结论意见及处理建议。
承担中心交办的其他工作。
(四)化药药学二部负责化学药物4~5类临床试验申请、进口药注册申请、进口再注册申请、相关补充申请及其他申请的药学研究资料及生物等效性试验资料的技术审评工作,提出药学专业和相应生物等效性资料的审评意见并形成药学专业审评报告。
负责化学药物4~5类临床试验申请以及5~6类注册申请、进口药临床试验申请、进口再注册申请、相关补充申请及其他申请的综合评价工作,形成技术审评报告,并提出明确结论意见及处理建议。
承担中心交办的其他工作。
(五)生物制品药学部负责生物制品临床试验申请、注册申请及相关补充申请的药学研究资料的技术审评工作,提出药学专业审评意见并形成药学专业审评报告。
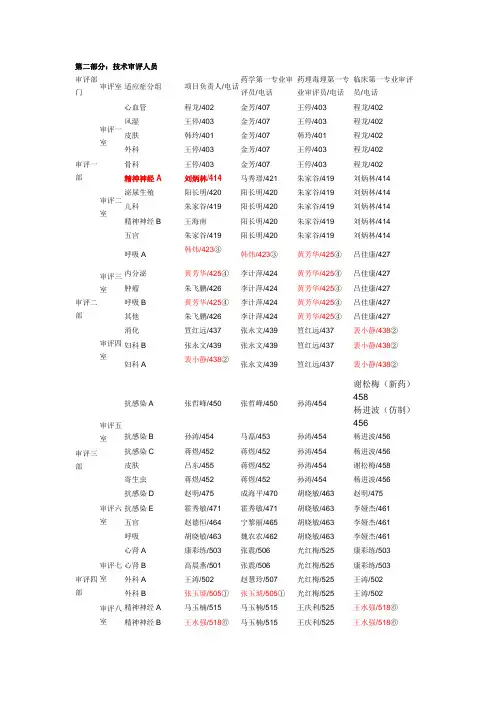
第二部分:技术审评人员审评部门审评室适应症分组项目负责人/电话药学第一专业审评员/电话药理毒理第一专业审评员/电话临床第一专业审评员/电话审评一部审评一室心血管程龙/402 金芳/407 王停/403 程龙/402风湿王停/403 金芳/407 王停/403 程龙/402皮肤韩玲/401 金芳/407 韩玲/401 程龙/402外科王停/403 金芳/407 王停/403 程龙/402骨科王停/403 金芳/407 王停/403 程龙/402审评二室精神神经A 刘炳林/414 马秀璟/421 朱家谷/419 刘炳林/414 泌尿生殖阳长明/420 阳长明/420 朱家谷/419 刘炳林/414 儿科朱家谷/419 阳长明/420 朱家谷/419 刘炳林/414 精神神经B 王海南阳长明/420 朱家谷/419 刘炳林/414 五官朱家谷/419 阳长明/420 朱家谷/419 刘炳林/414审评二部审评三室呼吸A韩炜/423③韩炜/423③黄芳华/425④吕佳康/427 内分泌黄芳华/425④李计萍/424 黄芳华/425④吕佳康/427肿瘤朱飞鹏/426 李计萍/424 黄芳华/425④吕佳康/427呼吸B 黄芳华/425④李计萍/424 黄芳华/425④吕佳康/427其他朱飞鹏/426 李计萍/424 黄芳华/425④吕佳康/427审评四室消化笪红远/437 张永文/439 笪红远/437 裴小静/438②妇科B 张永文/439 张永文/439 笪红远/437 裴小静/438②妇科A裴小静/438②张永文/439 笪红远/437 裴小静/438②审评三部审评五室抗感染A 张哲峰/450 张哲峰/450 孙涛/454谢松梅(新药)458杨进波(仿制)456抗感染B 孙涛/454 马磊/453 孙涛/454 杨进波/456抗感染C 蒋煜/452 蒋煜/452 孙涛/454 杨进波/456皮肤吕东/455 蒋煜/452 孙涛/454 谢松梅/458寄生虫蒋煜/452 蒋煜/452 孙涛/454 杨进波/456审评六室抗感染D 赵明/475 成海平/470 胡晓敏/463 赵明/475抗感染E 霍秀敏/471 霍秀敏/471 胡晓敏/463 李娅杰/461五官赵德恒/464 宁黎丽/465 胡晓敏/463 李娅杰/461呼吸胡晓敏/463 魏农农/462 胡晓敏/463 李娅杰/461审评四部审评七室心肾A 康彩练/503 张震/506 光红梅/525 康彩练/503心肾B 高晨燕/501 张震/506 光红梅/525 康彩练/503外科A 王涛/502 赵慧玲/507 光红梅/525 王涛/502外科B 张玉琥/505①张玉琥/505①光红梅/525 王涛/502审评八室精神神经A 马玉楠/515 马玉楠/515 王庆利/525 王水强/518⑥精神神经B 王水强/518⑥马玉楠/515 王庆利/525 王水强/518⑥精神神经C 许真玉/514 许真玉/514 王庆利/525 赵建中/519 其他陈海峰/513 许真玉/514 王庆利/525 赵建中/519审评五部审评九室肿瘤A 陈晓媛/526⑤何伍/533 王海学/530 陈晓媛/526⑤放射彭健/531 何伍/533 王海学/530 陈晓媛/526⑤肿瘤B+妇科张宁/532 张宁/532 王海学/530 陈晓媛/526⑤审评十室内分泌B 张杰/543 王亚敏/547 张若明/542 张杰/543内分泌A 王亚敏/547 王亚敏/547 张若明/542 张杰/543消化B 卓宏/548 李志万/539 张若明/542 卓宏/548消化A 张若明/542 李志万/539 张若明/542 杨焕/538审评五部生物制品室体外诊断试剂高恩明/554 张丽/558血液制品罗建辉/549 罗建辉/549 王海学/530 陈晓媛/526⑤预防用生物制品高恩明/554 高恩明/554 张若明/542 杨焕/538治疗用生物制品(妇科)常卫红/555 赵超/559 王海学/530 陈晓媛/526⑤治疗用生物制品(呼吸)常卫红/555 赵超/559 胡晓敏/463 李娅杰/461 治疗用生物制品(精神神经)常卫红/555 赵超/559 王庆利/525 王水强/518 治疗用生物制品(抗感染)常卫红/555 赵超/559 孙涛/454 谢松梅/458 治疗用生物制品(抗肿瘤、放射)罗建辉/549 罗建辉/549 王海学/530 陈晓媛/526⑤治疗用生物制品(内分泌)赵超/559 赵超/559 张若明/542 张杰/543 治疗用生物制品(皮肤)常卫红/555 赵超/559 孙涛/454 谢松梅/458 治疗用生物制品(外科)常卫红/555 赵超/559 王海学/530 王涛/502 治疗用生物制品(五官)常卫红/555 赵超/559 胡晓敏/463 李娅杰/461 治疗用生物制品(消化)赵超/559 赵超/559 张若明/542 杨焕/538 治疗用生物制品(心肾)赵超/559 赵超/559 王海学/530 康彩练/503。
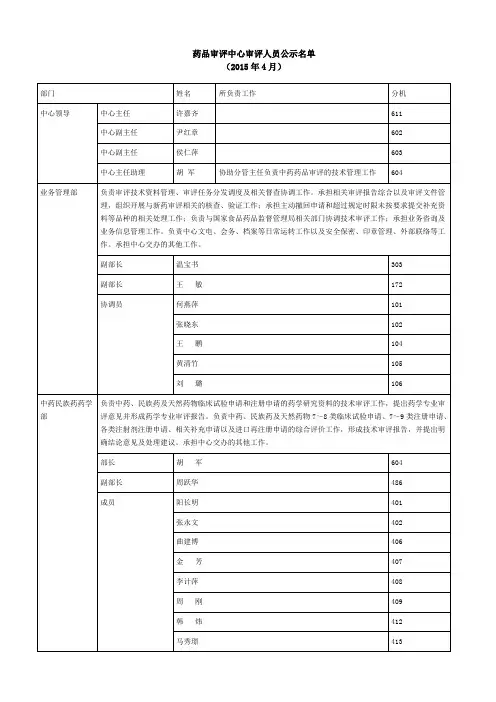

江西省药品监督管理局关于公布江西省医疗器械审评咨询专家库专家名单的通知正文:---------------------------------------------------------------------------------------------------------------------------------------------------- 江西省药品监督管理局关于公布江西省医疗器械审评咨询专家库专家名单的通知赣药监械注〔2021〕19号各设区市、赣江新区、省直管试点县(市)市场监督管理局,各有关单位:为保证医疗器械技术审评工作依法、科学、高效、公正,推动我省医疗器械产业高质量发展,经遴选和审核,决定将邱嘉旋等192人作为江西省医疗器械审评咨询专家库专家。
本次医疗器械审评咨询专家库建设工作按照“存量更新”和“新增遴选”两个步骤,兼顾了省直部门和各设区市相关单位。
我局重大、复杂医疗器械技术审评事项,将根据审评需要,从专家库中挑选专家召开专家咨询会,同时开展日常咨询工作。
各设区市、赣江新区、省直管试点县(市)市场监督管理局等单位如有相关工作需要,也可向我局申请使用专家库资源。
专家库实行动态管理,省局医疗器械注册处牵头组织药品认证审评中心等部门做好专家库的日常管理工作。
联系人:康明联系电话:*************附件:江西省医疗器械审评咨询专家库专家名单江西省药品监督管理局2021年10月22日附件江西省医疗器械审评咨询专家库专家名单序号姓名专业领域工作单位1邱嘉旋口腔颌面外科南昌大学第一附属医院2鄢艳肾内科南昌大学第一附属医院3唐城普外科南昌大学第一附属医院4李映良普外科南昌大学第一附属医院5段剑神经外科南昌大学第一附属医院6詹剑华烧伤科南昌大学第一附属医院7王艳霞烧伤科南昌大学第一附属医院8裴重刚眼科南昌大学第一附属医院9江红群耳鼻喉南昌大学第一附属医院10张志远耳鼻喉南昌大学第一附属医院11何林生产科南昌大学第一附属医院12张发明信息科南昌大学第一附属医院13李春超声医学科南昌大学第一附属医院14王建宁护理部南昌大学第一附属医院15程晓华临床试验研究中心南昌大学第一附属医院16冯珍康复科南昌大学第一附属医院17文冰口腔科南昌大学第一附属医院18何来昌放射科南昌大学第一附属医院19祝新根神经外科南昌大学第二附属医院20张焱神经外科南昌大学第二附属医院21卢明巍神经外科南昌大学第二附属医院22罗军康复医学科南昌大学第二附属医院23刘月辉耳鼻喉南昌大学第二附属医院24宋莉口腔科南昌大学第二附属医院25仲庐云口腔科南昌大学第二附属医院26郑玲莉口腔科南昌大学第二附属医院27黄年根消化内窥镜室南昌大学第二附属医院28宋凌菁泌尿外科南昌大学第二附属医院29谭布珍妇产科南昌大学第二附属医院30吴洁华ICU病房南昌大学第二附属医院31殷小龙眼科南昌大学第二附属医院32罗振中麻醉科南昌大学第二附属医院33吴庆骨科南昌大学第二附属医院34张贝消化内科南昌大学第二附属医院35魏明检验科南昌大学第二附属医院36熊晓云护理部南昌大学第二附属医院37杨立文整形美容科南昌大学第二附属医院38敖检根社会医学与卫生事业管理南昌大学第二附属医院39蔡平基建科南昌大学第四附属医院40徐江霞检验科南昌大学第四附属医院41陈南萍针灸南昌大学第四附属医院42魏洪武口腔医学南昌大学第四附属医院43李志勇药学南昌大学第四附属医院44付小君消化内科南昌大学第四附属医院45杨宏武神经内科南昌大学第四附属医院46陈凯云药物分析南昌大学第四附属医院47霍亚南内分泌科江西省人民医院48肖祖克呼吸内科江西省人民医院49姜敏临床医学(呼吸内科)江西省人民医院50钟爱民肾内科江西省人民医院51刘鸿肾内科江西省人民医院52汪国武耳鼻喉江西省人民医院53李蓉检验科江西省人民医院54桂晓美检验科江西省人民医院55刘小兵麻醉科江西省人民医院56张伟普外科江西省人民医院57朱遵伟泌尿外科江西省人民医院58徐荣春放射科江西省人民医院59付艺斌放射科江西省人民医院60杨春丽ICU江西省人民医院61赖全图B超室江西省人民医院62王文丁生物学江西省人民医院63胡建新药学江西省人民医院64王联辉电子与通信工程江西省人民医院65陈丽萍大内科江西省儿童医院66段君凯小儿心内科江西省儿童医院67柯江维检验科江西省儿童医院68林珊眼科江西省儿童医院69肖煜麻醉科江西省儿童医院70刘晓姝护理部江西省儿童医院71李岚呼吸科江西省儿童医院72王伟口腔科江西省中医院73薛汉荣呼吸科江西省中医院74余航康复科江西省中医院75余奕军麻醉科江西省中医院76姜浩医保科江西省中医院77陈洁病理科江西省中医院78王万春外科江西省中医院79黄世俊信息科江西省中医院80杨军平临床医学江西省中医院81孙前谱临床医学江西省中医院82杨安金中药学江西省中医院83黄淑晖医学遗传中心江西省妇幼保健院84辛才林辅助生殖科江西省妇幼保健院85汪利群生殖健康科江西省妇幼保健院86龚逞豪妇科江西省妇幼保健院87曾莹肿瘤科江西省妇幼保健院88李凌肿瘤科江西省妇幼保健院89杨健牙体牙髓病科南昌大学附属口腔医院90曾利伟口腔修复科南昌大学附属口腔医院91李东方口腔修复科南昌大学附属口腔医院92廖岚口腔医学、口腔材料学南昌大学附属口腔医院93李志华口腔正畸南昌大学附属口腔医院94王予江口腔医学南昌大学附属口腔医院95欧晓艳口腔医学南昌大学附属口腔医院96赵豫口腔医学南昌大学附属口腔医院97张齐龙神经内科江西省胸科医院98陈乐蓉内科学江西省胸科医院99刘珍琼医学检验江西省胸科医院100熊景良临床医学江西省胸科医院101韩斌德临床医学江西省胸科医院102宋军福临床医疗江西省胸科医院103廖银根药剂科江西省皮肤病专科医院104朱永军医学美容科江西省皮肤病专科医院105万祥辉检验科江西省肿瘤医院106唐清美骨伤江西省中西医结合医院107陈超丽眼科江西省中西医结合医院108廖琦外科南昌市第一医院109罗和国麻醉科南昌市第一医院110朱波产科南昌市第一医院111赵恒医疗系南昌市第一医院112姜梅护理学南昌市洪都中医院113占海燕中药江西省精神病院114俞慧强统计学南昌大学115黄鹏流行病与卫生统计学;循证医学南昌大学116郑辉烈流行病与卫生统计学南昌大学117段隆振信息工程学院南昌大学118夏春华药学南昌大学119赖卫华食品学院南昌大学120郑莉萍生殖医学南昌大学121刘峰化学南昌大学122胡剑材料学华东交通大学123敖海勇材料学华东交通大学124周建民仪器华东交通大学125胡国良机械工程华东交通大学126陈齐平机械工程华东交通大学127XXX 机械工程华东交通大学128邬冠华材料科学与工程南昌航空大学129徐勇材料加工工程南昌航空大学130宋仁杰有机化学南昌航空大学131陈学岗测试与光电工程学院南昌航空大学132陈哲材料化学南昌工程学院133付雪峰计算机科学与技术南昌工程学院134聂望计算机软件工程江西中医药大学135郑琴中药学江西中医药大学136章新友物理江西中医药大学137管咏梅药学江西中医药大学138郑里翔中西医结合基础江西中医药大学139张锐药物分析江西中医药大学140汪灿华机械工程江西中医药大学141严志宏分析化学江西中医药大学142方海红药学江西科技师范大学143杨禹哲理化专业室江西省检验检测认证总院144陈良炜医学计量江西省检验检测认证总院145张俊勇电气测量技术及仪表江西省检验检测认证总院146孙江晖仪表及测试系统江西省检验检测认证总院147兰海有源设备类:热学、低温技术;电子仪器江西省检验检测认证总院148周敬电子信息工程江西省检验检测认证总院149黄丽琼压力容器、工程力学江西省检验检测认证总院150聂文昕测控技术与仪器江西省检验检测认证总院151甘蓓生物化学与分子生物学江西省产品质量监督检测院152颜瑛动物科学江西省产品质量监督检测院153王磊食品科学与工程江西省产品质量监督检测院154林黛琴分析化学江西省产品质量监督检测院155缪延晖中药制药江西省质量和标准研究院156汪秋雨冶金工程江西省质量和标准研究院157刘杰临床医学江西省卫生健康检查评价中心158邓晰博软件工程江西省人社宣传中心159周晓软件工程江西省工业和信息产品监督检验院160靳亮微生物研究所江西省科学院161余炅中医外科江西省中医药研究院162熊钧计算机及应用江西省就业中心163李欣药学宜春市人民医院164万林峰药学宜春市人民医院165谢晓峰普外科上饶市立医院166陈怡坤消化内科上饶市人民医院167黄夏雨中医学、临床医学景德镇市中医医院168郑华临床医学景德镇市第二人民医院169周任兵预防医学鹰潭市人民医院170喻伟麟药学鹰潭市人民医院171李坤麻醉新余市人民医院172朱良辉药用植物江西省医疗器械检测中心,173朱才庆生物化工江西省医疗器械检测中心,174罗荣药物化学江西省医疗器械检测中心,175郭晟药理江西省医疗器械检测中心,176李艳药学江西省医疗器械检测中心,177肖小华中药药理江西省医疗器械检测中心,178王丽静中药学江西省医疗器械检测中心,179王晖中药学江西省医疗器械检测中心,180袁海铭中药学江西省医疗器械检测中心,181胡红刚药物分析江西省医疗器械检测中心,182张凌志生物医学工程江西省医疗器械检测中心,183周鹃应用化学江西省药品检查员中心184吴凡临床医学江西省药品检查员中心185蔡锦尚计算机科学与技术江西省药品检查员中心186梁国嫔药学江西省药品检查员中心187李存金药学江西省药品检查员中心188聂君华临床医学江西省药品不良反应监测中心189焦卫红食品机械江西省药品不良反应监测中心190钟长鸣药理江西省药品不良反应监测中心191刘宁药物分析江西省药品检验检测研究院192朱碧君化学制药江西省药品检验检测研究院——结束——。
国家食品药品监督管理总局药品审评中心审评员管理暂行办法(试行)第一章总则第一条为推进药品审评审批制度改革,深化国家食品药品监督管理总局药品审评中心(以下简称“中心”)人事制度改革,规范药品审评人员管理,保障审评员的合法权益,根据《事业单位人事管理条例》、《人事部关于在事业单位试行人员聘用制度意见》以及药品医疗器械审评审批制度改革工作意见等法规政策,结合药品审评工作实际,制定本办法。
第二条本办法所称审评员,是指在规定的岗位范围内,按照聘用合同管理,从事药品审评工作的专业技术人员,包括事业编制内和事业编制外审评员。
第三条中心按照“招得到、用得好、留得住、退得出”的原则,建立科学、规范、有效的审评员管理制度。
第二章岗位设置第四条根据审评工作需要,科学合理设置审评岗位,坚持按需设岗、精简高效、按岗聘用、分级管理。
第五条根据药品审评职责任务和岗位任职条件,分级设置审评岗位。
审评岗位包括:首席审评员、高级审评员、主审审评员、审评员。
其中主审审评员岗位分为6档,审评员岗位分为4档。
药品审评实行首席审评员负责制,首席审评员对技术审评工作进行总把关,经中心授权签发技术审评意见。
第六条根据审评任务数量、审评任务结构、产业发展趋势等因素合理确定并调整各审评相关学科、各专业审评岗位职数和比例。
第七条各级审评岗位的主要职责如下:(一)首席审评员:负责药品安全、有效、质量可控方面的技术把关,并根据中心授权签发技术审评意见;制定并实施药品审评专业技术领域的学科建设规划,负责跟踪把握国内外本专业领域学科发展前沿趋势,构建药品审评专业技术领域的科学化审评体系;牵头开展药品审评规范、指导原则体系、审评共性问题的研究,组织审评团队解决疑难品种和评审疑难问题;指导和培养其他审评人员开展工作。
(二)高级审评员:负责建立或完善药品审评专业技术领域的科学化审评体系;负责组织开展本专业领域相关技术标准和指导原则的起草工作;负责对本专业领域的疑难问题提出处理意见;指导和培养主审审评员和审评员开展工作。
38-1-药品审评重大改革与发展决策专家咨询委员会123-药品安全及风险管理专家咨询委员会45-中医药理论及方剂学专家咨询委员会67-中药生产工艺及全程质量控制专家咨询委员会89-中药质量分析及中药材专家咨询委员会1011-化药药学专家咨询委员会121314-生物制品药学专家咨询委员会151617-药理毒理专家咨询委员会1819-生物药剂学和临床药理学专家咨询委员会2021-生物统计专家咨询委员会2223-儿科药品专家咨询委员会2425-法律、经济、社会专家咨询委员会专家咨询委员会2627-风湿免疫、骨科、外科和皮肤科疾病中医临床专家咨询委员会2829-肾病及泌尿生殖疾病中医临床专家咨询委员会3031-心系病中医临床专家咨询委员会3233-肺系病中医临床专家咨询委员会3435-血液及肿瘤疾病中医临床专家咨询委员会3637-内分泌代谢疾病中医临床专家咨询委员会3839-脑病中医临床专家咨询委员会4041-脾胃及肝胆病中医临床专家咨询委员会4243-眼科及耳鼻喉科疾病中医临床专家咨询委员会4445-妇科疾病中医临床专家咨询委员会4647-风湿及免疫系统疾病临床专家咨询委员会4849-麻醉及镇痛药品临床专家咨询委员会50。