2018年全国卷Ⅰ化学高考试题(含答案)
- 格式:doc
- 大小:522.00 KB
- 文档页数:7

绝密★启用前2018年普通高等学校招生全国统一考试理科综合能力测试化学部分一、选择题:每小题 6分。
在每小题给出的四个选项中,只有一项是符合题目 要求的。
7 .硫酸亚铁锂(LiFePQ )电池是新能源汽车的动力电池之一。
采用湿法冶金工 艺回收废旧硫酸亚铁锂电池正极片中的金属,其流程如下:卜列叙述错误的是A.合理处理废旧电池有利于保护环境和资源再利用B.从“正极片”中可回收的金属元素有 Al 、Fe 、LiC. “沉淀”反应的金属离子为Fe 3+D.上述流程中可用硫酸钠代替碳酸钠 8 .下列说法错误的是A.蔗糖、果糖和麦芽糖均为双糖B.酶是一类具有高选择催化性能的蛋白质C.植物油含不饱和脂肪酸酯,能使 Br?CCl 4褪色D.淀粉和纤维素水解的最终产物均为葡萄糖9 .在生成和纯化乙酸乙酯的实验过程中,下列操作未涉及的是L^AIO 工滤液X 加”凡SO/HNOJ二雪牌酸把铁锲流海 ---------- L 含Li, P,小等滤液题速炭黑等穗渣含Li 沉淀10 . M 是阿伏加德罗常数的值,下列说法正确的是A. 16.25 g FeCl 3水解形成的Fe (OH >胶体粒子数为0.1 N AB. 22.4 L (标准状况)氨气含有的质子数为 18NC. 92.0 g 甘油(丙三醇)中含有羟基数为 1.0 MD. 1.0 mol CH 4与CI 2在光照下反应生成的 CHCl 分子数为1.0N A11.环之间共用一个碳原子的化合物称为螺环化合物,螺 [2,2]戊烷(.一'・•.) 是最简单的一种。
下列关于该化合物的说法错误的是 A.与环戊烯互为同分异构体 B.二氯代物超过两种 C 所有碳原子均处同一平面D 生成1 mol C 5H 12至少需要2 mol H 212.主族元素 W X 、Y 、Z 的原子序数依次增加,且均不大于 20。
W X 、Z 最外 层电子数之和为10; W 与Y 同族;W 与Z 形成的化合物可与浓硫酸反应,其 生成物可腐蚀玻璃。

2018 年全国高考理综 (Ⅰ)卷化学试题部分参考答案一、选择题:每小题 6 分,在每小题给出的四个选项中,只有一选项是符合题目要求的。
7.磷酸亚铁锂( LiFePO4)电池是新能源汽车的动力电池之一。
采用湿法冶金工艺回收废旧磷酸亚铁锂电池正极片中的金属,其流程如下:NaAlO2 溶液沉淀正极片碱溶含 Li、Fe、P 等滤液碱溶含 4滤渣H2SO4/滤液LiFePOHNO3 Na2CO3炭黑等滤渣含锂沉淀下列叙述错误的是..A.合理处理废旧电池有利于保护环境和资源再利用B.从“正极片”中可回收的金属元素有Al、 Fe、 LiC.“沉淀”反应的金属离子为Fe3+D.上述流程中可用硫酸钠代替碳酸钠【答案分析】 D。
硫酸锂可溶于水,不能形成沉淀,所以上述最后从滤液中将锂形成沉淀而从滤液中分离的目的,不宜用硫酸钠。
8.下列说法错误的是A.蔗糖、果糖和麦芽糖均为双糖B.酶是一类具有高选择催化性能的蛋白质C.植物油含有不饱和脂肪酸甘油酯,能使Br2/CCl4褪色D.淀粉和纤维素水解的最终产生均为葡萄糖【答案与分析】 A。
果糖属于单糖。
9.在生成和纯化乙酸乙酯的实验过程中,下列操作未涉及的是乙醇、冰醋酸浓硫酸饱和碳酸钠溶液A B C D【答案与分析】D。
实验室用乙醇与乙酸酯化反应制备并分离乙酸乙酯的方法是用分液法,而不能采用加热蒸发结晶法,10.??A是阿伏加得罗常数的值,下列说法正确的是A. 16.25gFeCl3 水解形成的 Fe(OH)3胶体粒子数为 0.1??AB. 22.4L(标准状况下)氩气含有的质子数为18??AC . 92.0g 甘油(丙三醇)中含有羟基数为 1.0??A. 4 与 Cl2 在光照下反应生成 3 分子数为1.0??A D 1.0molCH CH Cl 【答案与分析】 B 。
盐类水解的程度是很小的, A 不对;隋性气体属于单原子分子,1mol 的氩气 在标准状况下所占的体积为22.4L ,所含的电子数和质子数相等,均为 18mol ,B 正确; 1mol 甘油 (丙三醇)中含有 3?? 的羟基, C 错误;CH 4 与 CL2在光照的条件下反应生成的产物中含有 CH3、 ?? ClCH 2Cl 2 、CHCl 及 CCl ,则生成物中含有的 CH 少于 , D 不对。

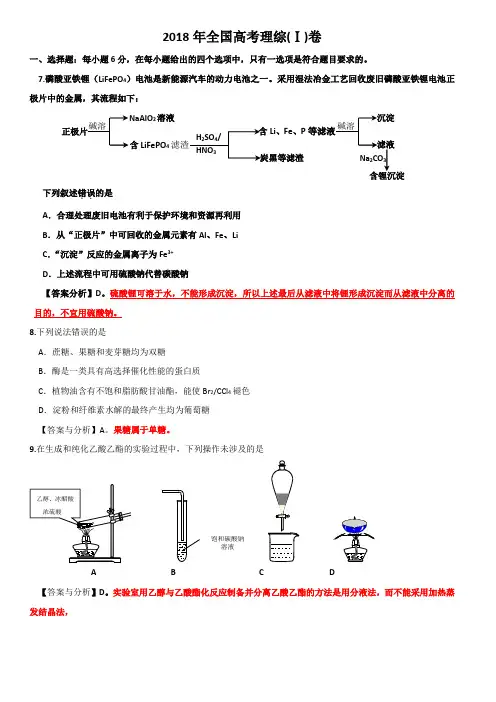
2018年全国统一高考化学试卷(新课标Ⅰ)一、选择题(共7小题,每小题6分,满分42分)1.(6分)磷酸亚铁锂(LiFePO4)电池是新能源汽车的动力电池之一,采用湿法冶金工艺回收废旧磷酸亚铁锂电池正极片中的金属,其流程如下:下列叙述错误的是()A.合理处理废旧电池有利于保护环境和资源再利用B.从“正极片”中可回收的金属元素有Al、Fe、LiC.“沉淀”反应的金属离子为Fe3+ D.上述流程中可用硫酸钠代替碳酸钠2.(6分)下列说法错误的是()A.蔗糖、果糖和麦芽糖均为双糖B.酶是一类具有高选择催化性能的蛋白质*C.植物油含不饱和脂肪酸酯,能使Br2/CCl4褪色D.淀粉和纤维素水解的最终产物均为葡萄糖3.(6分)在生成和纯化乙酸乙酯的实验过程中,下列操作未涉及的是()A.B.C.D.4.(6分)N A是阿伏加德罗常数的值,下列说法正确的是()A.,水解形成的Fe(OH)3为胶体粒子数为B.(标准状况)氩气含有的质子数为18N AC.甘油(丙三醇)中含有羟基数为D.与Cl2在光照下生成CH3Cl的分子数为5.(6分)环之间共用一个碳原子的化合物称为螺环化合物,螺(2,2)戊烷()是最单的一种,下列关于该化合物的说法错误的是()【A.与环戊烯互为同分异构体B.二氯化物超过两种C.所有碳原子均处同一平面D.生成1molC5H12,至少需要2molH26.(6分)主族元素W、X、Y、Z的原子序数依次增加,且均不大于20.W、X、Z最外层电子数之和为10;W与Y同族;W与Z形成的化台物可与浓硫酸反应,其生成物可腐蚀玻璃。
下列说法正确的是()A.常温常压下X的单质为气态B.Z的氢化物为离子化合物C.Y和Z形成的化合物的水溶液呈碱性D.W与Y具有相同的最高化合价7.(6分)最近我国科学家设计了一种CO2+H2S协同转化装置,实现对天然气中CO2和H2S 的高效去除。
示意图如右所示,其中电极分别为ZnO@石墨烯(石墨烯包裹的ZnO)和石墨烯,石墨烯电极区发生反应为:①EDTA﹣Fe2+﹣e﹣=EDTA﹣Fe3+②2EDTA﹣Fe3++H2S=2H++S+2EDTA﹣Fe2+该装置工作时,下列叙述错误的是()A.阴极的电极反应:CO2+2H++2e﹣═CO+H2OB.协同转化总反应:CO2+H2S═CO+H2O+S,C.石墨烯上的电势比ZnO@石墨烯上的低D.若采用Fe3+/Fe2+取代EDTA﹣Fe3+/EDTA﹣Fe2+,溶液需为酸性二、解答题(共3小题,满分43分)8.(14分)醋酸亚铬[(CH3COO)2Cr•2H2O]为砖红色晶体,难溶于冷水,易溶于酸,在气体分析中用作氧气吸收剂。
2018年全国高考理综(Ⅰ)卷一、选择题:每小题6分,在每小题给出的四个选项中,只有一选项是符合题目要求的。
7.磷酸亚铁锂(LiFePO 4)电池是新能源汽车的动力电池之一。
采用湿法冶金工艺回收废旧磷酸亚铁锂电池正极片中的金属,其流程如下:下列叙述错误..的是 A .合理处理废旧电池有利于保护环境和资源再利用 B .从“正极片”中可回收的金属元素有Al 、Fe 、Li C .“沉淀”反应的金属离子为Fe 3+ D .上述流程中可用硫酸钠代替碳酸钠【答案分析】D 。
硫酸锂可溶于水,不能形成沉淀,所以上述最后从滤液中将锂形成沉淀而从滤液中分离的目的,不宜用硫酸钠。
8.下列说法错误的是A .蔗糖、果糖和麦芽糖均为双糖B .酶是一类具有高选择催化性能的蛋白质C .植物油含有不饱和脂肪酸甘油酯,能使Br 2/CCl 4褪色D .淀粉和纤维素水解的最终产生均为葡萄糖 【答案与分析】A 。
果糖属于单糖。
9.在生成和纯化乙酸乙酯的实验过程中,下列操作未涉及的是A B C D【答案与分析】D 。
实验室用乙醇与乙酸酯化反应制备并分离乙酸乙酯的方法是用分液法,而不能采用加热蒸发结晶法,2溶液 LiFePO 4Li 、Fe 、P滤液 Na 2CO 3 含锂沉淀饱和碳酸钠溶液10.是阿伏加得罗常数的值,下列说法正确的是A.16.25gFeCl3水解形成的Fe(OH)3胶体粒子数为0.1B.22.4L(标准状况下)氩气含有的质子数为18C.92.0g甘油(丙三醇)中含有羟基数为1.0D.1.0molCH4与Cl2在光照下反应生成CH3Cl分子数为1.0【答案与分析】B。
盐类水解的程度是很小的,A不对;隋性气体属于单原子分子,1mol的氩气在标准状况下所占的体积为22.4L,所含的电子数和质子数相等,均为18mol,B正确;1mol甘油(丙三醇)中含有3的羟基,C错误;CH4与CL2在光照的条件下反应生成的产物中含有CH3Cl、CH2Cl2、CHCl3及CCl4,则生成物中含有的CH3Cl少于1mol,D不对。

绝密★启用前2018年普通高等学校招生全国统一考试(全国I卷)化学试题注意事项:1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑,如需改动,用橡皮擦干净后,再选涂其它答案标号。
回答非选择题时,将答案写在答题卡上,写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 Li 7 C 12 N 14 O 16 Na 23 S 32 Cl 35.5 Ar 40 Fe 56 I 127一、选择题:本题共6个小题,每小题6分。
在每小题给出的四个选项中,只有一项是符合题目要求的。
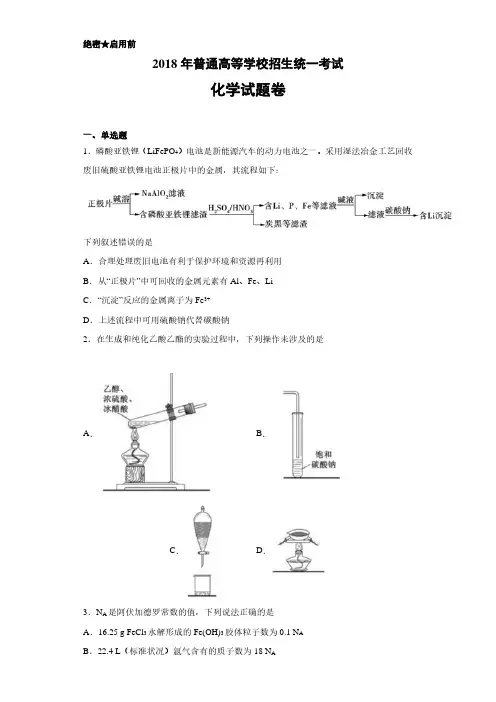
7.硫酸亚铁锂(LiFePO4)电池是新能源汽车的动力电池之一。
采用湿法冶金工艺回收废旧硫酸亚铁锂电池正极片中的金属,其流程如下:下列叙述错误的是A.合理处理废旧电池有利于保护环境和资源再利用B.从“正极片”中可回收的金属元素有Al、Fe、LiC.“沉淀”反应的金属离子为Fe3+D.上述流程中可用硫酸钠代替碳酸钠8.下列说法错误的是A.蔗糖、果糖和麦芽糖均为双糖B.酶是一类具有高选择催化性能的蛋白质C.植物油含不饱和脂肪酸酯,能使Br₂/CCl4褪色D.淀粉和纤维素水解的最终产物均为葡萄糖9.在生成和纯化乙酸乙酯的实验过程中,下列操作未涉及的是10.N A是阿伏加德罗常数的值,下列说法正确的是A.16.25 g FeCl3水解形成的Fe(OH)3胶体粒子数为0.1 N AB.22.4 L(标准状况)氨气含有的质子数为18N AC.92.0 g甘油(丙三醇)中含有羟基数为1.0N AD.1.0 mol CH4与Cl2在光照下反应生成的CH3Cl分子数为1.0N A11.环之间共用一个碳原子的化合物称为螺环化合物,螺[2,2]戊烷()是最简单的一种。
下列关于该化合物的说法错误的是A.与环戊烯互为同分异构体B.二氯代物超过两种C.所有碳原子均处同一平面D生成1 mol C5H12至少需要2 mol H212.主族元素W、X、Y、Z的原子序数依次增加,且均不大于20。

2018年普通高等学校招生全国统一考试理科综合能力测试注意事项:1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑,如需改动,用橡皮擦干净后,再选涂其它答案标号。
回答非选择题时,将答案写在答题卡上,写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
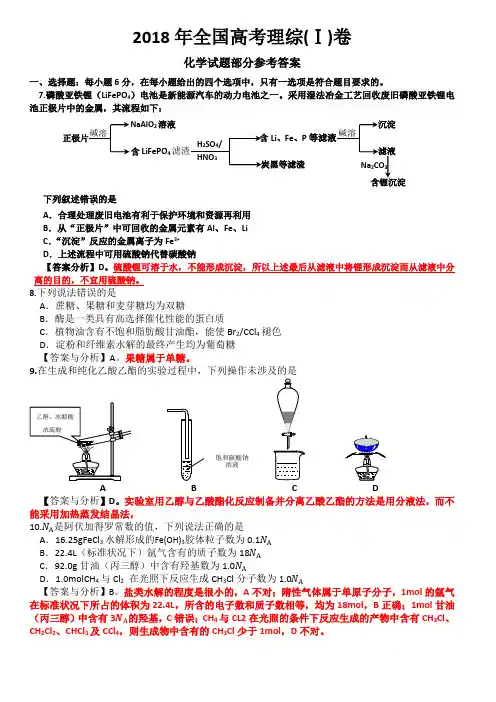
学·科网可能用到的相对原子质量:H 1 Li 7 C12N14O16 Na 23 S 32 Cl 35.5 Ar 40 Fe 56 I 127一、选择题7.硫酸亚铁锂(LiFePO4)电池是新能源汽车的动力电池之一。
采用湿法冶金工艺回收废旧硫酸亚铁锂电池正极片中的金属,其流程如下:下列叙述错误的是A.合理处理废旧电池有利于保护环境和资源再利用B.从“正极片”中可回收的金属元素有Al、Fe、LiC.“沉淀”反应的金属离子为Fe3+D.上述流程中可用硫酸钠代替碳酸钠8.下列说法错误的是A.蔗糖、果糖和麦芽糖均为双糖B.酶是一类具有高选择催化性能的蛋白质C.植物油含不饱和脂肪酸酯,能使Br₂/CCl4褪色D.淀粉和纤维素水解的最终产物均为葡萄糖9.在生成和纯化乙酸乙酯的实验过程中,下列操作未涉及的是10.N A是阿伏加德罗常数的值,下列说法正确的是A.16.25 g FeCl3水解形成的Fe(OH)3胶体粒子数为0.1 N AB.22.4 L(标准状况)氨气含有的质子数为18N AC.92.0 g甘油(丙三醇)中含有羟基数为1.0N AD.1.0 mol CH4与Cl2在光照下反应生成的CH3Cl分子数为1.0N A11.环之间共用一个碳原子的化合物称为螺环化合物,螺[2,2]戊烷()是最简单的一种。
下列关于该化合物的说法错误的是A.与环戊烯互为同分异构体B.二氯代物超过两种C.所有碳原子均处同一平面D生成1 mol C5H12至少需要2 mol H212.主族元素W、X、Y、Z的原子序数依次增加,且均不大于20。
2018年全国高考理综(Ⅰ)卷化学试题部分参考答案一、选择题:每小题6分,在每小题给出的四个选项中,只有一选项是符合题目要求的。
7.磷酸亚铁锂(LiFePO 4)电池是新能源汽车的动力电池之一。
采用湿法冶金工艺回收废旧磷酸亚铁锂电池正极片中的金属,其流程如下:下列叙述错误..的是 A .合理处理废旧电池有利于保护环境和资源再利用 B .从“正极片”中可回收的金属元素有Al 、Fe 、Li C .“沉淀”反应的金属离子为Fe 3+ D .上述流程中可用硫酸钠代替碳酸钠【答案分析】D 。
硫酸锂可溶于水,不能形成沉淀,所以上述最后从滤液中将锂形成沉淀而从滤液中分离的目的,不宜用硫酸钠。
8.下列说法错误的是A .蔗糖、果糖和麦芽糖均为双糖B .酶是一类具有高选择催化性能的蛋白质C .植物油含有不饱和脂肪酸甘油酯,能使Br 2/CCl 4褪色D .淀粉和纤维素水解的最终产生均为葡萄糖 【答案与分析】A 。
果糖属于单糖。
9.A B C D【答案与分析】D 。
实验室用乙醇与乙酸酯化反应制备并分离乙酸乙酯的方法是用分液法,而不能采用加热蒸发结晶法,10.N A 是阿伏加得罗常数的值,下列说法正确的是A .16.25gFeCl 3水解形成的Fe(OH)3胶体粒子数为0.1N AB .22.4L (标准状况下)氩气含有的质子数为18N AC .92.0g 甘油(丙三醇)中含有羟基数为1.0N AD .1.0molCH 4与Cl 2 在光照下反应生成CH 3Cl 分子数为1.0N A【答案与分析】B 。
盐类水解的程度是很小的,A 不对;隋性气体属于单原子分子,1mol 的氩气在标准状况下所占的体积为22.4L ,所含的电子数和质子数相等,均为18mol ,B 正确;1mol 甘油(丙三醇)中含有3N A 的羟基,C 错误;CH 4与CL2在光照的条件下反应生成的产物中含有CH 3Cl 、CH 2Cl 2、CHCl 3及CCl 4,则生成物中含有的CH 3Cl 少于1mol ,D 不对。

2018年全国统一考试新课标Ⅰ卷化学试题详解一、选择题(共7小题,每小题6分,满分42分)7.(6.00分)磷酸亚铁锂(LiFePO4)电池是新能源汽车的动力电池之一,采用湿法冶金工艺回收废旧磷酸亚铁锂电池正极片中的金属,其流程如下:下列叙述错误的是()A.合理处理废旧电池有利于保护环境和资源再利用B.从“正极片”中可回收的金属元素有Al、Fe、LiC.“沉淀”反应的金属离子为Fe3+D.上述流程中可用硫酸钠代替碳酸钠【分析】正极片经碱溶可得到NaAlO2,可说明含有Al元素,含有磷酸亚铁锂的滤渣加入硫酸、硝酸,可除去炭黑,得到含有P、Fe、Li的滤液,加入碱液,生成的沉淀为Fe(OH)3,滤液加入碳酸钠,可生成碳酸锂沉淀,以此解答该题。
【解答】解:A.合理处理废旧电池,可减少污染性废水的排放,且回收含有Al、Fe等金属,可再利用,故A正确;B.由以上分析可知从“正极片”中可回收的金属元素有Al、Fe、Li等,故B正确;C.硝酸具有强氧化性,可氧化亚铁离子生成铁离子,则“沉淀”反应的金属离子为Fe3+,故C正确;D.加入硫酸钠,不能生成含Li沉淀,故D错误。
故选:D。
【点评】本题为2018年高考全国卷,以元素化合物知识为载体考查物质的分离、提纯,有利于培养学生的分析能力和实验能力,树立积极的环境保护意识和资源的合理运用,题目难度不大。
8.(6.00分)下列说法错误的是()A.蔗糖、果糖和麦芽糖均为双糖知己知彼,百战不殆!B.酶是一类具有高选择催化性能的蛋白质C.植物油含不饱和脂肪酸酯,能使Br2/CCl4褪色D.淀粉和纤维素水解的最终产物均为葡萄糖【分析】A.果糖为单糖;B.绝大多数酶是蛋白质;C.植物油为高级脂肪酸甘油酯,烃基含不饱和碳碳双键;D.多糖最终水解产物为单糖。
【解答】解:A.蔗糖和麦芽糖均为双糖,果糖为单糖,故A错误;B.绝大多数酶是蛋白质,少数具有生物催化功能的分子不是蛋白质,如复合酶,故B错误;C.植物油为液态油脂,分子的烃基中含不饱和碳碳双键,这种脂肪酸酯,能使Br2/CCl4褪色,发生加成反应,故C正确;D.淀粉和纤维素为多糖,一定条件下水解的最终产物均为葡萄糖,故D正确;故选:AB。

2018年高考全国卷1化学试题答案解析2018年高考全国卷1化学试题解析版硫酸亚铁锂(LiFePO4)电池是新能源汽车的动力电池之一,采用湿法冶金工艺回收废旧硫酸亚铁锂电池正极片中的金属。
其回收流程如下:A。
合理处理废旧电池有利于保护环境和资源再利用。
B。
从正极片中可回收的金属元素有Al、Fe、Li。
C。
“沉淀”反应的金属离子为Fe3+。
D。
上述流程中可用硫酸钠代替碳酸钠。
答案:D解析:正极片碱溶时铝转化为偏铝酸钠,滤渣中含有磷酸亚铁锂,加入硫酸和硝酸酸溶,过滤后滤渣是炭黑,得到含Li、P、Fe的滤液,加入碱液生成氢氧化铁沉淀,滤液中加入碳酸钠生成含锂的沉淀,据此解答。
详解:废旧电池中含有重金属,随意排放容易污染环境,因此合理处理废旧电池有利于保护环境和资源再利用。
从流程的转化可知,从正极片中可回收的金属元素有Al、Fe、Li。
得到含Li、P、Fe的滤液,加入碱液生成氢氧化铁沉淀,因此“沉淀”反应的金属离子是Fe。
硫酸锂能溶于水,因此上述流程中不能用硫酸钠代替碳酸钠。
答案选D。
本题以废旧电池的回收为载体考查金属元素的回收,明确流程中元素的转化关系是解答的关键,题目难度不大。
在生成和纯化乙酸乙酯的实验过程中,下列操作未涉及的是:A。
A。
B。
B。
C。
C。
D。
D答案:D详解:A、螺[2,2]戊烷与环戊烯分子式相同但结构不同,因此互为同分异构体,A正确;B、根据螺[2,2]戊烷分子中氢原子的种类可知,二氯代物最多有4种,B错误;C、螺[2,2]戊烷分子中的所有碳原子不处于同一平面,因为螺环结构中的碳原子存在空间位阻,C错误;D、生成1 mol C5H12需要10 mol H2因为螺[2,2]戊烷分子中有10个氢原子,氢原子守恒,D 正确。
答案选C。
点睛:本题考查对螺环化合物的基本概念和结构特点的理解,同时也考查了对氢原子守恒定律的应用。
注意选项B的干扰,需要根据分子中氢原子的种类进行判断。
A、螺[2,2]戊烷和环戊烯的分子式分别为C5H8虽然结构不同,但它们是互为同分异构体的关系,因此A 正确;B、分子中的8个氢原子完全相同,二氯代物中可以取代同一个碳原子上的氢原子,也可以取代相邻或不相邻的碳原子上的氢原子,所以二氯代物的种类超过两种,B正确;C、由于分子中4个碳原子均是饱和碳原子,而与饱和碳原子相连的4个原子一定构成四面体,因此分子中所有碳原子不可能均处在同一平面上,C错误;D、戊烷比螺[2,2]戊烷多4个氢原子,因此生成1 mol C5H12至少需要2 mol H2D正确。
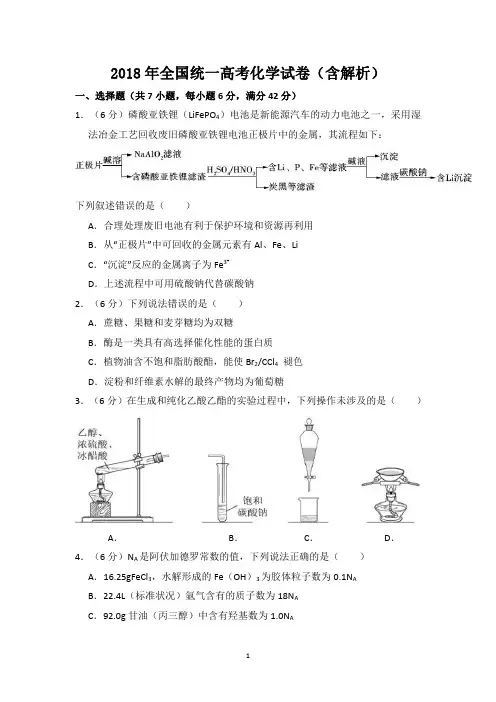
2018年全国统一高考化学试卷(含解析)一、选择题(共7小题,每小题6分,满分42分)1.(6分)磷酸亚铁锂(LiFePO4)电池是新能源汽车的动力电池之一,采用湿法冶金工艺回收废旧磷酸亚铁锂电池正极片中的金属,其流程如下:下列叙述错误的是()A.合理处理废旧电池有利于保护环境和资源再利用B.从“正极片”中可回收的金属元素有Al、Fe、LiC.“沉淀”反应的金属离子为Fe3+D.上述流程中可用硫酸钠代替碳酸钠2.(6分)下列说法错误的是()A.蔗糖、果糖和麦芽糖均为双糖B.酶是一类具有高选择催化性能的蛋白质C.植物油含不饱和脂肪酸酯,能使Br2/CCl4褪色D.淀粉和纤维素水解的最终产物均为葡萄糖3.(6分)在生成和纯化乙酸乙酯的实验过程中,下列操作未涉及的是()A.B.C.D.4.(6分)N A是阿伏加德罗常数的值,下列说法正确的是()A.16.25gFeCl3,水解形成的Fe(OH)3为胶体粒子数为0.1N AB.22.4L(标准状况)氩气含有的质子数为18N AC.92.0g甘油(丙三醇)中含有羟基数为1.0N AD.1.0molCH4与Cl2在光照下生成CH3Cl的分子数为1.0N A5.(6分)环之间共用一个碳原子的化合物称为螺环化合物,螺(2,2)戊烷()是最简单的一种,下列关于该化合物的说法错误的是()A.与环戊烯互为同分异构体B.二氯化物超过两种C.所有碳原子均处同一平面D.生成1molC5H12,至少需要2molH2 6.(6分)主族元素W、X、Y、Z的原子序数依次增加,且均不大于20.W、X、Z最外层电子数之和为10;W与Y同族;W与Z形成的化合物可与浓硫酸反应,其生成物可腐蚀玻璃。
下列说法正确的是()A.常温常压下X的单质为气态B.Z的氢化物为离子化合物C.Y和Z形成的化合物的水溶液呈碱性D.W与Y具有相同的最高化合价7.(6分)最近我国科学家设计了一种CO2+H2S协同转化装置,实现对天然气中CO2和H2S的高效去除。
2018全国高考化学试卷(含答案和解析)学校:___________姓名:___________班级:___________考号:___________评卷人得分一、单选题1.磷酸亚铁锂(LiFePO4)电池是新能源汽车的动力电池之一。
采用湿法冶金工艺回收废旧硫酸亚铁锂电池正极片中的金属,其流程如下:下列叙述错误的是A.合理处理废旧电池有利于保护环境和资源再利用B.从“正极片”中可回收的金属元素有Al、Fe、LiC.“沉淀”反应的金属离子为Fe3+D.上述流程中可用硫酸钠代替碳酸钠2.在生成和纯化乙酸乙酯的实验过程中,下列操作未涉及的是A.B.C.D.3.N A是阿伏加德罗常数的值,下列说法正确的是A.16.25g FeCl3水解形成的Fe(OH)3胶体粒子数为0.1N AB.22.4L(标准状况)氩气含有的质子数为18N AC.92.0g甘油(丙三醇)中含有羟基数为1.0N AD.1.0mol CH4与Cl2在光照下反应生成的CH3Cl分子数为1.0N A4.环之间共用一个碳原子的化合物称为螺环化合物,螺[2,2]戊烷()是最简单的一种。
下列关于该化合物的说法错误的是()A.与环戊烯互为同分异构体B.二氯代物超过两种C.所有碳原子均处同一平面D.生成1molC5H12至少需要2molH25.主族元素W、X、Y、Z的原子序数依次增加,且均不大于20。
W、X、Z最外层电子数之和为10;W与Y同族;W与Z形成的化合物可与浓硫酸反应,其生成物可腐蚀玻璃。
下列说法正确的是A.常温常压下X的单质为气态B.Z的氢化物为离子化合物C.Y和Z形成的化合物的水溶液呈碱性D.W与Y具有相同的最高化合价6.最近我国科学家设计了一种CO2+H2S协同转化装置,实现对天然气中CO2和H2S 的高效去除。
示意图如图所示,其中电极分别为ZnO@石墨烯(石墨烯包裹的ZnO)和石墨烯,石墨烯电极区发生反应为:①EDTA-Fe2+-e-=EDTA-Fe3+②2EDTA-Fe3++H2S=2H++S+2EDTA-Fe2+该装置工作时,下列叙述错误的是A.阴极的电极反应:CO2+2H++2e-=CO+H2OB.协同转化总反应:CO2+H2S=CO+H2O+SC.石墨烯上的电势比ZnO@石墨烯上的低D.若采用Fe3+/Fe2+取代EDTA-Fe3+/EDTA-Fe2+,溶液需为酸性试卷第2页,总18页7.化学与生活密切相关。
2018年全国统一高考化学试卷(新课标Ⅰ)一、选择题(共7小题,每小题6分,满分42分)1.(6分)磷酸亚铁锂(LiFePO4)电池是新能源汽车的动力电池之一,采用湿法冶金工艺回收废旧磷酸亚铁锂电池正极片中的金属,其流程如下:下列叙述错误的是()A.合理处理废旧电池有利于保护环境和资源再利用B.从“正极片”中可回收的金属元素有Al、Fe、LiC.“沉淀”反应的金属离子为Fe3+ D.上述流程中可用硫酸钠代替碳酸钠2.(6分)下列说法错误的是()A.蔗糖、果糖和麦芽糖均为双糖 B.酶是一类具有高选择催化性能的蛋白质C.植物油含不饱和脂肪酸酯,能使Br2/CCl4褪色D.淀粉和纤维素水解的最终产物均为葡萄糖3.(6分)在生成和纯化乙酸乙酯的实验过程中,下列操作未涉及的是()A.B. C.D.4.(6分)N A是阿伏加德罗常数的值,下列说法正确的是()A.16.25gFeCl3,水解形成的Fe(OH)3为胶体粒子数为0.1N AB.22.4L(标准状况)氩气含有的质子数为18N AC.92.0g甘油(丙三醇)中含有羟基数为1.0N AD.1.0molCH4与Cl2在光照下生成CH3Cl的分子数为1.0N A5.(6分)环之间共用一个碳原子的化合物称为螺环化合物,螺(2,2)戊烷()是最单的一种,下列关于该化合物的说法错误的是()A.与环戊烯互为同分异构体 B.二氯化物超过两种C.所有碳原子均处同一平面 D.生成1molC5H12,至少需要2molH26.(6分)主族元素W、X、Y、Z的原子序数依次增加,且均不大于20.W、X、Z最外层电子数之和为10;W与Y同族;W与Z形成的化台物可与浓硫酸反应,其生成物可腐蚀玻璃。
下列说法正确的是()A.常温常压下X的单质为气态 B.Z的氢化物为离子化合物C.Y和Z形成的化合物的水溶液呈碱性 D.W与Y具有相同的最高化合价7.(6分)最近我国科学家设计了一种CO2+H2S协同转化装置,实现对天然气中CO2和H2S的高效去除。
绝密★启用前2018年普通高等学校招生全国统一考试(全国I卷)化学试题注意事项:1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑,如需改动,用橡皮擦干净后,再选涂其它答案标号。
回答非选择题时,将答案写在答题卡上,写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 Li 7 C 12 N 14 O 16 Na 23 S 32 Cl 35.5 Ar 40 Fe 56 I 127一、选择题:本题共6个小题,每小题6分。
在每小题给出的四个选项中,只有一项是符合题目要求的。
7.硫酸亚铁锂(LiFePO4)电池是新能源汽车的动力电池之一。
采用湿法冶金工艺回收废旧硫酸亚铁锂电池正极片中的金属,其流程如下:下列叙述错误的是A.合理处理废旧电池有利于保护环境和资源再利用B.从“正极片”中可回收的金属元素有Al、Fe、LiC.“沉淀”反应的金属离子为Fe3+D.上述流程中可用硫酸钠代替碳酸钠8.下列说法错误的是A.蔗糖、果糖和麦芽糖均为双糖B.酶是一类具有高选择催化性能的蛋白质C.植物油含不饱和脂肪酸酯,能使Br₂/CCl4褪色D.淀粉和纤维素水解的最终产物均为葡萄糖9.在生成和纯化乙酸乙酯的实验过程中,下列操作未涉及的是10.N A是阿伏加德罗常数的值,下列说法正确的是A.16.25 g FeCl3水解形成的Fe(OH)3胶体粒子数为0.1 N AB.22.4 L(标准状况)氨气含有的质子数为18N AC.92.0 g甘油(丙三醇)中含有羟基数为1.0N AD.1.0 mol CH4与Cl2在光照下反应生成的CH3Cl分子数为1.0N A11.环之间共用一个碳原子的化合物称为螺环化合物,螺[2,2]戊烷()是最简单的一种。
下列关于该化合物的说法错误的是A.与环戊烯互为同分异构体B.二氯代物超过两种C.所有碳原子均处同一平面D生成1 mol C5H12至少需要2 mol H212.主族元素W、X、Y、Z的原子序数依次增加,且均不大于20。
2018年全国统一高考化学试卷(新课标Ⅰ)一、选择题(共7小题,每小题6分,满分42分)1.(6分)磷酸亚铁锂(LiFePO4)电池是新能源汽车的动力电池之一,采用湿法冶金工艺回收废旧磷酸亚铁锂电池正极片中的金属,其流程如下:下列叙述错误的是()A.合理处理废旧电池有利于保护环境和资源再利用B.从“正极片”中可回收的金属元素有Al、Fe、LiC.“沉淀”反应的金属离子为Fe3+ D.上述流程中可用硫酸钠代替碳酸钠2.(6分)下列说法错误的是()A.蔗糖、果糖和麦芽糖均为双糖 B.酶是一类具有高选择催化性能的蛋白质C.植物油含不饱和脂肪酸酯,能使Br2/CCl4褪色D.淀粉和纤维素水解的最终产物均为葡萄糖3.(6分)在生成和纯化乙酸乙酯的实验过程中,下列操作未涉及的是()A.B. C.D.4.(6分)N A是阿伏加德罗常数的值,下列说法正确的是()A.16.25gFeCl3,水解形成的Fe(OH)3为胶体粒子数为0.1N AB.22.4L(标准状况)氩气含有的质子数为18N AC.92.0g甘油(丙三醇)中含有羟基数为1.0N AD.1.0molCH4与Cl2在光照下生成CH3Cl的分子数为1.0N A5.(6分)环之间共用一个碳原子的化合物称为螺环化合物,螺(2,2)戊烷()是最单的一种,下列关于该化合物的说法错误的是()A.与环戊烯互为同分异构体 B.二氯化物超过两种C.所有碳原子均处同一平面 D.生成1molC5H12,至少需要2molH26.(6分)主族元素W、X、Y、Z的原子序数依次增加,且均不大于20.W、X、Z最外层电子数之和为10;W与Y同族;W与Z形成的化台物可与浓硫酸反应,其生成物可腐蚀玻璃。
下列说法正确的是()A.常温常压下X的单质为气态 B.Z的氢化物为离子化合物C.Y和Z形成的化合物的水溶液呈碱性 D.W与Y具有相同的最高化合价7.(6分)最近我国科学家设计了一种CO2+H2S协同转化装置,实现对天然气中CO2和H2S的高效去除。
绝密★启用前2018年普通高等学校招生全国统一考试理科综合能力测试注意事项:1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。
如需改动,用橡皮擦干净后,再选涂其它答案标号。
回答非选择题时,将答案写在答题卡上。
写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H1Li7C12N14O16Na23S32Cl35.5Ar40Fe56I127一、选择题:本题共13小题,每小题6分,共78分。
在每小题给出的四个选项中,只有一项是符合题目要求的。
7.磷酸亚铁锂(LiFePO4)电池是新能源汽车的动力电池之一。
采用湿法冶金工艺回收废旧磷酸亚铁锂电池正极片中的金属,其流程如下:下列叙述错误的是A.合理处理废旧电池有利于保护环境和资源再利用B.从“正极片”中可回收的金属元素有Al、Fe、LiC.“沉淀”反应的金属离子为3FeD.上述流程中可用硫酸钠代替碳酸钠8.下列说法错误的是A.蔗糖、果糖和麦芽糖均为双糖B.酶是一类具有高选择催化性能的蛋白质C.植物油含不饱和脂肪酸酯,能使Br/CCl褪色24D.淀粉和纤维素水解的最终产物均为葡萄糖9.在生成和纯化乙酸乙酯的实验过程中,下列操作未涉及的是10.A N 是阿伏加德罗常数的值。
下列说法正确的是A .16.25g 3FeCl 水解形成的3Fe(OH)胶体粒子数为0.1A NB .22.4L (标准状况)氩气含有的质子数为18A NC .92.0g 甘油(丙三醇)中含有羟基数为1.0AN D .1.0mol 4CH 与2Cl 在光照下反应生成的3CH Cl 分子数为A1.0N 11.环之间共用一个碳原子的化合物称为螺环化合物,螺[2.2]戊烷()是最简单的一种。
下列关于该化合物的说法错误的是A .与环戊烯互为同分异构体B .二氯代物超过两种C .所有碳原子均处同一平面D .生成1mol 512C H 至少需要2mol 2H 12.主族元素W 、X 、Y 、Z 的原子序数依次增加,且均不大于20。
2018年普通高等学校招生全国统一考试(全国卷1)理科综合能力测试化学部分生物:1-6、29-32、37-38化学:7-13、26-28、35-36物理:14-21、22-25、33-34注意事项:1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑,如需改动,用橡皮擦干净后,再选涂其它答案标号。
回答非选择题时,将答案写在答题卡上,写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
学·科网可能用到的相对原子质量:H 1 Li 7 C 12 N 14 O 16 Na 23 S 32 Cl 35.5 Ar 40 Fe 56 I 127 一、选择题:本题共13个小题,每小题6分。
在每小题给出的四个选项中,只有一项是符合题目要求的。
7.硫酸亚铁锂(LiFePO4)电池是新能源汽车的动力电池之一。
采用湿法冶金工艺回收废旧硫酸亚铁锂电池正极片中的金属,其流程如下:下列叙述错误的是A.合理处理废旧电池有利于保护环境和资源再利用B.从“正极片”中可回收的金属元素有Al、Fe、LiC.“沉淀”反应的金属离子为Fe3+D.上述流程中可用硫酸钠代替碳酸钠8.下列说法错误的是A.蔗糖、果糖和麦芽糖均为双糖B.酶是一类具有高选择催化性能的蛋白质C.植物油含不饱和脂肪酸酯,能使Br₂/CCl4褪色D.淀粉和纤维素水解的最终产物均为葡萄糖9.在生成和纯化乙酸乙酯的实验过程中,下列操作未涉及的是10.N A是阿伏加德罗常数的值,下列说法正确的是A.16.25 g FeCl3水解形成的Fe(OH)3胶体粒子数为0.1 N AB.22.4 L(标准状况)氨气含有的质子数为18N AC.92.0 g甘油(丙三醇)中含有羟基数为1.0N AD.1.0 mol CH4与Cl2在光照下反应生成的CH3Cl分子数为1.0N A11.环之间共用一个碳原子的化合物称为螺环化合物,螺[2,2]戊烷()是最简单的一种。
绝密★启用前2018年普通高等学校招生全国统一考试理科综合能力测试可能用到的相对原子质量:H 1 Li 7 C 12 N 14 O 16 Na 23 S 32 Cl 35.5 Ar 40 Fe 56 I 127一、选择题:本题共7个小题,每小题6分。
共42分,在每小题给出的四个选项中,只有一项是符合题目要求的。
7.磷酸亚铁锂(LiFePO4)电池是新能源汽车的动力电池之一。
采用湿法冶金工艺回收废旧磷酸亚铁锂电池正极片中的金属,其流程如下:下列叙述错误的是A.合理处理废旧电池有利于保护环境和资源再利用B.从“正极片”中可回收的金属元素有Al、Fe、LiC.“沉淀”反应的金属离子为Fe3+D.上述流程中可用硫酸钠代替碳酸钠8.下列说法错误的是A.蔗糖、果糖和麦芽糖均为双糖B.酶是一类具有高选择催化性能的蛋白质C.植物油含不饱和脂肪酸酯,能使Br2/CCl4褪色D.淀粉和纤维素水解的最终产物均为葡萄糖9.在生成和纯化乙酸乙酯的实验过程中,下列操作未涉及的是10.N A是阿伏加德罗常数的值。
下列说法正确的是A.16.25 g FeCl3水解形成的Fe(OH)3胶体粒子数为0.1 N AB.22.4 L(标准状况)氩气含有的质子数为18N AC.92.0 g甘油(丙三醇)中含有羟基数为1.0N AD.1.0 mol CH4与Cl2在光照下反应生成的CH3Cl分子数为1.0N A11.环之间共用一个碳原子的化合物称为螺环化合物,螺[2,2]戊烷()是最简单的一种。
下列关于该化合物的说法错误的是学&科网A.与环戊烯互为同分异构体B.二氯代物超过两种C.所有碳原子均处同一平面D.生成1 mol C5H12至少需要2 mol H212.主族元素W、X、Y、Z的原子序数依次增加,且均不大于20。
W、X、Z最外层电子数之和为10;W与Y同族;W与Z形成的化合物可与浓硫酸反应,其生成物可腐蚀玻璃。
下列说法正确的是A.常温常压下X的单质为气态B.Z的氢化物为离子化合物C.Y和Z形成的化合物的水溶液呈碱性D.W与Y具有相同的最高化合价13.最近我国科学家设计了一种CO2+H2S协同转化装置,实现对天然气中CO2和H2S的高效去除。
示意图如图所示,其中电极分别为ZnO@石墨烯(石墨烯包裹的ZnO)和石墨烯,石墨烯电极区发生反应为:①EDTA-Fe2+-e-=EDTA-Fe3+②2EDTA-Fe3++H2S=2H++S+2EDTA-Fe2+该装置工作时,下列叙述错误的是A.阴极的电极反应:CO2+2H++2e-=CO+H2OB.协同转化总反应:CO2+H2S=CO+H2O+SC.石墨烯上的电势比ZnO@石墨烯上的低D.若采用Fe3+/Fe2+取代EDTA-Fe3+/EDTA-Fe2+,溶液需为酸性三、非选择题:共58分,第26~28题为必考题,每个试题考生都必须作答。
第34~35题为选考题,考生根据要求作答。
(一)必考题:共43分。
26.(14分)醋酸亚铬[(CH3COO)2Cr·2H2O]为砖红色晶体,难溶于冷水,易溶于酸,在气体分析中用作氧气吸收剂。
一般制备方法是先在封闭体系中利用金属锌作还原剂,将三价铬还原为二价铬;二价铬再与醋酸钠溶液作用即可制得醋酸亚铬。
实验装置如图所示。
回答下列问题:(1)实验中所用蒸馏水均需经煮沸后迅速冷却,目的是_________。
仪器a的名称是_______。
(2)将过量锌粒和氯化铬固体置于c中,加入少量蒸馏水,按图连接好装置,打开K1、K2,关闭K3。
①c中溶液由绿色逐渐变为亮蓝色,该反应的离子方程式为___________________________。
②同时c中有气体产生,该气体的作用是___________________________。
(3)打开K3,关闭K1和K2。
c中亮蓝色溶液流入d,其原因是________ ;d中析出砖红色沉淀。
为使沉淀充分析出并分离,需采用的操作是_________、_______、洗涤、干燥。
(4)指出装置d可能存在的缺点_________________________________________________。
27.(14分)焦亚硫酸钠(Na2S2O5)在医药、橡胶、印染、食品等方面应用广泛。
回答下列问题:(1)生产Na2S2O5,通常是由NaHSO3过饱和溶液经结晶脱水制得。
写出该过程的化学方程式_____________________________________________。
(2)利用烟道气中的SO2生产Na2S2O5的工艺为:①pH=4.1时,Ⅰ中为_________________溶液(写化学式)。
②工艺中加入Na2CO3固体、并再次充入SO2的目的是_______________________________。
(3)制备Na2S2O5也可采用三室膜电解技术,装置如图所示,其中SO2碱吸收液中含有NaHSO3和Na2SO3。
阳极的电极反应式为_____________。
电解后,_____________室的NaHSO3浓度增加。
将该室溶液进行结晶脱水,可得到Na2S2O5。
(4)Na 2S 2O 5可用作食品的抗氧化剂。
在测定某葡萄酒中Na 2S 2O 5残留量时,取50.00 mL 葡萄酒样品,用0.01000 mol·L −1的碘标准液滴定至终点,消耗10.00 mL 。
滴定反应的离子方程式为_____________________________________________________________________,该样品中Na 2S 2O 5的残留量为____________g·L −1(以SO 2计)。
28.(15分)采用N 2O 5为硝化剂是一种新型的绿色硝化技术,在含能材料、医药等工业中得到广泛应用。
回答下列问题:(1)1840年 Devil 用干燥的氯气通过干燥的硝酸银,得到N 2O 5,该反应的氧化产物是一种气体,其分子式为___________。
(2)F. Daniels 等曾利用测压法在刚性反应器中研究了25℃时N 2O 5(g )分解反应:其中NO 2二聚为N 2O 4的反应可以迅速达到平衡。
体系的总压强p 随时间t 的变化如下表所示(t =∞时,N 2O 5(g )完全分解):t /min0 40 80 160 260 1300 1700 ∞ p /kPa 35.8 40.3 42.5 45.9 49.2 61.2 62.3 63.1 ①已知:2N 2O 5(g )2N 2O 4(g )+O 2(g ) ΔH 1=−4.4 kJ·mol −1 2NO 2(g ) N 2O 4(g ) ΔH 2=−55.3 kJ·mol −1则反应N 2O 5(g )=2NO 2(g )+12O 2(g )的ΔH =_______ kJ·mol −1。
②研究表明,N 2O 5(g )分解的反应速率v =2×10−3×25N O p (kPa·min −1)。
t =62 min 时,测得体系中2O p =2.9 kPa ,则此时的25N O p =________ kPa ,v =_______ kPa·min −1。
③若提高反应温度至35℃,则N 2O 5(g )完全分解后体系压强p ∞(35℃)____63.1 kPa (填“大于”“等于”或“小于”),原因是___________________________________________。
④25℃时N2O4(g)2NO2(g)反应的平衡常数K p=_______kPa(K p为以分压表示的平衡常数,计算结果保留1位小数)。
(3)对于反应2N2O5(g)→4NO2(g)+O2(g),R.A.Ogg提出如下反应历程:第一步N2O5NO3+NO2快速平衡第二步NO2+NO3→NO+NO2+O2 慢反应第三步NO+NO3→2NO2快反应其中可近似认为第二步反应不影响第一步的平衡。
下列表述正确的是__________(填标号)。
A.v(第一步的逆反应)>v(第二步反应)B.反应的中间产物只有NO3C.第二步中NO2与NO3的碰撞仅部分有效D.第三步反应活化能较高35.[化学——选修3:物质结构与性质](15分)Li是最轻的固体金属,采用Li作为负极材料的电池具有小而轻、能量密度大等优良性能,得到广泛应用。
回答下列问题:(1)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为_____、_____(填标号)。
A.B.C.D.(2)Li+与H−具有相同的电子构型,r(Li+)小于r(H−),原因是______。
(3)LiAlH4是有机合成中常用的还原剂,LiAlH4中的阴离子空间构型是______、中心原子的杂化形式为______。
LiAlH4中,存在_____(填标号)。
A.离子键B.σ键C.π键D.氢键(4)Li2O是离子晶体,其晶格能可通过图(a)的B orn−Haber循环计算得到。
可知,Li原子的第一电离能为kJ·mol−1,O=O键键能为kJ·mol−1,Li2O晶格能为kJ·mol−1。
(5)Li2O具有反萤石结构,晶胞如图(b)所示。
已知晶胞参数为0.4665 nm,阿伏加德罗常数的值为N A,则Li2O的密度为______g·cm−3(列出计算式)。
36.[化学——选修5:有机化学基础](15分)化合物W可用作高分子膨胀剂,一种合成路线如下:回答下列问题:(1)A的化学名称为_____________________ 。
(2)②的反应类型是______________ 。
(3)反应④所需试剂、条件分别为_____________________ 。
(4)G的分子式为______________ 。
2018年普通高等学校招生全国统一考试理科综合参考答案7.D 8.A 9.D 10.B 11.C 12.B13.C 26.(14分)(1)去除水中溶解氧分液(或滴液)漏斗 (2)①Zn+2Cr 3+Zn 2++2Cr 2+ ②排除c 中空气(3)c 中产生H 2使压强大于大气压(冰浴)冷却 过滤 (4)敞开体系,可能使醋酸亚铬与空气接触27.(14分)(1)2NaHSO 3Na 2S 2O 5+H 2O (2)①NaHSO 3②得到NaHSO 3过饱和溶液 (3)2H 2O -4e -4H ++O 2↑ a(4)2-25S O +2I 2+3H 2O 22-4SO +4I -+6H + 0.12828.(15分)(1)O 2(2)①53.1②30.0 6.0×10-2 ③大于 温度提高,体积不变,总压强提高;NO 2二聚为放热反应,温度提高,平衡左移,体系物质的量增加,总压强提高 ④13.4 (3)AC 35.(15分)(1)DC (2)Li +核电荷数较大(3)正四面体 sp 3 AB (4)520 4982908(5)73A 87416(0.466510)N -⨯+⨯⨯ 36.(15分)(1)氯乙酸(2)取代反应(3)乙醇/浓硫酸、加热(4)C 12H 18O 3 (5)羟基、醚键(6)、 (7)。