高等工程热力学-第一章、热力学基本原理及定义
- 格式:ppt
- 大小:1.76 MB
- 文档页数:69


高等工程热力学介绍热力学是研究能量转化和热效应的科学。
而高等工程热力学则是在原有的基础上针对工程领域的应用进行深入研究的学科。
本文将介绍高等工程热力学的基本概念、原理和应用,以及相关的一些实例。
热力学基本概念热力学的基本概念有热力学系统、热力学过程、热力学性质等。
一个热力学系统是指进行能量交换的物理系统,可以是封闭系统、开放系统或者孤立系统。
热力学过程是指系统从一种状态变换到另一种状态的过程,可以是等温过程、绝热过程、等压过程等。
热力学性质是指描述热力学系统的特性,比如温度、压力、体积等。
热力学原理高等工程热力学基于热力学原理进行研究。
其中,热力学第一定律是能量守恒原理,它表明能量不能被创造或者毁灭,只能从一种形式转换为另一种形式。
热力学第二定律是能量传递的方向性原理,它表明热量自然地从高温物体流向低温物体,而不会反向流动。
熵增原理是热力学第二定律的数学表述,它描述了系统熵的增加趋势。
熵是一个衡量系统有序程度的指标,它的增加代表了能量的不可逆损失。
高等工程热力学应用高等工程热力学的应用十分广泛,涉及到多个工程领域。
以下是一些常见的应用实例:热力学循环分析高等工程热力学经常用于分析热力学循环,如蒸汽动力循环、制冷循环等。
通过对循环中各个组成部分的能量转换和损失进行研究,可以优化循环的效率和性能。
热传导计算在工程中,热传导是一个重要的问题。
高等工程热力学可以通过研究热传导的原理和机制,优化工程中的热传导问题,提高热传导的效率。
热力学系统优化通过对热力学系统进行优化设计,可以提高能量转换效率,降低能量消耗。
高等工程热力学可以通过分析系统的热力学性质,找到最优化的设计方案。
新能源开发高等工程热力学也可以应用于新能源的开发。
通过对新能源的高温特性、热力学性质进行研究,可以优化新能源的利用方式,提高能源利用效率。
结论高等工程热力学是热力学在工程领域中的应用和发展。
它通过研究热力学原理和原理的应用,优化工程中的能量转换和热效应问题。

⼯程热⼒学概念整理⼯程热⼒学与传热学概念整理⼯程热⼒学第⼀章、基本概念1.热⼒系:根据研究问题的需要,⼈为地选取⼀定范围内的物质作为研究对象,称为热⼒系(统),建成系统。
热⼒系以外的物质称为外界;热⼒系与外界的交界⾯称为边界。
2.闭⼝系:热⼒系与外界⽆物质交换的系统。
开⼝系:热⼒系与外界有物质交换的系统。
绝热系:热⼒系与外界⽆热量交换的系统。
孤⽴系:热⼒系与外界⽆任何物质和能量交换的系统3.⼯质:⽤来实现能量像话转换的媒介称为⼯质。
4.状态:热⼒系在某⼀瞬间所呈现的物理状况成为系统的状态,状态可以分为平衡态和⾮平衡态两种。
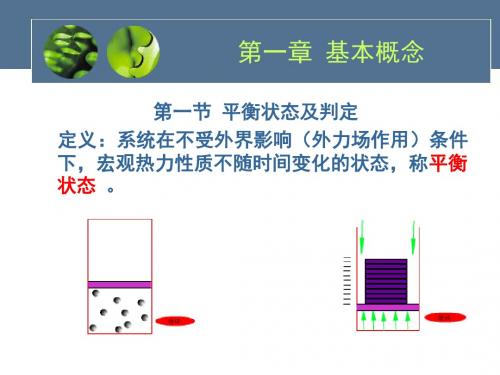
5.平衡状态:在没有外界作⽤的情况下,系统的宏观性质不随时间变化的状态。
实现平衡态的充要条件:系统内部与外界之间的各种不平衡势差(⼒差、温差、化学势差)的消失。
6.强度参数:与系统所含⼯质的数量⽆关的状态参数。
⼴延参数:与系统所含⼯质的数量有关的状态参数。
⽐参数:单位质量的⼴延参数具有的强度参数的性质。
基本状态参数:可以⽤仪器直接测量的参数。
7.压⼒:单位⾯积上所承受的垂直作⽤⼒。
对于⽓体,实际上是⽓体分⼦运动撞击壁⾯,在单位⾯积上所呈现的平均作⽤⼒。
8.温度T:温度T是确定⼀个系统是否与其它系统处于热平衡的参数。
换⾔之,温度是热⼒平衡的唯⼀判据。
9.热⼒学温标:是建⽴在热⼒学第⼆定律的基础上⽽不完全依赖测温物质性质的温标。
它采⽤开尔⽂作为度量温度的单位,规定⽔的汽、液、固三相平衡共存的状态点(三相点)为基准点,并规定此点的温度为273.16K。
10状态参数坐标图:对于只有两个独⽴参数的坐标系,可以任选两个参数组成⼆维平⾯坐标图来描述被确定的平衡状态,这种坐标图称为状态参数坐标图。
11.热⼒过程:热⼒系从⼀个状态参数向另⼀个状态参数变化时所经历的全部状态的总和。
12.热⼒循环:⼯质由某⼀初态出发,经历⼀系列状态变化后,⼜回到原来初始的封闭热⼒循环过程称为热⼒循环,简称循环。
13.准平衡过程:由⼀系列连续的平衡状态组成的过程称为准平衡过程,也成准静态过程。



第一章工程热力学基础第一节工质热力状态的基本参数一、状态与状态参数状态:热力系统中某瞬间表现的工质热力性质的总状况。
状态参数:描述工质状态特性的各种状态的宏观物理量。
如:温度(T )、压力(P )、比容(υ)或密度(ρ)、内能(u )、焓(h )、熵(s )、自由能(f )、自由焓(g )等。
状态参数的数学特性:1.1212x x dx 表明:状态的路径积分仅与初、终状态有关,而与状态变化的途径无关。
2.dx =0表明:状态参数的循环积分为零基本状态参数:可直接或间接地用仪表测量出来的状态参数。
如:温度、压力、比容或密度温度:宏观上,是描述系统热力平衡状况时冷热程度的物理量。
微观上,是大量分子热运动强烈程度的量度BTwm 22式中22wm —分子平移运动的动能,其中m 是一个分子的质量,w 是分子平移运动的均方根速度;B —比例常数;T —气体的热力学温度。
热力学第零定律:如两个物体分别和第三个物体处于热平衡,则它们彼此之间也必然处于热平衡。
摄氏度与热力学温度的换算:tT 2732.压力:垂直作用于器壁单位面积上的力,称为压力,也称压强。
f Fp 式中:F —整个容器壁受到的力,单位为牛顿(N );f —容器壁的总面积(m 2)。
微观上:分子热运动产生的垂直作用于容器壁上单位面积的力。
nBTwm n p 322322式中:P —单位面积上的绝对压力;n —分子浓度,即单位容积内含有气体的分子数V N n ,其中N 为容积V 包含的气体分子总数。
压力测量依据:力平衡原理压力单位:MPa相对压力:相对于大气环境所测得的压力。
工程上常用测压仪表测定的压力。
以大气压力为计算起点,也称表压力。
g p B p (P>B )H B p (P<B )式中B —当地大气压力P g —高于当地大气压力时的相对压力,称表压力;H —低于当地大气压力时的相对压力,称为真空值。
注意:只有绝对压力才能代表工质的状态参数3.比容:比容:单位质量工质所具有的容积。



1.第一章 基本概念及定义 2.热能动力装置:从燃料燃烧中得到热能,以及利用热能所得到动力的整套设备(包括辅助设备)统称热能动力装置。
3.工质:热能和机械能相互转化的媒介物质叫做工质,能量的转换都是通过工质状态的变化实现的。
4.高温热源:工质从中吸取热能的物系叫热源,或称高温热源。
5.低温热源:接受工质排出热能的物系叫冷源,或称低温热源。
6.热力系统:被人为分割出来作为热力学分析对象的有限物质系统叫做热力系统。
7.闭口系统:如果热力系统与外界只有能量交换而无物质交换,则称该系统为闭口系统。
(系统质量不变) 8.开口系统:如果热力系统与外界不仅有能量交换而且有物质交换,则称该系统为开口系统。
(系统体积不变) 9.绝热系统:如果热力系统和外界间无热量交换时称为绝热系统。
(无论开口、闭口系统,只要没有热量越过边界) 10.孤立系统:如果热力系统和外界既无能量交换又无物质交换时,则称该系统为孤立系统。
11.表压力:工质的绝对压力>大气压力时,压力计测得的差数。
12.真空度:工质的绝对压力<大气压力时,压力计测得的差数,此时的压力计也叫真空计。
13.平衡状态:无外界影响系统保持状态参数不随时间而改变的状态。
充要条件是同时到达热平衡和力平衡。
14.稳定状态:系统参数不随时间改变。
(稳定未必平衡) 15.准平衡过程(准静态过程):过程进行的相对缓慢,工质在平衡被破环后自动恢复平衡所需的时间很短,工质有足够的时间来恢复平衡,随时都不致显著偏离平衡状态,那么这样的过程就称为准平衡过程。
它是无限接近于平衡状态的过程。
16.可逆过程:完成某一过程后,工质沿相同的路径逆行回复到原来的状态,并使相互作用所涉及的外界亦回复到原来的状态,而不留下任何改变。
可逆过程=准平衡过程+没有耗散效应(因摩擦机械能转变成热的现象)。
17.准平衡与可逆区别:准平衡过程只着眼工质内部平衡;可逆过程是分析工质与外界作用产生的总效果,不仅要求工质内部平衡,还要求工质与外界作用可以无条件逆复。



