2020年化学物质之分类观
- 格式:doc
- 大小:417.50 KB
- 文档页数:11

第一节 物质的分类课时1 简单分类法及其应用目标与素养:1.认识物质的分类方法和依据,学会对常见物质分类。
(宏观辨识)2.感受分类在科研和学习中的重要作用。
(社会责任)一、常见的分类方法1.交叉分类法(1)含义:根据不同的分类标准,对同一事物进行多种分类的一种分类方法。
即对事物以不同的标准进行分类。
(2)举例①Na 2CO 3⎩⎨⎧ 按其组成的阳离子来分类,属于钠盐按其组成的阴离子来分类,属于碳酸盐按其溶解性来分类,属于可溶盐②将不同的物质与它所属的类别进行连线。
2.树状分类法(1)含义:对同类事物按照某些属性进行再分类的分类方法,即对同类事物进行再分类。
(2)举例微点拨:交叉分类法是对同一物质以不同的分类标准或角度进行分类,属交叉关系;树状分类法是对同类物质按不同的属性进行逐级分类,各级之间为从属关系,同级之间为并列关系。
二、分类方法的应用分类可以帮助我们更好地认识物质的性质,找出各类物质之间的关系: Ca ――→①CaO ――→②Ca (OH )2――→③CaCO 3 C ――→④CO 2――→⑤H 2CO 3――→⑥CaCO 3――→⑦CaO举例写出有关序号的一种化学方程式并注明反应类型(答案不唯一,合理即可)。
①2Ca +O 2===2CaO ;化合反应。
②CaO +H 2O===Ca(OH)2;化合反应。
③Ca(OH)2+Na 2CO 3===CaCO 3↓+2NaOH ;复分解反应。
④C +O 2=====点燃CO 2;化合反应。
⑤CO 2+H 2O===H 2CO 3;化合反应。
⑥H 2CO 3+Ca(OH)2===CaCO 3↓+2H 2O ;复分解反应。
⑦CaCO 3=====高温CaO +CO 2↑;分解反应。
CO +CuO=====△Cu +CO 2是置换反应吗?提示:不是。
1.判断正误(正确的打“√”,错误的打“×”)(1)交叉分类法是对一种物质的多角度分类法。

2020高中化学必备知识点:在化学中,物质是如何分类的?按不同的角度,物质的分类有多种。
如氧化物若按组成元素可分为金属氧化物和非金属氧化物。
化合物若按原子成键特点可分为禽子化合物和共价化合物;若按熔融状态或水溶液中能否导电可分为电解质和非电解质。
1、混合物( 1 )定义:由几种不同的单质或化合物组成的物质。
(2 )特点:无固定组成的物质;无固定的熔、沸点。
(3)范围①高分子(如蛋白质、淀粉、纤维素、聚合物)②分散系(如溶液、胶体、浊液等)③同分异构体(如邻、间、对三种二甲苯)④同素异形体(如白磷和红磷、氧气和臭氧)⑤其他(如混凝土、泥沙)( 4 )常见特殊名称的混合物①固态混合物:合金、漂白粉、铅热剂、黑火药、水泥、玻璃、陶瓷等。
②液态混合物;氨水、氯水、盐酸、浓硫酸、浓硝酸、福尔马林、水玻璃、石油、石油的各种馏…分等。
③气态混合物:辛气、永煤气、夭然气、焦炉气、高炉煤气、石油气、裂解气等。
2 .纯净物( 1 )定义:由一种单质或化合物组成的物质。
( 2 )特点:有固定的组成和性质;有固定的熔、沸点。
( 3 )绝对纯净的物质是没有的,纯净是相对的。
3 .金属( 1 )定义:由金属元素组成的单质叫金属。
( 2 )金属的通性①金属具有金属光泽,一般具有延展性,是电、热的良导体。
金属这些性质跟金属晶体里的自由电子有关。
②金属在通常状况下,除汞是液体外,其余都是固体。
银的导电和导热性最好;铂的延展性最突出;饿的密度最大;钨的熔点最高(3683K )( 3 )结构特点:金属原子价电子比较少且原子半径相对较大,在化学反应中容易失电子,因此金属一般具有较强的还原性。
4 .非金属(1 )定义:由非金属元素组成的单质叫非金属。
(2 )非金属的物理性质月卜金属和金属相反,一般没有金属光泽,不是电和热的良导体,没有延展性。
通常状况下,非金属有的是固体,有的是气体,只有澳是液体。
非金属固体大多数属于分子晶体,熔沸点较低,但有的非金属固体如金刚石属于原子晶体,熔沸点很高。

化学品分类标准化学品是指由两种或两种以上的元素经化学反应得到的物质,它们广泛应用于工业生产、农业生产、医药卫生、科研教育等领域。
为了管理和监控化学品的使用和生产,制定了一系列的化学品分类标准,以便对化学品进行准确的归类和管理。
首先,化学品可以按照其用途和性质进行分类。
根据用途不同,化学品可以分为工业化学品、农业化学品、医药化学品、日用化学品等。
而按照性质来划分,则可以分为有机化学品、无机化学品、高分子化合物等。
这种分类方法可以帮助我们更好地了解化学品的具体用途和特性,从而更好地进行管理和监控。
其次,化学品还可以根据其对人体和环境的危害程度进行分类。
根据危害程度的不同,化学品可以分为剧毒化学品、易制毒化学品、易制爆化学品、危险化学品等。
这种分类方法可以帮助我们更好地采取相应的防护措施,减少化学品对人体和环境造成的危害。
另外,化学品还可以按照其物理状态进行分类。
根据物理状态的不同,化学品可以分为固体化学品、液体化学品、气体化学品等。
这种分类方法可以帮助我们更好地进行储存和运输,确保化学品在使用过程中的安全性。
此外,化学品还可以按照其化学结构进行分类。
根据化学结构的不同,化学品可以分为醇类、醚类、酮类、酯类、酸类、碱类等。
这种分类方法可以帮助我们更好地了解化学品的组成和特性,从而更好地进行使用和管理。
总的来说,化学品的分类标准多种多样,可以根据不同的需求和目的进行选择和应用。
通过科学合理的分类方法,可以更好地对化学品进行管理和监控,确保其在使用过程中的安全性和可控性。
同时,也可以更好地推动化学品行业的发展,促进社会经济的持续健康发展。
因此,对化学品分类标准的研究和应用具有重要的意义,值得我们深入探讨和研究。
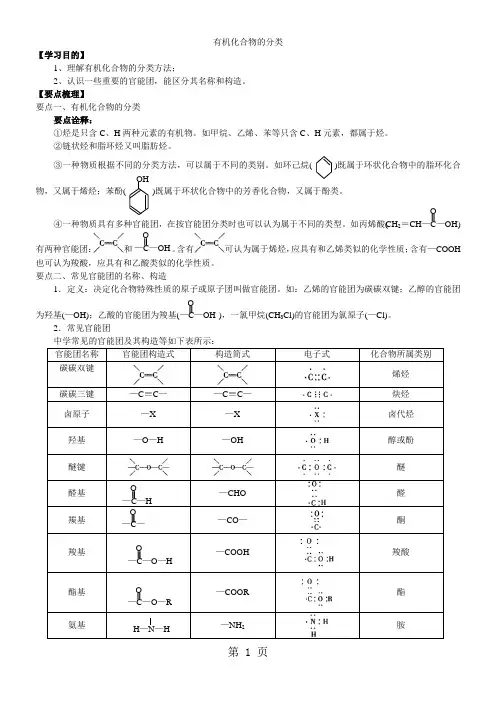
有机化合物的分类【学习目的】1、理解有机化合物的分类方法;2、认识一些重要的官能团,能区分其名称和构造。
【要点梳理】要点一、有机化合物的分类要点诠释:①烃是只含C 、H 两种元素的有机物。
如甲烷、乙烯、苯等只含C 、H 元素,都属于烃。
②链状烃和脂环烃又叫脂肪烃。
③一种物质根据不同的分类方法,可以属于不同的类别。
如环己烷 )既属于环状化合物中的脂环化合物,又属于烯烃;苯酚 )既属于环状化合物中的芳香化合物,又属于酚类。
④一种物质具有多种官能团,在按官能团分类时也可以认为属于不同的类型。
如丙烯酸( )有两种官能团:和 。
含有可认为属于烯烃,应具有和乙烯类似的化学性质;含有—COOH 也可认为羧酸,应具有和乙酸类似的化学性质。
要点二、常见官能团的名称、构造1.定义:决定化合物特殊性质的原子或原子团叫做官能团。
如:乙烯的官能团为碳碳双键;乙醇的官能团 为羟基(—OH);乙酸的官能团为羧基( ),一氯甲烷(CH 3Cl)的官能团为氯原子(—Cl)。
2.常见官能团中学常见的官能团及其构造等如下表所示:官能团名称 官能团构造式构造简式电子式化合物所属类别碳碳双键烯烃 碳碳三键 —C ≡C — —C ≡C —炔烃 卤原子 —X —X 卤代烃 羟基 —O —H—OH醇或酚 醚键醚 醛基 —CHO醛羰基—CO —酮羧基 —COOH羧酸酯基—COOR酯氨基—NH 2胺OHCH 2=CH —C —OHO—C —OH O —C —OH O—C —H O —C — O—C —O —HO—C —O —R OH —N —H要点诠释:①官能团是中性基团,不带电荷。
②官能团决定有机物的主要化学性质,但一样的官能团连接的方式和位置不同,化学性质也有所不同。
③分子中含有两种或两种以上的官能团时,该分子可能具有多方面的性质,假设多种官能团之间互相影响,又可能表现出特殊性质,如羟基与链烃相连时形成的是醇,而直接与苯环相连时形成的是酚。

化学品类别划分
1. 无机化学品:包括无机酸、碱、盐、金属、非金属等。
例如,盐酸、氢氧化钠、氯化钠、铜、硫磺等。
2. 有机化学品:包括有机化合物,如烃类、醇类、醛类、酮类、羧酸类、胺类等。
例如,甲烷、乙醇、甲醛、丙酮、乙酸、苯胺等。
3. 精细化学品:包括染料、颜料、涂料、香料、化妆品、洗涤剂、胶粘剂等。
这些化学品通常具有特定的功能和用途,用于改善产品的性能和外观。
4. 农用化学品:包括农药、化肥、植物生长调节剂等。
这些化学品用于农业生产,以保护作物、防治病虫害、提高产量和质量。
5. 医药化学品:包括原料药、制剂、生物制药等。
这些化学品用于制药工业,用于治疗和预防各种疾病。
6. 食品化学品:包括食品添加剂、保鲜剂、调味剂等。
这些化学品用于食品加工和保鲜,以改善食品的口感、色泽、香味和保质期。
7. 环保化学品:包括水处理剂、废气处理剂、固废处理剂等。
这些化学品用于环境保护,以净化水质、空气和土壤。
8. 高分子材料:包括塑料、橡胶、纤维、涂料、胶粘剂等。
这些化学品由高分子化合物制成,具有特殊的物理和化学性质,广泛应用于各个领域。
这只是一些常见的化学品类别划分,实际上还有很多其他的分类方法和特殊用途的化学品。
化学品的分类有助于理解其性质、用途和潜在风险,对于安全使用和管理化学品非常重要。

第01讲物质的分类知识导航模块一物质的分类知识精讲一、同素异形体1. 定义:由同一种元素形成的几种性质不同的单质,叫做这种元素的同素异形体。
2. 实例:金刚石、石墨和C60;O2和O3;红磷和白磷。
3. 产生原因:(1)组成分子的原子数目和成键方式不同,如:氧气(O2)和臭氧(O3)。
(2)原子的排列方式不同,如:金刚石和石墨。
思考与交流:由同种元素组成的物质,一定是纯净物吗?易错提醒由同种元素组成的物质,不一定是纯净物。
如氧气(O2)和臭氧(O3)的混合物。
二、物质的分类方法1. 树状分类法按照一定标准对同类事物进行再分类,如:氧化物的分类(1)酸性氧化物:与水反应只生成相应价态的酸,或与碱反应只生成一种盐和水的氧化物。
如:SO2+ H2O === H2SO3;SO2+ 2NaOH === Na2SO3 + H2O(2)碱性氧化物:与水反应只生成相应价态的碱,或与酸反应只生成一种盐和水的氧化物。
如:Na2O + H2O === 2NaOH;Na2O + 2HCl=== 2NaCl + H2O明辨是非(1)碱性氧化物一定是金属氧化物()(2)金属氧化物一定是碱性氧化物()(3)酸性氧化物一定是非金属氧化物()(4)非金属氧化物一定是酸性氧化物()易错提醒(1)碱性氧化物一定是金属氧化物。
(2)金属氧化物不一定是碱性氧化物,如Mn2O7。
(3)酸性氧化物不一定是非金属氧化物,如Mn2O7。
(4)非金属氧化物不一定是酸性氧化物,如CO。
2. 交叉分类法对同一物质按不同的标准进行分类明辨是非(1)Na2SO4、KNO3都是含氧酸盐()(2)HNO3既属于一元酸又属于含氧酸,这种分类方法是树状分类法()(3)Na2CO3含有氧元素,属于氧化物()(4)CuSO4·5H2O属于混合物()(5)2Na2O2+2H2O===4NaOH +O2↑是置换反应()(6)只由一种元素组成的物质,可能是混合物()经典例题题型一:物质的分类【例1】(2021·浙江高一月考)根据物质的组成与性质进行分类,CO2属于A.碱B.碱性氧化物C.酸D.酸性氧化物【变1-1】(2021·云南文山壮族苗族自治州·砚山县第三高级中学高一期中)下列各组物质中,按单质、化合物、混合物顺序排列的是A.铁、四氧化三铁、烧碱B.氯气、纯碱、石灰水C.水银、空气、干冰D.二氧化硫、水蒸气、盐酸【变1-2】(2021·三台县芦溪中学高一开学考试)关于物质分类正确的组成是A.A B.B C.C D.D【例2】(2020·长春市第一五一中学高一期中)下列说法中正确的是A.Na2SO4·10H2O是混合物B.同种分子构成的物质一定是纯净物C.混合物肯定由两种以上元素组成D.含有氧元素的化合物都是氧化物【变2】(2020·福建省南安市柳城中学高一期中)下列有关氧化物的判断正确的是A.凡是含氧的化合物均可称为氧化物B.依据性质不同氧化物只能分为酸性氧化物和碱性氧化物C.酸性氧化物都能与碱反应生成盐和水D.金属氧化物一定是碱性氧化物【例3】(2020·三亚华侨学校高一月考)下列树状分类法正确的是A.纯净物⎧⎧⎪⎨⎨⎩⎪⎩金属单质单质非金属单质化合物B.物质⎧⎪⎧⎨⎨⎪⎩⎩混合物溶液纯净物化合物C.化合物⎧⎪⎧⎧⎪⎨⎪⎪⎪⎩⎪⎨⎪⎨⎪⎪⎪⎪⎪⎪⎪⎩⎩有机物氧化物酸非氧化物无机物碱盐D.纯净物⎧⎧⎪⎪⎪⎨⎨⎪⎩⎪⎪⎩单质无机物氧化物化合物有机物【变3-1】(2020·福建省晋江市养正中学高一月考)根据物质的组成与性质等可将物质按不同的方式进行分类,下列说法中不正确...的是A.Na2CO3既属于钠盐又属于碳酸盐B.甲图所示的分类方法属于树状分类法C.酸性氧化物一定是非金属氧化物D.碱性氧化物一定是金属氧化物【变3-2】(2020·抚松县第五中学高一期中)下列图示错误的是A.B.C.D.【例4】(2021·云南省大姚县第一中学高一月考)请对下列化合物:①NaCl、②HCl、③CaCl2、④CuO、⑤H2O、⑥Fe2O3进行分类:(1)依据通常状况下物质的_______为标准分类,属于固体的是_______,属于液体的是_______,属于气体的是_______。

2020中考化学试题分类汇编——专题三十八:物质的分类1.(2020铜仁)生活中的下列物质属于纯净物的是()A.酱油B.豆浆C.海水D.氧气2.(2020河北)下列分类正确的是A. 冰、干冰、可燃冰都是氧化物B. 金属、玻璃、石墨都是导体C. 钙、锌、碘都是人体必需元素D. 钳子、羊角锤、定滑轮都省力杠杆3.(2020辽宁)下列物质属于氧化物的是A. 氯酸钾B. 臭氧C. 硫化氢D. 五氧化二磷4.(2020黑龙江)推理是学习化学常用的思维方法,下列推理正确的是()A. 燃烧都伴有发光、放热现象,所以有发光、放热现象的一定是燃烧B. 单质是由同种元素组成的纯净物,所以由同种元素组成的纯净物一定是单质C. 酸溶液能使紫色石蕊溶液变红,所以能使紫色石蕊变红的溶液一定是酸溶液D. 溶液一定是混合物,所以混合物一定是溶液5.(2020大庆)运用分类法学习和研究化学物质,能够收到事半功倍的效果,下列分类正确的是()类别/选项混合物单质氧化物碱盐A.A B.B C.C D.D6.(2020牡丹江)人类的日常生活需要洁净的水,高铁酸钾(K2FeO4)是一种新型高效水处理剂。
下列关于高铁酸钾说法正确的是()A.高铁酸钾中钾、铁、氧三种元素的质量比为2:1:4B.高铁酸钾中含有氧气C.高铁酸钾是混合物D.高铁酸钾是由钾、铁、氧元素组成的7.(2020陕西)认识物质是学习化学的基础。
下列物质属于单质的是()A.空气B.干冰C.液氧D.生铁8.(2020天津)下列物质中,属于纯净物的是()A.洁净的空气 B.水泥砂浆C.液氮D.汽水9.(2020金昌)下列生活中常见的物质属于纯净物的是()A.矿泉水B.白酒C.干冰D.苏打水10.(2020呼伦贝尔)下列物质按照混合物、氧化物、单质顺序排列的是()A .空气、二氧化锰、氧气B .海水、氯酸钾、氢气C .氧化铁、锰酸钾、水D .硫酸铜、高锰酸钾、二氧化碳11.(2020吉林)生铁和钢都是铁的合金,它们都属于( ) A .混合物 B .纯净物 C .单质D .化合物12.(2020沈阳)下列物质属于氧化物的是( ) A .CaO B .O 3 C .KClO 3D .ZnCl 213.(2020内江)对物质进行分类是学习化学的常用方法,下列分类不正确的是( ) A .N 2——单质B .SO 2——氧化物C .CaCO 3——酸D .NaOH ——碱14.(2020贵港)在化学反应24422Cu+2H SO ( )CuSO +SO +2H O 加热浓中没有涉及到的物质类别是( ) A .单质 B .氧化物C .酸D .碱15.(2020郓城)下列物质属于纯净物的是( ) A .氯酸钾B .不锈钢C .自来水D .空气16.(2020海南)海南岛存在大面积富硒土壤。


专题二物质的组成、性质和分类挖命题【考情探究】分析解读物质的组成、性质和分类在高考中考查的难度较小,涉及的内容主要为与生产、生活有关的知识点。
分散系属于低频考点,高考中多在“一题多点”题目中出现,考查的内容多为溶液、浊液及胶体的辨析。
将物质的组成、性质及分类知识与传统文化、化学史相结合进行考查是高考的主要考查方式,考查考生的科学态度与社会责任素养。
【真题典例】破考点【考点集训】考点一物质的组成、性质和分类1.我国科技创新成果斐然。
下列成果中以制备非金属单质为主要目的的是( )答案A2.下列典籍记载的文字中,涉及置换反应的是( )A.以曾青(主要成分为硫酸铜)涂铁,铁赤色如铜(出自《抱朴子》)B.凡石灰(主要成分为碳酸钙),经火焚炼为用(出自《天工开物》)C.以毛袋漉去曲滓(酒糟),又以绢滤曲汁于瓮中(出自《齐民要术》)D.铅山县有苦泉(含硫酸铜),挹其水熬之,则成胆矾(出自《梦溪笔谈》)答案A3.我国出土的文物呈现了瑰丽的历史文化。
下列文物中,主要成分属于合金的是( )答案D4.唐代中药学著作《新修本草》中,有关于“青矾”的记录为“本来绿色,新出窟未见风者,正如琉璃,……,烧之赤色”。
据此推测,“青矾”的主要成分为( )A.CuSO4·5H2OB.FeSO4·7H2OC.KAl(SO4)2·12H2OD.ZnSO4·7H2O答案B考点二分散系1.下列说法中正确的是( )A.可用丁达尔效应区分溶液与胶体B.生石灰与水混合的过程只发生物理变化C.O3是由3个氧原子构成的化合物D.CuSO4·5H2O是一种混合物答案A2.下列有关胶体的说法中不正确的是( )A.胶体均为无色透明的液体B.利用丁达尔效应可以区分胶体和溶液C.胶体中分散质粒子的直径在1~100 nm之间D.向沸水中逐滴加入少量FeCl3饱和溶液,可制得Fe(OH)3胶体答案A3.下列水处理剂的工作原理与胶体有关的是( )A.活性炭B.氯气C.明矾D.次氯酸钠答案C过专题【五年高考】考点一物质的组成、性质和分类A组自主命题·天津卷题组1.(2014天津理综,1,6分)化学与生产、生活息息相关,下列叙述错误..的是( )A.铁表面镀锌可增强其抗腐蚀性B.用聚乙烯塑料代替聚乳酸塑料可减少白色污染C.大量燃烧化石燃料是造成雾霾天气的一种重要因素D.含重金属离子的电镀废液不能随意排放答案BB组统一命题、省(区、市)卷题组2.(2018课标Ⅲ,7,6分)化学与生活密切相关。


2020年高考化学一轮复习:物质的组成、性质和分类一、选择题(本题共10小题,每小题只有一个选项符合题意)1.清华大学的科学家将古老的养蚕技术与时兴的碳纳米管和石墨烯结合,发现通过给蚕宝宝喂食含有碳纳米管和石墨烯的桑叶,可以获得更加牢固的蚕丝纤维。
已知:当把石墨片剥成单层之后,这种只有一个碳原子厚度的单层就是石墨烯。
下列说法正确的是() A.蚕丝纤维的主要成分是纤维素B.石墨烯像烯烃一样,是一种有机物C.碳纳米管和石墨烯互为同素异形体D.碳纳米管具有丁达尔效应解析:选C A项,蚕丝的主要成分是蛋白质,错误;B项,石墨烯是单质,属于无机物,错误;C项,碳纳米管和石墨烯是碳元素的不同单质,互为同素异形体,正确;D项,碳纳米管在合适的分散剂中才能形成胶体分散系,错误。
2.化学与生产和生活密切相关。
下列过程中没有发生化学变化的是()A.氯气作水的杀菌消毒剂B.硅胶作袋装食品的干燥剂C.二氧化硫作纸浆的漂白剂D.肥皂水作蚊虫叮咬处的清洗剂解析:选B氯气作水的杀菌消毒剂是利用氯气与水反应生成的次氯酸的强氧化性,发生了化学变化;硅胶作袋装食品的干燥剂,是因为硅胶疏松多孔,具有吸收水分的作用,没有发生化学变化;二氧化硫作纸浆的漂白剂是因为二氧化硫可与某些有色物质发生化学反应生成不稳定的无色物质;肥皂的主要成分为高级脂肪酸钠,肥皂水作蚊虫叮咬处的清洗剂是利用高级脂肪酸钠在水中发生水解反应使溶液呈碱性的性质,发生了化学变化。
3.最近我国科研人员发现在温和的反应条件下,甲烷和二氧化碳在锌修饰的H-ZSM-5分子筛(催化剂)上可一步转化为乙酸。
CH4、CO2和CH3COOH均属于() A.有机物B.共价化合物C.电解质D.离子化合物解析:选B CH4、CO2和CH3COOH均属于共价化合物。
4.化学与生产、生活密切相关。
下列说法中,不正确的是()A.“血液透析”利用了胶体的性质B.服用铬含量超标的药用胶囊会对人体健康造成危害C.人类超量碳排放及氮氧化物和二氧化硫的排放是形成酸雨的主要原因D.绿色化学的核心是利用化学原理从源头上减少和消除工业生产对环境的污染解析:选C氮氧化物和二氧化硫的排放是形成酸雨的主要原因,C错误。
2020年全国中考化学试题分类(一)——物质的变化、性质和分类一.选择题(共43小题)1.(2020•济宁)对CO2、C2H2、H2CO3、Ca(HCO3)2、Na2CO3五种物质的判断,正确的是()A.C2H2、H2CO3都是有机物B.CO2、H2CO3都属于氧化物C.Ca(HCO3)2、Na2CO3都属于盐D.H2CO3、Na2CO3溶液都显酸性2.(2020•甘孜州)下列关于物质类别的判断错误的是()A.空气是混合物B.不锈钢属于合金C.矿泉水是一种溶液D.纯碱属于碱3.(2020•乐山)分类是化学学习中常用的思维方法,下列有关物质分类正确的是()A.酸:盐酸硫酸硝酸B.碱:烧碱纯碱氨水C.有机物:甲烷乙醇一氧化碳D.混合物:高锰酸钾海水合金4.(2020•济宁)通过一步化学反应,不能实现下列物质间转化的是()A.C→CO B.H2O2→O2C.BaCl2→Ba(OH)2D.NaCl→NaNO35.(2020•德阳)化学能指导我们更好地认识、改造和应用物质。
从物质分类角度分析,下列属于纯净物的是()A.空气B.牛奶C.蒸馏水D.粗盐6.(2020•重庆)下列物质属于纯净物的是()A.钛合金B.大理石C.蒸馏水D.煤7.(2020•威海)下列对物质的分类,不正确的是()A.单质B.化合物C.化合物D.混合物8.(2020•杭州)工业上可通过如下反应制取氧化钠:2NaNO3+10Na6Na2O+N2↑,下列相关说法正确的是()A.反应物NaNO3属于氧化物B.生成物N2的化学性质由氮气分子(N2)保持C.该反应属于复分解反应D.反应前后只有氮元素化合价发生变化9.(2020•黔西南州)分类是学习和研究化学的一种常用方法。
下列分类正确的是()A.酸:NaHCO3、H2SO4B.氧化物:SO2、KMnO4C.黑色固体:CuO、Fe2O3D.具有还原性的物质:C、H210.(2020•天水)下列物质分类正确的是()A.单质:氢气、空气B.氧化物:氧化铜、干冰C.酸:硝酸、硫酸铜D.碱:火碱、纯碱11.(2020•百色)下列物质属于氧化物的是()A.NaCl B.Au C.NO2D.KOH12.(2020•百色)习总书记说:“垃圾分类回收是一种新时尚”。
金属和非金属概念的含义;物理变化与化学考点1 分子、原子、离子等概念的含义1.(2019·广东学业水平测试T1)走近蛋糕店时,可闻到浓浓的奶香味,这表明( ) A .分子不可再分 B .分子可再分 C .分子是静止不动的D .分子在不停运动2.(2018·广东学业水平测试T3)牛奶、豆腐等食物中富含钙,这里的“钙”应理解为( ) A .单质 B .元素 C .原子D .分子3.(2017·广东学业水平测试T7)海带中含有丰富的碘,这里的“碘”应理解为()A.元素B.分子C.单质D.原子1.构成物质的三种基本粒子(分子、原子、离子)的比较(1)不同点①分子是保持物质化学性质的最小微粒;②原子是化学变化中的最小微粒;③带有电荷的原子或原子团叫作离子。
带正电荷的离子叫作阳离子,带负电荷的离子叫作阴离子。
(2)相同点都很小,处于永恒运动之中,粒子间都有空隙,同种粒子性质相同,不同种粒子性质各异。
(3)联系2.元素:是质子数相同的同一类原子的总称。
核电荷数或质子数是划分元素种类的唯一标准。
3.原子团:由几个原子组成的原子集团。
[温馨提示](1)原子构成分子,分子构成物质。
原子可直接构成物质。
(2)同类的原子总称为元素,元素又组成物质。
元素是一个宏观的概念,与分子、原子不同,它只论种类,不论个数,没有数量意义。
(2018·广东1月学业水平测试)在贝类和苹果等食物中含有丰富的锌,这里的“锌”应理解为() A.单质B.分子C.元素D.氧化物[解析]在贝类和苹果等食物中含有丰富的锌,这里的“锌”指的是元素,是化合状态。
[答案] C(2018·广东学业水平测试)干冰可用于制作舞台烟雾,干冰的升华过程体现了() A.分子在不停运动B.分子不可再分C.分子是最小的微粒D.分子之间没有间隙[解析]干冰可用于制作舞台烟雾,是因为干冰的分子是在不停运动的,向四周扩散,制作舞台烟雾,故A 选项正确。
(新教材)人教版高中化学必修一第一章第1节《物质的分类及转化》优质说课稿今天我说课的内容是部编人教版(新教材)高中化学必修1第一章第1节《物质的分类及转化》。
第一章主要讲述物质及其变化。
世界是由物质构成的,目前人类发现和合成的物质已超过1亿种。
对于这么多的物质和更为丰富的化学变化,人们是怎样认识和研究的呢?分类是认识和研究物质及其变化的一种常用的科学方法。
通过分类,可以将纷繁复杂的物质分成不同的类别,还可以从离子、电子等微观视角揭示化学反应的规律。
依据物质类别和元素价态,可以解释和预测物质的性质,设计物质间的转化途径。
通过第一章学习,从宏观辨识与微观探析、变化观念与平衡思想、证据推理与模型认知、科学探究与创新意识、科学态度与社会责任5个方面培养学生化学学科核心素养。
本章共有三节,本课是第一节,主要讲述物质的分类及转化,承载着实现本章教学目标的任务。
为了更好地教学,下面我将从课程标准、教材分析、教学目标和核心素养、教学重难点、学情分析、教学准备、教学方法、教学过程等方面进行说课。
一、说课程标准。
普通高中化学课程标准(2017版2020年修订):【内容要求】“2.1 元素与物质:认识元素可以组成不同种类的物质,根据物质的组成和性质可以对物质进行分类;同类物质具有相似的性质,一定条件下各类物质可以相互转化;认识元素在物质中可以具有不同价态,可通过氧化还原反应实现含有不同价态同种元素的物质的相互转化。
认识胶体是一种常见的分散系。
”由此标准可以看出,本课学习主题属于“常见的无机化合物及其应用”这一部分。
二、说教材。
本课是人教版化学必修1第一章《化学物质及其变化》第一节内容,是完成初高中课程内容衔接的重要载体,其将初中所学的单一、孤立的物质及反应梳理扩展为高中阶段多样、系统的物质反应体系,渗透分类观、物质转化观等化学学科学习的基本思想方法,旨在用其发现物质及变化的规律,并预测物质的性质及可能发生的变化。
本课以图片导入,共有“物质的分类”和“物质的转化”两部分内容。
第二章化学物质及其变化第一节物质的分类学习目标1、了解物质分类的方法和依据,认识分类方法的应用。
2、了解分散系的含义及分类,知道胶体是一种常见的分散系。
3、了解胶体的特性及其应用。
4、感受分类方法对化学学科研究和化学学习的重要应用。
知识点一简单分类法及其应用一、纯净物的分类1、交叉分类法(1)含义:根据不同的分类标准,对同一事物进行多种分类的一种分类方法。
(2)举例Ⅰ、碳酸钠的交叉分类:2、树状分类法(1)含义:对同类事物按照某些属性进行再分类的分类方法,即对同类事物进行再分类。
(2)举例规律总结:1、纯净物的一般分类2、两种分类方法的特点与区别例题1、分类法是一种行之有效,简单易行的科学方法,人们在认识事物时可以采取多种分类方法,下列关于“Na2CO3”的分类不正确的是( B)A、化合物B、氧化物C、碳酸盐D、钠盐例题2、根据某种共性,可将CO2、SO2归为一类氧化物。
下列物质也属于同类氧化物的是( B)A.CaCO3B.SO3C.CuO D.KMnO4例题3、按照物质的树状分类法和交叉分类法,HNO3应属于( D)①酸②氢化物③氧化物④含氧酸⑤难挥发性酸⑥一元酸⑦化合物⑧混合物A.①②③④⑤⑥⑦B.①④⑤⑥C.①⑧D.①④⑥⑦例题4、从对化合物的分类方法出发,指出下列各组物质中与其他类型不同的一种物质是(1)Na2O CaO SO2 CuO ______ SO2___________(2)NaCl KCl NaClO3CaCl2 _____ NaClO3_________(3)HClO3KClO3HCl NaClO3 _____ HCl _________(4)NaHCO3Ca(HCO3)2NH4HCO3K2CO3 ____ K2CO3______例题5、利用交叉分类法,请你说出Na2SO4可能属于的类型名称是____硫酸盐、钠盐________。
例题6、请尝试对你所学过的化学物质和化学反应进行分类,并与同学交流。
2020年高考化学一轮复习教学案第二章元素与物质世界第一节元素与物质的分类考纲点击1.了解分类法在化学科学研究和化学学习中的重要作用,能根据物质的组成和性质对物质进行分类。
2.理解混合物和纯净物、单质和化合物的概念,理解酸、碱、盐、氧化物的概念及其相互关系。
3.了解分散系的概念、分类方法,掌握胶体的概念、重要性质及应用,了解胶体是一种常见的分散系,掌握Fe(OH)3胶体的制备方法。
一、物质的组成1.元素、物质及微粒间的关系(1)宏观上物质是由元素组成的,微观上物质是由______、______或______构成的。
(2)元素:具有__________________________的一类原子的总称。
(3)元素与物质的关系(4)元素在物质中的存在形态①游离态:元素以______形式存在的状态。
②化合态:元素以________形式存在的状态。
(5)元素、物质及微粒间的关系如下图所示2.同素异形体(1)____________________叫同素异形体。
同素异形体的形成有两种方式:①分子中原子个数不同,如O2和O3;②原子排列方式不同,如金刚石、石墨及C60。
(2)同素异形体之间的性质差异主要体现在______性质上,同素异形体之间的转化属于______变化。
3.混合物和纯净物(1)纯净物:______________________________。
(2)混合物:__________________________________。
特别提示:由同一种元素组成的物质不一定是纯净物,如O2和O3互为同素异形体;由相同的两种元素组成的物质也不一定是纯净物,如CO和CO2、H2O与H2O2均是由两种元素组成的不同物质。
即时训练1判断正误(用“√”或“×”填写)。
A.蛋白质和油脂都属于高分子化合物,一定条件下都能水解。
()B.Al、Fe、Cu三者对应的氧化物均为碱性氧化物。
()C.Al、Fe、Cu三者的单质放置在空气中均只生成氧化物。
专题讲座化学物质之分类观——物质的分类方法和分类依据复习目标:考纲要求要求层次考点细化(1)从组成上对物质进行分类,如:混合物和纯净物、单质和化合物、金属和非金属等(2)根据物质组成和性质理解酸、碱、盐、氧化物的分类及其相互联系ⅡⅡ1.根据物质的分类方法,掌握物质的类别的判断。
2.根据物质的类别,初步学会物质性质推测的基本方法。
【引言】分类的思想是中学化学中的一种基本的、也是最重要的思想方法。
它可以帮助我们整体把握学科知识体系、理解学科基本概念和系统掌握化学各板块知识,所以它在中学化学的学习中有着极其重要的作用。
【讲解】我们必须弄明白:为什么要分类?如何来分类?(1)化学物质有很多,在研究中,我们总是利用同类物质具有“相似性质”,来推测物质的性质,然后有目的地验证这些性质,最终认识物质的性质。
简单地说,给物质分类就是归纳物质的共性,为推测“陌生物质”性质服务。
(2)分类的依据:根据物质之间的共同点...和差异性,把研究的对象区分为不同种类的逻辑方法。
一般来说,凡是归为同一类的对象,它们必然在质上有共性,必然有质的内在联系,异类必有质的差异性。
即同类物质具有相似点,这些“相似点”包括:物质的组成、物质的结构、物质的性质、物质的其他特征等。
(3)分类方法:树状分类法(可以理解为:系统中的“包含与被包含”的关系)交叉分类法【活动一】下列物质:金属铁、金属锌、木炭、CuO、CaCO3、H2SO4、NaOH、Ba(O H)2、NaCl、CuSO4。
有人根据不同的依据进行了如下分类,请指出分类的依据和物质类别。
分类依据分类类别名称类别一:金属铁、金属锌、木炭类别二:CuO、CaCO3、H2SO4、NaOH、Ba(OH)2、NaCl、CuSO4类别一:SO2、SO3、N2O5类别二:CuO、Fe2O3、Na2O类别三:Al2O3、ZnO类别四:NO、CO类别一:稀H2SO4、NaCl(aq)类别二:Fe(OH)3胶体、鸡蛋白液、淀粉液类别三:Cu(OH)2浊液类别一:NH3、CO2、NO、Cl2O7、CH3CH2OH类别二:H2SO4、NaOH、CH3COOH、NaCl、BaSO4活动总结:【活动二】 分类是研究物质性质的基本方法。
通过分类掌握概念间的联系与区别(即:“同类”中抓“异”(不同点)、“对立”中抓“同”(相同点)。
例如: 1、指出下列“同类”概念的不同点。
(1)同位素、同素异形体、同分异构体、同系物、同类物、同一物质; (2)溶解平衡、化学平衡、水解平衡、电离平衡;(3)酸性的强弱、酸的强弱、酸的浓度、pH ,酸的氧化性和氧化性酸; (4)电离、电解、电镀、电精炼; (5)水化、水解、水合2、指出下列“对立”概念的相同点。
(1)中和、水解;(2)溶解、结晶; (3)加成、消去; (4)电解池、原电池; (5)电解质、非电解质 【活动三】 根据下列图示,请指出物质类别及分类依据。
归纳总结:根据物质的组成(特别是微观组成)对物质进行分类的主要应用,是可以预测并记忆物质的性质。
例如:请根据下列框示以及物质的组成,预测物质的化学性质。
随堂练习:1、某合作学习小组讨论辨析以下说法:①粗盐和酸雨都是混合物;②沼气和水煤气都已可再生能源;③冰和干冰既是纯净物又是化合物;④不锈钢和目前流通的硬币都是合金;⑤盐酸和食醋既是化合物又是酸;⑥纯碱和熟石灰都是碱;⑦豆浆和雾都是胶体。
上述说法正确的是( )。
A .①②③④B .①②⑤⑥C .③⑤⑥⑦D .①③④⑦ 2、下列物质按不同类别分组,所得组合最不合理的是( )。
(1)糖类 (2)塑料 (3)石油 (4)蛋白质 (5)合成纤维 (6)棉花 (7)陶瓷 (8)玻璃 (9)天然气FeCl 3________(阳离子) ______________________________ ____________________________________________________________ ______________________________化学性质__________ ________(阴离子) ____________________________________________________________ ______________________________ ______________________________化学性质(10)水泥(11)合成橡胶(12)煤(13)油脂(14)羊毛A.(1)、(4)、(13) B.(2)、(5)、(11)C.(7)、(8)、(10)、(14) D.(3)、(9)、(12)3、试分析下列说法是否正确?对错误的说法应通过举例指出错误之所在。
A.由不同原子组成的纯净物一定是化合物B.非金属氧化物一定是酸性氧化物;碱性氧化物一定是金属氧化物C.含金属元素的离子不一定都是阳离子D.胆矾是纯净物,水泥是混合物4、判断下列说法是否正确,若不正确,请简述理由。
①非金属氧化物一定是酸性氧化物。
②酸性氧化物不一定是非金属氧化物。
③金属氧化物一定是碱性氧化物。
④碱性氧化物一定是金属氧化物。
⑤Na2O和Na2O2均能与H2O反应生成NaOH,故二者都是碱性氧化物。
⑥能与酸反应生成盐和水的氧化物一定是碱性氧化物。
⑦能与碱反应生成盐和水的氧化物一定是酸性氧化物。
5.分类是化学学习和研究的常用手段,下列分类依据和结论都正确的是() A.H2O、HCOOH、Cu2(OH)2CO3均含有氧元素,都是氧化物B.HClO、H2SO4(浓)、HNO3均具有氧化性,都是氧化性酸C.HF、CH3COOH、CH3CH2OH都易溶于水,都是电解质D.HCOOH、H2CO3、H2SO4分子中均含有两个氢原子,都是二元酸6.下表中每组均有4个选项,请从中挑选出1个选项,它跟另3个选项属于不同的分类,请将7.(1)如果按照某种标准能将FeSO4、Na2SO3、NO划归为同一类物质,则下列物质中也能划归为此类物质的是________。
A.KMnO4B.Al2(SO4)3C.KClO3D.K2HPO4(2)现有下列五种气体:H2、O2、NO、NH3、NO2,以上气体的制备反应中,有一反应在原理上与其他反应都不能归为同一类型,请写出实验室制取该气体的化学方程式:_______________________________________________________________________。
附:无机化合物分类:1.氧化物(1)酸性氧化物(CO2、SO2、SO3、N2O5、Mn2O7、CrO3等)(2)碱性氧化物(Na2O、CaO、K2O、Fe2O3、CuO、Al2O3、MgO等)(3)两性氧化物(Al2O3、ZnO等)(4)不成盐氧化物(CO、NO等)(5)过氧化物(Na2O2、H2O2等)(6)特殊氧化物(Fe3O4、Pb3O4、KO2、KO3等)2.酸(1)按酸根分:含氧酸:H2SO4、HNO3、H3PO4、HClO4等无氧酸:HCl、HF、HBr、H2S等(2)按H+数分:一元酸:HCl、HNO3、HClO、HClO4、HBr、HI等二元酸:H2SO4、H2CO3、H2SO3、H2S、H2SiO3等(3)按强弱分:强酸:H2SO4、HNO3、HClO4、HBr、HI、HCl等中强酸:H2SO3弱酸:HF、H2S、H2CO3、H2SiO3、HClO等(4)按氧化性分:氧化性酸:H2SO4(浓)、HNO3、HClO、HMnO4等还原性酸:H2SO3、HBr、HI、H2C2O4(草酸)等(5)按沸点分:挥发性酸:H2CO3、H2SO3、HNO3、HCl、HBr、HI等难挥发性酸:H2SO4、H3PO4等(6)按稳定性分:稳定性酸:H2SO4、H3PO4等不稳定性酸:H2CO3、H2SO3、HNO3、HClO等3.碱(1)按性质分:强碱:NaOH、KOH、Ba(OH)2、Ca(OH)2等弱碱:NH3·H2O(2)按OH-数分:一元碱:NaOH、KOH、LiOH等二元碱:Ba(OH)2、Ca(OH)2、Cu(OH)2、Mg(OH)2等多元碱:Al(OH)3、Fe(OH)3等(3)按溶解性分:可溶性碱:NaOH、KOH、Ba(OH)2等微溶性碱:Ca(OH)2难溶性碱:Cu(OH)2、Mg(OH)2、Al(OH)3、Fe(OH)3等4.盐(1)按组成分:正盐:Na2SO4、Na3PO4、Na2CO3、Na2SO3等酸式盐:NaHCO3、NH4HCO3、Ca(HCO3)2、NaHSO3、NaH2PO4等碱式盐:Cu2(OH)2CO3等复盐:KAl(SO4)2·12H2O等络盐:Ag(NH3)2OH、Fe(SCN)3等(2)按酸根分:含氧酸盐:Na2SO4、Na2CO3、Na2SO3等无氧酸盐:、MgCl2、AlCl3、Na2S等(3)按形成分:强酸强碱盐:Na2SO4、NaCl等强酸弱碱盐:AlCl3、FeCl3、Fe2(SO4)3、NH4Cl等强碱弱酸盐:Na2CO3、Na2SO3等弱酸弱碱盐:(NH4)2CO3、CH3COONH4等(4)其他:无机盐:NH4Cl有机盐:CH3COONa、C2H5ONa、C6H5ONa等5.特殊化合物氢化物:LiH、NaH、CaH2、BaH2等碳化物:CaC2、Al4C3、SiC等氮化物:Mg3N2、AlN、Si3N4等课堂学案第一部分基本概念第二讲化学物质之分类观——物质的分类方法和分类依据考纲要求要求层次考点细化(1)从组成上对物质进行分类,如:混合物和纯净物、单质和化合物、金属和非金属等(2)根据物质组成和性质理解酸、碱、盐、氧化物的分类及其相互联系ⅡⅡ1.根据物质的分类方法,掌握物质的类别的判断。
2.根据物质的类别,初步学会物质性质推测的基本方法。
【活动一】下列物质:金属铁、金属锌、木炭、CuO、CaCO3、H2SO4、NaOH、Ba(O H)2、NaCl、CuSO4。
有人根据不同的依据进行了如下分类,请指出分类的依据和物质类别。
分类依据分类类别名称类别一:金属铁、金属锌、木炭类别二:CuO、CaCO3、H2SO4、NaOH、Ba(OH)2、NaCl、CuSO4类别一:SO2、SO3、N2O5类别二:CuO、Fe2O3、Na2O类别三:Al2O3、ZnO类别四:NO、CO类别一:稀H2SO4、NaCl(aq)类别二:Fe(OH)3胶体、鸡蛋白液、淀粉液类别三:Cu(OH)2浊液类别一:NH3、CO2、NO、Cl2O7、CH3CH2OH类别二:H2SO4、NaOH、CH3COOH、NaCl、BaSO4活动总结:【活动二】分类是研究物质性质的基本方法。