乙二醇二甲醚的介电常数
- 格式:doc
- 大小:11.84 KB
- 文档页数:1

乙二醇二甲醚聚合物电解质
乙二醇二甲醚聚合物电解质是一种由聚(乙二醇二甲醚)(PEGDME,分子量500h/mol)制成的凝胶聚合物电解质。
这种电解质具有较高的沸点(>250℃)、低蒸汽压和出色的电化学稳定性,是一种理想的增塑剂。
在制备过程中,将纯度99.95%的LiTFSI溶解于分子量为500g/mol的PEGDME中,获得混合溶液。
然后将PVDF-HFP共混物(2801)溶解于丙酮中,然后将前面获得的PEGDME溶液与丙酮溶液混合,并在常温下搅拌4小时混合均匀。
然后将该溶液在聚四氟乙烯片上刮成薄膜,然后在50℃下干燥,除去残余的丙酮。
这种凝胶聚合物电解质命名为GPE-X,其中X代表PVDF-HFP的含量(50%、40%、30%、20%),锂盐浓度为1:20(醚基O:Li=20,摩尔量比)。
如需了解更多关于乙二醇二甲醚聚合物电解质的信息,建议查阅化学类书籍或论文,或咨询相关化学专家。

乙二醇二甲醚相对原子质量介绍乙二醇二甲醚(Ethylene Glycol Dimethyl Ether)是一种有机化合物,化学式为C4H10O2,相对原子质量为90.12 g/mol。
它是一种无色液体,具有低毒性和良好的溶解性能,在许多工业领域中有广泛的应用。
本文将详细探讨乙二醇二甲醚的性质、制备方法、应用领域以及安全注意事项。
性质乙二醇二甲醚是一种无色液体,具有特殊的气味。
其相对原子质量为90.12 g/mol,密度为0.86 g/cm³,沸点为84-86°C,熔点为-57°C。
乙二醇二甲醚可与水和大多数有机溶剂混溶,具有良好的溶解性能。
它属于挥发性溶剂,易燃,应储存在阴凉、通风的地方。
制备方法乙二醇二甲醚的制备方法有多种,以下是其中两种常用的方法:1. 乙二醇和甲醇的酯交换反应该方法是通过乙二醇和甲醇之间的酯交换反应制备乙二醇二甲醚。
具体步骤如下:1. 将乙二醇和甲醇按一定摩尔比例加入反应釜中。
2. 加入酯交换催化剂,如碱金属盐类或酸性离子交换树脂。
3. 在适当的温度和压力下进行反应,通常反应温度为100-150°C,反应时间为数小时至数十小时。
4. 反应结束后,进行产品分离和纯化,得到乙二醇二甲醚。
2. 甲醇和环氧乙烷的反应该方法是通过甲醇和环氧乙烷之间的反应制备乙二醇二甲醚。
具体步骤如下: 1. 将甲醇和环氧乙烷按一定摩尔比例加入反应釜中。
2. 加入酸性催化剂,如硫酸或磷酸。
3. 在适当的温度和压力下进行反应,通常反应温度为60-100°C,反应时间为数小时至数十小时。
4. 反应结束后,进行产品分离和纯化,得到乙二醇二甲醚。
应用领域乙二醇二甲醚在许多工业领域中有广泛的应用,以下是其中几个主要领域:1. 溶剂乙二醇二甲醚具有良好的溶解性能,可作为溶剂在化学合成、涂料、油墨、胶粘剂等领域中使用。
它能够溶解许多有机物,有助于反应物的混合和传质,提高反应速率和产率。

常见有机溶剂极性表- [科研]环已烷:-0.2、石油醚(Ⅰ类,30~60℃)、石油醚(Ⅱ类,60~90℃)、正已烷:0.0、甲苯:2.4、二甲苯:2.5、苯:2.7、二氯甲烷: 3.1、异丙醇:3.9、正丁醇:3.9、四氢呋喃:4.0、氯仿:4.1、乙醇:4.3、乙酸乙酯:4.4、甲醇:5.1、丙酮:5.1、乙腈: 5.8、乙酸:6.0、水:10.2水(最大) > 甲酰胺> 乙腈> 甲醇> 乙醇> 丙醇> 丙酮>二氧六环> 四氢呋喃> 甲乙酮> 正丁醇> 乙酸乙酯>乙醚> 异丙醚> 二氯甲烷>氯仿>溴乙烷>苯>四氯化碳>二硫化碳>环己烷>己烷>煤油(最小)用介电常数来表示极性大小,比水极性大的有下列三种:水80.103(20摄氏度)乙二醇碳酸酯89.6(40摄氏度)甲酰胺111.0(20摄氏度)N-甲基甲酰胺182.4(25摄氏度)Hexane(己烷) 0.06 0.33 69 210Cyclohexane(环己烷) 0.10 1.00 81 210Isooctane(异辛烷) 0.10 0.53 99 210Trifluoroacetic acid(三氟乙酸)0.10 -- 72 --Trimethylpentane(三甲基戊烷)0.10 0.47 99 215Cyclopentane(环戊烷) 0.20 0.47 49 210n-heptane(庚烷) 0.20 0.41 98 200Butyl chloride(丁基氯; 丁酰氯) 1.00 0.46 78 220Trichloroethylene(三氯乙烯; 乙炔化三氯)1.00 0.57 87 273Carbon tetrachloride(四氯化碳) 1.60 0.97 77 265Trichlorotrifluoroethane(三氯三氟代乙烷)1.90 0.71 48 231i-propyl ether(丙基醚; 丙醚) 2.40 0.37 68 220Toluene(甲苯) 2.40 0.59 111 285p-xylene(对二甲苯) 2.50 0.65 138 290Chlorobenzene(氯苯) 2.70 0.80 132 --o-dichlorobenzene(领二氯苯) 2.70 1.33 180 295Ethyl ether(二乙醚; 醚) 2.90 0.23 35 220Benzene(苯) 3.00 0.65 80 280Isobutyl alcohol(异丁醇) 3.00 4.70 108 220Methylene chloride(二氯甲烷) 3.40 0.44 40 245Ethylene dichloride(二氯化乙烯) 3.50 0.79 84 228n-butanol(丁醇) 3.90 2.95 117 210n-butyl acetate(醋酸丁酯; 乙酸丁酯)4.00 --- 126 254n-propanol(丙醇) 4.00 2.27 98 210Methyl isobutyl ketone 4.20 -- 119 330Tetrahydrofuran( 四氢呋喃)4.20 0.55 66 220ethanol 4.30 1.20 79 210Ethyl acetate 4.30 0.45 77 260i-propanol(丙醇) 4.30 2.37 82 210Chloroform(氯仿) 4.40 0.57 61 245Methyl ethyl ketone(甲基乙基酮) 4.50 0.43 80 330Dioxane(二恶烷; 二氧六环; 二氧杂环己烷)4.80 1.54 102 220 Pyridine(吡啶) 5.30 0.97 115 305Acetone(丙酮) 5.40 0.32 57 330Nitromethane(硝基甲烷)6.00 0.67 101 380Acetic acid(乙酸)6.20 1.28 118 230Acetonitrile(乙腈) 6.20 0.37 82 210Aniline(苯胺) 6.30 4.40 184 --Dimethyl formamide(二甲基甲酰胺) 6.40 0.92 153 270 Methanol6.60 0.60 65 210Ethylene glycol(乙二醇)6.90 19.90 197 210Dimethyl sulfoxide() 7.20 2.24 189 268water 10.20 1.00 100 268一般有机溶剂根据“相似相溶”的原理来进行选择化合物名称极性粘度沸点吸收波长i-pentane(异戊烷) 0 - 30 - n-pentane(正戊烷) 0 0.23 36 210 Petroleum ether(石油醚) 0.01 0.3 30~60 210 Hexane(己烷) 0.06 0.33 69 210 Cyclohexane(环己烷) 0.1 1 81 210 Isooctane(异辛烷) 0.1 0.53 99 210 Trifluoroacetic acid(三氟乙酸) 0.1 - 72 - Trimethylpentane(三甲基戊烷) 0.1 0.47 99 215 Cyclopentane(环戊烷) 0.2 0.47 49 210 n-heptane(庚烷) 0.2 0.41 98 200 Butyl chloride(丁基氯; 丁酰氯) 1 0.46 78 220 Trichloroethylene(三氯乙烯; 乙炔化三氯) 1 0.57 87 273 Carbon tetrachloride(四氯化碳) 1.6 0.97 77 265 Trichlorotrifluoroethane(三氯三氟代乙烷) 1.9 0.71 48 231 i-propyl ether(丙基醚; 丙醚) 2.4 0.37 68 220 Toluene(甲苯) 2.4 0.59 111 285 p-xylene(对二甲苯) 2.5 0.65 138 290 Chlorobenzene(氯苯) 2.7 0.8 132 - o-dichlorobenzene(邻二氯苯) 2.7 1.33 180 295 Ethyl ether(二乙醚; 醚) 2.9 0.23 35 220 Benzene(苯) 3 0.65 80 280 Isobutyl alcohol(异丁醇) 3 4.7 108 220 Methylene chloride(二氯甲烷) 3.4 0.44 240 245 Ethylene dichloride(二氯化乙烯) 3.5 0.78 84 228 n-butanol(正丁醇) 3.7 2.95 117 210 n-butyl acetate(醋酸丁酯;乙酸丁酯) 4 - 126 254 n-propanol(丙醇) 4 2.27 98 210 Methyl isobutyl ketone(甲基异丁酮) 4.2 - 119 330 Tetrahydrofuran(四氢呋喃) 4.2 0.55 66 220 Ethyl acetate(乙酸乙酯) 4.30 0.45 77 260 i-propanol(异丙醇) 4.3 2.37 82 210 Chloroform(氯仿) 4.4 0.57 61 245Methyl ethyl ketone(甲基乙基酮) 4.5 0.43 80 330 Dioxane(二恶烷; 二氧六环; 二氧杂环己烷) 4.8 1.54 102 220 Pyridine(吡啶) 5.3 0.97 115 305 Acetone(丙酮) 5.4 0.32 57 330 Nitromethane(硝基甲烷) 6 0.67 101 330 Acetic acid(乙酸) 6.2 1.28 118 230 Acetonitrile(乙腈) 6.2 0.37 82 210 Aniline(苯胺) 6.3 4.4 184 - Dimethyl formamide(二甲基甲酰胺) 6.4 0.92 153 270 Methanol(甲醇) 6.6 0.6 65 210 Ethylene glycol(乙二醇 ) 6.9 19.9 197 210 Dimethyl sulfoxide(二甲亚砜 DMSO) 7.2 2.24 189 268 Water(水)10.2 1 100 268下图是混合有机溶剂极性顺序(由小到大,括号内表示的是混合比例)溶剂极性顺序表液氨 -33.35℃ 特殊溶解性:能溶解碱金属和碱土金属剧毒性、腐蚀性液态二氧化硫 -10.08 溶解胺、醚、醇苯酚、有机酸、芳香烃、溴、二硫化碳,多数饱和烃不溶剧毒甲胺 -6.3 是多数有机物和无机物的优良溶剂,液态甲胺与水、醚、苯、丙酮、低级醇混溶,其盐酸盐易溶于水,不溶于醇、醚、酮、氯仿、乙酸乙酯中等毒性,易燃二甲胺 7.4 是有机物和无机物的优良溶剂,溶于水、低级醇、醚、低极性溶剂强烈刺激性石油醚不溶于水,与丙酮、乙醚、乙酸乙酯、苯、氯仿及甲醇以上高级醇混溶与低级烷相似乙醚 34.6 微溶于水,易溶与盐酸.与醇、醚、石油醚、苯、氯仿等多数有机溶剂混溶麻醉性戊烷 36.1 与乙醇、乙醚等多数有机溶剂混溶低毒性二氯甲烷 39.75 与醇、醚、氯仿、苯、二硫化碳等有机溶剂混溶低毒,麻醉性强二硫化碳 46.23 微溶与水,与多种有机溶剂混溶麻醉性,强刺激性溶剂石油脑与乙醇、丙酮、戊醇混溶较其他石油系溶剂大丙酮 56.12 与水、醇、醚、烃混溶低毒,类乙醇,但较大1,1-二氯乙烷 57.28 与醇、醚等大多数有机溶剂混溶低毒、局部刺激性氯仿 61.15 与乙醇、乙醚、石油醚、卤代烃、四氯化碳、二硫化碳等混溶中等毒性,强麻醉性甲醇 64.5 与水、乙醚、醇、酯、卤代烃、苯、酮混溶中等毒性,麻醉性,四氢呋喃 66 优良溶剂,与水混溶,很好的溶解乙醇、乙醚、脂肪烃、芳香烃、氯化烃吸入微毒,经口低毒己烷 68.7 甲醇部分溶解,比乙醇高的醇、醚丙酮、氯仿混溶低毒。

第1部分化学品及企业标识化学品中文名:乙二醇二甲醚化学品英文名:1,2-dimethoxyethaneCAS号:110-71-4分子式:C4H10O2分子量:90.12产品推荐及限制用途:工业及科研用途。
第2部分危险性概述紧急情况概述:高度易燃液体和蒸气。
吸入有害。
GHS危险性类别:易燃液体类别2急性吸入毒性类别4生殖毒性类别1B标签要素:象形图:警示词:危险危险性说明:H225高度易燃液体和蒸气H332吸入有害防范说明:•预防措施:——P210远离热源/火花/明火/热表面。
禁止吸烟。
——P233保持容器密闭。
——P240容器和装载设备接地/等势联接。
——P241使用防爆的电气/通风/照明/设备。
——P242只能使用不产生火花的工具。
——P243采取防止静电放电的措施。
——P280戴防护手套/穿防护服/戴防护眼罩/戴防护面具。
——P261避免吸入粉尘/烟/气体/烟雾/蒸气/喷雾。
——P271只能在室外或通风良好处使用。
——P201使用前取得专用说明。
——P202在阅读并明了所有安全措施前切勿搬动。
•事故响应:——P303+P361+P353如皮肤(或头发)沾染:立即脱掉所有沾染的衣服。
用水清洗皮肤/淋浴。
——P370+P378火灾时:使用灭火器灭火。
——P304+P340如误吸入:将人转移到空气新鲜处,保持呼吸舒适体位。
——P312如感觉不适,呼叫解毒中心/医生——P308+P313如接触到或有疑虑:求医/就诊。
•安全储存:——P403+P235存放在通风良好的地方。
保持低温。
——P405存放处须加锁。
•废弃处置:——P501按当地法规处置内装物/容器。
物理和化学危险:高度易燃液体和蒸气。
健康危害:吸入有害。
环境危害:无资料第3部分成分/组成信息第4部分急救措施急救:吸入:脱离现场至空气新鲜处。
如呼吸困难,给输氧。
呼吸、心跳停止,立即进行心肺复苏术。
就医皮肤接触:脱去污染的衣着,用肥皂水和清水彻底冲洗皮肤。

乙二醇二甲醚结构式乙二醇二甲醚(Ethylene Glycol Dimethyl Ether)是一种具有广泛应用的有机化合物。
它的化学式为C4H10O3,结构式如下所示:CH3-O-CH2-CH2-O-CH3乙二醇二甲醚是一种无色、具有可燃性的液体,具有较低的挥发性和良好的溶解性。
它可以在常温下与水混溶,并且可以与多种有机溶剂相容。
乙二醇二甲醚的物理性质使其成为许多工业和实验室中重要的溶剂和中间体。
乙二醇二甲醚在合成化学中有着广泛的应用。
它可以作为有机合成中的溶剂,用于催化剂的还原、酯化反应、醚化反应等。
乙二醇二甲醚在药物合成中也扮演着重要的角色,它可以用作药物的溶剂、中间体和反应媒介。
此外,乙二醇二甲醚还可以作为涂料、染料和橡胶工业中的添加剂。
乙二醇二甲醚的应用不仅局限于化学领域,在其他领域也得到了广泛的应用。
例如,在电子行业中,乙二醇二甲醚可以用作电解质,用于电池和电容器中。
在汽车工业中,乙二醇二甲醚可以用作燃料添加剂,提高燃料的燃烧效率。
此外,乙二醇二甲醚还可以用于清洁剂、润滑剂和防冻剂的制造。
乙二醇二甲醚的安全性是使用它的重要考虑因素之一。
虽然乙二醇二甲醚具有低毒性和低挥发性,但仍需注意避免长时间暴露和吸入。
在使用乙二醇二甲醚时,应采取适当的防护措施,如佩戴防护手套和护目镜,并确保在通风良好的环境中操作。
总的来说,乙二醇二甲醚是一种重要的有机化合物,具有广泛的应用领域。
它的化学性质和物理性质使其成为合成化学、药物合成和工业生产中不可或缺的溶剂和中间体。
然而,在使用乙二醇二甲醚时,我们也要注意其安全性和环境影响,遵循正确的操作规程,以确保人身安全和环境保护。

本文摘自再生资源回收-变宝网()
乙二醇二甲醚性质与稳定性
乙二醇二甲醚无色液体。
熔点-58℃(-71℃),沸点84℃,相对密度0.8665(20/4℃),折光率1.3796,闪点0℃。
能与水、醇混溶,溶于烃类溶剂。
有强烈醚样气味。
一、乙二醇二甲醚的性质
1.化学性质:性质稳定,不易发生反应。
但能与碘化氢、溴化氢、浓硫酸反应。
酸性催化剂存在时,高温能发生分解。
在150℃以下对碱金属稳定,金属钠可用乙二醇二烷基醚干燥。
但
分解。
与活性小的Grignard试剂如甲基氯化镁在通常条件下不发生反应,但加热到150~200℃时与活性大的试剂如甲基碘化镁作用而分解。
对碱金属的氢化物稳定,可作氢化铝锂的稳定剂、精制剂。
在氧的作用下生成过氧化物,光和热对过氧化物的生成有促进作用。
生成的过氧化物不稳定,分解成醛、酮、酸及其他杂质。
二、乙二醇二甲醚的稳定性
2.稳定性稳定
3.禁配物强氧化剂、强酸
4.避免接触的条件空气、光照
5.聚合危害不聚合
本文摘自变宝网-废金属_废塑料_废纸_废品回收_再生资源B2B交易平台网站;变宝网官网:/?cj
买卖废品废料,再生料就上变宝网,什么废料都有!。

二甲醚介电常数随温度变化特性及应用研究郭琳;刘圣华【摘要】为了精确获得某温度下二甲醚液体的质量,研究二甲醚静态介电常数随温度的变化行为,对273K至323K温度区间二甲醚饱和液体和饱和蒸汽进行了测量.实验结果表明,二甲醚静态介电常数大小随温度存在反相关的变化规律,利用获得的实验数据拟合得到在不同温度下二甲醚液体的介电常数变化曲线.二甲醚饱和蒸汽在温度区间277.5K~318K下,介电常数较大且几乎无变化.在圆柱形电容式传感器模型中进行二甲醚液体液位测量的实验验证,实验计算值与实际观测值之间的误差分布在3.7%~6.5%.应用实验结果,借鉴二甲醚饱和蒸汽与饱和液体密度与温度之间的关系数据,便可精确求出在某温度下二甲醚液体的质量.文中的研究成果对二甲醚工业燃料的应用与控制起到基础性作用.【期刊名称】《西北大学学报(自然科学版)》【年(卷),期】2016(046)001【总页数】6页(P71-76)【关键词】二甲醚;介电常数;电容法;液位测量【作者】郭琳;刘圣华【作者单位】商洛学院电信学院,陕西商洛726000;西安交通大学能源与动力工程学院,陕西西安710049;西安交通大学能源与动力工程学院,陕西西安710049【正文语种】中文【中图分类】TB971;TK121二甲醚取代柴油作为汽车燃料,是未来重要的可替代再生能源之一,作为一种低黏度、易挥发的清洁燃料,相对于柴油和LNG燃料,汽车尾气排放更低[1-2]。
在现有文献中,给出了二甲醚的许多基本物性参数,例如凝固点、沸点、临界参数、蒸汽压和液相密度、导热系数等热物性,以及常用液体如水、甲醇、酒精和正丙醇等的物理性质的实验数据[3-5]。
但是,作者并未发现关于二甲醚的介电常数的试验数据。
本文中,通过实验获得二甲醚静态介电常数随温度的变化行为和对应关系。
目前二甲醚的存量测量常用液位测量法,比如浮子液位计、差压液位计和超声波液位计等,包括接触式和非接触式,它们依靠液位高低来指示二甲醚的量,由于二甲醚易气化,液化二甲醚的质量包括液相和气相两部分[4-5],液位测量法未考虑在温度、压力和液位变化时液相二甲醚密度的变化,其次也未考虑气相二甲醚的量,从而给测量带来很大误差。

物质名温度介电常数三甲基苯20 1.9苯20 2.3对二甲苯20 2.3三甲苯20 2.3间二甲苯20 2.4甲苯20 2.4三乙胺25 2.4二甲苯20 2.4萘20 2.5三甲胺25 2.5己酸71 2.6戊酸20 2.6乙醛22 2.9正丁酸20 2.9丁酸20 3乙苯24 3呋喃25 3丙酸14 3.1辛酸18 3.2脲22 3.5二乙胺20 3.7乙酸2 4.1苯甲醚20 4.3乙醚20 4.3苯甲醚24 4.3苯乙酮24 17.3苯甲醛20 17.8苯乙醚21 4.5丁酸乙脂19 5.1丁酸乙脂19 5.1丁酸甲酯20 5.6 乙酸20 6.2乙胺21 6.3乙酸甲酯25 6.7 甲酸乙脂25 7.1 苯胺20 7.3正丁醇19 7.8丁酸酐-7 12丁酸酐20 12吡啶20 12.5二苯甲酮20 13苯甲醇20 13丁醛26 13.4戊酮25 13.9环己醇25 15戊纯20 15.8茴香醛20 15.8乙二胺18 16甲丙酮14 16.8丁醇(1)20 17.8 环己酮20 18.2苯乙腈20 18.3丁酮20 18.5异丁醇20 18.7丙酮25 20.7丁腈21 20.7乙酸酐19 21甲醛23酒精25 24.3苯甲腈20 26丙腈20 27.7甲醇25 32.6乙二醇20 37乙二醇25 37乙腈21 37.5乙酰胺20 41丙二腈36 47甲酸16 58水20 80.4工业酒精16~31环氧乙烷25 14氯甲烷-4~12.6氧化铝9.3~11.5极性次序:己烷和石油醚< 环己烷<四氯化碳<三氯乙烯<二硫化碳<甲苯<苯<二氯甲烷<氯仿<乙醚<THF<乙酸乙酯<丙酮<丙醇<乙醇<甲醇<水<吡啶<乙酸常用溶剂的极性顺序: 水(极性最大),甲酰胺,乙睛,甲醇,乙醇,丙醇,丙酮,二氧六环,四氢呋喃,甲乙酮,正丁醇, 醋酸乙酯,乙醚,异丙醚,二氯甲烷,氯仿,溴乙烷,苯,氯丙烷,甲苯,四氯化碳,二硫化碳,环己烷,己烷,庚烷,煤油(极性最小),请参考!在结晶和重结晶纯化化学试剂的操作中,溶剂的选择是关系到纯化质量和回收率的关键问题。
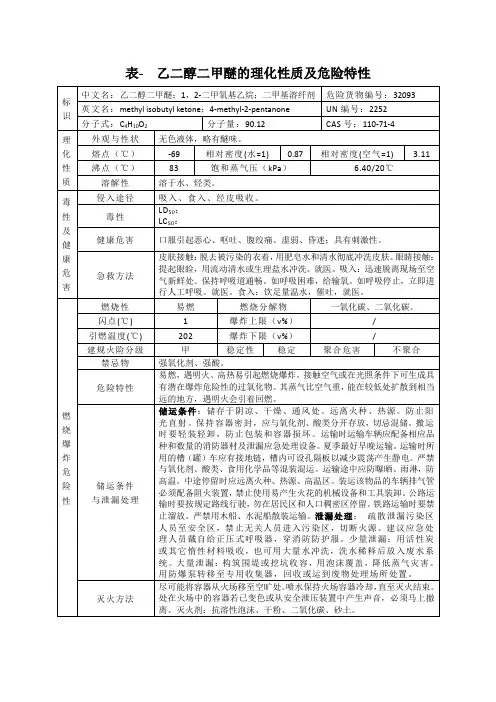
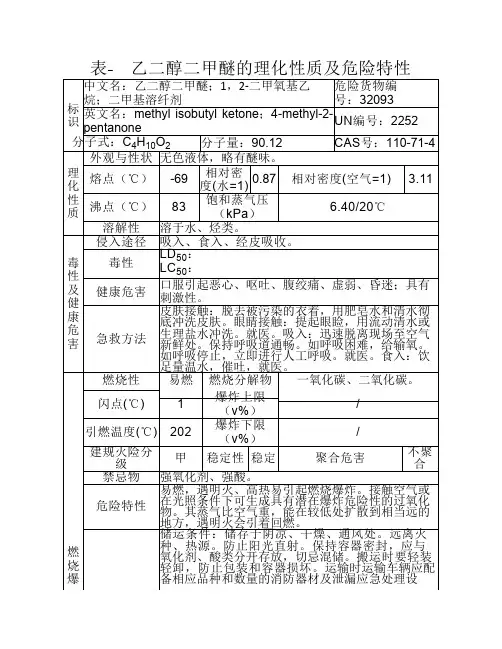
乙二醇二甲醚物质安全数据表英文名称ethyleneglycoldimethylether 主要成分乙二醇二甲醚中文名称2 1,2-二甲氧基乙烷含量%英文名称2 1,2-dimethoxyethane 熔点(℃) -69 沸点(℃) 83 CAS No. 110-71-4 相对密度0.87 (水=1) 3.11 (空气=1) 分子式C4H10O2 危险性类别第3.2类中闪点易燃液体分子量90.12 饱和蒸气压 6.40(20℃) (kPa)外观与性状无色液体,略有醚味。
溶解性溶于水、烃类。
主要用途用作溶剂、医药抽提剂、有机合成中间体。
危险性概述健康危害口服引起恶心、呕吐、腹绞痛、虚弱、昏迷。
具有刺激性。
防护措施工程控制生产过程密闭,全面通风。
提供安全淋浴和洗眼设备。
呼吸系统高浓度蒸气接触可佩戴过滤式防毒面具(半面罩)。
眼睛防护一般不需要特殊防护,高浓度接触时可戴化学安全防护眼镜。
环境危害身体防护穿防静电工作服。
手防护戴橡胶耐油手套。
燃爆危险本品易燃,具刺激性。
其它工作现场禁止吸烟、进食和饮水。
工作完毕,淋浴更衣。
注意个人清洁卫生。
急救措施皮肤接触脱去污染的衣着,用肥皂水和清水彻底冲洗皮肤。
消防措施危险特性易燃,遇明火、高热易引起燃烧爆炸。
与氧化剂能发生强烈反应。
接触空气或在光照条件下可生成具有潜在爆炸危险性的过氧化物。
其蒸气比空气重,能在较低处扩散到相当远的地方,遇火源会着火回燃。
眼睛接触提起眼睑,用流动清水或生理盐水冲洗。
就医。
燃烧产物吸入迅速脱离现场至空气新鲜处。
保持呼吸道通畅。
如呼吸困难,给输氧。
如呼吸停止,立即进行人工呼吸。
就医。
灭火方法食入饮足量温水,催吐。
就医。
泄露应急处理迅速撤离泄漏污染区人员至安全区,并进行隔离,严格限制出入。
切断火源。
建议应急处理人员戴自给正压式呼吸器,穿防静电工作服。
尽可能切断泄漏源。
防止流入下水道、排洪沟等限制性空间。
小量泄漏:用活性炭或其它惰性材料吸收。
也可以用大量水冲洗,洗水稀释后放入废水系统。
乙二醇二甲醚电池级
乙二醇二甲醚(EDM, DEDM)是一种性能优良的非质子极性溶剂,可以用于多种应用,包括作为气体吸收剂、萃取剂和脱漆剂。
在电子化学领域,乙二醇二甲醚也有广泛的应用,可以作为非水溶液电解质溶剂,用于电化学设备、充电电池以及有机化合物电解反应等。
电池级的乙二醇二甲醚是一种特殊的等级,适用于电池制造过程中的使用。
它需要满足一系列严格的质量标准,包括但不限于外观(无色透明液体)、溶剂残留量、水分含量、酸度以及电导率等。
这些严格的质量标准确保了电池级乙二醇二甲醚在电池制造中的性能和稳定性。
电池级乙二醇二甲醚的供应通常包括不同的包装规格,以适应不同的需求和运输要求。
例如,常见的包装规格有25升包装、200升包装、5升包装以及500毫升小瓶包装等。
供应商通常还会提供相关的技术文档,如MSDS资料和第三方SGS检测报告,以证明其产品的质量和合规性。
请注意,具体的产品信息、质量标准和包装规格可能会因供应商和生产商的不同而有所差异。
因此,在选择和使用电池级乙二醇二甲醚时,建议直接联系供应商或生产商以获取最准确和最新的信息。
乙二醇二甲醚螯合金属离子乙二醇二甲醚(ethylene glycol dimethyl ether,缩写EGDME)是一种常用的有机溶剂,它具有良好的溶解性、较低的挥发性和较高的比表面积,广泛应用于化学合成、催化反应和电化学领域。
此外,乙二醇二甲醚还具有良好的螯合性质,可以与金属离子形成稳定的配合物,为研究金属离子的性质和应用提供了新的途径。
乙二醇二甲醚螯合金属离子可以通过两种方式进行:配位作用和络合反应。
在配位作用中,乙二醇二甲醚的氧原子与金属离子形成配位键,通过共享电子对的方式与金属离子结合。
在络合反应中,乙二醇二甲醚通过氧原子与金属离子进行弱键的相互作用,形成络合物。
乙二醇二甲醚与金属离子的络合反应具有很高的选择性。
根据金属离子的不同性质和乙二醇二甲醚的分子结构,可以选择性地螯合某种金属离子,从而实现对金属离子的分离和富集。
这种选择性螯合的能力在环境污染物的检测和分析中具有重要意义。
例如,乙二醇二甲醚可以选择性地螯合有毒重金属离子,如汞离子、铅离子和镉离子,从而实现对这些离子的富集和分离。
乙二醇二甲醚螯合金属离子还可以用于催化反应。
乙二醇二甲醚作为配体可以与金属离子形成配合物,增强金属离子的催化活性。
这是因为乙二醇二甲醚的配位能力可以改变金属离子的电子结构,使其更容易参与反应。
此外,乙二醇二甲醚还可以通过与金属离子形成络合物来调节反应的速率和选择性,从而实现对反应过程的控制。
乙二醇二甲醚螯合金属离子还在电化学领域具有重要的应用。
乙二醇二甲醚可以作为电解质溶剂,在电化学反应中提供离子传输的通道。
乙二醇二甲醚与金属离子的络合反应可以提高电解质的导电性能,从而提高电化学反应的效率。
此外,乙二醇二甲醚的螯合性质还可以用于制备金属离子选择电极,实现对特定金属离子的检测和测量。
乙二醇二甲醚作为一种具有良好螯合性质的有机溶剂,在化学合成、催化反应和电化学领域具有重要的应用价值。
通过与金属离子形成稳定的配合物,乙二醇二甲醚可以实现对金属离子的分离和富集,提高金属离子的催化活性,调节反应的速率和选择性,以及提高电化学反应的效率。
二乙二醇二甲醚
产品名称二乙二醇二甲醚英文名:Diethylene glycol di-methyl ether, DGDE.
分子式 C6H14O3
分子量 134.18
CAS NO 111-96-6
物性无色透明液体,微有醚气味.
沸点(101.3kPa):159.76℃,
比重(25℃/4℃):0.9467,
折射率(25℃):1.4097,
闪点:60℃(闭杯). 63℃(开杯)
粘度(25℃)0.981mPa.s
表面张力:(25℃) 29.5 mN/m.
企业标准 Q/JLH001—2001
技术指标项目规格
外观无色透明液体
纯度(GC)%≥ 99.5
水含量%≤ 0.05
酸度(以HAC计)%≤ 0.020
过氧化物(以H2O2计)%≤ 0.005
溶解性:可与水/醇/醚/烃类混溶.
用途本品为非质子极性溶剂,可用于极性有机反应,阴离子聚合、配位离子聚合反应的溶剂,可作还原、烷基化和缩合等反应溶剂,还可作为格氏和类似合成的介质,也用作无污染清洗剂、萃取剂、稀释剂、医药助剂及树脂溶剂.
包装 190kg/铁桶装 ( UN NO.3271 货物类别:3.3类包装类别Ⅲ ) 序号分子结构 CAS 登录号产品名称分子式
1 111-96-6 二乙二醇二甲醚; 二甘醇二甲醚; 双(2-甲氧基乙基)
醚;2-methoxyethyl ether;bis(2-methoxyethyl) ether; diethylene glycol dimethyl ether C6H14O3。