化工原理 第九章3
- 格式:ppt
- 大小:534.50 KB
- 文档页数:18


化⼯原理-第九章-液体精馏化⼯原理-第九章-液体精馏(⼀)测试⼀⼀.选择题1.蒸馏是利⽤各组分()不同的特性实现分离的⽬的。
CA 溶解度;B 等规度;C 挥发度;D 调和度。
2.在⼆元混合液中,沸点低的组分称为()组分。
CA 可挥发;B 不挥发;C 易挥发;D 难挥发。
3.()是保证精馏过程连续稳定操作的必不可少的条件之⼀。
AA 液相回流;B 进料;C 侧线抽出;D 产品提纯。
4.在()中溶液部分⽓化⽽产⽣上升蒸⽓,是精馏得以连续稳定操作的⼀个必不可少条件。
CA 冷凝器;B 蒸发器;C 再沸器;D 换热器。
5.再沸器的作⽤是提供⼀定量的()流。
DA 上升物料;B 上升组分;C 上升产品;D 上升蒸⽓。
6.冷凝器的作⽤是提供()产品及保证有适宜的液相回流。
BA 塔顶⽓相;B 塔顶液相;C 塔底⽓相;D 塔底液相。
7.冷凝器的作⽤是提供塔顶液相产品及保证有适宜的()回流。
BA ⽓相;B 液相;C 固相;D 混合相。
8.在精馏塔中,原料液进⼊的那层板称为()。
CA 浮阀板;B 喷射板;C 加料板;D 分离板。
9.在精馏塔中,加料板以下的塔段(包括加料板)称为()。
BA 精馏段;B 提馏段;C 进料段;D 混合段。
10.某⼆元混合物,进料量为100 kmol/h ,x F = 0.6,要求塔顶x D 不⼩于0.9,则塔顶最⼤产量为()。
(则W=0) BA 60 kmol/h ;B 66.7 kmol/h ;C 90 kmol/h ;D 100 kmol/h 。
11.精馏分离某⼆元混合物,规定分离要求为D x 、w x 。
如进料分别为1F x 、2F x 时,其相应的最⼩回流⽐分别为1min R 、2min R 。
当21F F x x >时,则()。
AA .2min 1min R R <;B .2min 1min R R =;C .2min 1min R R >;D .min R 的⼤⼩⽆法确定12.精馏的操作线为直线,主要是因为()。


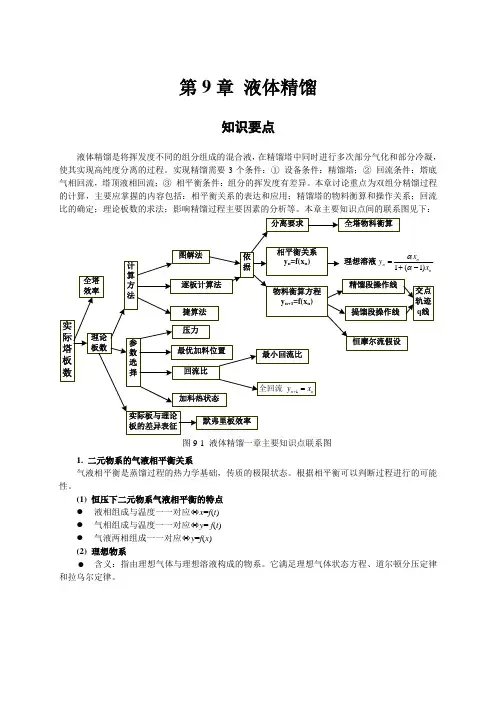
第9章液体精馏知识要点液体精馏是将挥发度不同的组分组成的混合液,在精馏塔中同时进行多次部分气化和部分冷凝,使其实现高纯度分离的过程。
实现精馏需要3个条件:①设备条件:精馏塔;②回流条件:塔底气相回流,塔顶液相回流;③相平衡条件:组分的挥发度有差异。
本章讨论重点为双组分精馏过程的计算,主要应掌握的内容包括:相平衡关系的表达和应用;精馏塔的物料衡算和操作关系;回流比的确定;理论板数的求法;影响精馏过程主要因素的分析等。
本章主要知识点间的联系图见下:图9-1 液体精馏一章主要知识点联系图1. 二元物系的气液相平衡关系气液相平衡是蒸馏过程的热力学基础,传质的极限状态。
根据相平衡可以判断过程进行的可能性。
(1) 恒压下二元物系气液相平衡的特点●液相组成与温度一一对应⇔x=f(t)●气相组成与温度一一对应⇔y= f(t)●气液两相组成一一对应⇔y=f(x)(2) 理想物系含义:指由理想气体与理想溶液构成的物系。
它满足理想气体状态方程、道尔顿分压定律和拉乌尔定律。
拉乌尔定律相对挥发度/1/1A A A B B B p x y xp x y xναν-===⋅- (9-1)11y xy xα-=⋅- (气相服从道尔顿分压定律) 相对挥发度α愈是大于1 ,则y 愈是大于x ,物系愈容易分离。
● 泡点方程x -toB ooA Bp p x p p -=- (9-2) ● 露点方程y -to A BA A Bp p p y p p p -=⋅- (9-3) ● 相平衡方程y-x()11xy xαα=+- (9-4)● t -y (x )相图两端点A 与B :端点A 代表纯易挥发组分A(x =1),端点B 代表纯难挥发组分B(x =0)。
两线:t -x 线为泡点线,泡点与组成x 有关;t-y 线为露点线,露点与组成y 有关。
3区:t -x 线以下为过冷液体区;t-y 线以上为过热蒸汽区;在t-x 与t -y 线之间的区域为气液共存区,只有体系落在气液共存区才能实现一定程度的分离。




第九章液体精馏1 概述 1.1 蒸馏的目的和依据 (1)目的:分离液体混合物 (2)依据:混合液中各组分挥发度 的不同第九章液体精馏9.1 概述 9.1.1 蒸馏的目的和依据(1)目的:分离液体混合物 (2)依据:混合液中各组分挥发度的不同 挥发度——表征物质挥发程度的量。
pA pB 相平衡时: ν A = 、ν B = xA xBy A yB ν A >ν B ∴ > x A xByA > xAA—轻组分,B—重组分9.1.2 工业蒸馏过程 (1)平衡蒸馏(闪蒸)(2)简单蒸馏9.1.3 精馏操作的经济性 操作费用:加热、冷凝所消耗的费用 操作压强: 技术上:P↑,气、液平衡(饱和)温度↑,冷凝易, 汽化难。
z 对热敏性物质,常采用低压或真空操作。
z经济上:高压、真空精馏都将增加设备投资,应作优化 选择。
z9.2. 双组分溶液的气液相平衡9.2.1 理想物系气液相平衡(1)汽液两相平衡的自由度 相律:F = N–Φ + 2 双组分物系: 独立组分数N=2 相数Φ=2 自由度F=2 描述双组分平衡物系的参数:6个 温度-t,总压-P,两相组成-yA,yB,xA,xB。
双组分物系的组成满足: ¾归一关系: y A + y B = 1 ¾相平衡关系:y A = f ( xA )xA + xB = 1∴独立参数仅有:P,t,xA(yA)。
蒸馏操作中,P是选定的,因此温度与浓度必有一 一对应关系。
(2)双组分理想物系的液相组成-温度(泡点)关系式 理想溶液满足拉乌尔定律:0 p A = x A PA0 pB = x B PB总压: 组成: ∴P = PA + PBxB = 1 − xAPA0 x A + PB0 (1 − x A ) = P0 = f (t ) QPA AP − PB0 ∴x = 0 A PA − PB0P − f B (t ) ∴ xA = f A (t ) − f B (t )——泡点方程 —— x~t关系纯组分的饱和蒸汽压与温度的关系可用安托因方程描述: 安托因方程ln P 0 = A − B t+C(3)双组分理想物系的气相组成-温度(露点)关系0 p A PA xA Q yA = = P P——道尔顿分压定律 拉乌尔定律PA0 P − PB0 ∴ yA = 0 0 P PA − PB——露点方程0 0 PA P − PB f A (t ) P − fB (t ) yA = ⋅ 0 = ⋅ 0 P PA − PB P f A (t ) − fB (t )—— y~t关系(4)双组分物系的t~x(y)图和y~x图bta问题:a,b两点哪一个温度较高?(5) y~x的近似表达式与相对挥发度α定义:易挥发(轻)组分为A, 难挥发(重)组分为B, p 则: ν A = p A ν B = B xA xBPA PB > xA x BνA 相对挥发度:α = ν A >ν B νB yA yB 当气相服从道尔顿分压定律时,α = xA xBα= ∴ p A /x A P ⋅ y A /x A = p B /x B P ⋅ y B /x B yA x =α ⋅( A ) yB xB对于二元溶液,则:yA xA =α ⋅( ) 1 − yA 1 − xA∴ y=α⋅x 1 + (α − 1)x- 相平衡方程⋅∴=+−αxy 1(α1)x-相平衡方程讨论:z 上式反映了双组分物系平衡时两相浓度的关系。


化工原理第九章吸附分离
吸附分离,也称为吸收或吸收分离,是指利用一定的相互作用“粘合剂”或“吸附剂”使混合物中一些组成部分粘合或吸附到该粘合剂或吸附剂上,从而使混合物中一些组分有机地被分离出来的过程。
它是一种新型的分离方法,有可能替代传统的分离工艺,是现代化工的一项重要技术。
吸附分离的原理:吸附分离可以分为物理吸附和化学吸附两种形式。
物理吸附是指物质相互作用的结果,包括空气、气体、液体、溶剂等。
物理吸附是指在一些固体表面上建立的物理性相互作用,其实质是由于表面粗糙形成的能量障碍,而在能量障碍的阻碍下,物质相互作用,物质就被吸附在这种固体表面上。
如果这种固体表面在特定的温度和压力条件下,具有良好的表面化学稳定性,即可建立有效的物理吸附。
化学吸附又叫做专配吸附,是指物质间由于共价作用形成的固体表面和溶剂之间的作用过程。
它是一种特殊的吸附作用,是由于固体表面上化学基团构成的膜层,以及溶剂中的其中一种物质,在化学反应中形成化学键而发生的吸附作用。
吸附分离的应用:吸附分离已被广泛应用于催化剂分离、石油的湿气处理、空气净化、废气处理、提纯溶剂等行业。