晶体的类型及性质
- 格式:doc
- 大小:171.50 KB
- 文档页数:8

晶体的四种基本类型和特点晶体是由于原子、分子或离子排列有序而形成的固态物质。
根据晶体的结构特点,晶体可以分为四种基本类型:离子晶体、共价晶体、金属晶体和分子晶体。
1. 离子晶体离子晶体由正离子和负离子通过离子键结合而成。
正负离子之间的电荷吸引力使得离子晶体具有高熔点和脆性。
离子晶体的晶格结构稳定,形成高度有序的排列。
常见的离子晶体有氯化钠(NaCl)、氧化镁(MgO)等。
离子晶体在溶液中能够导电,但在固态下通常是绝缘体。
2. 共价晶体共价晶体由共价键连接的原子或分子组成。
共价键是由原子间的电子共享形成的,因此共价晶体具有很高的熔点和硬度。
共价晶体的晶格结构复杂多样,具有很高的化学稳定性。
典型的共价晶体包括金刚石(C)和硅(Si)。
共价晶体通常是绝缘体或半导体,由于共价键的稳定性,其导电性较弱。
3. 金属晶体金属晶体由金属原子通过金属键结合而成。
金属键是由金属原子间的电子云形成的,因此金属晶体具有良好的导电性和热传导性。
金属晶体的晶格结构常为紧密堆积或面心立方等紧密排列。
金属晶体的熔点通常较低,而且具有良好的延展性和韧性。
典型的金属晶体有铁(Fe)、铜(Cu)等。
4. 分子晶体分子晶体由分子通过弱相互作用力(如范德华力)结合而成。
分子晶体的晶格结构不规则,分子间的距离和角度较大。
由于分子间的相互作用力较弱,分子晶体通常具有较低的熔点和软硬度。
典型的分子晶体有水(H2O)、冰、石英(SiO2)等。
分子晶体在固态下通常是绝缘体,但某些分子晶体在溶液中能够导电。
总结起来,离子晶体由正负离子通过离子键结合,具有高熔点和脆性;共价晶体由共价键连接,具有高熔点和硬度;金属晶体由金属原子通过金属键结合,具有良好的导电性和热传导性;分子晶体由分子通过弱相互作用力结合,具有较低的熔点和软硬度。
这四种基本类型的晶体在结构、性质和应用上都有明显的差异。
研究晶体的类型和特点对于理解物质的性质和应用具有重要意义。


晶体相关知识点总结一、基本概念1. 晶体的定义晶体是由原子、离子或分子按照一定的规则排列而形成的固体结构。
晶体具有高度有序性,具有一定的周期性和对称性。
晶体是凝聚态物质的一种主要形式,占据了固态物质的绝大部分。
2. 晶体的种类根据晶体结构的不同,晶体可以分为离子晶体、共价晶体、金属晶体和分子晶体等几种基本类型。
不同类型的晶体具有不同的物理性质和化学性质。
3. 晶体的分类根据晶体的外部形态,晶体可以分为单斜晶、正交晶、菱形晶、六方晶、四方晶、立方晶等几种基本类型。
不同类型的晶体具有不同的外部形态和对称性。
二、晶体结构1. 晶体的晶体结构晶体结构是指晶体中原子、离子或分子的排列方式和规律。
晶体结构可以分为周期性结构和非周期性结构两种形式。
周期性结构是指晶体中原子、离子或分子的排列具有一定的周期性,具有明显的晶格和对称性。
非周期性结构是指晶体中原子、离子或分子的排列没有明显的周期性,没有规则的晶格和对称性。
2. 晶体的晶格晶体的晶格是指晶体中原子、离子或分子所构成的三维空间排列的规则结构。
晶格可以分为周期性晶格和非周期性晶格两种类型。
周期性晶格是指晶格具有明显的周期性,有规则的排列和对称性。
非周期性晶格是指晶格没有明显的周期性,没有规则的排列和对称性。
3. 晶体的晶胞晶胞是指晶体中最小的具有完整晶体结构的基本单位。
晶胞可以分为原胞和扩展晶胞两种类型。
原胞是指晶体中最小的具有完整晶体结构的基本单位,包含了一个或多个原子、离子或分子。
扩展晶胞是指原胞在晶体结构中的重复排列,是构成晶体的基本单位。
三、晶体的生长1. 晶体生长的基本过程晶体生长是指在溶液、熔体或气相中,原子、离子或分子从溶液中萃取并在已生成的晶体上沉积,形成新晶体的过程。
晶体生长的基本过程包括成核、生长和成形几个阶段,成核是指溶液中原子、离子或分子聚集形成晶体的核心;生长是指晶体核心上原子、离子或分子的进一步沉积和排列生长;成形是指晶体的表面形态和结晶过程。

晶体类型分类晶体类型分类导言:晶体是具有周期性排列的原子、离子或分子的固体物质,它们的结构和性质对于我们理解和应用材料科学非常重要。
由于晶体的种类繁多,如何对其进行分类成为了一个关键问题。
在本篇文章中,我们将探讨晶体类型的分类方法,并深入研究各个分类的特点和应用。
第一部分:基于元素组成的晶体分类1. 金属晶体:金属晶体由金属原子组成,具有高导电性和高热导性。
金属晶体可进一步分为面心立方晶体、体心立方晶体和密堆积晶体等几种不同的结构类型。
这些不同的结构类型决定了金属的性质和应用领域。
2. 离子晶体:离子晶体由阳离子和阴离子组成,它们通过离子键相互吸引而形成稳定的晶体结构。
离子晶体具有高熔点、良好的溶解性和电解性能。
常见的离子晶体包括氯化钠和氧化铁等。
3. 共价晶体:共价晶体由共价键相连的原子构成,这种键的特点是电子对的共享。
共价晶体常见的是碳元素的几种晶体形式,如金刚石和石墨等。
共价晶体通常具有高硬度、高熔点和高热稳定性。
第二部分:基于结构的晶体分类1. 伍德结构分类法:根据晶体的基本结构单元(BPU)的排列方式,晶体可以分为14种不同的布拉维格点群。
这些布拉维格点群包括立方晶系、四方晶系、正交晶系等,每种布拉维格点群都有其独特的晶体结构及性质。
2. 米勒-布拉弗指数:米勒-布拉弗指数是描述晶体晶面方向的一种方法,通过指数确定了晶面的交点位置。
通过分析晶面的指数,我们可以了解晶体的晶面结构以及晶体的对称性。
第三部分:基于物质性质的晶体分类1. 光学性质:晶体对于不同波长的光可以表现出多种不同的性质,如吸收、反射和折射等。
通过研究晶体的光学性质,我们可以了解晶体的结构和成分,从而推断其物理和化学性质。
2. 声学性质:晶体的结构和成分也会影响其声学性质,如声速和声子态密度等。
通过测量晶体的声学性质,我们可以了解晶体的结构和内部缺陷。
结论:晶体的分类方法多种多样,不同的分类方法可以从不同的角度解析晶体的结构和性质。
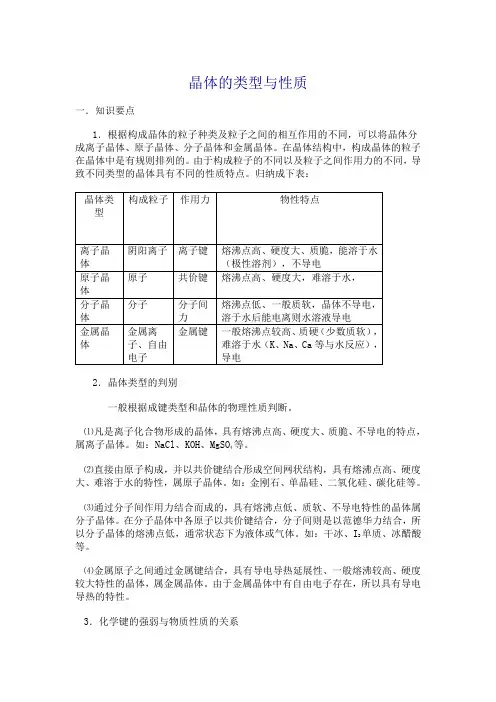
晶体的类型与性质一.知识要点1.根据构成晶体的粒子种类及粒子之间的相互作用的不同,可以将晶体分成离子晶体、原子晶体、分子晶体和金属晶体。
在晶体结构中,构成晶体的粒子在晶体中是有规则排列的。
由于构成粒子的不同以及粒子之间作用力的不同,导致不同类型的晶体具有不同的性质特点。
归纳成下表:2.晶体类型的判别一般根据成键类型和晶体的物理性质判断。
⑴凡是离子化合物形成的晶体,具有熔沸点高、硬度大、质脆、不导电的特点,等。
属离子晶体。
如:NaCl、KOH、MgSO4⑵直接由原子构成,并以共价键结合形成空间网状结构,具有熔沸点高、硬度大、难溶于水的特性,属原子晶体。
如:金刚石、单晶硅、二氧化硅、碳化硅等。
⑶通过分子间作用力结合而成的,具有熔沸点低、质软、不导电特性的晶体属分子晶体。
在分子晶体中各原子以共价键结合,分子间则是以范德华力结合,所单质、冰醋酸以分子晶体的熔沸点低,通常状态下为液体或气体。
如:干冰、I2等。
⑷金属原子之间通过金属键结合,具有导电导热延展性、一般熔沸较高、硬度较大特性的晶体,属金属晶体。
由于金属晶体中有自由电子存在,所以具有导电导热的特性。
3.化学键的强弱与物质性质的关系离子晶体中,离子键键能的大小与离子的半径、离子所带的电荷数、离子的核电荷数有关,一般起决定作用的主要是离子半径的大小。
离子半径小,阴、阳离子间的静电作用力大,离子键键能就大,离子晶体的熔沸点就高,硬度也大。
原子晶体中共价键键能的大小与成键的原子半径有关,原子半径越小,键长越短,键能就越大,晶体的熔沸点就越高,硬度也就越大。
分子晶体中分子与分子之间的作用力为范德华力,其能量较小。
对于组成和结构相似的物质,其分子间的作用力随相对分子质量的增大而增大,熔沸点也随之增高。
还与分子的极性有关,分子极性大,分子间作用力大,熔沸点高。
金属晶体中金属离子半径越小,离子电荷数越大,其金属离子与自由电子间的作用力越强,金属的熔沸点就越高。
4.石墨晶体具有层状结构的特点,层内原子间以共价键的方式形成平面网状结构(相当于原子晶体),层与层之间以范德华力结合(相当于分子晶体),层与层间有自由电子存在,晶体具有导电性(相当于金属晶体),所以石墨是一种过渡性或混合型晶体。


晶体的类型与性质作者:李金洲来源:《神州·中旬刊》2013年第06期摘要:四种晶体所涉及的知识点多,学生经常把性质张冠李戴,本文就知识点加以总结,应用图表把性质、代表物加以分析,并配有练习,能够使学生轻松掌握该知识点。
关键词:离子晶体原子晶体分子晶体金属晶体一、知识点精讲1、晶体类型及性质比较*注意:⑴四种晶体类型的化学式表示的意义不同:离子晶体、原子晶体中化学式表示的分别是阴阳离子最简比和原子最简比,从而有的资料上把离子晶体和原子晶体看成是巨型分子;分子晶体中表示的是单个的分子。
⑵晶体讨论的是固态形式,而我们通常讨论化学性质时,不仅仅讨论其固态形式,包括其液态、气态和其水溶液。
2、化学键与分子间作用力的比较3、化学键和分子间作用力对物理、化学性质的影响(1)不同晶体类型的硬度大小、熔沸点高低等物理性质由于化学键键能比较大,使得其硬度较大和熔沸点较高,所以原子晶体、离子晶体和金属晶体分别大于和高于分子晶体。
但必须注意得是融化过程中原子晶体、离子晶体和金属晶体破坏的是化学键而分子晶体是分子间作用力(有的是氢键)。
(2)晶体性质的比较:比较晶体的硬度大小、熔沸点高低等物理性质的依据是:原子晶体→共价键键能→键长→由原子半径决定。
如:金刚石>晶体硅离子晶体→离子键强弱→离子半径和离子所带电荷数决定。
如:NaCl金属晶体→金属键→金属阳离子半径、所带的电荷数、自由电子的多少而定。
阳离子半径越小,所带的电荷越多,自由电子越多,相互作用就越大,熔点就会相应升高。
如:熔点KNa>K>Rb>Cs。
分子晶体→分子间力→结构相似的情况下由相对分子质量决定(分子有氢键例外)(3)氢键对分子晶体物理性质的影响⑴对溶解度的影响,分子中有氢键的可以在水中溶解,如NH3极易溶于水。
⑵对熔沸点的影响,分子中有氢键的相对而言熔沸点较高,如氧族元素中H2O的熔沸点最高。
⑶解释一些反常现象,如冰的密度小于水。

质对市爱慕阳光实验学校高三化学晶体的类型和性质【本讲主要内容】晶体的类型和性质【知识掌握】【知识点精析】1. 晶体的概念晶体是经过自然结晶而形成的具有规那么几何外形的固体。
自然结晶可以是液态物质降温变成固体的过程,也可是蒸发溶剂析出晶体的过程。
比方:水结成冰,海水蒸发得到的食盐固体。
晶体的宏观结构特点:有规那么的几何外形。
晶体的微观结构特点:构成晶体的微粒空间排列有规那么。
构成晶体的粒子有:分子、原子、离子。
晶体内部粒子间的作用有:离子键〔离子晶体〕、共价键〔原子晶体〕、分子间的作用力〔又叫范德瓦耳斯力,分子晶体〕,甚至氢键〔氢键不是化学健,是一种比拟强的范德瓦耳斯力,特殊的分子晶体,如:冰〕。
2. 晶体的分类根据构成晶体的粒子种类及粒子间的相互作用不同,可将晶体分为假设干类型,如:离子晶体、分子晶体、原子晶体、金属晶体。
〔1〕离子晶体①离子间通过离子键结合而成的晶体叫做离子晶体。
构成离子晶体的粒子是阴离子和阳离子。
离子晶体中离子间的作用是离子键。
离子化合物的晶体是离子晶体。
②典型离子晶体的结构模型NaCl晶体的结构模型 CsCl晶体的结构模型晶胞的概念:晶体中可以重复的最小单元。
③离子晶体的物理性质由于离子晶体离子键的能量较大,阴阳离子之间具有稳的结合方式,所以离子晶体的硬度较大、难于压缩,具有较高的熔点和沸点。
④离子晶体熔化、溶解过程中,均破坏离子键。
氯化钠晶体熔化变成液态,离子能够自由移动,离子键被破坏;氯化钠晶体溶于水中,电离成自由移动的离子,也破坏了离子键。
离子晶体固态时不导电,但熔化或溶解过程中,均能产生自由移动的阴、阳离子而导电。
〔2〕分子晶体①分子间作用力〔范德瓦耳斯力〕:分子间作用力比化学键弱得多,它对物质的熔点、沸点有影响。
②分子晶体的概念分子间以分子间的作用力相结合的晶体叫做分子晶体。
构成分子晶体的粒子是分子。
构成分子晶体的粒子间的作用是分子间作用力〔即范德瓦耳斯力〕。
由分子构成的物质在固态时都属于分子晶体。

晶体类型分类
一、金属晶体
金属晶体是由金属原子组成的晶体,其特点是金属原子之间通过金属键相互连接。
金属晶体具有良好的导电性和导热性,因为金属键的自由电子能够自由移动。
金属晶体通常具有高硬度和高熔点,因为金属键的强度较高。
常见的金属晶体包括铁、铜、铝等。
二、离子晶体
离子晶体是由阳离子和阴离子通过离子键相互连接而成的晶体。
离子晶体具有高熔点和脆性,因为离子键的强度较高。
离子晶体在溶液中可以导电,因为离子在溶液中能够自由移动。
常见的离子晶体包括氯化钠、碳酸钙等。
三、共价晶体
共价晶体是由非金属原子通过共价键相互连接而成的晶体。
共价晶体通常具有高硬度和高熔点,因为共价键的强度较高。
共价晶体中的原子通常以三维网状结构排列,形成稳定的晶体结构。
常见的共价晶体包括金刚石、石英等。
四、分子晶体
分子晶体是由分子通过分子间力相互连接而成的晶体。
分子晶体通常具有较低的熔点和较低的硬度,因为分子间力较弱。
分子晶体在溶液中通常不导电,因为分子在溶液中不能自由移动。
常见的分子
晶体包括蔗糖、苯等。
不同类型的晶体具有不同的结构和性质,它们在材料科学、化学和物理等领域有着广泛的应用。
通过研究不同类型的晶体,我们可以深入理解物质的性质和行为,为材料设计和应用提供指导。
总结一下,晶体类型可以分为金属晶体、离子晶体、共价晶体和分子晶体。
每种类型的晶体都具有独特的结构和性质,对于材料科学和化学研究有着重要的意义。
通过深入了解晶体类型,我们可以更好地理解物质的本质,并为材料设计和应用提供指导。

晶体的五种类型晶体是由原子或者分子沿着一定规律排列而成的具有长程有序结构的固体物质。
晶体的类型多种多样,根据其结构和性质的不同,可以将晶体分成五种类型:离子晶体、共价晶体、金属晶体、分子晶体和非晶态材料。
1.离子晶体离子晶体是由阴阳离子组成的晶体,其特点是具有良好的电解质性质。
这类晶体的结构稳定,通常具有高熔点和硬度,是常见的岩石和矿石。
典型的离子晶体包括氯化钠(NaCl)、氧化镁(MgO)和硫酸钙(CaSO4)等。
离子晶体的性质主要由其中阳离子和阴离子的相互排列和结合方式所决定。
2.共价晶体共价晶体是由共价键连接的原子或者分子构成的晶体,其特点是硬度大,熔点高,化学性质稳定。
典型的共价晶体包括金刚石(碳)、硅化铝(Al2O3)和碳化硅(SiC)等。
共价晶体的结构稳定,常用作磨料、切割工具和高温材料等。
3.金属晶体金属晶体是由金属原子以金属键连接而成的晶体,其特点是导电性好、变形性高、具有典型的金属性质。
金属晶体的结构通常为紧密堆积,具有良好的韧性和延展性,是制造工程材料、电子材料和建筑材料的重要基础。
典型的金属晶体包括铁(Fe)、铜(Cu)和铝(Al)等。
4.分子晶体分子晶体是由分子之间的范德华力或氢键连接而成的晶体,其特点是化学性质多变,易溶于溶剂。
分子晶体的结构通常不规则,具有良好的可溶性和透明性,是重要的有机功能材料和药物。
典型的分子晶体包括碘化银(AgI)、萘(C10H8)和苯酚(C6H5OH)等。
5.非晶态材料非晶态材料是指由无序排列的原子或者分子构成的非晶体,其特点是没有明显的长程有序结构,通常具有非晶态固体的性质,如良好的可塑性和韧性。
非晶态材料的结构通常为玻璃状或胶状,常用作包装材料、光学材料和电子材料。
典型的非晶态材料包括玻璃、橡胶和塑料等。
总之,晶体的类型多种多样,每种类型的晶体都具有其独特的结构和性质。
通过研究不同类型的晶体,可以更好地理解晶体的结构和形成机制,为材料科学和工程技术的发展提供重要的理论和实践基础。
1、晶体类型判别:分子晶体:大部分有机物、几乎所有酸、大多数非金属单质、所有非金属氢化物、部分非金属氧化物。
原子晶体:仅有几种,晶体硼、晶体硅、晶体锗、金刚石、金刚砂(SiC)、氮化硅(Si3N4)、氮化硼(BN)、二氧化硅(SiO2)、氧化铝(Al2O3)、石英等;金属晶体:金属单质、合金;离子晶体:含离子键的物质,多数碱、大部分盐、多数金属氧化物;2、不同晶体的熔沸点由不同因素决定:离子晶体的熔沸点主要由离子半径和离子所带电荷数(离子键强弱)决定,分子晶体的熔沸点主要由相对分子质量的大小决定,原子晶体的熔沸点主要由晶体中共价键的强弱决定,且共价键越强,熔点越高。
3晶体熔沸点高低的判断?(1)不同类型晶体的熔沸点:原子晶体>离子晶体>分子晶体;金属晶体(除少数外)>分子晶体;金属晶体熔沸点有的很高,如钨,有的很低,如汞(常温下是液体)。
(2)同类型晶体的熔沸点:①原子晶体:结构相似,半径越小,键长越短,键能越大,熔沸点越高。
如金刚石>氮化硅>晶体硅。
②分子晶体:组成和结构相似的分子,相对分子质量越大,分子间作用力越强,晶体熔沸点越高。
如CI4>CBr4>CCl4>CF4。
若相对分子质量相同,如互为同分异构体,一般支链数越多,熔沸点越低,特殊情况下分子越对称,则熔沸点越高。
若分子间有氢键,则分子间作用力比结构相似的同类晶体强,故熔沸点特别高。
③ 金属晶体:所带电荷数越大,原子半径越小,则金属键越强,熔沸点越高。
如Al >Mg >Na >K 。
④ 离子晶体:离子所带电荷越多,半径越小,离子键越强,熔沸点越高。
如KF >KCl >KBr >KI 。
1.60C 与现代足球(如图6-1)有很相似的结构,它与石墨互为 ( ) A .同位素 B .同素异形体 C .同分异构体 D .同系物2.下列物质为固态时,必定是分子晶体的是 ( )A .酸性氧化物B .非金属单质C .碱性氧化物D .含氧酸 3.金属的下列性质中,不能用金属晶体结构加以解释的是 ( ) A .易导电 B .易导热 C .有延展性 D .易锈蚀4.氮化硅(43N Si )是一种新型的耐高温耐磨材料,在工业上有广泛的用途,它属于 ( ) A .原子晶体 B .分子晶体 C .金属晶体 D .离子晶体5.水的状态除了气、液和固态外,还有玻璃态。
晶体结构与晶体的性质晶体是由具有周期性、有序排列的原子、离子或分子构成的固体物质。
晶体结构与晶体的性质密切相关,本文将探讨晶体结构对晶体性质的影响。
一、晶体结构的分类晶体结构可以分为离子晶体结构、共价晶体结构和金属晶体结构三种类型。
1. 离子晶体结构离子晶体结构是由正负离子相互排列而成。
离子晶体结构的特点是阵列有序、结构稳定、点阵规则,并且具有高熔点和脆性。
典型的离子晶体有氯化钠(NaCl)、氧化镁(MgO)等。
2. 共价晶体结构共价晶体结构是由共价键相连的原子构成。
共价晶体结构的特点是强度高、硬度大、熔点高,且导电性能差。
经典的共价晶体有金刚石、硅等。
3. 金属晶体结构金属晶体结构是由金属离子组成。
它具有电子云海模型,金属结构中电子自由流动,因此具有良好的导电性和导热性。
典型的金属晶体有铜、铁等。
二、晶体结构对晶体性质的影响晶体结构对晶体的物理、化学性质产生重要影响。
1. 物理性质晶体的物理性质与其晶体结构紧密相关。
晶体结构的不同决定着晶体的硬度、电导率、光学性质等。
以硬度为例,离子晶体结构由于离子之间的强烈静电吸引力,使得晶体的结构相对稳定,因而具有较高的硬度。
金属晶体结构中由于存在金属键,金属之间的层状排列可以很容易滑动,故金属具有较低的硬度。
而共价晶体结构由于共用电子对,原子之间更加紧密结合,具有更高的硬度。
另外,晶体的电导率与晶体结构也有关。
金属晶体由于自由电子的存在,具有良好的导电性。
而离子晶体和共价晶体由于存在离子或共价键的束缚,电子不易流动,因此具有较差的导电性。
2. 化学性质晶体结构也会影响晶体的化学性质。
晶体结构中原子、离子或分子之间的距离和排列方式决定了晶体的化学反应活性。
以溶解性为例,离子晶体结构中离子间的静电吸引力较大,导致离子结构比较稳定,难于溶解。
而共价晶体结构中,原子之间的共价键相对较强,其溶解性较差。
金属晶体由于金属之间的自由电子,容易与外界发生化学反应。
此外,晶体结构对晶体的光学性质也有重要影响。
晶体的类型1 结晶结晶是物理化学中有序分子组织,可按单元晶体,网晶体和晶体液以及其他方式进行分类。
它有单质晶体、复合晶体以及晶液等类型,可以是流动固体、固体溶剂和离子溶液等物质。
它们有着不同的结构特征以及相应的物理性质。
2 晶体类型1. 单质晶体:是由单一的原子或离子分子所构成的晶体,如碳酸钙、铝矿、石英、汞灰石和四方水晶等,它们的晶体结构比较简单,由能够形成分子簇小结构的原子组成。
2. 复合晶体:是由离子或分子组成的晶体,其中离子和分子之间形成规则的晶体排列,例如有机晶体、块状晶体、点阵晶体等。
3. 晶液:晶液是固态物质的液态形式,由有序排列的磁性晶体矿物构成,具有晶体的特性,但又有液体的灵活性。
3 区别1. 构造的不同:单质晶体由原子或分子组成,而复合晶体由离子和分子组成;晶液是晶体的液态形式,由有序磁晶矿物组成,类似于固体状态。
2. 物理性质的不同:对比单质晶体和复合晶体,单质晶体的熔点通常比复合晶体低。
晶液比其他结晶形式的物质更具流动性,可以把其他物质溶解起来。
3. 热稳定性的不同:单质晶体更稳定,而复合晶体和晶液则容易受到热量的影响。
因此,在高温下,中性物质可以转变为其他形式,而单质晶体仍可以保持稳定。
4 应用结晶具有重要的科学意义和工业应用,这些晶格结构及其物理性质将决定所研究物质的关键应用性能。
工业界常常使用晶体材料以改善以下性能:结晶的组成可以影响到化学和物理性能,如导电率、密度、硬度、结晶时间、折射率等;晶体形状也受调控,如上下抛物面、圆锥、柱体、棱柱和球形等;某些晶体的表面也可以实现光的控制,这对于制备太阳能电池、冷光灯和电子显示屏有重大意义。
因此,结晶是各种科学研究以及工业应用中必不可少的一环,对于对结晶了解、掌握和利用很有必要。
晶体的类型与性质知识规律总结晶体类型离子晶体分子晶体原子晶体金属晶体定义离子间通过离子键相结合而成的晶体分子间以分子间作用力相结合的晶体相邻原子间以共价键相结合而形成的空间网状结构的晶体金属阳离子和自由电子之间的较强作用形成的单质晶体构成粒子阴、阳离子分子原子金属离子、自由电子粒子间作用力离子间肯定有离子键,可能有原子间的共价键分子间:分子间作用力。
可能有分子内共价键(稀有气体例外)共价键金属离子和自由电子之间较强的相互作用代表物NaCl,NaOH,MgSO4干冰,I2,P4,H2O 金刚石,SiC,晶体硅,SiO2镁、铁、金、钠熔、沸点熔点、沸点较高熔点、沸点低熔点、沸点高熔点、沸点差异较大(金属晶体熔沸点一般较高,少部分低)导热性不良不良不良良好导电性固态不导电,熔化或溶于水导电固态和液态不导电,溶于水可能导电不导电。
有的能导电,如晶体硅,但金刚石不导电。
晶体、熔化时都导电硬度硬度较大硬度很小硬度很大硬度差异较大溶解性多数易溶于水等极性溶剂相似相溶难溶解难溶于水(钠、钙等与水反应)决定熔点、沸点高主要因素离子键强弱分子间作用力大小共价键强弱金属键强弱二、几种典型的晶体结构①、NaCl晶体1)在NaCl晶体的每个晶胞中,Na+占据的位置有 2 种。
顶点8个,面心6个2)Cl-占据的位置有 2 种。
棱上12个,体心1个3)在NaCl晶体中,每个Na+周围与之等距离且最近的Na+有 12个;每个Cl-周围与之等距离且最近的Cl-有 12 个。
4)在NaCl晶体中每个Na+同时吸引着6个Cl-,每个Cl-同时也吸引着 6个Na+,向空间延伸,形成NaCl晶体。
5)每个晶胞平均占有 4 个Na+和 4 个Cl-。
1molNaCl能构成这样的晶胞个。
6) Na+与其等距紧邻的6个Cl-围成的空间构型为_____正八面体_________②、CsCl晶体1)每个Cs+同时吸引着8 个Cl-,每个Cl-同时吸引着8 个Cs+;2)在CsCl晶体中,每个Cs+周围与它等距离且最近的Cs+有6个,每个Cl-周围与它等距离且最近的Cl-有 6 个;3)一个CsCl晶胞有 1 个Cs+和 1 个Cl-组成;4)在CsCl晶体中,Cs+与Cl-的个数比为1:1 。
晶体的类型及性质二. 知识重点:1. 复习有关化学键的知识2. 晶体的类型:(1)离子晶体 (2)原子晶体 (3)分子晶体 (4)金属晶体4. 性质与结构的关系:形成晶体的作用力强弱直接影响晶体的物理性质。
5. 常见的几种晶体模型:(NaCl 、CsCl 、干冰、金刚石及2SiO 等)【典型例题】[例1] 下列物质的熔点由高到低排列,正确的是( )A. Cs K Na Li >>>B. CsCl RbCl KCl NaCl >>>C. 2222I Br Cl F >>>D. 金刚石>硅>碳化硅解析:根据晶体类型判断熔沸点高低的规律为:(一般) 原子晶体>离子晶体>分子晶体而同类晶体内熔、沸点高低判断规律是:原子晶体内原子的半径越小,形成共价键的键长短,键能大则键牢固,熔沸点高。
离子晶体内阴、阳离子的半径越小,离子所带电荷越多则形成的离子键越牢固,熔沸点越高。
相同结构的分子形成晶体,相对分子质量越大,分子间作用力越强,熔、沸点越高。
金属晶体的熔沸点高低取决于金属离子的半径和自由电子数,离子半径小,自由电子数多,则熔沸点高。
故应选A 、B 。
答案:A 、B [例2] 下图表示一些晶体中的某些结构,它们分别是NaCl 、CsCl 、干冰、金刚石、石墨结构中的某一种的某一部分。
A B CD E(1)其中代表金刚石的是 (填编号字母,下同),其中每个碳原子最接近且距离相等。
金刚石属于 晶体。
(2)其中代表石墨的是 ,其每个正六边形占有的碳原子数平均为 个。
mol 1石墨中碳原子数与所形成的共价键数之比为 。
(3)其中表示NaCl 的是 ,每个+Na 周围与它最接近且距离相等的+Na 有 个。
(4)代表CsCl 的是 ,它属于 晶体,每个+Cs 与 个-Cl 紧邻。
(5)代表干冰的是 ,它属于 晶体,每个2CO 分子与 个2CO 分子紧邻。
(6)上述五种物质熔点由高到低的排列顺序为: 。
解析:解此题首先要记住几种晶体的基本模型。
金刚石为D ,石墨为E ,干冰为B ,NaCl 为A ,CsCl 为C ,然后根据晶体的组成及空间构型回答后面问题。
值得注意的应为(2)和(3)、(4)、(5)中粒子紧邻的数值关系。
(2)当碳原子通过共用电子对形成六元环时,每一个碳原子被三个环所共用,则形成一个正六边形平均碳原子为:2316=⨯。
同理所成共价键被2个正六边形共同,则形成键数平均为:3216=⨯,二者之比为3:2。
(3)、(4)、(5)中先选择一个原子,寻找等距离且最近的原子。
答案:(1)D ;原子晶体 (2)E ;2;3:2 (3)A ;12(4)C ;离子;8(5)B ;分子;12(6)B C A D E >>>>[例3] 下列化学式表示物质分子的是( )A. 42SO NaB. 2SiOC. 42SO HD. Al解析:在四种晶体中,只有分子晶体才存在真正的分子,所以四个备选答案中只有42:SO H C 才是分子晶体,存在真正的分子。
答案:C[例4] 如图所示晶体结构是一种具有优良的压电、铁电、电光等功能的晶体材料的最小结构单元(晶胞)。
晶体内与每个“Ti ”紧邻的氧原子数和这种晶体材料的化学式分别是(各元素所带电荷均已略去)( )A. 8;128O BaTiB. 8;94O BaTiC. 6;3BaTiOD. 3;32O BaTi△ Ba ○ Ti ● O解析:解此类题要先了解分割法,上图为一个晶胞,它来自一种晶体的一部分,则顶点粒子是切割后只剩81,则Ti 原子个数为:1818=⨯,棱上的粒子是切割后只剩41,则O 原子个数为:34112=⨯,立方体中心(体心)有一个完整的原子,则Ba 原子个数为:1,化学式为:3BaTiO ,由图可见将该晶胞中任一顶点Ti 为中心,补足晶胞,使其由81还原为1,可知有6个O 原子紧邻。
答案:C【模拟试题】一. 选择题:1. 金属的下列性质与自由电子无关的是( )A. 密度大小B. 导电性C. 延展性D. 导热性 2. 下列说法正确的是( )A. NaCl 易溶于水,难溶于汽油B. 4P 具有正四面体结构,所以它是原子晶体C. 分子晶体中分子间作用力越大,其化学性质越稳定D. 离子晶体一般具有较高的熔点和沸点3. 硒有两种同素异形体:灰硒和红硒。
灰硒溶于三氯甲烷,红硒溶于二硫化碳,它们都不溶于水,则灰硒和红硒的晶体是( )A. 原子晶体B. 分子晶体C. 金属晶体D. 以上均有可能4. 共价键、金属键、离子键和分子间作用力都是构成物质的粒子间的不同作用,含有以上所说的两种作用的晶体是( )A. 2SiO 晶体B. 4CCl 晶体C. 2MgCl 晶体D. NaOH 晶体 5. 下列物质按熔点从低到高的顺序排列的是( ) A. F 2、2Cl 、2Br 、2IB. Li 、Na 、K 、RbC. HF 、HCl 、HBr 、HID. Si 、SiC 、2SiO 、NaCl6. 在海洋底部存在大量称为“可燃冰”的物质,其蕴藏量是地球上煤、石油的几百倍,因而是一种等待开发的巨大能源物质。
初步查明可燃冰是甲烷、乙烷等可燃性气体的水合物。
有关可燃冰的下列推测中不正确的是( )A. 高压、低温有助于可燃冰的形成B. 常温、常压下可燃冰是一种稳定的物质C. 可燃冰的微粒间可能存在一种比范德华力更强的相互作用力D. 构成可燃冰的原子间存在极性共价键7. 各晶体中其中任何1个原子都被相邻的4个原子所包围,以共价键形成四面体结构,并向空间伸展形成立体网状结构的是( )A. 甲烷B. 石墨C. 晶体硅D. 水晶 8. 1993年世界10大科技新闻称,中国科学家徐志傅和美国科学家共同合成了世界上最大的碳氢化合物,其中1个分子是由1134个碳原子和1146个氢原子构成。
关于该物质的下列说法中错误的是( )A. 该物质属于烃类B. 常温下呈固态C. 具有类似金刚石的硬度D. 能在空气中燃烧9. 食盐晶体如下图所示。
在晶体中●表示+Na ,○表示-Cl 离子。
已知食盐的密度为3-⋅cm g ρ,NaCl 的摩尔质量为1-⋅mol Mg ,阿伏加德罗常数为N ,则在食盐晶体里+Na 离子和-Cl 离子的核间距大约是( )A.cm N M32ρ B.cm N M32ρ C.cmN N32ρ D.cm N M38ρ10. 下列关系正确的是( )A. 离子半径:++-->>>3Al Na F ClB. 熔点:石英>食盐>冰>干冰C. 结合+H 能力:--->>232324CO SO SOD. 热稳定性:HF HCl S H PH >>>23二. 填空题:11. A 、B 、C 为同周期元素,已知A 元素的原子K 、L 层电子数之和比M 、L 层电子数之和大1,B 元素原子与同周期其他元素的原子相比半径最小,C 元素原子的最外层电子数与核外电子层相同。
(1)写出上述三种元素符号和名称:A : 、B : 、C : 。
(2)B 元素的阴离子的结构示意图为 。
(3)B 元素单质的晶体类型是 ,C 元素的晶体中微粒间较强的相互作用是 ,A 、B 两元素形成的化合物的电子式为 ,其晶体类型为 。
(4)将C 的单质与A 的氧化物的水溶液共热发生反应的离子方程式为 。
(5)在B 与C 形成的化合物的水溶液中,放入少量A 单质的现象为 ,发生反应的离子方程式为 。
12. A 、B 两元素的最外层都只有一个电子。
A 的原子序数等于B 的原子序数的11倍,A 的离子的电子层结构跟周期表中非金属性最强的元素的阴离子的电子层结构相同,元素C 与B 易五形成化合物C B 2,该化合物常温下呈液态。
则:(1)A 的原子结构示意图为 ,在固态时属于 晶体。
(2)C 在固态时属于 晶体。
B 与C 形成化合物C B 2的化学式为 ,电子式为;它是由键形成的分子,在固态时属于晶体。
13. 溴化碘(IBr)是一种卤素互化物,它有很高的化学活性,有许多性质跟卤素单质相似。
它在常温、常压下是深红色固体,熔点41℃,沸点116℃。
固体溴化碘是晶体,含有键。
溴化碘与水反应,生成一种无氧酸和一种含氧酸,反应方程式是。
【试题答案】一.1. A2. AD3. B4. BD5. A6. B7. C8. C9. B提示:NaCl mol 1的体积:mol cm M 3ρ,1个NaCl 晶体的体积:个3cm N M ρ,21个NaCl 晶体的边长:32N Mρ,即等于+Na 与-Cl 的核间距。
注:每一个NaCl 晶体的晶胞含4个NaCl 。
1个NaCl 晶体的体积为晶胞中2个立方体。
10. AB 二. 11.(1)Na 、钠;Cl 、氯;Al 、铝(2)(3)分子晶体;金属键;-∙∙∙∙∙∙∙⨯+][Cl Na ;离子晶体(4)===+-OHAl 22↑+-2232H AlO(5)A 在液面上游动,发出嘶嘶声并有白色沉淀生成;===+++O H Al Na 23626 ++↑+↓Na H OH Al 63)(22312.(1);金属(2)分子;O H 2;H O H ∙⨯∙∙∙∙∙⨯;极性;极性;分子13. 分子;极性;HBr HIO O H IBr +=+2【励志故事】学会感动(接上期)丁大卫的普普通通的话,让我从另一个角度认识了我们的国旗,也让我的眼泪不听话地掉下来。
当崔永元问丁大卫在中国感觉苦不苦时,丁大卫说,很好的,比如这次你们中央台就让我这样一个平凡的人来做嘉宾,而且还让我坐飞机,吃很好的饭菜。
我看见崔永元有些不好意思地脸红了,他幽默地说:"我觉得你挺像我们中国的一个人;雷锋!"丁大卫想了想,说:"还真有点儿像。
"大伙儿"轰"地一声善意地笑开了。
"只是,雷锋挺平常的,他只是一个凭良心做事的人,这样的人不应该只有一个,每个人都应该做得到的!"他认真地补充道。
没有人再笑了,就连崔永元的脸上都显出了小学生的表情。