分子晶体和原子晶体
- 格式:ppt
- 大小:2.01 MB
- 文档页数:5


晶体,一般包括离子晶体、分子晶体、原子晶体、金属晶体四种类型。
一、依据构成晶体的微粒和微粒间的作用判断(1)离子晶体的构成微粒是阴、阳离子,微粒间的作用是离子键。
(2)原子晶体的构成微粒是原子,微粒间的作用是共价键。
(3)分子晶体的构成微粒是分子,微粒间的作用为分子间作用力。
(4)金属晶体的构成微粒是金属阳离子和自由电子,微粒间的作用是金属键。
二、依据物质的分类判断(1)金属氧化物(如K2O、Na2O2等)、强碱(NaOH、KOH等)和绝大多数的盐类是离子晶体。
(2)大多数非金属单质(除金刚石、石墨、晶体硅等)、非金属氢化物、非金属氧化物(除SiO2外)、几乎所有的酸、绝大多数有机物(除有机盐外)是分子晶体。
(3)常见的单质类原子晶体有金刚石、晶体硅、晶体硼等,常见的化合类原子晶体有碳化硅、二氧化硅等。
(4)金属单质是金属晶体。
三、依据晶体的熔点判断。
(1)离子晶体的熔点较高。
(2)原子晶体的熔点很高。
(3)分子晶体的熔点低。
(4)金属晶体多数熔点较高,但有少数熔点相当低。
四、依据导电性判断。
(1)离子晶体溶于水及熔融状态时能导电。
(2)原子晶体一般为非导体。
(3)分子晶体为非导体,而分子晶体中的电解质(主要是酸和强极性非金属氢化物)溶于水,使分子内的化学键断裂形成自由移动的离子,也能导电。
(4)金属晶体是电的良导体。
五、依据硬度和机械性能判断。
(1)离子晶体硬度较大、硬而脆。
(2)原子晶体硬度大。
(3)分子晶体硬度小且较脆。
(4)金属晶体多数硬度大,但也有硬度较小的,且具有延展性。
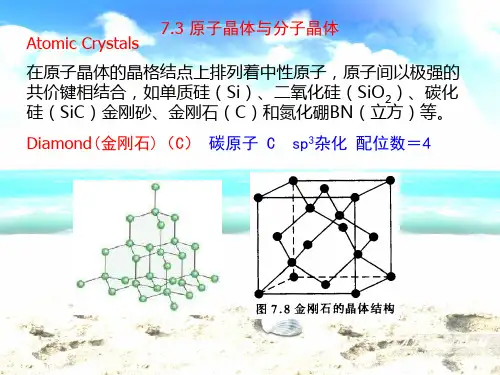

分子晶体和原子晶体
1、分子晶体和原子晶体区别:
(1)单体结构不同。
分子晶体一般是有物质分子构成,而原子晶体一般有单个原子构成;
(2)晶体内作用力不同。
分子晶体一般是通过分子间范德华力作用形成,而原子晶体一般通过原子共价键作用形成;
(3)物理性质不同。
分子晶体一般硬度、熔点较低,而原子晶体一般硬度、熔点很高。
比如白糖属于分子晶体,而钻石属于原子晶体,二者硬度、熔点差别很大;
(4)存在形式有差异。
分子晶体一般有固、液、气三种存在形式,而原子晶体一般只有固体存在形式。
分子晶体典型代表:
1、所有非金属氢化物;
2、大部分非金属单质(稀有气体形成的晶体也属于分子晶体),如:卤素(X2)、氧气、硫(S8)、氮(N2)、白磷(P4)、C60等(金刚石,和单晶硅等是原子晶体);
3、部分非金属氧化物,如:CO2、SO2、SO3、P4O6、P4O10等(如SiO2是原子晶体) ;
4、几乎所有的酸;
5、绝大多数有机化合物,如:苯、乙酸、乙醇、葡萄糖等 ;
6、所有常温下呈气态的物质、常温下呈液态的物质(除汞外)、
易挥发的固态物质。
原子晶体类型:
1、某些金属单质:晶体锗(Ge)等;
2、某些非金属化合物:氮化硼(BN)晶体、碳化硅、二氧化硅等;
3、非金属单质:金刚石、晶体硅、晶体硼等。

第三章第二节分子晶体与原子晶体第一课时分子晶体教学目标1、使学生了解分子晶体的组成粒子、结构模型和结构特点及其性质的一般特点。
2、使学生了解晶体类型与性质的关系。
3、使学生理解分子间作用力和氢键对物质物理性质的影响。
4、知道一些常见的属于分子晶体的物质类别。
5、使学生主动参与科学探究,体验研究过程,激发他们的学习兴趣。
教学重点、难点重点掌握分子晶体的结构特点和性质特点难点是氢键的方向性和氢键对物体物理性质的影响从三维空间结构认识晶胞的组成、结构教学方法建议:运用模型和类比方法诱导、分析、归纳教学过程:[引入]我们已经知道,固体有晶体和非晶体之分,绝大多数常见的固体是晶体。
现在给出下列晶体的熔点:甲烷(-182.5℃)氮(-210.1℃)金刚石(3900℃)氧化铝(2030℃),氯化钠(801℃)同为晶体,为什么它们的熔点及其性质有如此大的差异呢?物质结构决定物质性质,我们需要探讨晶体的内部结构来回答这个问题。
分类研究是科学研究的基本方法之一,根据晶体结构的不同,我们把年个吨毫2分为若干类型,其中,只含分子的晶体称为分子晶体。
一、分子晶体1、定义:含分子的晶体称为分子晶体也就是说:分子间以分子间作用力相结合的晶体叫做分子晶体分子,就属于分子晶体问:还有哪些属于分子晶看图,如:碘晶体中只含有I2体?2、较典型的分子晶体有非金属氢化物,部分非金属单质,部分非金属氧化物,几乎所有的酸,绝大多数有机物的晶体。
3、分子间作用力和氢键过度:首先让我们回忆一下分子间作用力的有关知识阅读必修2 科学视野教师诱导:分子间存在着一种把分子聚集在一起的作用力叫做分子间作用力,也叫范徳华力。
分子间作用力对物质的性质有怎么样的影响?学生回答:一般来说,对于组成和结构相似的物质,相对分子量量越大分子间作用力越大,物质的熔、沸点也越高。
教师诱导:但是有些氢化物的熔点和沸点的递变却与此不完全符合,如:NH3、H2 O和HF的沸点就出现反常。




HXC60P106, P1010都形成分子晶体,只有很少的一部分和______SiO2,碳化硅,第二节分子晶体和原子晶体一、分子晶体(一)、概念:分子间以______________________ (_____________ , ________________ )相结合的晶体叫分子晶体。
注意:(1)构成分子晶体的粒子是 ______________________ 。
(2 )在分子晶体中,分子内的原子间以结合,而相邻分子靠或相互吸引。
(3 )范德华力化学键的作用:(4 )分子晶体熔化破坏的是O(二)•分子晶体的物理特性:(1)___ 的熔点和沸点,(2) ______________ 的硬度,________ 挥发, _________ 升华(3)—般都是________ 体,固体和熔融状态都__________________ 导电。
(4)分子晶体的溶解性与溶质和溶剂的分子的___________________ 相关一一____________________思考:1、为什么分子晶体熔沸点低、易挥发、易升华、硬度小?原因:分子晶体发生这些变化时_只破坏 __________________________ , ________________ 很弱,克服它时需要的能量小。
所以分子晶体熔沸点低、易挥发、易升华、硬度小。
2、为什么分子晶体在晶体和熔融状态均不导电?它们在晶体和熔融状态均不存在_______________________ 。
部分分子晶体溶于水在水分子作用下发生_____________ 导电,如HCI, H2S04 ;有些溶于水与水反应生成_______________________________ 而导电,晶体硼等。
)(四)分子晶体结构特征1. ______________________________ __ 分子密堆积每个分子周围有______________ 个紧邻的分子,如:C60、干冰、12、02——不具有分子密堆积特征P1,CH4,2,冰中1个水分lmol冰周I韦]有mol氢键。