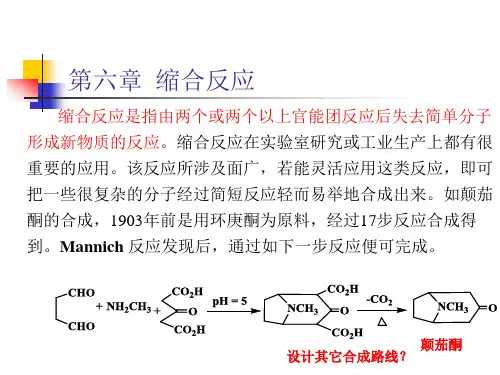
第六节_α_β-_不饱和醛、酮.
- 格式:ppt
- 大小:1.67 MB
- 文档页数:58




![[理学]第六章 羰基化合物的反应](https://uimg.taocdn.com/f28edb13f111f18583d05a59.webp)



第十一章醛和酮第一节醛、酮的分类和命名一、分类二、命名1.醛、酮的系统命名以包含羰基的最长碳链为主链,看作母体。
从靠近羰基的一端开始,依次标明碳原子的位次。
在醛分子中,醛基总是处于第一位,命名时可不加以标明。
酮分子中羰基的位次(除丙酮、丁酮外)必须标明,因为它有位置异构体。
醛、酮碳原子的位次,除用1,2,3,4,…表示外,有时也用α,β,γ…希腊字母表示。
α是指官能团羰基旁第一个位置,β是指第二个位置…。
酮中一边用α,β,γ…,另一边用α’ β’ γ’…。
ⅰ含醛基、酮基的碳链上的氢被芳环或环烷基取代,就把芳环或环烷基当作主链上的取代基看待:ⅱ醛基与芳环、脂环或杂环上的碳原子直接相连时,它们的命名可在相应的环系名称之后加-“醛”字。
ⅲ当芳环上不但连有醛基,而且连有其它优先主官能团时,则醛基可视作取代基,用甲酰基做词头来命名。
2. 酮还有另一种命名法根据羰基所连的两个烃基名来命名,把较简单的烃基名称放在前面,较复杂的烃基名称放在后面,最后加“酮”字。
后面是母体如含有两个以上羰基的化合物,可用二醛、二酮等,醛作取代基时,可用词头“甲酰基”或“氧代”表示;酮作取代时,用词头“氧代”表示。
英文羰基做取代基时用“oxo”(氧代)表示不饱和醛、酮的命名是从靠近羰基一端给主链编号。
第二节醛、酮的物理性质和光谱性质一、物理性质除甲醛是气体外,十二个碳原子以下的醛、酮都是液体,高级的醛、酮是固体。
低级醛常带有刺鼻的气味,中级醛则有花果香,所以C8~C13的醛常用于香料工业。
低级酮有清爽味,中级酮也有香味。
羰基中,碳和氧以双键相结合,碳原子用三个sp2杂化轨道形成三个σ键,其中一个是和氧形成一个σ键,这三个键在同一个平面上。
碳原子剩下来的一个p轨道和氧的一个p轨道与这三个σ键所形成的平面垂直,彼此重叠形成一个π键由于氧的电负性吸引电子的能力很强,所以羰基是一个极性基团,具有一个偶极矩,负极向氧一面,正极朝向碳的一面。
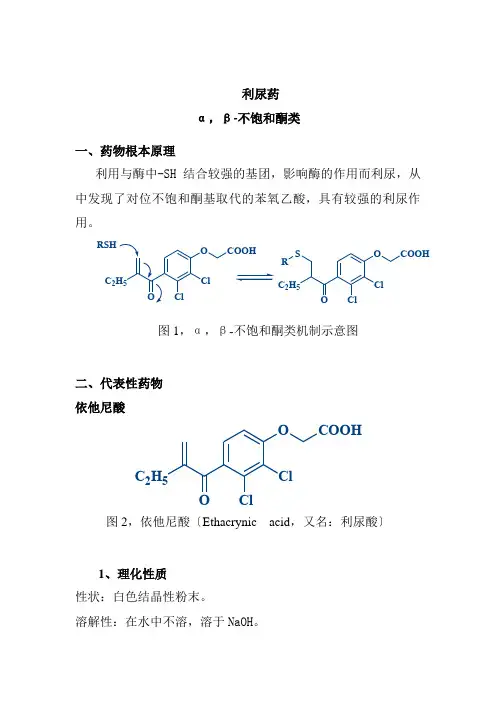
利尿药α,β-不饱和酮类一、药物根本原理利用与酶中-SH 结合较强的基团,影响酶的作用而利尿,从中发现了对位不饱和酮基取代的苯氧乙酸,具有较强的利尿作用。
COOH C 2RSH O COOH Cl Cl C 2H 5S R图1,α,β-不饱和酮类机制示意图二、代表性药物依他尼酸OCOOH Cl Cl C 2H 5O图2,依他尼酸〔Ethacrynic acid ,又名:利尿酸〕1、理化性质性状:白色结晶性粉末。
溶解性:在水中不溶,溶于NaOH 。
稳定性:α、β—不饱和酮的结构,在水溶液中不稳定,尤其在碱性溶液中易分解。
2、作用利尿作用强而迅速——强效利尿药,需同服氯化钾。
3、用途临床上用于充血性心力衰竭,急性肺水肿、肾性水肿等。
肾功能衰竭者慎用。
4、区别反响溶于H2SO4→→黄色H2O→→乳白色,冷高锰酸钾→→退色加NaOH煮沸→→→甲醛浓H2SO4酸化变色酸→→深蓝色三、药理作用1、对水、电解质排泄的影响〔1〕利尿作用,尿钠、钾、氯、磷和镁等离子排泄增加,而对尿钙排泄减少。
本类药物作用机制主要抑制远端小管前段和近端小管〔作用较轻〕对氯化钠的重吸收,从而增加远端小管和集合管的Na-K交换,K分泌增多。
其作用机制尚未完全明了。
本类药物都能不同程度地抑制碳酸酐酶活性,故能解释其对近端小管的作用。
本类药还能抑制磷酸二酯酶活性,减少肾小管对脂肪酸的摄取和线粒体氧耗,从而抑制肾小管对Na、Cl-的主动重吸收。
〔2〕降压作用。
除利尿排钠作用外,可能还有肾外作用机制参与降压,可能是增加胃肠道对Na的排泄。
2、对肾血流动力学和肾小球滤过功能的影响由于肾小管对水、Na重吸收减少,肾小管内压力升高,以及流经远曲小管的水和Na增多,刺激致密斑通过管-球反射,使肾内肾素、血管紧张素分泌增加,引起肾血管收缩,肾血流量下降,肾小球入球和出球小动脉收缩,肾小球滤过率也下降。
肾血流量和肾小球滤过率下降,以及对亨氏袢无作用,是本类药物利尿作用远不如袢利尿药的主要原因。
固相合成α,β-不饱和酮实验目的1.学会用固相合成法α,β-不饱和酮2.会用WC - 1 型显微熔点测定仪测定熔点3.会用Br uk er Dp x - 400型核磁共振仪测定核磁共振谱4.会用FT / I R - 8101 红外光谱仪测定红外光谱实验原理有机化学反应一般都在溶剂中进行, 因为它们能很好地溶解有机物, 保证物料混合均匀和能量交换稳定, 有利于分子间的相互碰撞, 提高反应产率. 但有机溶剂的毒性和难以回收又成为环境污染的主要因素. 面对传统的合成方法受到的严重挑战, 化学家和化工界已把注意力集中到从本源上杜绝废弃物的产生, 致力于合成手段的战略革新, 于是绿色合成应运而生. 固相有机合成是绿色合成的重要组成部分,因为它不使用溶剂, 并且无论在反应速度、产物收率, 还是选择性方面, 均较溶液中的反应有显著优势. 由于这种反应操作简单, 加热、研磨、振荡及超声波辐射都可以加速反应, 并且避免了因使用溶剂而造成的能耗高、污染环境、毒害性和爆燃性等缺陷, 是理想的合成方法.K noeven a g el 缩合反应是形成碳碳键的有效方法, 一般在液相条件下进行. 近年来固相K no even a g el 反应也陆续有报道. 本实验是在无溶剂的条件下芳香醛与2, 3 - 二氢- 1 - 茚酮或3, 4 - 二氢- 1( 2H ) - 萘酮在固态N aO H 催化下室温研磨反应, 方便地得到缩合产物α,β- 不饱和酮( 2 - 芳亚甲基- 2, 3 -二氢- 1 - 茚酮和2 - 芳亚甲基- 3, 4 - 二氢- 1( 2H ) - 萘酮) .On +A r C H ON a O HG r i n d i n g r.t.OnC H A r1 2 3仪器与试剂玛瑙研钵; 熔点采用WC - 1 型显微熔点测定仪测定( 温度未校正) ; 核磁共振谱采用Br uk er Dp x - 400型核磁共振仪测定, 溶剂( DM S O - d 6 ) , T M S 为内标; 红外光谱用FT / I R - 8101 红外光谱仪测定( K Br 压片) ; 芳香醛、3, 4 - 二氢- 1( 2 H ) - 萘酮和2, 3 - 二氢- 1 - 茚酮为分析纯.实验步骤称取2, 3 - 二氢- 1 - 茚酮( 3, 4 - 二氢- 1 ( 2H ) - 萘酮) ( 1) 2 mmo l、芳香醛( 2) 2 mmo1 于玛瑙研钵中, 并加入4 m mol 的N aO H , 室温研磨, 反应体系颜色逐渐加深. 研磨3~ 5 min 后, 反应完成. 用水洗涤以除去其中的N aOH . 用95% 乙醇重结晶即得到纯净的产物. 反应结果见表1 .结果与讨论表 1 给出了2, 3 - 二氢- 1 - 茚酮( 3, 4 - 二氢- 1( 2H ) - 萘酮) 与芳香醛在室温固相氢氧化钠作用下的反应时间、产率.2 - ( 4 - 甲氧基苯亚甲基) - 2,3 - 二氢- 1 - 茚酮( 3 a) mp: 134 ~ 135 . I R : 3 082, 2 944, 2 841, 1 692,16 24, 1 516 , 1 424, 1 31 3, 1 252, 1 18 4, 1 123, 1 099,1 0 24, 9 57, 9 25, 823, 787, 735, 674, 558, 541 , 525c m- 1.1H N M R : 3 85( 3H , s, O CH 3 ) , 4 11 ( 2H , s,CH 2 ) ,7 07 ~ 7 09 ( 2 H , m, A r H ) , 7 4 6 ~ 7 81( 7H , m, A r H , C H ) . C17H 14 O 2 , 计算值( % )C,81 5 8; H , 5 64. 实测值( % ) : C, 81 20; H , 5 8 4.2 - 苯亚甲基- 2,3 - 二氢- 1 - 茚酮( 3 b) mp : 101 ~ 10 2. I R : 3 062, 2 94 1, 2 843 , 1 6 60, 1 58 9, 1 491,1 4 59, 1 434, 1 3 18, 1 29 6, 1 183 , 1 140 , 1 022, 954,927, 883, 796, 756, 741, 696, 653 , 564 , 538 , 519c m- 1.1H N M R : 4 11 ( 2H , s, CH 2 ) , 7 30 ~ 7 44( 5H , m , A r H ) , 7 50 ~ 7 62( 2 H , m, A r H ) , 7 70~ 7 8 2( 3 H , m, A r H , C H ) . C16 H 12 O , 计算值( % ) :C, 87 2 5; H ,5 49. 实测值( % ) : C, 87 88; H , 5 2 9.2 - ( 4 - 溴苯亚甲基) - 2 ,3 - 二氢- 1 - 茚酮( 3c) mp: 178~ 179 . I R : 3 0 45, 2 930 , 2 850, 1 6 94, 1 62 2,14 86, 1 465 , 1 326, 1 2 73, 1 18 0, 1 152 , 1 0 72, 9 54, 9 15, 8 20, 7 86, 7 37, 67 1,64 9, 55 8, 51 3 cm- 1.1H N M R: 4 12( 2H, s, CH2 ) , 7 47~ 7 52( 2H, m, A r H ) , 7 67~ 7 80( 7H , m, A r H , C H ) . C16 H11 Br O , 计算值( % ) : C, 64 24; H , 3 71. 实测值( % ) : C, 64 00 ; H , 3 91.2 - ( 2 - 氯苯亚甲基) - 2,3 - 二氢- 1 - 茚酮( 3 d) mp: 149~ 150 . I R : 3 063, 2 941 , 2 840, 1 6 98, 1 623,1 5 86, 1 465 , 1 434, 1 416, 1 328 , 1 2 95, 1 273 , 1 1 85, 1 133 , 1 0 87, 1 03 7, 959, 917 , 8 93, 738 , 7 00, 669,571, 560 c m- 1.1H N M R :4 11 ( 2H , s , CH2 ) , 7 45 ~ 7 52 ( 3H , m , A r H ) , 7 60 ~ 7 62 ( 1 H , m,A r H ) , 7 65~ 7 96 ( 5H , m, A r H , C H ) . C1 6 H 11 ClO , 计算值( % ) : C, 75 4 5; H , 4 35. 实测值( % ) : C,75 2 5; H , 445.2 - ( 4 - 氯苯亚甲基) - 2 ,3 - 二氢- 1 - 茚酮( 3e) mp: 173~ 174 . I R : 3 0 32, 2 940 , 2 850, 1 69 6, 1 624,15 62, 1 490 , 1 467, 1 418, 1 327 , 1 2 96, 1 205 , 1 1 82, 1 152 , 1 1 23, 1 09 3, 954, 929 , 9 17, 821 , 7 29, 698,670,6 58, 5 13 c m- 1.1H N M R : 4 11( 2H , s , CH 2 ) ,7 47~ 7 57 ( 4H , m, A r H ) , 7 6 6~ 7 82( 5 H , m,A r H , C H ) . C16 H 11 ClO, 计算值( % ) : C, 75 45; H , 4 3 5. 实测值( % ) : C, 75 6 5; H , 4 15.2 - ( 4 - 甲基苯亚甲基) - 2,3 - 二氢- 1 - 茚酮( 3f ) mp : 132 ~ 134 . I R : 3 060 , 2 9 14, 2 85 9, 1 688,16 23, 1 581 , 1 511, 1 463, 1 4 12, 1 32 8, 1 296 , 1 270 , 1 209, 1 183, 1 1 53, 1 0 97, 1 03 6, 954, 92 9, 817,789,7 38, 674, 557, 522 c m- 1.1H N M R : 2 3 7 ( 3H , s, CH3 ) ,4 1 0 ( 2H , s, CH 2 ) , 7 45 ~ 7 53( 3H , m , A r H ) , 7 60 ~ 7 81 ( 6H , m, A r H ,C H ) . C17 H 14 O, 计算值( % ) : C, 87 15; H , 6 02. 实测值( % ) : C, 87 05; H , 621.2 - ( 3, 4 - 二甲氧基苯亚甲基) - 2 ,3 - 二氢- 1 - 茚酮( 3g ) m p: 17 0 ~ 171 . I R , 3 05 0, 2 9 59, 2 837,1 6 84, 1 618 , 1 512, 14 43, 1 421, 1 32 5, 1 295, 1 20 3, 1 184, 1 1 42, 1 02 1, 980, 940 , 9 22, 849 , 7 87, 738,67 5, 616, 591, 550 c m-1.1HN M R : 3 84 ( 3H , s, OCH3 ) , 3 87 ( 3H , s, OCH3 , 4 13( 2H , s, CH2 ) ,7 09( 1H , d , J = 8H 2 , A r H ) , 7 37 ~ 7 4 0( 2H , m, A r H ) , 7 46 ~ 75 3( 2H , m, A r H ) , 7 68 ~ 7 78 ( 3H ,m, A r H , C H ) . C18 H 16 O 3 , 计算值( % ) : C, 77 12; H , 5 75 . 实测值( % ) : C, 77 32 ; H , 5 55.2 - ( 4 - 甲基苯亚甲基) - 3, 4 - 二氢- 1 ( 2H ) -萘酮( 3h ) mp : 1 20~ 12 1 . I R :3 060 ( b ) , 2 9 58, 2 843,2 3 60, 2 341 , 1 586, 1 5 08, 14 55, 1 31 7, 1 29 7, 1 249 , 1 136, 9 48, 816 , 7 89, 740 ,5 22 cm- 1.1H N M R :2 36( 3H , s , CH 3 ) , 2 93( 2H , t , J = 8 0 H z, C3H ) ,3 09 ( 2H ,t , J = 8 0 H z, C4H ) , 7 28 ( 2H , d, J =8 0 H z, A r H ) , 7 3 7 ~ 7 45 ( 4H , m, A r H ) , 7 5 6 ~ 7 60 ( 1H , m, A r H ) , 7 70 ( 1H , s, C H ) , 7 96( 1H , d , J = 80 H z, A r H ) . C18 H 16 O, 计算值( % ) : C, 87 06; H , 6 4 9. 实测值( % ) : C, 87 1 3;H , 6 55.2 - ( 4 - 甲氧基苯亚甲基) - 3, 4 - 二氢- 1 ( 2H ) - 萘酮( 3i) mp : 108 ~ 1 09 . I R :3 0 75, 3 0 27, 2 996,622 9 46, 2 836, 1 66 6, 1 6 01, 1 508, 1 45 4, 14 39, 1 300, 1 22 3, 1 1 77, 1 033 , 95 0, 8 41, 744, 532c m- 1.1H N M R : 2 91 ( 2H , t, J =6 0 H z, C3H ) , 3 05 ( 2H , t , J = 6 0 H z, C4H ) , 3 8 ( 3H , s,OCH 3 ) ,7 3 0( 2H , d, J =8 0 H z, A r H ) , 7 37 ~ 7 41 ( 4H , m, A r H ) , 7 5 1 ~ 7 6 0 ( 1H , m, A r H ) , 7 70( 1H , s , C H ) , 7 98 ( 1H , d, J = 8 0 H z, A r H ) . C18 H 16 O2 , 计算值( % ) : C, 81 7 9; H , 6 1 0. 实测值( % ) : C, 81 88; H , 6 04.2 - ( 4 - 氯苯亚甲基) -3 ,4 - 二氢- 1( 2H ) - 萘酮( 3 j ) mp : 1 34~ 135 . I R : 3 075, 3 036 , 2 9 46, 2 361,1 6 68, 1 600 , 1 561 , 1 489, 1 456, 1 3 17, 1 2 23, 1 09 4, 1 01 2, 948, 84 0, 743,7 05, 520 cm- 1.1H N M R :2 92 ( 2H , t , J = 6 0 H z , C3H ) , 3 05( 2H , t, J = 60 H z , C4H ) , 7 36 ~ 7 43 ( 2H , m, A r H ) , 7 5 0~7 60( 5H , m , A r H ) , 7 69( 1H , s , C H ) ,7 96( 1 H , d, J = 8 0 H z, A r H ) . C17 H 13 ClO , 计算值( % ) : C,75 9 8; H , 4 88. 实测值( % ) : C, 75 92; H , 4 9 5.2 - ( 4 - 溴苯亚甲基) -3 ,4 - 二氢- 1( 2 H ) - 萘酮( 3 k) mp : 150 ~ 15 1 . I R : 3 05 2,3 03 0, 2 9 45, 2 360,2 3 41, 1 66 7, 1 59 3, 1 558 , 1 485 , 1 455, 1 317, 1 297, 1 2 23, 1 0 71, 9 47,8 38, 5 18 c m- 1.1H N M R : 2 95( 2H , t , J = 6 0 H z , C3H ) , 3 0 7( 2H , t, J = 6 0H z, C4H ) , 7 3 8~ 7 44 ( 2H , m, A r H ) , 7 49 ( 2H , d,J = 8 0 H z, A r H ) , 7 5 7~ 7 66( 3H , m, A r H ) , 7 68 ( 1H , s, C H ) , 7 97 ( 1H , d, J = 8 0 H z, A r H ) .C17 H1 3 Br O, 计算值( % ) : C, 65 19; H , 4 1 8. 实测值( % ) : C, 65 1 2; H , 4 09.2 - ( 2 - 氯苯亚甲基) -3 ,4 - 二氢- 1( 2H ) - 萘酮( 3 l) mp : 1 04~ 105 . I R : 3 062, 2 948 , 2 8 90, 2 840,2 3 60, 2 341 , 1 665 , 1 591, 1 560, 1 4 53, 1 2 94, 1 24 8, 1 22 0, 954, 80 4, 738, 7 12, 687 cm- 1.1H N M R :2 90 ( 2H , t , J = 8 0 H z, C3H ) , 3 07 ( 2H , t , J = 8 0 H z, C4H ) , 7 32 ( 2H , m, A r H ) , 7 38 ~ 7 43( 4H , m , A r H ) , 7 50 ~ 7 5 9( 1H , m, A r H ) , 7 7 1( 1H , s, C H ) , 7 95 ( 1H , m , A r H ) . C17 H 13 ClO , 计算值( % ) : C, 7 5 98 ; H , 4 8 8. 实验( % ) : C, 75 89; H , 4 79 .2 - ( 2, 4 - 二氯苯亚甲基) - 3, 4 - 二氢- 1 ( 2H ) - 萘酮( 3 m) mp : 99 ~ 10 0 . I R : 3 07 2, 3 024, 2956,2 3 61, 2 342 , 1 66 3, 1 60 5, 1 46 9, 1 3 81, 1 3 14, 1 245, 1 134, 1 052 , 952, 840, 740, 705, 563 cm- 1.1H N M R : 2 93 ( 2H , t , J = 8 0 H z, C3H ) , 3 08 ( 2H , t , J = 8 0 H z, C4H ) , 7 31 ~ 7 45 ( 3H , m, A r H ) ,7 51 ( 1H , d , J = 8 0 H z, A r H ) , 7 60~ 7 70 ( 2H , m , A r H ) , 7 73( 1H , s , C H ) , 7 97 ( 1 H , m, A r H ) .C17 H1 2 Cl2 O , 计算值( % ) : C, 67 35 ; H , 3 99. 实测值( % ) : C, 67 29; H , 4 0 1.2 - ( 3, 4 - 二氯苯亚甲基) -3 ,4 - 二氢- 1 ( 2H ) - 萘酮( 3 n) m p: 148 ~ 149 . I R : 3 0 69, 3 03 0, 2 942,2 8 85, 2 3 60, 2 34 2, 1 668, 1 59 1, 1 547, 1 4 70, 1 315 , 1 297, 1 2 48, 1 22 3, 1 128 , 832 , 743 , 577c m- 1.1H N M R : 2 95( 2H , t , J =6 0 H z, C3H ) , 3 05 ( 2 H , t , J = 6 0 H z, C4H ) ,7 38 ~ 7 44 ( 2H ,m, A r H ) , 7 5 2( 1H , d, J = 8 0 H z , A r H ) , 7 56 ~ 7 7 2( 3 H , m, A r H ) , 7 8 0( 1H , s , C H ) , 7 96 ( 1H ,d, J = 8 0 H z , A r H ) . C17 H12 Cl2 O , 计算值( % ) : C, 6 7 35 ; H , 3 99. 实测值( % ) : C, 67 29; H , 3 92 .结果表明: 2, 3 - 二氢- 1 - 茚酮( 3 , 4 - 二氢- 1( 2 H ) - 萘酮) 与芳香醛固相反应生成α,β-不饱和酮, 反应在较短的时间( 3~ 5 min) 内即可完成并获得较高的产率. 可能是在固相有机反应中, 由于没有溶剂分子的介入, 反应体系的微环境不同于溶液中的, 造成了反应部位的局部高浓度, 提高了反应速率. 氢氧化钠的用量对该反应也有一定的影响. 研究表明, 氢氧化钠用量小于反应中的用量时, 难以获得满意的目的产物. 由于固相反应无需使用有机溶剂, 既节约了原料, 又避免了环境污染, 而且后处理较液相反应简单得多, 为合成该类化合物提供了一种方便、有效、环境友好的方法.。
合成α,β-不饱和缩酮(醛)的研究
沈巍巍;阳年发;杨利文;王攀登;李继超
【期刊名称】《化学试剂》
【年(卷),期】2007(29)5
【摘要】以对甲苯磺酸为催化剂,通过苄叉丙酮与-1,2-丙二醇反应合成了苄叉丙酮-1,2-丙二醇缩酮。
较系统的研究了反应溶剂、酮醇物质的量比、催化剂用量等诸因素对产品收率的影响,在n(酮)∶n(醇)=1∶3,催化剂用量为6.5 g/mol(酮),甲苯为带水剂的条件下反应一段时间,再额外加入催化量对甲苯磺酸与少量醇,继续反应,产品收率达到98%。
此条件对于其他的α,β-不饱和酮(醛)缩合反应亦适宜。
【总页数】3页(P305-306)
【关键词】α,β-不饱和酮(醛);缩醛;缩酮;对甲苯磺酸
【作者】沈巍巍;阳年发;杨利文;王攀登;李继超
【作者单位】湘潭大学化学学院
【正文语种】中文
【中图分类】O623.54
【相关文献】
1.FeCl3-漆酚树脂催化合成酯、缩醛和缩酮的研究 [J], 但悠梦;李佳凤;米远祝;段正超
2.生物质基甘油缩醛和缩酮的合成研究进展 [J], 肖泽; 常春; 白净; 陈俊英; 李攀; 韩秀丽
3.以四氢呋喃为醛基砌块合成(E)-α-羟乙基-α,β-不饱和醛 [J], 濮伟雯;史永森;刘建峰;柯德宏;吴孝兰;许胜
4.用于合成不饱和醛和/或不饱和羧酸的催化剂 [J],
5.不饱和醛和不饱和羧酸合成用催化剂、其制备方法和使用该催化剂的不饱和醛和不饱和羧酸的合成方法 [J],
因版权原因,仅展示原文概要,查看原文内容请购买。