高中化学 第三章 第三节
- 格式:ppt
- 大小:3.23 MB
- 文档页数:25




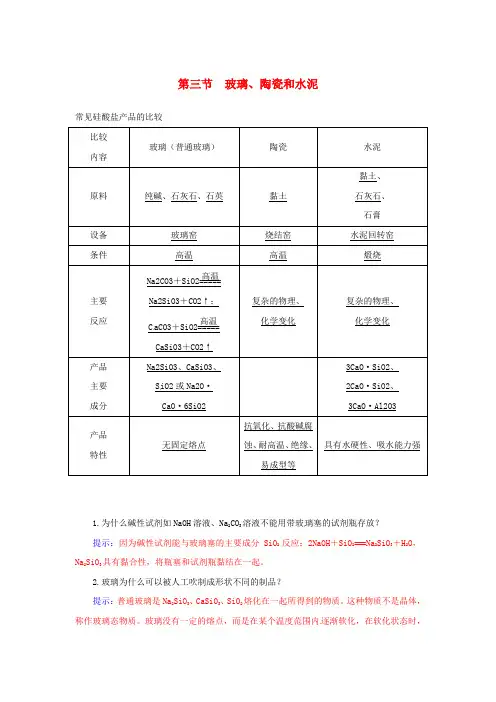
第三节玻璃、陶瓷和水泥常见硅酸盐产品的比较aCO3SiO21.为什么碱性试剂如NaOH溶液、Na2CO3溶液不能用带玻璃塞的试剂瓶存放?提示:因为碱性试剂能与玻璃塞的主要成分SiO2反应:2NaOH+SiO2===Na2SiO3+H2O,Na2SiO3具有黏合性,将瓶塞和试剂瓶黏结在一起。
2.玻璃为什么可以被人工吹制成形状不同的制品?提示:普通玻璃是Na2SiO3、CaSiO3、SiO2熔化在一起所得到的物质。
这种物质不是晶体,称作玻璃态物质。
玻璃没有一定的熔点,而是在某个温度范围内逐渐软化,在软化状态时,可以被吹制成任何形状的制品。
3.水泥在储存和运输过程中应注意什么?提示:由于水泥具有很强的吸水能力,能吸收空气中的水分并与之发生化学反应,故储存和运输水泥的过程中要注意防水、防潮。
►综合拓展一、几种玻璃的特性和用途二、水泥1.石膏的作用:调节水泥硬化时间。
2.用途。
(1)制成水泥砂浆:水泥、沙子和水的混合物。
(2)制混凝土:水泥、沙子和碎石的混合物。
3.水泥易被酸腐蚀。
由于水泥的主要成分是硅酸盐和铝酸盐,水泥中还含有少量的碳酸盐,所以水泥和水泥制品易被酸(如HCl、HNO3、H2SO4、CH3COOH等)腐蚀。
因此,水泥制品也要防止酸的腐蚀。
4.水泥的质量指标:我国的三个强度等级(42.5、52.5和62.5)表示常用硅酸盐水泥的性能。
等级越高,水泥的性能越好。
►尝试应用1.在面盆、痰盂等铁制品表面烧制搪瓷的目的是(A)A.防止铁生锈且美观B.增大厚度防止磨损C.增大硬度防止撞坏D.美观和杀菌消毒作用解析:在脸盆等铁制品表面烧制搪瓷,能够隔绝空气和水,不但能防止铁生锈,而且美观,A项正确;在茶缸和脸盆等铁制品表面烧制搪瓷的目的不是为了增大硬度,不能防止磨损,也不能杀菌消毒,B、C、D三项错误。
玻璃和陶瓷的新发展1.光导纤维:简称光纤。
(1)成分:SiO2(石英玻璃)。
(2)用途:制作光缆,还用于医疗、信息处理、传能传像、遥测遥控和照明等方面。

第三节金属晶体[核心素养发展目标] 1.宏观辨识与微观探析:能辨识常见的金属晶体,能从微观角度分析金属晶体中的构成微粒及微粒间的相互作用。
2.证据推理与模型认知:能利用金属晶体的通性推导晶体类型,从而理解金属晶体中各微粒之间的作用,理解金属晶体的堆积模型,并能用均摊法分析其晶胞结构。
一、金属键和金属晶体1.金属键(1)概念:金属阳离子与自由电子之间的强烈的相互作用。
(2)实质:金属原子脱落下来的价电子形成遍布整块晶体的“电子气〞,被所有原子所共用,从而把所有的金属原子维系在一起,形成一种“巨分子〞。
(3)特征:金属键没有方向性和饱和性。
2.金属晶体(1)金属晶体通过金属阳离子与自由电子之间的较强作用形成的晶体,叫做金属晶体。
(2)用电子气理论解释金属的性质(1)金属单质和合金都属于金属晶体。
(2)金属晶体中含有金属阳离子,但没有阴离子。
(3)金属导电的微粒是自由电子,电解质溶液导电的微粒是自由移动的阳离子和阴离子;前者导电过程中不生成新物质,为物理变化,后者导电过程中有新物质生成,为化学变化。
因而,二者导电的本质不同。
例1以下关于金属键的表达中,不正确的选项是( )A.金属键是金属阳离子和自由电子这两种带异性电荷的微粒间的强烈相互作用,其实质与离子键类似,也是一种电性作用B.金属键可以看作是许多原子共用许多电子所形成的强烈的相互作用,所以与共价键类似,也有方向性和饱和性C.金属键是带异性电荷的金属阳离子和自由电子间的相互作用,故金属键无饱和性和方向性D.构成金属键的自由电子在整个金属内部的三维空间中做自由运动[考点] 金属键和金属晶体[题点] 金属键的理解答案 B解析从基本构成微粒的性质看,金属键与离子键的实质类似,都属于电性作用,特征都是无方向性和饱和性;自由电子是由金属原子提供的,并且在整个金属内部的三维空间内运动,为整个金属的所有阳离子所共有,从这个角度看,金属键与共价键有类似之处,但两者又有明显的不同,如金属键无方向性和饱和性。


第3课时电解质溶液中微粒间的关系一、溶液中的守恒关系1.电荷守恒电解质溶液中阳离子所带的电荷总数与阴离子所带的电荷总数相等。
即电荷守恒,溶液呈电中性。
(1)解题方法①分析溶液中所有的阴、阳离子。
②阴、阳离子浓度乘以自身所带的电荷数建立等式。
(2)举例如:Na2CO3溶液中①Na+、H+、CO2-3、HCO-3、OH-。
②1×c(Na+)+1×c(H+)=2×c(CO2-3)+1×c(HCO-3)+1×c(OH-)。
化简得:c(Na+)+c(H+)=2c(CO2-3)+c(HCO-3)+c(OH-)。
2.元素质量守恒在电解质溶液中,由于某些离子发生水解或电离,离子的存在形式发生了变化,就该离子所含的某种元素来说,其质量在反应前后是守恒的,即元素质量守恒。
(1)解题方法①分析溶质中的特定元素的原子或原子团间的定量关系(特定元素除H、O元素外)。
②找出特征元素在水溶液中的所有存在形式。
(2)举例如:Na2CO3溶液中①n(Na+)n(CO2-3)=21,即n(Na+)=2c(CO2-3),CO2-3在水中部分会水解成HCO-3、H2CO3,共三种含碳元素的存在形式。
②c(Na+)=2[c(CO2-3)+c(HCO-3)+c(H2CO3)]。
3.质子守恒方法一:可以由电荷守恒与元素质量守恒推导出来。
如Na2CO3中将电荷守恒和元素质量守恒中的金属阳离子消去得c(OH-)=c(H+)+c(HCO-3)+2c(H2CO3)。
方法二:质子守恒是依据水的电离平衡:H2O H++OH-,水电离产生的H+和OH-的物质的量总是相等的,无论在溶液中由水电离出的H+和OH-以什么形式存在。
如:Na2CO3溶液中即c(OH-)=2c(H2CO3)+c(HCO-3)+c(H3O+)或c(OH-)=2c(H2CO3)+c(HCO-3)+c(H+)。
二、溶液中离子浓度比较的四种类型1.不同溶液中同一离子浓度比较要考虑溶液中其他离子对该离子的影响,如:在相同浓度的下列溶液中①NH4Cl,②CH3COONH4,③NH4HSO4,④(NH4)2SO4,⑤(NH4)2CO3,c(NH+4)由大到小的顺序:④>⑤>③>①>②。