2014年全国高考理综化学试题及答案
- 格式:docx
- 大小:1.05 MB
- 文档页数:9

2014年普通高等学校招生全国统一考试(新课标Ⅱ卷)理科综合试卷第Ⅰ卷一、选择题(每小题6分,只有一个符合题意)1、关于细胞的叙述,错误的是A.植物细胞的胞间连丝具有物质运输的作用B.动物细胞间的粘着性与细胞膜上的糖蛋白有关C.ATP水解释放的能量可用于细胞内的吸能反应D.哺乳动物的细胞可以合成蔗糖,也可以合成乳糖【答案】D【解析】本题考查的是细胞结构和化学成份这两个知识点。
细胞膜的功能之一信息传递,其方式如通过胞间连丝,A项正确。
糖蛋白与细胞相互识别有关,又与细胞间的粘着性有关,癌变后的细胞由于糖蛋白减少所以易转移和扩散, B项正确。
ATP水解后有能量可用于各项生命活动,如电能、热能等其他细胞内的吸能反应,C项正确。
蔗糖是植物内的一种二糖,在哺乳动物的细胞不可以合成,故D项是错误的。
2.同一动物个体的神经细胞与肌肉细胞在功能上是不同的,造成这种差异的主要原因是A.两者所处的细胞周期不同B.两者合成的特定蛋白不同C.两者所含有的基因组不同D.两者核DNA复制的方式不同【答案】B【解析】本题考查的是细胞分化这个知识点。
同一生物个体的不同细胞,在形态结构与功能上是不同的,是基因的选择性表达的结果,其DNA分子或遗传物质并没有差异,A、C、D都不正确,基因的选择性表达之后,形成了不同的蛋白质,使各细胞中的蛋白质有所不同,故B项正确。
3.关于在正常情况下组织液的生成与回流的叙述,错误的是A.生成与回流的组织液中氧气的含量相等B.组织液不断生成与回流,并保持动态平衡C.血浆中的有些物质经毛细血管动脉端进入组织液D.组织液中的有些物质经毛细血管静脉端进入血液【答案】D【解析】本题考查的是内环境成份这一个知识点。
内环境中的各种成份是处于动态平衡之中,氧气在生成的组织液中会高于回流的组织液,因为组织细胞在不断消耗氧气,这样氧气就能以自由扩散形式从组织液进入组织细胞,故A不正确,B正确。
因为毛细血管壁有一定通透性,所以血浆中的小分子物质可以透过毛细血管动脉端进入组织液,同理,组织液中的有些物质经毛细血管静脉端进入血液,血浆与组织液可以发生物质相互渗透。

绝密★启用前2014年普通高等学校招生全国统一考试(四川卷)理科综合·化学理科综合考试时间共150分钟。
试卷满分300分, 其中, 物理110分, 化学100分, 生物90分。
化学试题卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)。
第Ⅰ卷5至6页,第Ⅱ卷7至8页,共4页。
考生作答时,须将答案填在答题卡上,在本试卷、草稿纸上答题无效。
考试结束后,将本试题卷和答题卡一并交回。
可能用到的相对原子质量:N 14 O 16 S 32 Mn 55第Ⅰ卷(选择题 共42分)注意事项:必须使用2B 铅笔在答题卡上将所选答案对应的标号涂黑第Ⅰ卷共7题,每题6分。
每题给出的四个选项中,只有一项是符合题目要求的。
1. 化学与生活密切相关,下列说法不正确...的是 A. 乙烯可作水果的催熟剂 B. 硅胶可作袋装食品的干燥剂 C. 福尔马林可作食品的保鲜剂 D. 氢氧化铝可作胃酸的中和剂 2. 下列关于物质分类的说法正确的是 A. 金刚石、白磷都属于单质 B. 漂白粉、石英都属于纯净物 C. 氯化铵、次氯酸都属于强电解质 D. 葡萄糖、蛋白质都属于高分子化合物 3. 能正确表示下列反应的离子方程式的是A. Cl 2中通入NaOH 溶液:Cl 2 + OH —= Cl —+ ClO —+ H 2OB. NaHCO 3溶液中加入稀HCl :2-3CO + 2H + = CO 2↑ + H 2OC. AlCl 3溶液中加入过量稀氨水:Al 3+ + 4NH 3·H 2O = 2AlO —+ +44NH + 2H 2O D. 铜溶于稀硝酸:3Cu + 8H + + 32NO — = 3Cu 2+ + 2NO ↑ + 4H 2O5. 设N A 为阿伏加德罗常数的值。
下列说法正确的是A. 高温下,0.2 mol Fe 与足量水蒸气反应,生成的H 2分子数目为0.3N AB. 室温下,1 L pH=13的NaOH 溶液中,由水电离出的OH —离子数目为0.1N AC. 氢氧燃料电池正极消耗22.4 L (标准状况)气体时,电路中通过的离子数目为2N AD. 5NH4NO 32HNO 3 + 4N 2↑ + 9H 2O 反应中,生成28 g N 2时,转移的电子数目为3.75N A6. 下列溶液中粒子的物质的量浓度关系正确的是A. 0.1 mol/L NaHCO 3溶液与0.1 mol/L NaOH 溶液等体积混合,所得溶液中: c (Na +) > c (CO 32—) > c (HCO 3—) > c (OH —)B. 20 mL 0.1 mol/L CH 3COONa 溶液与10 mL 0.1 mol/L HCl 溶液混合后呈酸性,所得溶液中: ——+33(CH COO )(Cl )(CH COOH)(H )c c c c >>>C. 室温下,pH= 2 的盐酸与pH= 12的氨水等体积混合,所得溶液中:—++4(Cl )+(H )(NH )(OH )c c c c >+—D. 0.1 mol/L CH 3COOH 溶液与0.1 mol/L NaOH 溶液等体积混合,所得溶液中:+3(O H )(H )(C H C OO H )c c c>+—7. 在10 L 恒容密闭容器中充入X (g )和Y (g ),发生反应X(g) + Y(g) M(g) + N(g),所得实验数据如下表:下列说法正确的是A. 实验①中,若5 min 时测得 n (M) =0.050 mol ,则0至5 min 时间内,用N 表示的平均反应速率v (N) = 1.0×10--2 mol/minB. 实验②中,该反应的平衡常数K =2.0C. 实验③中,达到平衡时,X 的转化率为60%D. 实验④中,达到平衡时,b >0.060第Ⅱ卷(非选择题共58分)注意事项:必须使用0.5毫米黑色墨迹签字笔在答题卡上题目所指示的答题区域内作答。


2014年普通高等学校招生全国统一考试(浙江卷)理科综合化学试题解析教师:杭州新理想高复李良总体分析:这次化学试题应该来说学生得分不会很低,同样拿高分也不简单,由于28题实验题与29有机推断题稍简单,这样的题平时月考考60的同学这次有机会拿70分。
平时拿90分的同学未必考得出90分……7.下列说法不正确...的是A.光催化还原水制氢比电解水制氢更节能环保、更经济B.氨氮废水(含NH4+及NH3)可用化学氧化法或电化学氧化法处理C.某种光学检测技术具有极高的灵敏度,可检测到单个细胞(V=10-12L)内的数个目标分子,据此可推算该检测技术能测量到细胞内浓度约为10-12~10-11mol ·L-1的目标分子D.向汽油中添加甲醇后,该混合燃料的热值不变解析:答案D热值:1千克某种固体(气体)燃料完全燃烧放出的热量称为该燃料的热值,很明显加入甲醇带来的热值肯定改变。
这道题要选择错误答案一般同学都能得出正确答案,实战中还是那句话:其它答案说的那么有道理一般都是对的。
8.下列说法正确的是A.金属汞一旦洒落在实验室地面或桌面时,必须尽可能收集,并深埋处理B.用pH计、电导率仪(一种测量溶液导电能力的仪器)均可检测乙酸乙酯的水解程度C.邻苯二甲酸氢钾可用于标定NaOH溶液的浓度,假如称量邻苯二甲酸氢钾时电子天平读数比实际质量偏大,则测得的NaOH溶液浓度比实际浓度偏小D.向某溶液中加入茚三酮试剂,加热煮沸后溶液若出现蓝色,则可判断该溶液含有蛋白质解析:选择B这里面A答案明显不对,D答案茚三酮是检验氨基酸的,很多人或在BC中徘徊,C答案是错误的,由于称量邻苯二甲酸氢钾时电子天平读数比实际质量偏大,得到的邻苯二甲酸氢钾的实际浓度偏小,会使标准液实际浓度减小,使得实际消耗的邻苯二甲酸氢钾的体积增大,所以计算得到的得到的待测液浓度偏大。
B答案乙酸乙酯水解因为有乙酸的存在,酸度,离子浓度都会改变, 用pH计、电导率仪(一种测量溶液导电能力的仪器)均可检测乙酸乙酯的水解程度.9.如表所示的五种元素中,W 、X 、Y 、Z 为短周期元素,这四种元素的原子最外层电子数之和为22。

2014年高考全国卷I理综化学题7.下列化合物中同分异构体数目最少的是()A.戊烷B.戊醇C.戊烯D.乙酸乙酯8.化学与社会、生活密切相关。
对下列现象或事实的解释正确的是()选项现象或事实解释A 用热的烧碱溶液洗去油污Na2CO3可直接与油污反应B 漂白粉在空气中久置变质漂白粉中的CaCl2与空气中的CO2反应生成CaCO3C 施肥时,草木灰(有效成分为K2CO3)不能与NH4Cl混合使用K2CO3与NH4Cl反应生成氨气会降低肥效D FeCl3溶液可用于铜质印刷线路板制作FeCl3能从含有Cu2+的溶液中置换出铜9.已知分解1molH2O2放出热量98kJ。
在含少量I-的溶液中,H2O2分解的机理为:H2O2 + I-→H2O+IO-(慢) H2O2 + IO- →H2O+O2+ I–(快)下列有关该反应的说法正确的是()A.反应速率与I-浓度有关B.IO-也是该反应的催化剂C.反应活化能等于98kJ/mol D.υ(H2O2)=υ(H2O)=υ(O2)10.X、Y、Z均为短周期元素,X、Y处于同一周期,X、Z的最低价离子分别为X2-和Z-,Y+和Z-具有相同的电子层结构。
下列说法正确的是()A.原子最外层电子数:X>Y>Z B.单质沸点:X>Y>ZC.离子半径:X2->Y+>Z- D.原子序数:X>Y>Z11.溴酸银(AgBrO3)溶解度随温度变化曲线如图所示,下列说法错误的是()A.溴酸银的溶解是放热过程B.温度升高时溴酸银的溶解速度加快C.60℃时溴酸银的K w约等于6×10-4D.若硝酸银中含有少量溴酸银,可用重结晶方法提纯12.下列有关仪器使用方法或实验操作正确的是()A.洗净的锥形瓶和容量瓶可以放进烘箱中烘干B.酸式滴定管装标准溶液前,必须用溶液润洗C.酸碱滴定实验中,用待滴定溶液润洗锥形瓶以减小实验误差D.用容量瓶配标准溶液时,若加水超过刻度线,立即用滴管吸出多余的液体13.利用右图所示装置进行下列实验,能得出相应实验结论的是()选项①②③实验结论A 稀硫酸Na2S AgNO3与AgCl的浊液K sp(AgCl)>K sp(Ag2S)B 浓硫酸蔗糖溴水浓硫酸具有脱水性、氧化性C 稀盐酸Na2SO3Ba(NO3)2SO2与可溶性钡盐均可生成白色沉淀D 浓硝酸Na2CO3Na2SiO3溶液酸性:硝酸>碳酸>硅酸26.(13分)乙酸异戊酯是组成蜜蜂信息素的成分之一,具有香蕉的香味。
![2014高考全国理综化学II卷[附答案解析]](https://uimg.taocdn.com/f900f7ffa1c7aa00b52acbb5.webp)
2013年高考全国理综化学II卷可能用到的相对原子质量:H 1 C 12 N 14 O 16 F 19 Na 23 Al 27 S 32 Cl 35.5 K 39 Ca 40 Cr 52 Fe 56 Ni 59 Cu 64 Zn 65一、选择题:本题共7小题,每小题6分。
在每小题给出的四个选项中,只有一项是符合题目要求的。
7. 在一定条件下,动植物油脂与醇反应可制备生物柴油,化学方程式如下:下列叙述错误..的是A. 生物柴油由可再生资源制得B. 生物柴油是不同酯组成的混合物C. 动植物油脂是高分子化合物D. “地沟油”可用于制备生物柴油8. 下列叙述中,错误..的是A. 苯与浓硝酸、浓硫酸共热并保持55~60℃反应生成硝基苯B. 苯乙烯在合适条件下催化加氢可生成乙基环己烷C. 乙烯和溴的四氯化碳溶液反应生成1,2-二溴乙烷D. 甲苯与氯气在光照下反应主要生成2,4-二氯甲苯9. N0为阿伏伽德罗常数的值。
下列叙述正确的是A. 1.0L1.0mol·L-1的NaAlO2水溶液中含有的氧原子数为2N0B. 12g石墨烯(单层石墨)中含有六元环的个数0.5N0C. 25℃时pH=13的NaOH溶液中含有OH-的数目为0.1N0D. 1mol的羟基与1mol的氢氧根离子所含电子数均为9N010. 能正确表示下列反应的离子方程式A. 浓盐酸与铁屑反应:2Fe + 6H+ = 2Fe3+ + 3H2↑B. 钠与CuSO4溶液反应:2Na + Cu2+ = Cu↓+ 2Na+C. NaHCO3溶液与稀H2SO4反应:CO32- + 2H+ = H2O + CO2↑D. 向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2 + 2Fe3+ = 2Fe(OH)3 + 3Mg2+11. “ZEBRA”蓄电池的结构如图所示,电极材料多孔Ni/NiCl2和金属钠之间由钠离子导体制作的陶瓷管相隔。
下列关于该电池的叙述错误..的是A. 电池反应中有NaCl生成B. 电池的总反应是金属钠还原三价铝离子C. 正极反应为:NiCl2 + 2e- = Ni + 2Cl-D. 钠离子通过钠离子导体在两电极间移动12. 在1200时,天然气脱硫工艺中会发生下列反应:H2S(g) + 3/2O2(g) = SO2(g) + H2O(g) △H12H2S(g) + SO2(g) = 3/2S2(g) + 2H2O(g) △H2H2S(g) +1/2O2(g) = S(g) + H2O(g) △H32S(g) = S2(g) △H4则△H4的正确表达式为A. △H4 = 2/3(△H1 + △H2 - 3△H3)B. △H4 = 2/3(3△H3 - △H1 - △H2)C. △H4 = 3/2(△H1 + △H2 - 3△H3)D. △H4 = 3/2(△H1 - △H2 - 3△H3)13. 室温时,M(OH)2(s) M2+(aq) + 2OH-(aq) K sp = a。

2014年普通高等学校招生全国统一考试化学试题分类汇编专题四氧化还原反应1.(2014·上海单科化学卷,T19)下列反应与Na2O2+SO2→Na2SO4相比较,Na2O2的作用相同的是A.2Na2O2+CO2→2Na2CO3+O2B.2Na2O2+2SO3→2Na2SO4+O2C.Na2O2+H2SO4→Na2SO4+H2O2D.3Na2O2+Cr2O3→2Na2CrO4+Na2O【答案】D【解析】氧化还原反应Na2O2+SO2→Na2SO4中,Na2O2是氧化剂,SO2是还原剂;A、2Na2O2+CO2→2Na2CO3+O2反应中,Na2O2既是氧化剂也是还原剂,A不选;B、2Na2O2+2SO3→2Na2SO4+O2反应中,Na2O2既是氧化剂也是还原剂,B不选;C、Na2O2+H2SO4→Na2SO4+H2O2属于非氧化还原反应,C不选;D、3Na2O2+Cr2O3→2Na2CrO4+Na2O反应中,Na2O2是氧化剂,D选。
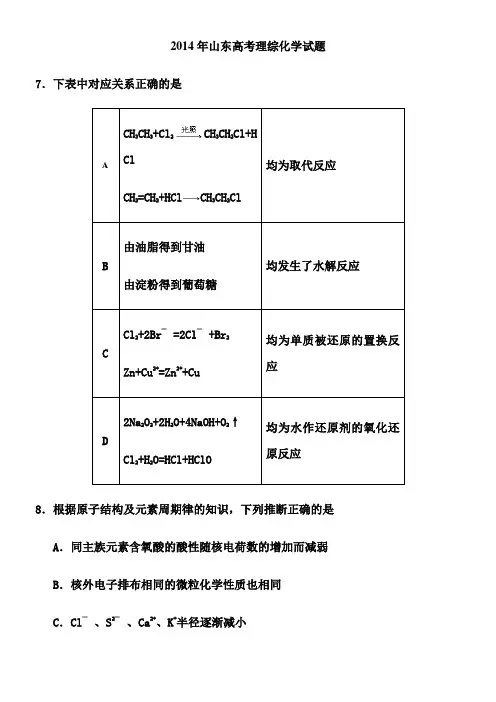
2.(2014·山东理综化学卷,T7)下表中对应关系正确的是2CH+HCl【答案】B【解析】A、CH2=CH2+HCl CH3CH2Cl为取代反应,A错误;B、由油脂得到甘油,属于酯类的水解反应。
由淀粉得到葡萄糖,属于糖类的水解反应,B正确;C、Zn+Cu2+=Zn2++Cu的单质Zn化合价升高,被氧化,C错误;D、Cl2+H2O=HCl+HClO反应中H2O既不是氧化剂也不是还原剂,D错误。
3.(2014·全国大纲版理综化学卷,T13)已知:将Cl2通人适量KOH溶液,产物中可能有KC1、KClO、KC1O3,且()()cc--C1C1O的值与温度高低有关。
当n(KOH)=amol时,下列有关说法错误的是A .若某温度下,反应后()()c c --C1C1O =11,则溶液中()()c c --C1C1O =12B . 参加反应的氯气的物质的量等于12amol C .改变温度,反应中转移电子的物质的量n e 的范围:12amol ≤n e ≤56amol D .改变温度,产物中KC1O 3的最大理论产量为17amol 【答案】D【解析】A 、令n (ClO —)=1mol ,反应后()()c c --C1C1O =11,则n (Cl —)=11mol ,电子转移守恒,5×n (ClO 3—)+1×n (ClO —)=1×n (Cl —),即5×n (ClO 3—)+1×1mol=1×11mol ,解得n (ClO 3—)=2mol ,故溶液中()()c c --C1C1O =12,A 正确;B 、由Cl 原子守恒可知,2n (Cl 2)=n (KCl )+n (KClO )+n (KClO 3),由钾离子守恒可知n (KCl )+n (KClO )+n (KClO 3)=n (KOH ),故参加反应的氯气的物质的量=12n (NaOH )=12amol ,B 正确;C 、氧化产物只有KClO 3时,转移电子最多,根据电子转移守恒5n (KCl )=n (KClO 3),由钾离子守恒:n (KCl )+n (KClO 3)=n (KOH ),故n (KClO 3)=16n (KOH )=16a mol ,转移电子最大物质的量=16a mol×5=56a mol ,氧化产物只有KClO 时,转移电子最少,根据电子转移守恒n (KCl )=n(KClO ),由钾离子守恒:n (KCl )+n (KClO )=n (KOH ),故n (KClO )=12n (KOH )= 12a mol ,,转移电子最小物质的量=12a mol×1=12a moll ,故反应中转移电子的物质的量ne 的范围:12a mol≤n e ≤56amol ,C 正确;D 、氧化产物只有KClO 3时,其物质的量最大,由C 中计算可知:n 最大(KClO 3)=16n (KOH )=16a mol ,D 错误。

2014年普通高等学校招生全国统一考试(浙江卷)理科综合化学试题相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 Al-27 S-32 Cl-35.5 K-39 Ca-40 Fe-56 Cu-64 Ba-1377.下列说法不正确...的是A.光催化还原水制氢比电解水制氢更节能环保、更经济B.氨氮废水(含NH4+及NH3)可用化学氧化法或电化学氧化法处理C.某种光学检测技术具有极高的灵敏度,可检测到单个细胞(V ≈10-12L)内的数个目标分子,据此可推算该检测技术能测量细胞内浓度约为10-12~10-11mol·L-1的目标分子D.向汽油中添加甲醇后,该混合燃料的热值不变8.下列说法正确的是A.金属汞一旦洒落在实验室地面或桌面时,必须尽可能收集,并深埋处理B.用pH计、电导率仪(一种测量溶液导电能力的仪器)均可监测乙酸乙酯的水解程度C.邻苯二甲酸氢钾可用于标定NaOH溶液的浓度。
假如称量邻苯二甲酸氢钾时电子天平读数比实际质量偏大,则测得的NaOH溶液浓度比实际浓度偏小D.向某溶液中加入茚三酮试剂,加热煮沸后溶液若出现蓝色,则可判断该溶液含有蛋白质9.如表所示的五种元素中,W、X、Y、Z为短周期元素,这四种元素的原子最外层电子数之和为22。
下列说法正确的是A.X、Y、Z三种元素最低价氢化物的沸点依次升高B.由X、Y和氢三种元素形成的化合物中只有共价键C.物质WY2、W3X4、WZ4均有熔点高、硬度大的特性D.T元素的单质具有半导体的特性,T与Z元素可形成化合物TZ410.下列说法正确的是A.乳酸薄荷醇酯()仅能发生水解、氧化、消去反应B.乙醛和丙烯醛()不是同系物,它们与氢气充分反应后的产物也不是同系物C.淀粉和纤维素在酸催化下完全水解后的产物都是葡萄糖D.CH3COOCH2CH3与CH3CH2COOCH3互为同分异构体,1H-NMR 谱显示两者均有三种不同的氢原子且三种氢原子的比例相同,故不能用1H-NMR来鉴别11.镍氢电池(NiMH)目前已经成为混合动力汽车的一种主要电池类型。

2014年普通高等学校招生全国统一考试理科综合能力测试一、选择题:本题共13小题,每小题6分。
在每小题给出的四个选项中,只有一项是符合题目要求的。
1. 关于细胞的叙述,错误的是A. 植物细胞的细胞连丝具有物资运输的作用B. 动物细胞间的粘着性细胞膜上的糖蛋白有关C. A TP水解释放的能量可用于细胞内的吸能反应D. 哺乳动物的细胞可以合成蔗糖,也可以合成乳糖2.同一动物个体的神经细胞与肌细胞在功能上是不同的,造成这种差异的主要原因是A.二者所处的细胞周期不同B. 二者合成的特定蛋白不同C. 二者所含有的基因组不同D. 二者核DNA的复制方式不同3.关于在正常情况下组织液生成与回流的叙述,错误的是A.生成与回流的组织液中氧气的含量相等B. 组织液不断生成与回流,并保持动态平衡C. 血浆中的有些物质经毛细血管动脉端进入组织液D. 组织液中的有些物质经毛细血管静脉端进入血液4.讲某植物花冠切成大小和形状相同的细条,分为a、b、c、d、e和f组(每组的细条数相等),取上述6组细条数分别置于不同浓度的蔗糖溶液中,浸泡相同时间后测量各组花冠细条的长度,结果如图所示。
假如蔗糖溶液与花冠细胞之间只有水分交换则A.试验后,a组液泡中的溶质浓度比b组的高B.浸泡导致f组细胞中液泡的失水量小于b组的C.A组细胞在蔗糖溶液中失水或吸水所耗ATP大于b组D.使细条在浸泡前后长度不变的蔗糖浓度介于0.4~0.5mol-L-1之间5.关于核酸的叙述,错误的是A.细胞核中发生的转录过程有RNA聚合酶的参与B.植物细胞的线粒体和叶绿素体中均可发生DNA的复制C.双链DNA分子中一条链上的磷酸和核糖是通过氨键链接的D.用甲基绿和吡罗红染色可观察DNA和RNA在细胞中的分布6.关于光合作用和呼吸作用的叙述,错误的是A.磷酸是光反应中合成A TP所需的反应物B.光合作用中叶绿素吸收光能不需要酶的参与C.人体在剧烈运动时所需要的能量由乳酸分解提供D.病毒核酸的复制需要宿主细胞的呼吸作用提供能量7.下列过程没有发生化学反应的是A.用活性炭去除冰箱中的异味B.用热碱水清除炊具上残留的污垢C.用浸泡过高锰酸钾溶液的硅藻土保鲜水果D.用含硅胶、铁粉的透气小袋与食品一起密封包装8.四联苯的一氯代物有A. 3种B. 4种C. 5种D. 6种9.下列反应中,反应后固体物质增重的是A.氢气通过灼热的CuO粉末B. 二氧化碳通过Na2O2粉末C. 铝与Fe2O3发生铝热反应D.将锌粒投入Cu(NO3)2溶液10.下列图示试验正确的是11.一定温度下,下列溶液的离子浓度关系式正确的是A. pH=5的H2S溶液中,c(H+)=c(HS-)=1×10-5mol·L-1B. pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1C. pH=2的H2C2O4溶液与pH=12的NaOH溶液任意比例混合:O)c(Na+)+c(H+)=c(OH-)+c(HC24D. pH相同的①CH3COONa②NaHCO3③NaCIO三种溶液的c(Na+):①>②>③12. 2013年3月我国科学家报道了如图所示的水溶液锂离子电池体系。
2014年山东高考理综化学试题7.下表中对应关系正确的是A CH3CH3+Cl2CH3CH2Cl+HClCH2=CH2+HCl CH3CH2Cl均为取代反应B由油脂得到甘油由淀粉得到葡萄糖均发生了水解反应CCl2+2Br‾=2Cl‾+Br2Zn+Cu2+=Zn2++Cu 均为单质被还原的置换反应D2Na2O2+2H2O+4NaOH+O2↑Cl2+H2O=HCl+HClO 均为水作还原剂的氧化还原反应8.根据原子结构及元素周期律的知识,下列推断正确的是 A.同主族元素含氧酸的酸性随核电荷数的增加而减弱 B.核外电子排布相同的微粒化学性质也相同C.Cl‾、S2‾、Ca2+、K+半径逐渐减小D.35Cl与3717Cl得电子能力相同179.等质量的下列物质与足量稀硝酸反应,放出NO物质的量最多的是A.FeO B. Fe2O3 C. FeSO4 D、Fe3O410.下列实验操作或装置(略去部分加持仪器)正确的是A.配制溶液 B.中和滴定C.制备乙酸乙酯 D.制取收集干燥氨气11.苹果酸的结构简式为,下列说法正确的是A.苹果酸中能发生酯化反应的官能团有2种B.1mol苹果酸可与3mol NaOH发生中和反应C.1mol苹果酸与足量金属Na反应生成生成1mol H2D.HOOC—CH2—CH(OH)—COOH与苹果酸互为同分异构体12.下列有关溶液组成的描述合理的是A.无色溶液中可能大量存在Al3+、NH4+、Cl‾、S2‾B.酸性溶液中可能大量存在Na+、ClO‾、SO42‾、I‾C.弱碱性溶液中可能大量存在Na+、K+、Cl‾、HCO3‾D.中性溶液中可能大量存在Fe3+、K+、Cl‾、SO42‾13.已知某温度下CH3COOH和NH3•H2O的电离常数相等,现向10mL浓度为0.1mol•L‾1的CH3COOH溶液中滴加相同浓度的氨水,在滴加过程中A.水的电离程度始终增大B.c(NH4+)/ c(NH3•H2O)先增大再减小C.c(CH3COOH)与c(CH3COO‾)之和始终保持不变D.当加入氨水的体积为10mL时,c (NH4+)= c (CH3COO‾)29.(17分)研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:2NO 2(g)+NaCl(s)NaNO3(s)+ClNO(g) K1∆H < 0 (I)2NO(g)+Cl 2(g)2ClNO(g) K2∆H < 0 (II)(1)4NO 2(g)+2NaCl(s)2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K= (用K1、K2表示)。

2014年高考全国1卷理综化学试题可能用到的相对原子质量:H 1 C 12 N 14 O 16 F 19 Al 27 P 31 S 32 Ca 40 Fe 56 Cu 64 Br 80 Ag 108一、选择题(每小题6分。
在每小题给出的四个选项中,只有一项是符合题目要求的)7.下列化合物中同分异构体数目最少的是( )A.戊烷B. 戊醇C. 戊烯D. 乙酸乙酯8.选项现象或事实解释A 用热的烧碱溶液洗去油污Na2CO3 可直接和油污反应B 漂白粉在空气中久置变质漂白粉中的 CaCl2 与空气中的 CO2 反应生成 CaCO3C 施肥时,草木灰(有效成分为 K2CO3)不能与 NH4Cl 混合使用K2CO3 与 NH4Cl 反应生成氨气会降低肥效D FeCl3 溶液可用于铜质印刷线路板制作FeCl3 能从含有 Cu2+的溶液中置换出铜9.2 2 2 2H2O2 + I−→H2O + IO−慢; H2O2 + IO−→H2O + O2 + I−快;下列有关该反应的说法正确的是( )A.反应的速率与 I−的浓度有关B. IO−也是该反应的催化剂C. 反应活化能等于 98 kJ·mol−1D. (H2O2)= (H2O)= (O2)10.W、X、Y、Z 均是短周期元素,X、Y 处于同一周期,X、Z 的最低价离子分别为 X2−和Z-,Y+和 Z-离子具有相同的电子层结构。
下列说法正确的是( )A.原子最外层电子数:X>Y>ZB. 单质沸点:X>Y>ZC. 离子半径:X2−>Y+>Z-D. 原子序数:X>Y>Z11.溴酸银(AgBrO3)溶解度随温度变化曲线如图所示,下列说法错误的是( )A.溴酸银的溶解是放热过程B.温度升高时溴酸银溶解速度加快C.60℃时溴酸银的K sp 约等于6×10-4D.若硝酸钾中含有少量溴酸银,可用重结晶方法提纯12.下列有关仪器的使用方法或实验操作正确的是( )A.洗净的锥形瓶和容量瓶可以放进烘箱中烘干B.酸式滴定管装标准液前,必须先用该溶液润洗C.酸碱滴定实验中,用待滴定溶液润洗锥形瓶以减少实验误差D.用容量瓶配溶液时,若加水超过刻度线,立即用滴定管吸出多余液体。
2014年高考真题—化学学科(福建理综化学卷)解析版6. 下列有关物质的应用正确的是()A 生石灰用作食品的抗氧化剂B 盐类都可用做调味品C 铝罐可久盛食醋D 小苏打是面包发酵粉的主要成分之一【答案】:D【解析】生石灰具有吸水性,可用作食品干燥剂,本身不具有还原性,无法用作食品的抗氧化剂,A错;只有部分盐类可以作为调味品,B 错;铝罐容易受食醋中的醋酸腐蚀而破裂,无法久盛食醋,C错;D正确。
7.下列关于乙醇的说法不正确的是()A 可用纤维素的水解产物制取B 可由乙烯通过加成反应制取C 与乙醛互为同分异构体D 通过取代反应可以制取乙酸乙酯【答案】:C【解析】纤维素的水解产物为葡萄糖,葡萄糖在酶的作用下可以生成乙醇,A正确;乙烯与水加成可制取乙醇,B正确;乙醇与乙酸反应生成乙酸乙酯既是酯化反应,又是取代反应,D正确;乙醇与乙醛的组成元素相同,但各元素比例不同(化学式不同),两者不是互为同分异构体,C错误。
8. 下列实验能达到目的的是()A 只滴加氨水鉴别NaCl、AlCl3、MgCl2、Na2SO4四种溶液B 将NH4Cl溶液蒸干制取NH4Cl固体C 用萃取分液的方法除去酒精中的水D 用可见光束照射以区别溶液和胶体【答案】:D【解析】氨水与NaCl、Na2SO4两种溶液均不反应,与AlCl3、MgCl2反应均生成难溶物,无法通过现象来区别四种溶液,A错;NH4Cl受热易分解,B错;酒精与水能任意比混溶,无法用萃取分液的方法除去酒精中的水,C错;用可见光束照射以区别溶液和胶体,是利用胶体的丁达尔效应,D正确。
9. 常温下,下列各组物质中,Y既能与X反应又能与Z反应的是()【答案】:B【解析】②中的SiO2不能与浓盐酸反应,C、D错;常温下③中的N2与H2不反应,A错;B正确10. 下列关于0.10mol·L-1NaHCO3溶液的说法正确的是()A 溶质的电离方程式为NaHCO3 = Na+ + H+ +CO32-B 25℃时,加水稀释后,n(Na+)与n(OH-)的乘积变大C 离子浓度关系:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+c(CO32-)D 温度升高,c(HCO3-)增大【答案】:B【解析】HCO3-是弱酸根离子,无法完全电离,A错;加水稀释,溶液中c(OH-)减小,但n(OH-)却增大,所以n(Na+)与n(OH-)的乘积变大,B正确;根据电荷守恒溶液中离子浓度关系应该为:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-),C错;温度升高,促进HCO3-水解,则c(HCO3-)减小,D错误。
2014年高考全国卷2理综化学真题D12-⋅L mol c NaOH 标准溶液滴定过剩的HCl ,到终点时消耗mL V 2NaOH 溶液。
氨的测定装置(已省略加热和夹持装置) ②氯的测定:准确称取样品X ,配成溶液后用AgNO 3标准溶液滴定,K 2CrO 4溶液为指示剂,至出现淡红色沉淀不再消失为终点(Ag 2CrO 4为砖红色)。
回答下列问题:(1)装置中安全管的作用原理是_①_。
(2)用NaOH 标准溶液滴定过剩的HCl 时,应使用_②_式滴定管,可使用的指示剂为_③_。
(3)样品中氨的质量分数表达式为_④_。
(4)测定氨前应该对装置进行气密性检验,若气密性不好测定结果将_⑤_(填“偏高”或“偏低”)。
(5)测定氯的过程中,使用棕色测定管的原因是_⑥_;滴定终点时,若溶液中15100.2)(--+⋅⨯=L mol Ag c ,)(24-CrO c 为_⑦_mol·L -1,(已知:K sp (Ag 2CrO 4)=1.12×10-12)(6)经测定,样品X 中钴、氨和氯的物质的量比为1:6:3,钴的化合价为_⑧_,制备X 的化学方程式为_⑨_,X 的制备过程中温度不能过高的原因是_⑩_。
(二)选考题:共45分,请考生从给出的3道物理题,3道化学题、2道生物体中每科任选一题做答,并用2B 铅笔在答题卡上把所选题目的题号涂黑,注意所做题目的题号必须与所涂题目的题号一致,在答题卡选答区域指定位置答题。
如果不涂、多涂均按所答第一题评分;多答则每学科按所答的第一题评分。
36.【化学——选修2:化学与技术】(15分)将海水淡化与浓海水资源化结合起来是综合利用海水的重要途径之一。
一般是先将海水淡化获得淡水,再从剩余的浓海水中通过一系列工艺流程提取其他产品。
回答下列问题:(1)下列改进和优化海水综合利用工艺的设想和做法可行的是 (填序号)。
①用混凝法获取淡水 ②提高部分产品的质量③优化提取产品的品种 ④改进钾、溴、镁等的提取工艺(2)采用“空气吹出法”从浓海水吹出2Br ,并用纯碱吸收。
2014年普通高等学校招生全国统一考试(新课标Ⅱ卷)7.下列过程没有发生化学反应的是()A.用活性炭去除冰箱中的异味B.用热碱水清除炊具上残留的油污C.用浸泡过高锰酸钾溶液的硅藻土保鲜水果D.用含硅胶、铁粉的透气小袋与食品一起密封包装【答案】A【解析】考察化学变化的概念。
活性炭除去冰箱中的异味是物理吸附作用。
热碱溶液有利于酯类物质的水解,可用热碱液除去油污;酸性高锰酸钾溶液吸收乙烯可以用来保存水果;铁粉可防止食品被氧化,硅胶可使食品保持干燥。
8.四联苯的一氯代物有()A.3种B.4种C.5种D.6种【答案】C【解析】考察同分异构体种类。
根据四联苯的两个对称轴,联苯的一氯代物有5种结构。
9.下列反应中,反应后固体物质增重的是()A.氢气通过灼热的CuO粉末B.二氧化碳通过Na2O2粉末C.铝与Fe2O3发生铝热反应D.将锌粒投入Cu(NO3)2溶液【答案】B【解析】考察化学反应中固体质量改变的分析。
氢气通过灼热的CuO粉末后,CuO→Cu固体的质量减小;二氧化碳通过Na2O2粉末后生成Na2CO3,固体的质量增大;铝与Fe2O3发生铝热反应生成Al2O3,固体的质量不变;将锌粒投入Cu(NO3)2溶液置换出铜,Zn→Cu,固体的质量减小。
10.下列图示实验正确的是()A.除去粗盐溶液中的不溶物B.碳酸氢钠受热分解C.除去CO气体中的CO2气体D.乙酸乙酯制备演示实验【答案】D【解析】察实验基本操作。
解析:A错,玻璃棒应靠在滤纸的三层处;B错,固体加热试管口应朝下;C错,进气管应伸长进入溶液中。
D正确,是乙酸乙酯的实验室制法。
11.一定温度下,下列溶液的离子浓度关系式正确的是()A.pH=5的H2S溶液中,c(H+)=c(HS-)=1×10-5mol•L-1B.pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1C.pH=2的H2C2O4溶液与pH=12的NaOH溶液任意比例混合:c(Na+)+c(H+)=c(OH-)+c(HC2O4-)D.pH相同的①CH3COONa②NaHCO3③NaClO三种溶液的c(Na+):①>②>③【答案】选择D 【解析】考察离子浓度的关系。
2014年普通高等学校招生全国统一考试(天津卷)理科综合能力测试化学部分第I 卷1.化学与生产、生活息息相关, 下列叙述错误的是A .铁表而镀锌可以增强其抗腐蚀性B .用聚乙烯塑料代替聚乳酸塑料可减少白色污染C .大量燃烧化石燃料是造成雾霾天气的一种重要因素D .含再金属离子的电镀废液不能随意排放2.实验室制备下列气体时,所用方法正确的是A .制氧气时,用Na 2O 2或H 2O 2作反应物可选择相同的气体发生装置B .制氯气时,用饱和NaHCO 3溶液和浓硫酸净化气体C .制乙烯时,用排水法或向上排空气法收集气体D .制二氧化氮时,用水或NaOH 溶液吸收尾气3.运用相关化学知识进行判断,下列结论错误的是A .某吸热反应能自发进行,因此该反应是熵增反应B .NH 4F 水溶液中含有HF ,因此NH 4F 溶液不能存放于玻璃试剂瓶中C .可燃冰主要甲烷与水在低温高压下形成的水合物晶体,因此可存在于海底D .增大反应物浓度可加快反应速率,因此用浓硫酸与铁反应能增大生成H 2的速率4.对右图两种化合物的结构或性质描述正确的是A .不是同分异构体B .分子中共平面的碳原了数相同C .均能与溴水反应D .可用红外光谱区分,但不能用核磁共振氢谱区分5.下列有关电解质溶液中粒子浓度关系正确的是A .pH=1的NaHSO 4溶液:c(H +)=c(SO 42-)十c(OH -)B .含有AgCl 和AgI 固体的悬浊液:c(Ag +)>c(C1-)=c(I -)C .CO 2的水溶液:c(H +)>c(HCO 3-)=2c(CO 32-)D .含等物质的量的NaHC 2O 4和Na 2C 2O 4的溶液:3c(Na +)=2[c(HC 2O 4-)+ c(C 2O 42-)+c(H 2C 2O 4)]6.已知:锂离子电池的总反应为:Li x C+Li 1-x CoO 2放电充电C+LiCoO 2锂硫电池的总反应为:2Li+S 放电充电Li2S有关上述两种电池说法正确的是A.锂离子电池放电时,Li+向负极迁移B.锂硫电池充电时,锂电极发生还原反应C.理论上两种电池的比能量相同D.右图表示用锂离子电池给锂硫电池充电第II卷7.(14分)元素单质及其化合物有广泛用途,请根据周期表中第三周期元素相关知识回答下列问题:(1)按原子序数递增的顺序(稀有气体除外),以下说法正确的是。
2014年普通高等学校招生全国统一考试(浙江卷)理科综合化学试题相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 Al-27 S-32 Cl-35.5 K-39 Ca-40 Fe-56 Cu-64 Ba-1377.下列说法不正确...的是A.光催化还原水制氢比电解水制氢更节能环保、更经济B.氨氮废水(含NH4+及NH3)可用化学氧化法或电化学氧化法处理C.某种光学检测技术具有极高的灵敏度,可检测到单个细胞(V≈10-12L)内的数个目标分子,据此可推算该检测技术能测量细胞内浓度约为10-12~10-11mol·L-1的目标分子D.向汽油中添加甲醇后,该混合燃料的热值不变8.下列说法正确的是A.金属汞一旦洒落在实验室地面或桌面时,必须尽可能收集,并深埋处理B.用pH计、电导率仪(一种测量溶液导电能力的仪器)均可监测乙酸乙酯的水解程度C.邻苯二甲酸氢钾可用于标定NaOH溶液的浓度。
假如称量邻苯二甲酸氢钾时电子天平读数比实际质量偏大,则测得的NaOH溶液浓度比实际浓度偏小D.向某溶液中加入茚三酮试剂,加热煮沸后溶液若出现蓝色,则可判断该溶液含有蛋白质9.如表所示的五种元素中,W、X、Y、Z为短周期元素,这四种元素的原子最外层电子数之和为22。
下列说法正确的是A.X、Y、Z三种元素最低价氢化物的沸点依次升高B.由X、Y和氢三种元素形成的化合物中只有共价键C.物质WY2、W3X4、WZ4均有熔点高、硬度大的特性D.T元素的单质具有半导体的特性,T与Z元素可形成化合物TZ410.下列说法正确的是A.乳酸薄荷醇酯()仅能发生水解、氧化、消去反应B.乙醛和丙烯醛()不是同系物,它们与氢气充分反应后的产物也不是同系物C.淀粉和纤维素在酸催化下完全水解后的产物都是葡萄糖D.CH3COOCH2CH3与CH3CH2COOCH3互为同分异构体,1H-NMR谱显示两者均有三种不同的氢原子且三种氢原子的比例相同,故不能用1H-NMR来鉴别11.镍氢电池(NiMH)目前已经成为混合动力汽车的一种主要电池类型。
2014年高考全国1卷理综化学试题可能用到的相对原子质量:H 1 C 12 N 14 O 16 F 19 Al 27 P 31 S 32 Ca 40 Fe 56 Cu 64 Br 80 Ag 108一、选择题(每小题6分。
在每小题给出的四个选项中,只有一项是符合题目要求的)7.下列化合物中同分异构体数目最少的是( )A.戊烷B. 戊醇C. 戊烯D. 乙酸乙酯8.9.2 2 2 2H2O2 + I−→H2O + IO−慢; H2O2 + IO−→H2O + O2 + I−快;下列有关该反应的说法正确的是( )A.反应的速率与 I−的浓度有关B. IO−也是该反应的催化剂C. 反应活化能等于 98 kJ·mol−1D. (H2O2)= (H2O)= (O2)10.W、X、Y、Z 均是短周期元素,X、Y 处于同一周期,X、Z 的最低价离子分别为 X2−和Z-,Y+和 Z-离子具有相同的电子层结构。
下列说法正确的是( )A.原子最外层电子数:X>Y>ZB. 单质沸点:X>Y>ZC. 离子半径:X2−>Y+>Z-D. 原子序数:X>Y>Z11.溴酸银(AgBrO3)溶解度随温度变化曲线如图所示,下列说法错误的是( )A.溴酸银的溶解是放热过程B.温度升高时溴酸银溶解速度加快C.60℃时溴酸银的K sp 约等于6×10-4D.若硝酸钾中含有少量溴酸银,可用重结晶方法提纯12.下列有关仪器的使用方法或实验操作正确的是( )A.洗净的锥形瓶和容量瓶可以放进烘箱中烘干B.酸式滴定管装标准液前,必须先用该溶液润洗C.酸碱滴定实验中,用待滴定溶液润洗锥形瓶以减少实验误差D.用容量瓶配溶液时,若加水超过刻度线,立即用滴定管吸出多余液体。
13. 利用右图所示装置进行下列实验,能得出相应实验结论的是( )浓硫酸具有脱水性、氧化性与可溶性钡盐均可以生二、非选择题:包括必考题和选考题两部分。
第26题~第28题为必考题,每个试题考生都必须做答。
绝密★启封并使用完毕前试题类型:2014年普通高等学校招生全国统一考试理科综合能力测试注意事项:1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。
2.答题前,考生务必将自己的姓名、准考证号填写在本试题相应的位置。
3.全部答案在答题卡上完成,答在本试题上无效。
4.考试结束后,将本试题和答题卡一并交回。
7.下列过程没有发生化学反应的是()A.用活性炭去除冰箱中的异味B.用热碱水清除炊具上残留的油污C.用浸泡过高锰酸钾溶液的硅藻土保鲜水果D.用含硅胶、铁粉的透气小袋与食品一起密封包装8.四联苯的一氯代物有()A.3种B.4种C.5种D.6种9.下列反应中,反应后固体物质增重的是()A.氢气通过灼热的CuO粉末B.二氧化碳通过Na2O2粉末C.铝与Fe2O3发生铝热反应D.将锌粒投入Cu(NO3)2溶液10.下列图示实验正确的是()A.除去粗盐溶液中的不溶物B.碳酸氢钠受热分解C .除去CO 气体中的CO2气体D .乙酸乙酯制备演示实验11.一定温度下,下列溶液的离子浓度关系式正确的是( )A .pH=5的H 2S 溶液中,c(H +)=c(HS -)=1×10-5mol•L -1B .pH=a 的氨水溶液,稀释10倍后,其pH=b ,则a=b+1C .pH=2的H2C2O4溶液与pH=12的NaOH 溶液任意比例混合:c(Na +)+c(H +)=c(OH -)+c(HC 2O 4-)D .pH 相同的①CH 3COONa ②NaHCO 3③NaClO 三种溶液的c(Na +):①>②>③12.2013年3月我国科学家报道了如图所示的水溶液锂离子电池体系,下列叙述错误的是( )A .a 为电池的正极B .电池充电反应为LiMn 2O 4=Li 1-x Mn 2O x +xLiC .放电时,a 极锂的化合价发生变化D .放电时,溶液中Li +从b 向a 迁移13.室温下,将1mol 的CuSO 4•5H 2O (s )溶于水会使溶液温度降低,热效应为△H 1,将1mol的CuSO 4(s)溶于水会使溶液温度升高,热效应为△H 2,CuSO 4•5H 2O 受热分解的化学方程式为:CuSO 4•5H 2O(s) =====△CuSO 4(s)+5H 2O(l),热效应为△H 3。
则下列判断正确的是( ) A .△H 2>△H 3 B .△H 1<△H 3 C .△H 1+△H 3=△H 2 D .△H 1+△H 2>△H 326.(13分)在容积为1.00L 的容器中,通入一定量的N 2O 4,发生反应N 2O 4(g)2NO 2(g),随温度升高,混合气体的颜色变深。
回答下列问题:(1)反应的△H 0(填“大于”“小于”);100℃时,体系中各物质浓度随时间变化如上图所示。
在0~60s 时段,反应速率v(N 2O 4)为 mol·L -1·s -1反应的平衡常数K 1为 。
(2)100℃时达到平衡后,改变反应温度为T ,c(N 2O 4)以0.0020 mol·L -1·s -1的平均速率降低,经10s 又达到平衡。
a:T 100℃(填“大于”“小于”),判断理由是 。
b:列式计算温度T 是反应的平衡常数K 2(3)温度T 时反应达平衡后,将反应容器的容积减少一半,平衡向 (填“正反应”或“逆反应”)方向移动,判断理由是 。
27、(15分)铅及其化合物可用于蓄电池,耐酸设备及X 射线防护材料等。
回答下列问题:(1)铅是碳的同族元素,比碳多4个电子层,铅在周期表的位置为 ① 周期,第 ②族:PbO 2的酸性比CO 2的酸性 ③ (填“强”或“弱”)。
(2)PbO 2与浓盐酸共热生成黄绿色气体,反应的化学方程式为 ④ 。
(3)PbO 2可由PbO 与次氯酸钠溶液反应制得,反应的离子方程式为⑤ :PbO 2也可以通过石墨为电极,Pb(NO 3)2和Cu(NO 3)2的混合溶液为电解液电解制取。
阳极发生的电极反应式 ⑥ ,阴极观察到的现象是⑦ :若电解液中不加入Cu(NO 3)2,阴极发生的电极反应式⑧ ,这样做的主要缺点是 ⑨ 。
(4)PbO 2在加热过程发生分解的失重曲线如下图所示,已知失重曲线上的a 点为样品失重4.0%(-×100%a 样品起始质量点固体质量样品起始质量)的残留固体,若a 点固体表示为PbO 2或mPbO 2·nPbO 2,列式计算x 值和m:n 值 ⑩ 。
28.(15分)某小组以CoCl 2·6H 2O 、过氧化氢、液氨、氯化铵固体为原料,在活性炭催化下,合成了橙黄色晶体X 。
为确定其组成,进行如下实验:①氨的测定:精确称取w g X ,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量10% NaOH 溶液,通入水蒸气,将样品溶液中的氨全部蒸出,用V 1 ml c 1 mol·L -1的盐酸溶液吸收。
蒸氨结束后取下接收瓶,用c 2 mol·L -1 NaOH 标准溶液滴定过剩的HCl ,到终点时消耗V 2 ml NaOH 溶液。
②氯的测定:准确称取样品X 配成溶液后用AgNO 3标准溶液滴定,K 2CrO 4溶液为指示剂,至出现砖红色沉淀不在消失为终点(Ag 2CrO 4为砖红色)。
回答下列问题:(1)装置中安全管的作用原理是 。
(2)用NaOH 标准溶液滴定过剩的HCl 时,应使用 式滴定管,可使用的指示剂为 。
(3)样品中氨的质量分数表达式为 。
(4)测定氨前应该对装置进行气密性检验,若气密性不好测定结果将 (填“偏高”或“偏低”)。
(5)测定氯的过程中,使用棕色滴定管的原因是 :滴定终点时,若溶液中c(Ag +)=2.0×10-5 mol·L -1 ,c(CrO 42-)为 mol·L -1 mol 。
(已知:Ksp(Ag 2CrO 4)= 1.12×10-12)(6)经测定,样品X 中钴、氨和氯的物质的量之比为1:6:3,钴的化合价为 。
制备X 的化学方程式为 :X 的制备过程中温度不能过高的原因是 。
36.[化学选修——2:化学与技术](15分) 1.水2.安全管3.10%NaOH 溶液4.样品液5.盐酸标准溶液6.冰盐水1264A 35B C氨的测定装置(已省略加热和夹持装置)将海水淡化和与浓海水资源化结合起来是综合利用海水的重要途径之一。
一般是先将海水淡化获得淡水,再从剩余的浓海水中通过一系列工艺提取其他产品。
回答下列问题:(1)下列改进和优化海水综合利用工艺的设想和做法可行的是(填序号)。
①用混凝法获取淡水②提高部分产品的质量③优化提取产品的品种④改进钾.溴.镁的提取工艺(2)采用“空气吹出法”从浓海水中吹出Br2,并用纯碱吸收。
碱吸收溴的主要反应是:Br2+Na2CO3+H2O 3+6NaHCO3,吸收1mol Br2时转移的电子为mol。
(3)海水提镁的一段工艺流程如下图:浓海水的主要成分如下:该工艺过程中,脱硫阶段主要反应的离子方程式为,产品2的化学式为,1L浓海水最多可得到产品2的质量为g。
(4)采用石墨阳极.不锈钢阴极电解熔融的氯化镁,发生反应的化学方程式为;电解时,若有少量水存在会造成产品镁的消耗,写出有关反应的化学方程式。
37、[化学——选修3:物质结构与性质](15分)周期表前四周期的元素a、b、c、d、e,原子序数依次增大。
A的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族;e的最外层只有1个电子,但次外层有18个电子。
回答下列问题:(1)b、c、d中第一电离能最大的是(填元素符号),e的价层电子轨道示意图为。
(2)a和其他元素形成的二元共价化合物中,分子呈三角锥形,该分子的中心原子的杂化方式为;分子中既含有极性共价键、又含有非极性共价键的化合物是(填化学式,写出两种)。
(3)这些元素形成的含氧酸中,分子的中心原子的价层电子对数为3的酸是;酸根呈三角锥结构的酸是。
(填化学式)(4)e和c形成的一种离子化合物的晶体结构如图1,则e离子的电荷为。
(5)这5种元素形成的一种1:1型离子化合物中,阴离子呈四面体结构;阳离子吴轴向狭长的八面体结构(如图2所示)。
该化合物中阴离子为,阳离子中存在的化学键类型有;该化合物加热时首先失去的组分是,判断理由是。
38.[化学—选修5:有机化学基础](15分)立方烷()具有高度的对称性、高致密性、高张力能及高稳定性等特点,因此合成立方烷及其衍生物成为化学界关注的热点。
下面是立方烷衍生物I的一种合成路线:回答下列问题:(1)C的结构简式为,E的结构简式为。
(2)③的反应类型为,⑤的反应类型为。
(3)化合物A可由环戊烷经三步反应合成:反应1的试剂与条件为:反应2的化学方程式为:反应3可用的试剂为。
(4)在I的合成路线中,互为同分异构体的化合物是(填化合物代号)。
(5)I与碱石灰共热可转化为立方烷,立方烷的核磁共振氢谱中有个峰。
(6)立方烷经消化可得到六硝基立方烷,其可能的结构有种。
答案7.A 8.C 9.B 10.D 11.D 12.C 13.BⅡ卷(一) 必考题26.(13分)(1) 大于 0.0010 0.36 mol·L -1(2)a :大于反应正方向吸热,反应向吸热方向进行,故温度升高b :K 2= (0.16 mol·L -1)2/(0.020 mol·L -1) =1.3 mol·L -1(3) 逆反应 对气体分子数增大的反应,增大压强平衡向逆反应方向移动27.(15分)(1) ①六 ②ⅣA ③ 弱(2)④PbO 2+4HCl(浓) =====△PbCl 2+Cl 2↑+2H 2O (3)⑤PbO+ClO -= PbO 2+Cl - ⑥ Pb 2++2H 2O - 2e - = PbO 2↓+ 4H +⑦石墨上包上铜镀层⑧Pb 2++2e - =Pb↓ ⑨不能有效利用Pb 2+(4)⑩x=2 -16%0.4239 =1.4 n m = 6.04.0= 32 28.(15分) (1)瓶A 中的压力过大时,安全管中的液面上升,使A 瓶中的压力稳定。
(2)碱 酚酞(或甲基红)(3)(4)偏低(5)防止硝酸银见光分解 2.8×10-3(6)+32CoCl 2 +NH 4Cl +10NH 3 + H 2O 2 = 2[Co(NH 3)6]Cl 3 + 2H 2O温度过高过氧化氢分解,氨气逸出36.[化学选修——2:化学与技术](15分)×100% (c 1V 1-c 2V 2)×10-3×17 w(1)②③④(2)35 (3)Ca 2++SO 42-= CaSO4↓ Mg(OH)2 69.6(4)37、[化学——选修3:物质结构与性质] (15分)(1) N( 2) sp 3 H 2O 2 N 2H 4(3)HNO 2 HNO 3 H 2SO 3(4)+1(5)H 2SO 4 共价键和配位键 H 2O H 2O 与Cu 2+的配位键比NH 3与Cu 2+的弱38.[化学—选修5:有机化学基础](15分) (1)(2)取代反应 消去反应(3) Cl 2/光照O 2/Cu (4) G 和H(5) 1(6) 3↑+22Cl Mg MgCl 电解Mg ↑++222H OH Mg O H 2)(高温。