化学反应与能量变化单元测试题(一)及答案
- 格式:doc
- 大小:93.50 KB
- 文档页数:5

&心学穴教肓2leduxom天津学大教育信息咨询有限公司TIANJIN XUEDA EDUCATION INFORMATION CONSULTING CO.,LTD高二化学选修4第章《化学反应与能量》单兀测试题姓名_____________ 考试时间:(60分钟,100分)2015/9/26 分数____________第I卷选择题(共48分)一、选择题(共12题,每小题只有1个选项符合题意,每小题4分,共48分)1. 2010年世界环境日,中国的主题是:低碳减排,绿色生活”号召公众从我做起,推进污染减排,践行绿色生活,为建设生态文明、构建环境友好型社会贡献力量。
下列有关做法不符合这一要求的是()。
A •在大力推广乙醇汽油的同时,研究开发太阳能电池和氢燃料电池汽车B •大力发展农村沼气,将废弃的农作物秸秆转化为清洁、高效的能源C. 研发高效低毒农药,降低蔬菜的农药残留量D. 以聚苯乙烯全面代替木材,生产包装盒、快餐盒等以减少木材的使用,保护森林2. 下列与化学反应能量变化相关的叙述正确的是()A .生成物总能量一定低于反应物总能量B .放热反应的反应速率总是大于吸热反应的反应速率C. 应用盖斯定律,可计算某些难以直接测量的反应焓变D. 同温同压下,H2(g) + Cl2(g)===2HCI(g)在光照和点燃条件下的AH不同3. 已知反应:① 101kPa 时,C(s) + 1/2O2(g) = CO (g) △ H1 = - 110.5kJ/mol②稀溶液中,H +(aq) + OH-(aq)=出0(1) △ H2=- 57.3kJ/mol下列结论正确的是()A .若碳的燃烧热用△ H3来表示,则△ H3<△ H1B .若碳的燃烧热用△ H3来表示,则△ 出>厶H1C.浓硫酸与稀NaOH溶液反应的中和热为57.3kJ/molD .稀醋酸与稀NaOH溶液反应生成1mol水,放出57.3kJ热量4. 生产液晶显示器的过程中使用的化学清洗剂NF3是一种温室气体,其存储能量的能力是CO2的12 000〜20 000倍,在大气中的寿命可长达740年之久,以下是几种化学键的键能:下列说法中正确的是()A .过程N2(g) T 2N(g放出能量B .过程N(g) + 3F(g) T NF(g)放出能量C.反应N2(g) + 3F2(g) T2NF(g)的AH>0D . NF3吸收能量后如果没有化学键的断裂与生成,仍可能发生化学反应5. 已知方程式2H2 (g)+ O2 ( g)= 2H2O (l) A H1=- 571.6kJ/mol,则关于方程式2H2O (l )= 2H2 ( g) + O2 (g) ;A H2= ?的说法正确的是()A .方程式中化学计量数表示分子数B .该反应的A H2大于零C.该反应A H2=- 571.6kJ/mol D .该反应与上述反应属于可逆反应6. 下列热化学方程式正确的是()A .甲烷的标准燃烧热为890.3 kJ mol -1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+ 2O2(g)===CO2(g)+ 2H2O(g)A H = - 890.3 kJ mol-1B. 500 C、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭容器中充分反应生成NH 3(g),放热19.3 kJ,其热化学方程式为:N2(g)+3H2(g). 催化剂.2NH3(g)-、500 C 30MPaA H = - 38.6 kJ mol 1C. 已知在120 C、101 kPa下,1 g H2燃烧生成水蒸气放出121 kJ热量,其热化学方程1120 C式为H2(g) + O2(g)=======H2O(g) AH = - 242 kJ/mol2101 kPaD. CO(g)的燃烧热是283.0 kJ mol-1,贝V 2CO2(g)===2CO(g) + O2(g)反应的AH = +283.0 kJ mol 17. 已知:① CH4(g) + 2O2(g)===CO2(g) + 2H2O(l) AH1;1CO(g) + 尹2(g) = CO2(g) △ H =与这些碳完全燃烧相比,损失的热量是A . 172.5 kJB . 1149 kJH 2S(g) + |O 2(g)=SO 2(g) + H 2O(g) A H 11H 2S(g) + 2O 2(g)=S(g) + H 2O(g) A H 3 则A H 4的正确表达式为()3A . A H 4 = 2(A H 1+ A H 2— 3A H 3)B . 3C . A H 4= 2( A H 1 + A H 2+ 3 A H 3)D .9.在36 g 碳不完全燃烧所得气体中,1C(s) + 2O 2(g) = CO(g) △ H = 2H 2S(g) + SO 2(g)==|s 2(g) + 2H 2O(g) A H 22S(g)=S 2(g)A H 43A H 4 = 2(3 A H 3- A H 1- A H 2)3A H 4 = 2( A H 1- A H 2- 3A H 3)C . 517.5 kJD . 283kJ10. S (单斜)和S (正交)是硫的两种同素异形体。

第六章《化学反应与能量》单元测试卷一、单选题(共15小题)1.已知氢气与溴蒸汽化合生成1 mol溴化氢时放出的能量51 kJ,1 mol H—H、Br—Br和H—Br键断裂时需要吸收的能量分别是436 kJ、a kJ和369 kJ则a为()A. 404B. 260C. 230D. 2002.关于化学反应的下列说法中正确的是()A.分子的种类和数目一定发生改变B.原子的种类和数目一定发生改变C.能量变化主要是由化学键变化引起的D.能量变化的大小与反应物的质量多少无关3.如图是以稀硫酸为电解质溶液的原电池装置,下列叙述正确的是()A.锌片上有气泡产生B.锌片为负极,铜片发生氧化反应C.电解质溶液中的H+向铜极移动D.电子流动方向:锌极→导线→铜极→电解质溶液→锌极4.一定温度下,恒容密闭容器中发生反应2NO2(g)2NO(g)+O2(g),达到平衡的标志是()①相同时间内,氧气的生成速率为n mol·L-1·s-1,二氧化氮的生成速率为2n mol·L-1·s-1①单位时间内生成n mol 氧气的同时生成2n mol的一氧化氮①混合气体的颜色不再变化①混合气体的密度保持不变①混合气体的平均相对分子质量不再改变①压强不再随时间变化而变化A. ①①①①B. ①①①C. ①①①D.全部5.银锌电池广泛用作各种电子仪器的电源,它的充电和放电过程可以表示为2Ag+Zn(OH)2Ag2O+Zn+H2O,其放电过程是原电池反应,在此电池放电时,负极上发生反应的物质是() A. AgB. Zn(OH)2C. Ag2OD. Zn6.鱼雷采用Al—Ag2O动力电池,以溶有氢氧化钾的流动海水为电解液,电池反应为2Al+3Ag2O +2KOH===6Ag+2KAlO2+H2O,下列说法错误的是()A. Ag2O为电池的正极B. Al在电池反应中被氧化C.电子由Ag2O极经外电路流向Al极D.溶液中的OH-向Al极迁移7.下列说法不正确的是()A.化学反应可分为吸热反应和放热反应B.化学反应中的能量变化都是以热能的形式表现出来C.化学反应的实质是旧键的断裂与新键的生成D.化学反应能量变化的实质是旧键断裂吸收的能量与新键形成释放的能量大小不同8.酒精燃烧的过程中,发生了能量的转化。
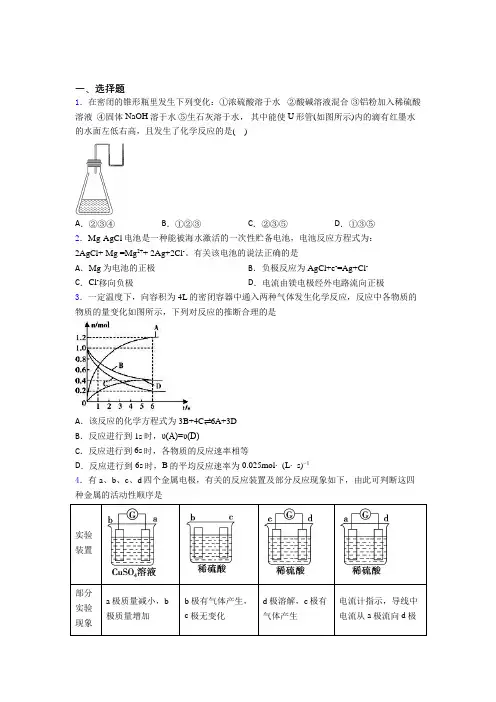
一、选择题1.在密闭的锥形瓶里发生下列变化:①浓硫酸溶于水②酸碱溶液混合③铝粉加入稀硫酸溶液④固体NaOH溶于水⑤生石灰溶于水,其中能使U形管(如图所示)内的滴有红墨水的水面左低右高,且发生了化学反应的是( )A.②③④B.①②③C.②③⑤D.①③⑤2.Mg-AgCl电池是一种能被海水激活的一次性贮备电池,电池反应方程式为:2AgCl+ Mg =Mg2++ 2Ag+2Cl-。
有关该电池的说法正确的是A.Mg为电池的正极B.负极反应为AgCl+e-=Ag+Cl-C.Cl-移向负极D.电流由镁电极经外电路流向正极3.一定温度下,向容积为4L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,下列对反应的推断合理的是A.该反应的化学方程式为3B+4C⇌6A+3DB.反应进行到1s时,υ(A)=υ(D)C.反应进行到6s时,各物质的反应速率相等D.反应进行到6s时,B的平均反应速率为0.025mol⋅(L⋅s)−14.有a、b、c、d四个金属电极,有关的反应装置及部分反应现象如下,由此可判断这四种金属的活动性顺序是实验装置部分实验现象a极质量减小,b极质量增加b极有气体产生,c极无变化d极溶解,c极有气体产生电流计指示,导线中电流从a极流向d极A.a>b>c>d B.b>c>d>a C.d>a>b>c D.a>b>d>c 5.一种以联氨(N2H4)为燃料的环保电池工作原理如图所示,电解质溶液显弱酸性,电池工作时产生稳定无污染的物质。
下列说法正确的是()A.在电极M充入N2H4,每消耗1molN2H4,会有4molH+通过质子交换膜B.该燃料电池工作时,化学能只能转化为电能C.N极的电极反应式为O2+2H2O+4e-=4OH-D.电极总反应式为N2H4+O2=N2+2H2O,电解质溶液的pH始终不变6.根据一定条件下NH4Cl有关转化过程的能量变化,判断下列说法不正确的是NH4Cl(s)=N(g)+4H(g)+Cl(g) △H1 NH4Cl(s)=NH3(g)+H(g)+Cl(g) △H2NH (g)+Cl-(g)=NH4Cl(s) △H3 Cl(g)+e-=Cl- (g) △H44A.△H4<△H1B.△H3<0C.△H1<△H2D.相同条件下,NH4Br和NH4I也进行类似转化,NH4Br的△H2比NH4I的大7.下列物质间的反应,其能量变化符合图示的是A.由Zn和稀H2SO4制氢气B.甲烷的燃烧C.Ba(OH)2·8H2O晶体和NH4Cl晶体混合搅拌D.氧化钙和水反应8.向某密闭容器中加入0.3 mol A、0.1 molC、和一定量的B三种气体。

一、选择题1.在密闭容器中进行反应:N2 + 3H2 (g) 高温、高压催化剂2NH3 (g),当反应达到限度时,下列说法正确的是 ( )A.N2、H2完全转化为NH3B.此时反应已停止C.生成2mol 氨气的同时,同时生成3mol H2D.氮气、氢气、氨气的浓度相等2.在温度不变的条件下,密闭容器中发生如下反应:N2+3H2⇌2NH3,下列叙述能够说明反应已经达到平衡状态的是A.容器中N2、H2、NH3共存B.N2与NH3的浓度相等C.容器中N2、H2、NH3的物质的量之比为1∶3∶2D.反应容器中压强不随时间变化3.“盐水动力”玩具车的电池以镁片、活性炭为电极,向极板上滴加食盐水后电池便可工作,电池反应为2Mg+O2+2H2O=2Mg(OH)2。
下列关于该电池的说法错误的是A.镁片作为正极B.食盐水作为电解质溶液C.电池工作时镁片逐渐被消耗D.电池工作时实现了化学能向电能的转化4.下列实验方案不能达到相应实验目的的是实验目的实验方案A制备CuSO4用稀硫酸、过氧化氢和铜粉反应B 加快酸性KMnO4与H2C2O4溶液的反应速率加入一粒黄豆大的MnSO4固体C 除去NaC1固体表面的少量KC1杂质用饱和NaC1溶液洗涤D 探究浓度对反应速率的影响向盛有同体积、不同浓度NaHSO3溶液的试管中同时加入同体积、同浓度NaC1O溶液,观察现象A.A B.B C.C D.D5.pH相同的盐酸和醋酸溶液分别与Zn反应,若最终Zn完全溶解且得到的H2的质量相等。
则下列判断正确的是( ) A .反应所需时间:醋酸>盐酸 B .整个反应阶段的平均速率: 醋酸>盐酸 C .反应起始的速率:醋酸<盐酸D .参加反应的Zn 质量:醋酸>盐酸6.根据一定条件下NH 4Cl 有关转化过程的能量变化,判断下列说法不正确的是 NH 4Cl(s)=N(g)+4H(g)+Cl(g) △H 1 NH 4Cl(s)=NH 3(g)+H(g)+Cl(g) △H 24NH +(g)+Cl -(g)=NH 4Cl(s) △H 3 Cl(g)+e -=Cl - (g) △H 4A .△H 4<△H 1B .△H 3<0C .△H 1<△H 2D .相同条件下,NH 4Br 和NH 4I 也进行类似转化,NH 4Br 的△H 2比NH 4I 的大7.利用反应6NO 2+8NH 3 == 7N 2+12H 2O 构成原电池的装置如图所示。

第六章《化学反应与能量》单元测试卷一、单选题(共15小题)1.一定温度下,一定体积的容器中发生反应:A(s)+3B(g)2C(g)+2D(g),下列描述中能说明该反应达到平衡的是()①A的质量不发生变化①单位时间内生成a mol A,同时消耗2a mol C①容器中的压强不再变化①混合气体的密度不再变化①n(A)①n(B)①n(C)①n(D)=1①3①2①2①B的浓度不变A. ①①①①B. ①①①①C. ①①①D. ①①①2.在2 L的密闭容器中,投入0.2 mol N2和0.6 mol H2,发生可逆反应N2(g)+3H2(g)2NH3(g),2 min后,生成0.04 mol NH3,下列说法中正确的是()A. 2 min内H2的反应速率为0.01 mol·L-1·min-1B.若2 min后,往容器中通入0.2 mol的氩气,则生成NH3的反应速率加快C.若混合气体的密度不再改变,则反应达到平衡状态D.若单位时间内有3 mol H—H键断裂,同时就有6 mol N—H键断裂,则反应达到平衡状态3.达康书记又追问环保局长:那么垃圾处理中,能随便焚烧吗?焚烧垃圾会降低GDP的。
在焚烧垃圾过程中发生了()A.吸热的非氧化还原反应B.吸热的氧化还原反应C.放热的非氧化还原反应D.放热的氧化还原反应4.碳酸钙与稀盐酸的反应为放热反应,生成二氧化碳的量与反应时间的关系如图所示。
下列结论不正确的是()A.反应开始2分钟内平均反应速率最大B.反应4分钟后平均反应速率最小C.反应开始4分钟内温度对反应速率的影响比浓度大D.反应4分钟后反应速率下降的原因是盐酸浓度逐渐减小5.小明做完铜锌原电池(稀硫酸为电解质溶液)的实验后,得出的下列结论和认识中正确的是() A.构成原电池正极和负极的材料必须是两种金属B.由铜、锌作电极与稀硫酸溶液组成的原电池中铜是负极C.电子通过稀硫酸溶液由锌流向铜,通过溶液时被氢离子得到而放出氢气D.铜锌原电池工作时,溶液的酸性降低6.据报道,某国一集团拟在太空建造巨大的集光装置,把太阳光变成激光用于分解海水制氢:2H2O===2H2↑+O2↑。

2021春(新教材)人教必修第二册第6章《化学反应与能量》含答案(新教材)必须第二册第6章化学反应与能量一、选择题1、某温度下,浓度都是1 mol·L-1的两种气体X2和Y2,在密闭容器中反应生成气体Z。
反应2 min后,测得参加反应的X2为0.6 mol·L-1,用Y2的变化表示的反应速率v(Y2)=0.1 mol·L-1·min-1,生成的c(Z)为0.4 mol·L-1,则该反应的化学方程式为()A.X2+2Y2===2XY2B.2X2+Y2===2X2YC.3X2+Y2===2X3Y D.X2+3Y2===2XY32、如图所示,对于A生成C的反应,下列所得结论正确的是()A.该反应为吸热反应B.该反应进行时,一定有能量放出C.A物质比C物质稳定D.该反应肯定很容易,不需要加热就可以进行3、镍镉(Ni—Cd)可充电电池可以发生如下反应:Cd(OH)2+2Ni(OH)2充电放电Cd+2NiO(OH)+2H2O,由此可知,该电池的负极材料是()A.Cd B.NiO(OH) C.Cd(OH)2D.Ni(OH)24、如图所示的装置中,M为活动性顺序位于氢之前的金属,N为石墨棒。
关于此装置的下列叙述中,不正确的是()A.N上有气体放出B.M为负极,N为正极C.是化学能转变为电能的装置D.导线中有电流通过,电流方向是由M到N5、可用于电动汽车的铝-空气燃料电池,通常以NaCl溶液或NaOH溶液作为电解质溶液,铝合金为负极,空气电极为正极。
下列说法正确的是()A.以NaCl溶液或NaOH溶液为电解液时,正极反应都为O2+2H2O+4e-===4OH -B.以NaOH溶液为电解液时,负极反应为Al+3OH--3e-===Al(OH)3↓C.以NaOH溶液为电解液时,电池在工作过程中电解质溶液的碱性保持不变D.电池工作时,电子通过外电路从正极流向负极6、在反应C(s)+CO2(g)2CO(g)中,不可能使反应速率明显增大的措施是()A.增大压强B.升高温度C.增大CO2的浓度D.增加碳的量7、我国锅炉燃煤采用沸腾炉逐渐增多,采用沸腾炉的好处在于()A.增大煤燃烧时的燃烧热B.减少炉中杂质气体(如SO2等)的形成C.使化学反应更容易进行D.使燃料燃烧充分,从而提高燃料的利用率8、在一定条件下,反应N2+3H22NH3在10 L的恒容密闭容器中进行,测得2 min内氮气的物质的量由20 mol减少到8 mol,则2 min后氮气的平均反应速率为()A.等于0.6 mol·L-1·min-1B.小于0.8 mol·L-1·min-1C.大于0.6 mol·L-1·min-1D.小于0.6 mol·L-1·min-19、下列实验现象或图像信息不能充分说明相应的化学反应是放热反应的是()选项 A B C D反应装置或图像实验现象或图反应开始后,反应物总能量反应开始后,温度计的水银像信息针筒活塞向右移动高于生成物总能量甲处液面低于乙处液面柱不断上升4溶液,产生H2的体积V(L)与时间t(min)的关系是()11、如图为锌、铜水果电池装置示意图,下列说法正确的是()A.铜片为负极,发生还原反应B.锌片上发生还原反应:Zn-2e-===Zn2+C.该装置将电能转变为化学能D.电子由锌片沿导线流向铜极12、.镁燃料电池具有能量高、使用安全方便、原材料来源丰富、成本低、燃料易于储运等特点。
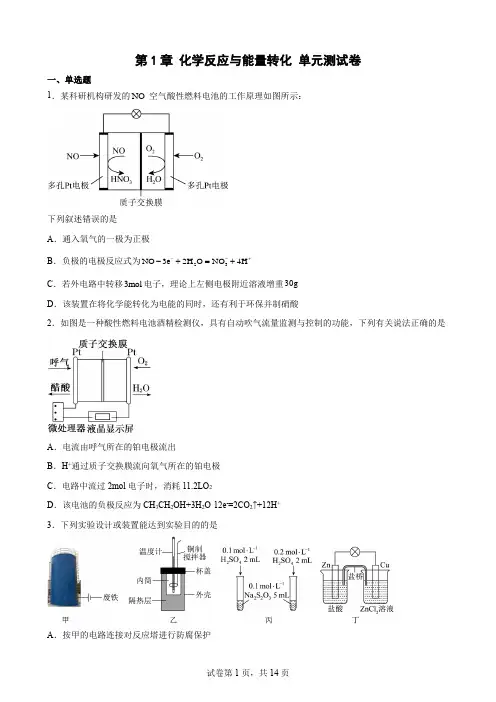
第1章 化学反应与能量转化 单元测试卷一、单选题1.某科研机构研发的NO -空气酸性燃料电池的工作原理如图所示:下列叙述错误的是 A .通入氧气的一极为正极B .负极的电极反应式为23NO 3e 2H O NO 4H --+-+=+C .若外电路中转移3mol 电子,理论上左侧电极附近溶液增重30gD .该装置在将化学能转化为电能的同时,还有利于环保并制硝酸2.如图是一种酸性燃料电池酒精检测仪,具有自动吹气流量监测与控制的功能,下列有关说法正确的是A .电流由呼气所在的铂电极流出B .H +通过质子交换膜流向氧气所在的铂电极C .电路中流过2mol 电子时,消耗11.2LO 2D .该电池的负极反应为CH 3CH 2OH+3H 2O -12e -=2CO 2↑+12H + 3.下列实验设计或装置能达到实验目的的是A .按甲的电路连接对反应塔进行防腐保护B .用乙测定中和反应的反应热C .用丙探究硫酸浓度对化学反应速率的影响D .按丁设计锌铜“双液原电池”实现化学能持续转化为电能4.在熔融盐体系中,通过电解2TiO 和2SiO 获得电池材料()TiSi ,电解装置如图,下列说法正确的是A .石墨电极为阴极,发生氧化反应B .电极A 的电极反应:2228H TiO SiO 8e TiSi 4H O =+-++++C .该体系中,石墨优先于Cl -参与反应D .电解时,阳离子向石墨电极移动5.用如图所示装置电解氯化钠溶液(X 、Y 是碳棒)。
下列判断正确的是A .Y 电极为正极B .X 电极为阳极C .Y 电极表面发生氧化反应D .X 电极表面有氯气生成6.锌铁液流电池由于安全、稳定、电解液成本低等优点成为电化学储能热点技术之一、下图为以24Zn(OH)/Zn -和3466Fe(CN)/Fe(CN)--作为电极氧化还原电对的碱性锌铁液流电池放电时工作原理示意图。
已知:聚苯并咪唑(PBI )膜允许-OH 离子通过。

第四章《化学反应与电能》测试题一、单选题(共15题)1.我国首创的海洋电池以铝板、铂网作电极,海水为电解质溶液,空气中的氧气与铝反应产生电流。
电池总反应为:4A1+3O 2+6H 2O=4Al(OH)3,下列判断正确的是 A .该电池通常只需要更换铂网就可继续使用 B .正极反应为:O 2+H 2O+2e -=2OH -C .铂电极做成网状,可增大与氧气的接触面积D .电池工作时,电子由铂网沿导线流向铝板2.化学与生产、生活密切相关。
下列与化学有关的事实及其相关的反应方程式书写正确的是 2PbSO 放电充电3CaCO (s)SO +222NO (g)2H O(l)+2Mg(s)+Cl (g)A .AB .BC .CD .D3.镁—次氯酸盐燃料电池的工作原理如图所示,该电池的总反应为Mg+ClO -+H 2O=Mg(OH)2+Cl -。
下列有关说法正确的是A .该燃料电池中镁作负极,发生还原反应B .该电池工作时,正极a 附近的pH 将不断增大C .负极的电极反应式为ClO -+2e -+H 2O=Cl -+2OH -D .b 电极发生还原反应,电路中每转移0.1mol 电子,理论上生成0.1molCl - 4.用如图装置设计Mg 与O 2的原电池反应,下列说法错误的是A .电子的移动方向由a 经外电路到bB .溶液中的OH −从a 极向b 极移动C .负极反应式为:Mg−2e −+2OH −=Mg(OH)2D .活性炭代替炭可以加快O 2在正极上的反应速率5.电解100mL 含c(H +)=0.3mol/L 的下列溶液,当电路中通过0.04mol 电子时,理论上析出金属质量最大的是A .0.10mol ·L -1Ag +B .0.20mol ·L -1Cu 2+C .0.30mol ·L -1Zn 2+D .0.40mol ·L -1Pb 2+6.湿法炼锌时,用于进行电解的电解液是含有Fe 2+、Fe 3+、Cu 2+ 、Cl -等杂质离子的硫酸锌溶液,必须除去。

化学必修II《化学反应与能量》单元测验(A卷)班别姓名学号常用相对原子质量:Al:27 Fe:56 Cu:64 Zn:65一、选择题(每题4分,共36分,每题只有一个选项)1.近年来,广州市的大部分公交车及部分出租车已采用LPG(液化石油气)作为汽车的燃料,其主要目的在于A.防止石油短缺 B.降低成本 C.减少对大气的污染 D.加大发动机的动力2.对化学反应限度的叙述,错误的是A.任何可逆反应都有一定的限度B. 化学反应的限度是不可改变的C.化学反应的限度与时间的长短无关D. 化学反应达到限度时,正逆反应速率相等3.一定条件下,可逆反应2A B+3C,在四种状态中处于平衡状态的是正反应速率逆反应速率A υA=2mol/(l.min)υB=2mol/(l.min)B υA=2mol/(l.min)υC=2mol/(l.min)C υA=1mol/(l.min)υB=2mol/(l.min)D υA=1mol/(l.min)υC=1.5mol/(l.min)4.A、B、C都是金属,A和C分别放入同浓度的稀硫酸中,A的反应速率比C快,A与B 和硫酸铜溶液组成原电池时,A的质量增加。
A、B、C三种金属的活动性顺序为A.A>B>C B.A>C>B C.B>A>C D.C>A>B5.在一个密闭容器中,盛有N2和H2,它们的起始浓度分别是1.8 mol·L-1和5.4 mol·L-1,在一定的条件下它们反应生成NH3,10min后测得N2的浓度是0.8 mol·L-1,则在这10min 内NH3的平均反应速率是A.0.1mol.L-1.min-1B.0.2mol.L-1.min-1C.0.3mol.L-1.min-1D.0.6mol.L-1.min-1 6.下列说法正确的是A. 凡是放热反应的发生均无需加热B.凡是需要加热后才能发生的反应是吸热反应C.伴有能量变化的物质变化都是化学变化D. 物质发生化学反应都伴随着能量变化7.下列叙述正确的是:A.酸和碱发生中和反应放出的热叫中和热B.1 mol酸和1 mol碱反应放出的热叫中和热C.酸碱中和生成1 mol 水放出的热叫中和热D.任何反应生成1 mol水放出的热叫中和热8.某原电池的总反应的离子方程式是:Zn+Cu2+=Zn2++Cu,此反应的原电池的正确组成是正极负极电解质溶液A Cu Zn HClB Zn Cu CuS04C Cu Zn CuS04D Cu Zn ZnCl29.甲烷燃料电池的化学反应为CH4 + 2O2 = CO2 + 2H2O,其中1个电极反应式为2O2 + 8H4 + 8e- = 4H2O下列叙述不正确...的是A.CH4通入负极 B.O2通入正极 C.正极发生氧化反应D.负极的电极反应式为:CH4 + 2H2O – 8e- = CO2 + 8H+二.选择题(每题只有一至两个选项,每题4分,共20分)10.关于燃料充分燃烧的说法不正确的是A.空气量越大越好 B.固体燃料块越大越好C.液体燃料燃烧时可以雾状喷出 D.温度必须达到着火点11.金刚石和石墨都是碳的单质,石墨在一定条件下可以转化为金刚石并需要吸收能量。

第一章化学反应及能量变化测评卷(B卷)(时间:90分钟满分:100分)第Ⅰ卷(选择题,共45分)一、选择题(每小题3分,共45分)1.下列说法不正确的是()A.在指定状态下各物质的焓值都是确定且是唯一的B.当同一个化学反应以不同的过程完成时,反应的焓变是不同的C.如果一个化学方程式通过其他几个化学方程式相加减而得到,则该反应的焓变为相关化学反应的焓变的代数和D.对于一个化学反应,无论经过哪些步骤从反应物变成生成物,反应的焓变是一样的解析:本题主要考查对盖斯定律的理解。
由于在指定状态下各物质的焓值是确定且是唯一的,因此无论经过哪些步骤从反应物变成生成物,反应焓变是一样的,即反应的焓变只与起始和终了状态有关,而与过程无关。
由盖斯定律知一个化学方程式是由其他几个方程式相加减得到,则该反应的焓变为几个化学方程式相加减得到,则该反应的焓变为几个化学方程式焓变的代数和。
答案:B2.已知1 mol白磷(s)转化成1 mol红磷(s),放出18.39 kJ热量,又知:4P(白,s)+5O2(g)===2P2O5(g)ΔH14P(红,s)+5O2(g)===2P2O5(g)ΔH2则ΔH1和ΔH2的关系正确的是()A.ΔH1=ΔH2B.ΔH1>ΔH2C.ΔH1<ΔH2D.无法确定解析:由题意知P(白,s)===P(红,s)ΔH=-18.39 kJ/mol,由盖斯定律知此方程式可由4P(白,s)+5O2(g)===2P2O5(s)ΔH1与4P(红,s)+5O2(g)===2P2O5(s)ΔH2相减除以4得到,即-18.39kJ/mol=ΔH1-ΔH24,ΔH1-ΔH2<0,得ΔH1<ΔH2。
答案:C3.科学家发现,不管化学反应是一步完成还是分几步完成,该反应的热效应是相同的。
已知在25℃,105 Pa时,1 mol石墨和1 mol 一氧化碳完全燃烧生成二氧化碳时的放热分别是ΔH=-393.5 kJ/mol和ΔH=-283 kJ/mol,下列说法或方程式正确的是() A.在相同条件下:2C(石墨,s)+O2(g)===2CO(g)ΔH=-110.5 kJ/molB.1 mol石墨不完全燃烧,生成CO2和CO混合气体时,放热504.0 kJC.在相同条件下,C(石墨,s)+CO2(g)===2CO(g)ΔH=+172.5 kJ/molD.已知金刚石不如石墨稳定,则石墨转变为金刚石需要吸热解析:由题意知,①C(石墨)+O2(g)===CO2(g)ΔH=-393.5 kJ/mol,②2CO(g)+O2(g)===2CO2(g)ΔH=-566.0 kJ/mol。

第六章《化学反应与能量》测试题一、单选题(共15题)1.在某一化学反应中,反应物A的浓度在10s内从0.8mol·L-1变为0.2mol·L-1,则在这10s内A的化学反应速率为A.0.02mol·L-1B.0.02mol·L-1·s-1C.0.06mol·L-1·s-1D.0.06mol·L-1·min-1 2.下列变化中属于吸热反应的是①冰融化成水①胆矾受热分解①三氧化硫溶于水①高锰酸钾分解制取氧气①生石灰与水反应生成熟石灰①石灰石高温分解①CO2+C 高温2CO①Ba(OH)2•8H2O与固体NH4Cl混合A.①①①①B.①①①①①C.①①①①①①D.①①①①①3.由下列实验中的操作及现象,不能够推出相关结论的是A.A B.B C.C D.D4.将镁片、铝片用导线连接并插入NaOH溶液中,关于该装置的叙述正确的是A.该装置将电能转化为化学能B.该装置使用的铝片不需要处理表面的氧化膜C.电子由镁片向铝片移动D.NaOH溶液更换为任何电解质溶液,铝片上都发生氧化反应5.一定条件下,可逆反应2A(g)B(g)+3C(g)处于平衡状态的是A .AB .BC .CD .D6.下列化学变化中,属于吸热反应的是 A .锌粒与稀硫酸的反应 B .()22Ba OH 8H O ⋅与4NH Cl 晶体的反应 C .甲烷在空气中燃烧D .Na 与2H O 反应7.已知某反应为放热反应,对于该反应,下列说法正确的是 A .生成物的总能量大于反应物的总能量B .已知石墨比金刚石稳定,可能是石墨转化为金刚石的反应C .可能是一个燃烧反应D .一定是在常温就能发生的反应8.化学与科技生产、生活环境等密切相关,下列说法错误的是 A .市售暖贴的发热原理是利用原电池加快氧化还原反应速率 B .电热水器用镁棒防止内胆腐蚀,利用了外加电源的阴极保护法 C .减少燃煤的使用改用风能、太阳能等能源,符合“低碳生活”理念 D .明矾能用于净水是因为铝离子水解生成的氢氧化铝胶体具有吸附性 9.下列说法中正确的是A .吸热反应的活化能大于放热反应的活化能B .用NaOH 溶液滴定盐酸,以甲基橙作指示剂,滴定终点时溶液pH=7C .向NaOH 溶液中滴加等体积等物质的量浓度的盐酸,溶液的导电性逐渐减小D .用23Na CO 溶液处理水垢中4CaSO 的离子方程式:2233Ca CO CaCO +-+=↓ 10.SO 2既是大气主要污染物之一,又在生产生活中具有广泛应用,如可生产SO 3并进而制得硫酸等,其反应原理为:2SO 2(g)+O 2(g)=2SO 3(g) ΔH=-196.6 kJ·mol -1。
一、选择题1.过量铁与少量稀硫酸反应,为了加快反应速率,但是又不影响生成氢气的总量,可以采取的措施是A.加入适量NaCl溶液B.加入适量的水C.加入几滴硫酸铜溶液D.再加入少量稀硫酸2.三元电池成为2019年我国电动汽车的新能源,其充电时总反应为:LiNi x Co y Mn z O2+6C(石墨)=Li1-a Ni x Co y Mn z O2+Li a C6,其电池工作原理如图所示,两极之间有一个允许特定的离子X通过的隔膜。
下列说法正确的是A.允许离子X通过的隔膜属于阴离子交换膜B.充电时,A为阴极,Li+被氧化C.可从无法充电的废旧电池的石墨电极中回收金属锂D.放电时,正极反应式为Li1-a Ni x Co y Mn z O2+aLi++ae-=LiNi x Co y Mn z O23.为比较Fe3+和Cu2+对H2O2分解反应的催化效果,甲、乙两位同学分别设计了如图甲、乙所示的实验。
下列叙述中不正确的是A.通过图甲实验产生气泡的快慢能比较Fe3+和Cu2+对H2O2分解的催化效果B.用图乙装置判断反应速率的大小,可测定反应产生相同气体体积所需的时间C.图乙实验中,如t s内针筒收集到V mL气体,则用O2表示的反应速率为VtmL/sD.为检查图乙装置的气密性,可关闭A处活塞,将注射器活塞推进一定距离后松开活塞,观察活塞是否回到原位4.根据一定条件下NH4Cl有关转化过程的能量变化,判断下列说法不正确的是NH4Cl(s)=N(g)+4H(g)+Cl(g) △H1 NH4Cl(s)=NH3(g)+H(g)+Cl(g) △H2 4NH (g)+Cl-(g)=NH4Cl(s) △H3 Cl(g)+e-=Cl- (g) △H4A .△H 4<△H 1B .△H 3<0C .△H 1<△H 2D .相同条件下,NH 4Br 和NH 4I 也进行类似转化,NH 4Br 的△H 2比NH 4I 的大 5.一定温度下,在一个容积为2L 的密闭容器中发生反应4A(s)3B(g)2C(g)D(g)++,经2min 达到平衡状态,此时B 反应了1.2mol ,下列说法正确的是A .充入2N (不参与反应)使压强增大可加快反应速率B .0~2min 内,A 的平均反应速率为110.4mol L min --⋅⋅C .平衡状态时,B 、C 的反应速率相等D .0~2min 内,C 的平均反应速率为110.2mol L min --⋅⋅6.资料显示:自催化作用是指反应产物之一使该反应速率加快的作用。
高二化学选修第一章化学测试题IMB standardization office【IMB 5AB- IMBK 08- IMB 2C】高二年级周考选修4第一章《化学反应与能量》单元测试题本试卷分第一部分(选择题)和第二部分(非选择题),满分100分,考试时间90分钟。
第一部分选择题(共45分)一选择题(1~12小题每小题只有一个正确选项,每小题2分,共24分,13~19每小题有一个或者两个选项正确,错选或多选不得分,每小题3分,共21分)1.未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生。
下列属于未来新能源标准的是()①天然气②煤③核能④石油⑤太阳能⑥生物质能⑦风能⑧氢能A.①②③④B.⑤⑥⑦⑧C.③⑤⑥⑦⑧D.③④⑤⑥⑦⑧2.下列变化属于吸热反应的是().①液态水气化②将胆矾加热变为白色粉末③浓硫酸稀释④氯酸钾分解制氧气⑤生石灰与水反应生成熟石灰⑥水煤气反应⑦二氧化碳与赤热的炭反应生成一氧化碳A.①④⑦B.②③⑥C.①④⑤D.②④⑥⑦3.下列反应中生成物总能量高于反应物总能量的是()A.碳酸钙受热分解B.乙醇燃烧C.铝粉与氧化铁粉末反应D.氧化钙溶于水4.已知:H2(g)+F2(g)===2HF(g)ΔH=-270kJ·mol-1,下列说法正确的是()A.常温常压下,氟化氢气体分解成的氢气和的氟气吸收270kJ热量B.1mol氢气与1mol氟气反应生成2mol液态氟化氢放出的热量小于270kJC.相同条件下,1mol氢气与1mol氟气的能量总和高于2mol氟化氢气体的能量D.2molH-F键的键能比1molH-H键和1molF-F键的键能之和小于270kJ5.下列热化学方程式中△H代表燃烧热的是()A、CH4(g)+3/2O2(g)=2H2O(l)+CO(g)△H1B、S(s)+3/2O2(g)=SO3(s)△H2C、C6H12O6(s)+6O2(g)=6CO2(g)+6H2O(l)△H3D、2CO(g)+O2(g)=2CO2(g)△H46.下列热化学方程式正确的是(注:H的绝对值均正确)()A.C2H5OH(l)+3O2(g)==2CO2(g)+3H2O(g);△H=—mol(燃烧热)B.NaOH(aq)+HCl(aq)==NaCl(aq)+H2O(l);△H=—mol(中和热)C.S(s)+3/2O2(g)==SO3(g);△H=—mol(反应热)D.2NO2==O2+2NO;△H=+mol(反应热)7、下列图像分别表示有关反应的反应过程与能量变化的关系据此判断下列说法中正确的是()A.石墨转变为金刚石是放热反应B.红磷比白磷稳定C.S(g)+O2(g)===SO2(g)ΔH1;S(s)+O2(g)===SO2(g)ΔH2;则ΔH1>ΔH2D.CO(g)+H2O(g)===CO2(g)+H2(g)ΔH>08、已知:Fe2O3(s)+3/2C(s)=3/2CO2(g)+2Fe(s)ΔH1C(s)+O2(g)=CO2(g)ΔH2则4Fe(s)+3O2(g)=2Fe2O3(s)的△H是()ΔH1+3ΔΔH2-2ΔH1ΔH1-3Δ2ΔH2-ΔH19.根据以下3个放热反应的热化学方程式:2H2S(g)+3O2(g)=2SO2(g)+2H2O(l)△H=Q1kJ/mol2H2S(g)+O2(g)=2S(s)+2H2O(l)△H=Q2kJ/mol2H2S(g)+O2(g)=2S(s)+2H2O(g)△H=Q3kJ/mol判断Q1、Q2、Q3三者关系正确的是()A.Q1>Q2>Q3B.Q1>Q3>Q2C.Q3>Q2>Q1D.Q2>Q1>Q310.已知1g氢气完全燃烧生成水蒸气时放出热量121kJ,且氧气中1molO=O键完全断裂时吸收热量496kJ,水蒸气中1molH—O键形成时放出热量463kJ,则氢气中1molH—H键断裂时吸收热量为().A.920kJB.557kJC.436kJD.188kJ11.已知:(1)Zn(s)+1/2O2(g)=ZnO(s)△H=-mol(2)2Ag(s)+1/2O2(g)=Ag2O(s)△H=-mol则Zn(s)+Ag2O(s)=ZnO(s)+2Ag(s)的△H等于()A.-mol B.-molC.-mol D.+mol12.热化学方程式C(s)+H2O(g)CO(g)+H2(g);△H=+mol表示(13.)14.A.碳和水反应吸收能量15.B.1mol碳和1mol水反应生成一氧化碳和氢气,并吸收热量16.C.1mol固态碳和1mol水蒸气反应生成一氧化碳气体和氢气,并吸热17.D.1个固态碳原子和1分子水蒸气反应吸热13.下列说法或表示法正确的是()A.等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多B.由C(石墨)→C(金刚石)ΔH=+119kJ·mol—1可知,石墨比金刚石稳定C.在稀溶液中:H++OH-===H2OΔH=-·mol—1,若将含1molCH3COOH的醋酸溶液与含1molNaOH的溶液混合,放出的热量小于D.在101kPa时,2gH2完全燃烧生成液态水,放出热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)===2H2O(l)ΔH=+·mol—114、下列热化学方程式正确的是(注:H的绝对值均正确)() A.C2H5OH(l)+3O2(g)==2CO2(g)+3H2O(g);△H=—mol(燃烧热)B.NaOH(aq)+HCl(aq)==NaCl(aq)+H2O(l);△H=—mol(中和热)C.S(s)+O2(g)==SO2(g);△H=—mol(反应热)D.2NO2==O2+2NO;△H=+mol(反应热)15、下列说法中正确的是()A.在化学反应过程中,发生物质变化的同时不一定发生能量变化B .破坏生成物全部化学键所需要的能量大于破坏反应物全部化学键所需要的能量时,该反应为吸热反应C .生成物的总能量大于反应物的总能量时,反应吸热,ΔH >0D .ΔH 的大小与热化学方程式的计量数有关 16.已知热化学方程式:①CO (g )+21O 2(g )=CO 2(g )ΔH=·mol -1 ②H 2(g )+21O 2(g )=H 2O (g );ΔH=·mol -1则下列说法正确的是()A .H 2的燃烧热为·mol -1B .由反应①、②可知右图所示的热化学方程式为 CO (g )+H 2O (g )=CO 2(g )+H 2(g ) ΔH=·mol -1C .H 2(g )转变成H 2O (g )的化学反应一定要释放能量D .根据②推知反应H 2(g )+21O 2(g )=H 2O (l );ΔH >·mol -117.下列说法中,正确的是( )A .在化学反应过程中,发生物质变化的同时不一定发生能量变化B .破坏生成物全部化学键所需要的能量大于破坏反应物全部化学键所需要的能量时,反应为吸热反应 C .反应产物的总焓大于反应物的总焓时,反应吸热,ΔH >0 D .ΔH 的大小与热化学方程式的计量系数无关 18.下列反应属于吸热反应的是 ()A .C 6H 12O 6(葡萄糖aq )+6O 26CO 2+6H 2OB .CH 3COOH +KOH =CH 3COOK +H 2OC .A+B =C+D ;ΔH <0D .破坏生成物全部化学键所需要的能量小于破坏反应物全部化学键所需要的能量 19.强酸与强碱的稀溶液发生中和反应的热效应为:H +(aq )+OH -(aq )=H 2O (l )△H =-·mol -1。
第二章《化学键化学反应与能量》综合练习2019.04.03一、单选题(每小题只有一个正确答案)1.镁燃料电池具有比能量高、使用安全方便、原材料来源丰富、成本低、燃料易于贮运等特点。
研究的燃料电池可分为镁—空气燃料电池、镁—海水燃料电池、镁—过氧化氢燃料电池、镁—次氯酸盐燃料电池。
如图为镁—次氯酸盐燃料电池的工作原理图,下列有关说法不正确的是( )A.放电过程中OH-移向正极B.电池的总反应式为Mg+ClO-+H2O Mg(OH)2↓+Cl-C.镁燃料电池中镁均为负极,发生氧化反应D.镁—过氧化氢燃料电池,酸性电解质中正极反应为H2O2+2H++2e-2H2O2.如图所示,大试管里充满某混合气体,置于光亮处,将滴管里的水挤入大试管后,烧杯中的水会进入大试管,大试管里的气体可能是()AN2、H2;BCO、O2;CNO2、O2;DCH4、Cl2.3.已知甲烷燃料电池的总反应方程式为CH4+2O2CO2+2H2O,其中1个电极的反应式为2O2+ 8H++8e-4H2O,下列叙述不正确的是( )A.通入甲烷的一极为负极 B.通入氧气的一极为正极C.正极发生氧化反应 D.负极的电极反应式为CH4+2H2O-8e-CO2+8H+4.下列各项中,不属于一次能源的是( )A.风能 B.电能 C.太阳能 D.核能5.下列电子式书写正确的是( )A. B. C. D.6.下列变化过程,能放出热量的过程有( )①液态水变成水蒸气②酸碱中和反应③浓硫酸稀释④固体氢氧化钠溶于水⑤H2在Cl2中燃烧⑥灼热的炭与CO2的反应⑦NH4Cl晶体与Ba(OH)2·8H2O混合搅拌A. 2个 B. 3个 C. 4个 D. 5个7.下列说法中正确的是( )A.高温高压条件下发生的反应一定是吸热反应B.常温常压下即能发生的反应一定是放热反应C.氨的催化氧化反应实验中移开加热装置后铂丝保持红热,表明该反应是放热反应D.化合反应都是放热反应,分解反应都是吸热反应8.在如图所示的装置中,a的金属活动性比氢强,b为碳棒,关于此装置的各种叙述中不正确的是( )A.碳棒上有气体放出,溶液的酸性减弱 B. a是正极,b是负极C.导线中有电子流动,电子从a极到b极 D. a极上的电极反应式为Zn-2e-Zn2+9.共价键、离子键和范德华力是构成物质时粒子间的不同作用力。
细心整理第一章《化学反响与能量》单元测试题本试卷分选择题和非选择题两局部,共 7 页,总分值 150 分,考试用时 90 分钟。
可能用到的原子量:H1 C12N14O16S32第一局部选择题〔共 90 分〕一、选择题〔此题包括 10 小题,每题 4 分,共 40 分,每题只有一个选项符合题意〕 1.以下表达正确的选项是 A .电能是二次能源B.水力是二次能源 C .自然气是二次能源D.水煤气是一次能源2.以下说法正确的选项是A. 物质发生化学变化都伴随着能量变化 B .任何反响中的能量变化都表现为热量变化C .伴有能量变化的物质变化都是化学变化 D .即使没有物质的变化,也可能有能量的变化3. 将来能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生。
以下属于将来能源标准的是①自然气②煤③核能④石油⑤太阳能⑥生物质能⑦风能⑧氢能A .①②③④B.⑤⑥⑦⑧C .③⑤⑥⑦⑧D.③④⑤⑥⑦⑧4. 以下各组热化学方程式中,△H >△H 的是①C(s)+O (g)===CO 1 (g)△H 2C(s)+O (g)===CO(g)△H22122②S(s)+O(g)===SO (g)△H S(g)+O (g)===SO (g)△H 221222③H (g)+O (g)===H O(l)△H 2H (g)+O (g)===2H O(l)△H22 2 1 2 2 2 2④CaCO (s)===CaO(s)+CO (g)△H CaO(s)+H O(l)===Ca(OH) (s)△H321222A .①B .④C .②③④D .①②③5. H 2(g)+Cl 2(g)=2HCl(g)△ H =―184.6kJ·mol -1,则反响 HCl(g)=H 2(g)+Cl 2(g)的△ H 为 A .+184.6kJ·mol -1B .―92.3kJ·mol -1 C .―369.2kJ·mol -1D .+92.3kJ·mol -16.以下反响中生成物总能量高于反响物总能量的是A .碳酸钙受热分解B .乙醇燃烧细心整理细心整理C.铝粉与氧化铁粉末反响D.氧化钙溶于水7.25℃、101kPa 下,2g 氢气燃烧生成液态水,放出 285.8kJ 热量,表示该反响的热化学方程式正确的选项是A.2H (g)+O (g)==2H O(1)△H=―285.8kJ/mol2 2 2B.2H (g)+O (g)==2H O(1)△H=+571.6kJ/mol2 2 2C.2H (g)+O (g)==2H O(g)△H=―571.6kJ/molD.H 2 (g)+O 2 (g)==H 2O(1)△H=―285.8kJ/mol2 2 28.氢气、一氧化碳、辛烷、甲烷的热化学方程式分别为:H (g)+O2(g)=H2O(l)△H=-285.8kJ/mol2CO(g)+O(g)=CO2(g)△H=-283.0kJ/mol 2C H (l)+25 O (g)=8CO (g)+9H O(l)△H=-5518kJ/mol8 18 2 2 2 2CH (g)+2O (g)=CO (g)+2H O(l)△H=-89.3kJ/mol4 2 2 2一样质量的氢气、一氧化碳、辛烷、甲烷完全燃烧时,放出热量最少的是A.H (g)B.CO(g)2C.C H (l)D.CH(g)8 18 49.热化学方程式:SO(g)+O2(g) SO2(g)△H=―98.32kJ/mol,在容器中充入32molSO2和 1molO2充分反响,最终放出的热量为A.196.64kJB.196.64kJ/molC.<196.64kJD.>196.64kJ10.:CH(g)+2O (g)==CO (g)+2H O(1)△H=―Q KJ/mol4 2 2 2 12H (g)+O (g)==2H O(g)△H=―Q KJ/mol2 2 2 22H (g)+O (g)==2H O(1)△H=―Q KJ/mol2 2 2 3常温下,取体积比为4:1的甲烷和氢气的混合气体11.2L〔已折合成标准状况〕,经完全燃烧后恢复至常温,则放出的热量为多少KJA.0.4Q +0.05Q B.0.4Q +0.05Q1 3 1 2C.0.4Q +0.1Q D.0.4Q +0.1Q1 3 1 2二、选择题〔此题包括 10 小题,每题 5 分,共 50 分。
一、选择题1.在密闭容器中进行反应:N2 + 3H2 (g) 高温、高压催化剂2NH3 (g),当反应达到限度时,下列说法正确的是 ( )A.N2、H2完全转化为NH3B.此时反应已停止C.生成2mol 氨气的同时,同时生成3mol H2D.氮气、氢气、氨气的浓度相等2.下列有关化学反应速率的说法正确的是A.用铁片和稀硫酸反应制取氢气时,改用98%的浓硫酸可以加快产生氢气的速率B.100mL2mol/L的盐酸跟锌片反应,加入适量的氯化钠溶液,反应速率不变C.NH3的催化氧化是一个放热的反应,所以,升高温度,反应的速率减慢D.在一定温度下固定容积的容器中,发生SO2的催化反应,充入He,反应速率不变3.有a、b、c、d四个金属电极,有关的反应装置及部分反应现象如下,由此可判断这四种金属的活动性顺序是实验装置部分实验现象a极质量减小,b极质量增加b极有气体产生,c极无变化d极溶解,c极有气体产生电流计指示,导线中电流从a极流向d极A.a>b>c>d B.b>c>d>a C.d>a>b>c D.a>b>d>c4.N2O和CO是环境污染性气体,可在Pt2O+表面转化为无害气体,其反应为:N2O(g)+CO(g)CO2(g)+N2(g)ΔH,有关化学反应的物质变化过程如图1所示,能量变化过程如图2所示,下列说法正确的是()A.由图1、2可知ΔH=ΔH1+ΔH2=ΔE2-ΔE1B.反应中加入Pt2O+可使反应的焓变减小C.由图2可知正反应的活化能小于逆反应的活化能D.1molN2O和1molCO的总能量小于1molCO2和1molN2的总能量5.三元电池成为2019年我国电动汽车的新能源,其充电时总反应为:LiNi x Co y Mn z O2+6C(石墨)=Li1-a Ni x Co y Mn z O2+Li a C6,其电池工作原理如图所示,两极之间有一个允许特定的离子X通过的隔膜。
下列说法正确的是A.允许离子X通过的隔膜属于阴离子交换膜B.充电时,A为阴极,Li+被氧化C.可从无法充电的废旧电池的石墨电极中回收金属锂D.放电时,正极反应式为Li1-a Ni x Co y Mn z O2+aLi++ae-=LiNi x Co y Mn z O26.一定温度下,将纯净的氨基甲酸铵(NH2COONH4)置于真空密闭恒容容器中(固体试样体积忽略不计)达到分解平衡:NH2COONH4(s)2NH3(g)+CO2(g)。
第一章《化学反应与能量》测试题原子量:H-1 O-16 C=12 Al-27 N-14 Ca- 40 V-51 Ni- 59 Cu-64一、单项选择题(每小题3分,共24分)1.下列反应属于吸热反应的是( )A. C 6H 12O 6(葡萄糖aq)+6O 2 6CO 2+6H 2OB. CH 3COOH+KOH CH 3COOK+H 2OC. 反应物的总能量大于生成物的总能量D .破坏反应物全部化学键所需能量大于破坏生成物全部化学键所需能量2.下列说法正确的是( )A .热化学方程式中,如果没有注明温度和压强,则表示反应热是在标准状况下测得的数据B .升高温度或加入催化剂,可以改变化学反应的反应热C .据能量守恒定律,反应物的总能量一定等于生成物的总能量D .物质发生化学变化一定伴随着能量变化3.下列各组热化学方程式中,△H 1>△H 2的是①C(s)+O 2(g)===CO 2(g) △H 1 C(s)+12O 2(g)===CO(g) △H 2②S(s)+O 2(g)===SO 2(g) △H 1 S(g)+O 2(g)===SO 2(g) △H 2③H 2(g)+12O 2(g)===H 2O(l) △H 1 2H 2(g)+O 2(g)===2H 2O(l) △H 2④CaCO 3(s)===CaO(s)+CO 2(g) △H 1 CaO(s)+H 2O(l)===Ca(OH)2(s) △H 2A .①B .②③④C .④D .①②③4. 已知H 2(g)+Cl 2(g)=2HCl(g) △H =―184.6kJ·m ol -1, 则反应HCl(g)=12H 2(g)+12Cl 2(g)的△H 为A .+184.6kJ·mol -1B .―92.3kJ·mol -1C .+92.3kJ·mol -1D .―369.2kJ·mol -15. 已知:(1)Zn (s )+12O 2(g )=== ZnO(s) ΔH= -348.3 kJ·mol -1,(2)2Ag(s)+ 12O 2(g )=== Ag 2O(s) ΔH= -31.0 kJ·mol -1,酶则Zn (s )+ Ag 2O(s) === ZnO(s)+ 2Ag(s)的ΔH 等于( )A . -317.3 kJ·mol -1B . -379.3 kJ·mol -1C .-332.8 kJ·mol -1D .317.3 kJ·mol -16. SF 6是一种优良的绝缘气体,分子结构中只存在S-F 键。
化学反应与能量变化单元测试题(一)
本试卷分第一部分(选择题)和第二部分(非选择题),满分100分,考试时间45分钟。
第一部分选择题(共42分)
一、选择题(每小题只有
..1.
个.选项符合题意,每小题4分,共24分。
)
1.下列说法不准确的是()A.任何化学反应都伴随有能量变化
B.化学反应中的能量变化都表现为热量的变化
C.反应物的总能量高于生成物的总能量时,发生放热反应
D.反应物的总能量低于生成物的总能量时,发生吸热反应
2.已知葡萄糖的燃烧热是2804 kJ/ mol,当它氧化生成1 g水时放出的热量是()A.26.0 kJ B.51.9 kJ C.155.8 kJ D.467.3 kJ 3.在四个不同的容器中,在不同的条件下实行合成氨反应,根据下列在相同时间内测得的结果判断,生成氨的反应速度最快的是( ) A.v(NH3)=0.1 mol/(L·min)
B.v(N2)=0.2 mol/(L·min)
C.v(N2)=0.1 mol/(L·min)
D.v(H2)=0.3 mol/(L·min)
4.下列热化学方程式中△H的值能表示可燃物的燃烧热的是()
A.H2 (g)+Cl2 (g)= 2HCl ;△H= -184.6kJ/mol
B.CH4(g)+2O2(g)= CO2(g)+2H2O(g);△H= -802.3kJ/mol
C.2H2(g)+O2(g)= 2H2O(l);△H= -571.6kJ/mol
D.CO(g)+1/2O2(g)= CO2(g);△H= -283kJ/mol
5. 已知:(1)Zn(s)+1
2
O2(g)===ZnO(s),ΔH= -348.3 kJ·mol-1,
(2)2Ag(s)+ 1
2
O2(g)=== Ag2O(s),ΔH= -31.0 kJ·mol-1,
则Zn(s)+ Ag2O(s)===ZnO(s)+ 2Ag(s)的ΔH等于()A.-379.3 kJ·mol-1B.-317.3 kJ·mol-1
C.-332.8 kJ·mol-1D.317.3 kJ·mol-1
6.根据以下3个热化学方程式:
2H2S(g)+3O2(g)=2SO2(g)+2H2O(l) △H=―Q1 kJ/mol
2H2S(g)+O2(g)=2S (s)+2H2O(l) △H=―Q2 kJ/mol
2H2S(g)+O2(g)=2S (s)+2H2O(g) △H=―Q3 kJ/mol
判断Q1、Q2、Q3三者关系准确的是( )
A.Q1>Q2>Q3 B.Q1>Q3>Q2C.Q3>Q2>Q1 D.Q2>Q1>Q3二、双项选择题(每小题有2.个.选项符合题意,错选0分,漏选3分,每小题6分,共18
分。
)
7.石墨与金刚石都是碳的单质,工业上常用石墨在一定条件下转化为金刚石的反应原理生产人造钻石.已知12 g石墨完全转化成金刚石时需要吸收E kJ的能量.则下列说法准确的是
( ) A.石墨不如金刚石稳定
B.金刚石不如石墨稳定
C.等质量的石墨和金刚石完全燃烧,金刚石放出的能量多
D.等质量的石墨和金刚石完全燃烧,石墨放出的能量多
8.将V1 mL 1.00 mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50 mL).下列叙述准确的是
( )
A.做该实验时环境温度不可能为22℃
B.该实验表明化学能能够转化为热能
C.NaOH溶液的浓度约为1.00 mol/L
D.该实验表明有水生成的反应都是放热反应
9. 下列热化学方程式准确的是(注:△H的绝对值均准确) ( )
A.C2H5OH(l)+3O2(g)==2CO2(g) +3H2O(g);△H=—1367.0 kJ/mol(燃烧热)
B.NaOH(aq) +HCl(aq) ==NaCl(aq) +H2O(l);△H=—57.3kJ/mol(中和热)
C.S(s) +O2(g) ==SO2(g);△H=—269.8kJ/mol(反应热)
D.2NO2==O2+2NO;△H=+116.2kJ/mol(反应热)
第二部分非选择题(共58分)
10.(10分,每空5分)
已知下列两个热化学方程式;
H2(g)+O2(g)==H2O(1) △H = -285.8 kJ·mol-1
C3H8(g)+5O2(g)==3CO2(g)+4H2O(1) △H = -2220.0 kJ·mol-1l
(1)实验测得H2和C3H8的混合气体共5mol,完全燃烧生成液态水时放热6264.5kJ,则混合气体中H2和C3H8的体积比是。
(2)已知:H2O(1)=H2O(g) △H = +44.0 kJ·mol-1,写出丙烷燃烧生成CO2和气态水的热式。
11.(12分,每空3分)
50 mL 0.50 mol/L盐酸与50 mL 0.55 mol/L NaOH溶液在如图
所示的装置中实行中和反应,通过测定反应过程中所放出的热量可计
算中和反应热.
回答下列问题:
(1)从实验装置上看,图中尚缺少的一种玻璃仪器是
________________________.
(2)大烧杯上如不盖硬纸板,求得的中和反应热数值________(填“偏大”、“偏小”、“无影响”).
(3)用相同浓度和体积的氨水代替NaOH溶液实行上述实验,测得的中和反应热数值会________(填“偏大”、“偏小”或“无影响”,下同);用50 mL 0.50 mol/L NaOH溶液实行上述实验,测得的中和反应热的数值会________.
12.(18分,每空3分)
在火箭推动器中装有还原剂肼(N2H4)和强氧化剂H2O2,当它们混合时,即产生大量的氮气和水蒸气,并放出大量的热量。
已知0.4mol液态肼和足量双氧水反应生成氮气和水蒸气时放出256.65KJ的热量。
(1)写出肼和过氧化氢的结构式肼______ ___,过氧化氢______
(2)上述反应应用于火箭推动剂,除释放出大量热量和快速产生大量气体外,还有一个很突出的优点是_____________________ _________。
(3)写出肼和双氧水反应的热化学方程式_____________________________。
(4)已知H2O(l)==H2O(g);△H=+44KJ/mol,则16g液态肼与足量双氧水反应生成氮气和液态水时,放出的热量是_________________。
(5)已知N2(g) + 2O2(g) == 2NO2(g);△H=+67.7KJ/mol,
N2H4(g) + O2(g) == N2(g)+2H2O(g);△H= —534KJ/mol,
则肼与NO2完全反应的热化学方程式为_______________________________。
13.(18分)红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g).反应过程和能量关系如图所示(图中的ΔH表示生成1 mol产物的数据).
根据上图回答下列问题:
(1)P和Cl2反应生成PCl3的热化学方程式是
______________________________________;(5分)
(2)PCl5分解成PCl3和Cl2的热化学方程式是
______________________________________;(5分)
(3)P和Cl2分两步反应生成1 mol PCl5的ΔH3=________,P和Cl2一起反应生成1 mol PCl5的ΔH4________ΔH3(填“大于”、“小于”或“等于”).(每空4分)
2012年下期高二化学单元测试题(一)
个.选项符合题意,每小题4分,共24分。
)
一、选择题(每小题只有
..1.
1、B
2、A
3、B
4、D
5、B
6、A
二、双项选择题(每小题有2.个.选项符合题意,错选0分,漏选3分,每小题6分,共18分。
)
7、BC 8、AB 9、BC
10.(10分)
(1)1:1(5分)
(2)C3H8(g)+5O2(g)===3CO2(g)+4H2O(g) △H=-2044.0 kJ·mol-1(5分)
11.(12分,每空3分)
(1)环形玻璃搅拌棒
(2)偏小
(3)偏小偏小
12.(18分,每空3分)
⑴
⑵产物为氮气和水,无污染
⑶N2H4(l) + 2H2O2(l) == N2(g)+4H2O(g);△H= —641.6KJ/mol,
⑷408.8KJ
⑸ 2N2H4(g) + 2NO2(g) == 3N2(g)+4H2O(g);△H= —1135.7KJ/mol,
13.(18分)
(1)3/2Cl2(g)+P(s)===PCl3(g) ΔH=-306 kJ/mol (5分)
(2)PCl5(g)===PCl3(g)+Cl2(g)ΔH=+93 kJ/mol (5分)
(3)-399 kJ/mol(4分)等于(4分)。