蛋白酪氨酸激酶小分子抑制剂
- 格式:ppt
- 大小:2.10 MB
- 文档页数:4


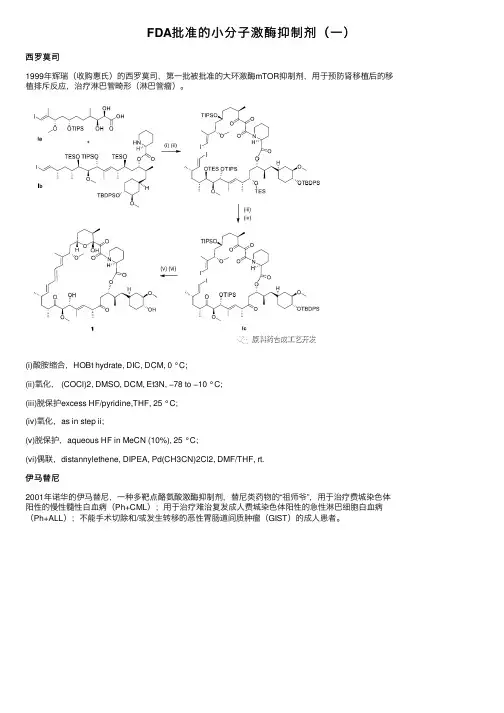
FDA批准的⼩分⼦激酶抑制剂(⼀)西罗莫司1999年辉瑞(收购惠⽒)的西罗莫司,第⼀批被批准的⼤环激酶mTOR抑制剂,⽤于预防肾移植后的移植排斥反应,治疗淋巴管畸形(淋巴管瘤)。
(i)酸胺缩合,HOBt hydrate, DIC, DCM, 0 °C;(ii)氧化, (COCl)2, DMSO, DCM, Et3N, −78 to −10 °C;(iii)脱保护excess HF/pyridine,THF, 25 °C;(iv)氧化,as in step ii;(v)脱保护,aqueous HF in MeCN (10%), 25 °C;(vi)偶联,distannylethene, DIPEA, Pd(CH3CN)2Cl2, DMF/THF, rt.伊马替尼2001年诺华的伊马替尼,⼀种多靶点酪氨酸激酶抑制剂,替尼类药物的“祖师爷”,⽤于治疗费城染⾊体阳性的慢性髓性⽩⾎病(Ph+CML);⽤于治疗难治复发成⼈费城染⾊体阳性的急性淋巴细胞⽩⾎病(Ph+ALL);不能⼿术切除和/或发⽣转移的恶性胃肠道间质肿瘤(GIST)的成⼈患者。
(i)羟醛缩合,NaOMe, PhMe, 25°C, 16 h;(ii)席夫碱,HNMe2, AcOH,PhMe, reflux, 1 h;(iii)亲核加成,NH2CN, HNO3, EtOH, reflux, 21 h;(iv)关环,NaOH, isopropanol, reflux, 12 h;(v) 还原,Pd/C, H2, THF,rt, 21 h;(vi) 酰基化,pyridine, rt, 24 h.吉⾮替尼2003年阿斯利康的吉⾮替尼,EGFR抑制剂,适⽤于具有表⽪⽣长因⼦受体(EGFR)基因敏感突变的局部晚期或转移性⾮⼩细胞肺癌(NSCLC)患者的治疗。
(i)蛋氨酸脱甲基,MeSO3H, L-methionine,100 °C;(ii)⼄酰化,Ac2O/pyridine;(iii)内酰胺氯代,SOCl2;(iv)SNAr反应,3-chloro-4-fluoroaniline;(v) 脱⼄酰基,NH4OH in MeOH;(vi)烷基化,N-morpholinopropyl bromide, K2CO3.厄洛替尼2004年基因泰克的厄洛替尼,EGFR抑制剂,⽤于两个或两个以上化疗⽅案失败的局部晚期或转移的⾮⼩细胞肺癌的三线治疗。

表皮生长因子受体酪氨酸激酶抑制剂的研究进展一、本文概述表皮生长因子受体(EGFR)酪氨酸激酶抑制剂(TKIs)是一类针对EGFR信号通路的关键药物,广泛应用于非小细胞肺癌、结直肠癌、头颈癌等多种癌症的治疗。
本文旨在综述近年来EGFR TKIs的研究进展,包括其作用机制、药物研发、临床应用以及面临的挑战等方面。
通过深入了解EGFR TKIs的研究现状和发展趋势,有望为癌症治疗提供新的思路和方法,进一步改善患者的生活质量和预后。
本文将从EGFR TKIs的作用机制出发,阐述其如何通过抑制EGFR 的酪氨酸激酶活性来阻断癌细胞的增殖和转移。
接着,我们将回顾EGFR TKIs的药物研发历程,介绍目前市场上主流的EGFR TKIs药物及其特点。
在此基础上,我们将重点关注EGFR TKIs在临床试验中的应用情况,包括其疗效、安全性以及耐药性等问题。
我们将探讨EGFR TKIs面临的挑战和未来发展方向,包括如何克服耐药性、提高治疗效果以及拓展新的适应症等。
通过本文的综述,我们希望能够为相关领域的研究者和临床医生提供有价值的参考信息,推动EGFR TKIs在癌症治疗中的进一步应用和发展。
二、EGFR-TK抑制剂的分类与机制表皮生长因子受体酪氨酸激酶抑制剂(EGFR-TK抑制剂)是近年来癌症治疗领域的重要突破,其通过抑制表皮生长因子受体(EGFR)的酪氨酸激酶活性,从而阻断细胞的生长、增殖和转移过程。
根据药物的作用机制和化学结构,EGFR-TK抑制剂主要分为两大类:可逆性抑制剂和不可逆性抑制剂。
可逆性抑制剂,如吉非替尼和厄洛替尼,能够与EGFR的ATP结合位点形成可逆性结合,从而竞争性地抑制酪氨酸激酶的活性。
这类药物对于EGFR敏感突变的非小细胞肺癌具有较好的疗效,但在长期治疗过程中,患者往往会出现耐药现象。
不可逆性抑制剂,如阿法替尼和奥希替尼,能够与EGFR的ATP 结合位点形成共价键,导致EGFR的永久性失活。

【一文囊括】中国已上市靶向药物使用特点写在前面靶向药物目前主要分为两类:大分子单抗类药物和小分子靶向药物,如激酶抑制剂。
小分子靶向药物主要集中在蛋白酪氨酸激酶剂,蛋白酶和其他种类。
蛋白酪氨酸激酶分为受体酪氨酸激酶以及非受体酪氨酸激酶。
受体酪氨酸激酶主要有表皮生长因子受体(EGFR),血管内表皮细胞生长因子受体(VEGFR)家族,血小板衍化生长因子受体(PDGFR)家族以及成纤维细胞生长因子受体(FGFR)家族。
非受体酪氨酸激酶主要有10大家族,其中明确与恶性肿瘤的发生密切相关的是四个家族:ABL家族,JAK家族,SRC家族以及FAK家族。
蛋白酶和其他种类主要包括:mTOR抑制剂,蛋白酶体抑制剂以及其他治疗多发性骨髓瘤的靶向药物。
(一)非小细胞肺癌(NSCLC)吉非替尼英文名:Gefitinib商品名:易瑞沙(Iressa)主要靶点:EGFR批准的适应症:EGFR敏感突变(19del或L858R)的局部晚期或转移性NSCLC。
推荐对所有患者的肿瘤组织进行EGFR突变检测,如果肿瘤组织标本不可评估,则可使用血液(血浆)标本中获取的循环肿瘤DNA(ctDNA)用于EGFR突变检测。
用法用量:本品的成人推荐剂量为250 mg/次,1日1次,口服,空腹或与食物同服。
如果有吞咽困难,可将片剂分散于半杯饮用水中(非碳酸饮料),不得使用其他液体。
将片剂丢入水中,无需压碎,搅拌至完全分散(约需10分钟),即刻饮下药液。
以半杯水冲洗杯子,饮下。
也可通过鼻-胃管给予该药液。
常见不良反应:皮疹、皮肤瘙痒、腹泻和甲沟炎等。
临床试验代表(中国人群研究):IPASS研究注意事项:与阿司匹林联合服用会减轻皮疹反应,若患者需同时使用华法林,则需频繁监测INR水平。
厄洛替尼英文名:Erlotinib商品名:特罗凯(Tarceva)主要靶点:EGFR,PDGFR,c-Kit批准的适应症:EGFR敏感突变(19del或L858R)的局部晚期或转移性NSCLC。
PI3K/AKT/mTORPI3K/AKT/mTOR是调节细胞周期的重要细胞内信号通路。
PI3K/AKT/mTOR信号通路与细胞的生长、存活、增殖、凋亡、血管生成、自吞噬过程中发挥着重要的生物学功能。
该通路是由磷脂酰肌醇3- 激酶(PI3Ks)、丝氨酸/苏氨酸蛋白激酶(Akt)和哺乳动物雷帕霉素靶蛋白(mTOR)组成。
PI3K/Akt/mTOR通路过程PI3K激活后产生PIP3, PIP3促使PDK1(phosphoinositide dependent kinase-1)磷酸化含有PH结构域的信号AKT蛋白(Ser308),从而活化AKT。
AKT有很多下游效应,可通过磷酸化多种酶、激酶和转录因子等下游因子,进而调节细胞的功能。
mTOR,是PI3K/Akt 下游的一种重要的丝氨酸-苏氨酸蛋白激酶,调节肿瘤细胞的自噬的经典通路。
PI3K/Akt/mTOR信号通路图按靶点分类:*PI3KPI3K,是一种胞内磷脂酰肌醇激酶,也具有丝氨酸/苏氨酸(Ser/Thr)激酶的活性。
能够通过PI3K诱发PIP3生成的激活因子,则能够激活Akt 信号途径,包括受体酪氨酸激酶、整合素、B 细胞和T 细胞受体、细胞因子受体、G 蛋白偶联受体等等。
*Akt又称PKB或Rac,是一种丝氨酸/苏氨酸特异性蛋白激酶B,在细胞存活和凋亡中起重要作用,如葡萄糖代谢、凋亡、细胞增殖、转录和细胞迁移。
Akt的Thr308可以被PDK1磷酸化,而被部分激活。
或者473位点上的丝氨酸被mTORC2磷酸化,激发Akt的完全酶活性。
*mTORmTOR是细胞生长和增殖的重要调节因子。
mTOR与其它蛋白质结合,形成两种不同蛋白质复合物,mTORC1和mTORC2,参与调节不同的细胞过程。
*GSK-3。
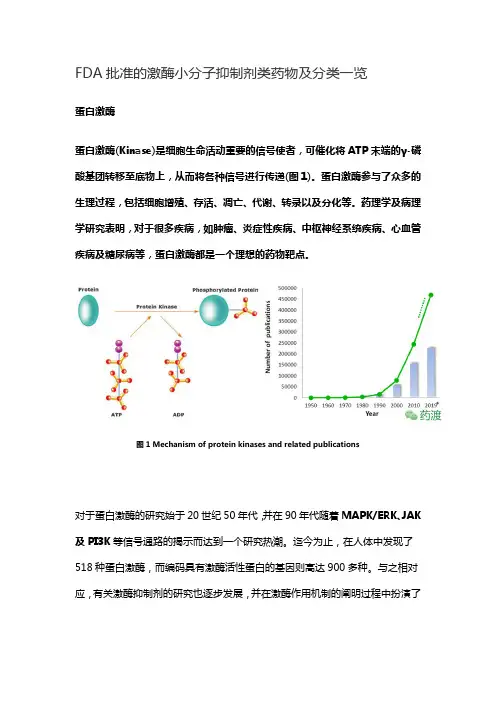
FDA批准的激酶小分子抑制剂类药物及分类一览蛋白激酶蛋白激酶(Kinase)是细胞生命活动重要的信号使者,可催化将ATP末端的γ-磷酸基团转移至底物上,从而将各种信号进行传递(图1)。
蛋白激酶参与了众多的生理过程,包括细胞增殖、存活、凋亡、代谢、转录以及分化等。
药理学及病理学研究表明,对于很多疾病,如肿瘤、炎症性疾病、中枢神经系统疾病、心血管疾病及糖尿病等,蛋白激酶都是一个理想的药物靶点。
图1 Mechanism of protein kinases and related publications对于蛋白激酶的研究始于20世纪50年代,并在90年代随着MAPK/ERK、JAK 及PI3K等信号通路的揭示而达到一个研究热潮。
迄今为止,在人体中发现了518种蛋白激酶,而编码具有激酶活性蛋白的基因则高达900多种。
与之相对应,有关激酶抑制剂的研究也逐步发展,并在激酶作用机制的阐明过程中扮演了重要角色,并成为重要的药物研究热点。
该领域研究的文献数量也是逐年上升,从侧面反映了其在基础研究和药物发现中的重要性。
蛋白激酶抑制剂及其分类过去的15年间,激酶抑制剂作为药物候选的研究取得了长足的进步,不论是基础研究还是在工业界。
在人体现有药物靶点里面,蛋白激酶家族成员占比高达10%(FDA批准药物分子靶点深度解读)。
2001年,第一个激酶抑制剂类药物Imatinib获得FDA批准,成为该领域发展的里程碑,此后十年该类药物以平均每年获批一种的速度稳步发展。
而在2012年1月至2015年2月期间,小分子激酶抑制剂类药物迎来爆发式发展,共有15种新药获得审批。
截至2016年12月底,共有31种小分子激酶抑制剂类药物获得审批,同时还有大量的化合物处于临床或临床前研究中。
除此之外,科研人员还解析了超过5000种的蛋白激酶或蛋白激酶-抑制剂复合体的晶体结构,且超过五分之一的人类蛋白激酶具有明确的小分子抑制剂。
因此,小分子激酶抑制剂已成为药物研发的一个热点领域。


新型蛋白酪氨酸激酶抑制剂类抗肿瘤药物的研究进展一、概要随着肿瘤发病机制的深入研究和抗肿瘤作用靶点的不断发现,蛋白酪氨酸激酶(PTK)作为信号转导中的关键酶,已经成为抗肿瘤药物研发的重要靶点之一。
PTK在细胞内的信号转导中扮演着至关重要的角色,与肿瘤细胞的生长、增殖、分化和凋亡密切相关。
新型蛋白酪氨酸激酶抑制剂类抗肿瘤药物的研究与开发,对于提高肿瘤治疗效果、改善肿瘤患者生活质量具有重要意义。
本文综述了近年来新型蛋白酪氨酸激酶抑制剂类抗肿瘤药物的研究进展。
我们介绍了PTK的分类及其作用机制,包括受体型和非受体型PTK在细胞信号转导中的作用。
我们详细阐述了PTK抑制剂的设计原理与策略,包括基于结构的小分子抑制剂、抗体药物以及多肽类药物等。
我们还介绍了PTK抑制剂在临床应用中的现状,包括已上市药物的疗效及安全性评价,以及正在研发的药物的临床试验进展。
通过对新型蛋白酪氨酸激酶抑制剂类抗肿瘤药物的深入研究,我们发现这类药物具有显著的抗肿瘤活性,并且在临床上已经取得了一定的疗效。
目前仍存在一些问题,如耐药性、副作用等,需要进一步研究和解决。
未来的研究方向将集中在优化药物结构、提高治疗效果、降低副作用等方面,以期开发出更加安全、有效的蛋白酪氨酸激酶抑制剂类抗肿瘤药物。
新型蛋白酪氨酸激酶抑制剂类抗肿瘤药物的研究进展迅速,为肿瘤治疗提供了新的思路和手段。
随着科学技术的不断进步和临床应用的不断推广,相信这类药物将在未来肿瘤治疗中发挥更加重要的作用。
1. 肿瘤治疗的挑战与现状作为一种复杂的生物学现象,一直是医学界面临的重大挑战。
尽管医学技术和治疗手段不断进步,肿瘤的治疗仍然面临着诸多难题。
肿瘤的异质性使得每一个病例都具有其独特的生物学特征,这为制定统一的治疗方案带来了极大的困难。
肿瘤细胞的快速增殖和侵袭性转移,使得传统的手术、放疗和化疗等手段往往难以彻底清除肿瘤细胞,且在治疗过程中容易产生耐药性。
许多抗肿瘤药物在杀灭肿瘤细胞的也会对正常细胞造成损伤,导致患者的生活质量下降。
小分子抑制剂的研究及其在药物设计中的应用药物研究一直是医学界的热门话题。
近年来,随着生物技术的不断发展和分子医学的兴起,小分子抑制剂成为了热门的研究领域之一。
小分子抑制剂通过特定作用于生物分子的结构域,抑制病理反应,从而达到治疗疾病的目的。
本文将从小分子抑制剂的定义、分类及其在药物设计中的应用等方面进行论述。
一、小分子抑制剂的定义和分类小分子抑制剂是指分子量在500Da以下的有机分子,可以特异性地结合目标蛋白的结构域,抑制其功能。
它是现代药物学领域中的一种新型药物。
由于小分子抑制剂分子结构简单、制备方法简便且具有高度的特异性,因此,广受研究者关注。
小分子抑制剂按其作用靶点可分为以下三类:酶抑制剂、受体拮抗剂和信号传导分子抑制剂。
它们的作用机制及应用范围也有所不同。
二、小分子抑制剂在药物设计中的应用小分子抑制剂在药物研发中的重要性越来越被人们所重视。
由于它分子结构的简单和制备的容易性,使得小分子抑制剂在药物设计中应用广泛,可应用于各种疾病的治疗。
1. 抗肿瘤药物小分子抑制剂在肿瘤治疗领域中得到了广泛应用。
例如,伊马替尼和吉非替尼等小分子抑制剂,可以作为Bcr-Abl酪氨酸激酶的抑制剂用于慢性粒细胞白血病的治疗,其疗效不言而喻。
2. 抗炎性药物小分子抑制剂还可以用于治疗与炎症有关的疾病。
例如,Celecoxib是一种选择性的COX-2抑制剂,可以阻止前列腺素合成,从而达到抗炎作用,常用于关节炎和其他疼痛情况。
3. 免疫调节药物除此之外,小分子抑制剂还可以作为免疫调节药物使用,以调节免疫系统的功能,从而达到抵抗某些疾病的目的。
例如,格列美脲是一种PPAR-gamma激动剂,可以用于调节糖尿病患者的胰岛素敏感性,减少血糖水平的升高。
三、小分子抑制剂的工程设计小分子抑制剂的研发需要借助计算模拟、药物化学、结构生物学等技术手段。
在工程设计阶段,小分子抑制剂应该满足以下特点:1. 高度特异性:小分子抑制剂应用于目标分子时,应该具有较高的特异性,以防止在体内出现副作用。
小分子多靶点酪氨酸激酶抑制剂原理【摘要】小分子多靶点酪氨酸激酶抑制剂具有重要的研究意义和临床应用前景。
本文首先介绍了小分子药物的多靶点作用机制,然后阐述了酪氨酸激酶在癌症治疗中的重要作用。
接着详细解析了小分子多靶点酪氨酸激酶抑制剂的原理,并总结了该领域的研究进展和应用前景。
未来,发展方向包括结构改进和亲和力提升,致力于提高药物的疗效和安全性。
本文强调了小分子多靶点酪氨酸激酶抑制剂在临床上的重要意义,为癌症患者提供新的治疗选择,具有巨大的发展潜力和医学意义。
【关键词】关键词:小分子多靶点酪氨酸激酶抑制剂、药物、多靶点作用、酪氨酸激酶、癌症治疗、研究背景、原理、研究进展、应用前景、未来发展方向、临床意义1. 引言1.1 小分子多靶点酪氨酸激酶抑制剂原理的意义小分子多靶点酪氨酸激酶抑制剂原理的意义可以从多个方面来解释。
这类药物的研究与开发可以为治疗多种疾病提供新的思路和途径。
传统药物往往只专注于单一的靶点,而小分子多靶点酪氨酸激酶抑制剂则可以同时作用于多个靶点,具有更广泛的生物活性和药理作用,有望在治疗复杂疾病中发挥更为显著的效果。
小分子多靶点酪氨酸激酶抑制剂的研究将有助于揭示药物与疾病之间更为复杂的相互作用机制。
通过深入研究药物与靶点之间的相互作用,可以更好地理解药物的作用机制和药效,为药物设计和改进提供更为有效的理论基础。
小分子多靶点酪氨酸激酶抑制剂的研究也将促进药物的个体化治疗。
不同患者对药物的反应存在差异,而多靶点抑制剂的个体化治疗策略可以根据患者的基因型、表型等个体特征来选择最适合的治疗方案,提高治疗效果并减少不良反应的发生。
小分子多靶点酪氨酸激酶抑制剂的研究具有重要的临床意义和应用前景。
1.2 小分子多靶点酪氨酸激酶抑制剂的研究背景随着癌症的高发率和治疗难度不断增加,寻找更有效的治疗方法成为当前医学领域的重要课题之一。
在癌症治疗领域,酪氨酸激酶被认为是一个重要的靶点,因为它参与了细胞的增殖、凋亡和转移等重要生物过程。