四川大学887物理化学考研历年真题及解析
- 格式:pdf
- 大小:424.09 KB
- 文档页数:5


若在几十年前,我们的父辈们或许还可以告诉我们,未来从事怎样的职业,会有很好的发展,不至于失业。
而如今,他们大抵再也不能如此讲话了,只因这个世界变化的如此之快,在这变化面前,他们大概比我们还要慌乱,毕竟他们是从传统的时代走来的,这个更新换代如此迅速的世界只会让他们措手不及。
但是,虽然如此,他们却可以告诉我们一条永远也不会过时的生存法则,那就是掌握不断学习的能力。
所以,经过各种分析考量我终于选择了考研这条路,当然,这是只是,千万条路中的一条。
只不过我认为,这条路可操作性比较强,也更符合我们当下国情。
幸运的是,我如愿以偿,考到自己希望的学校。
一年的努力奋斗,让自己从此走上了截然不同的人生道路。
秋冬轮回,又是一年春风吹暖。
在看到录取名单之后,我终于按捺不住发了我一条朋友圈,庆祝考研胜利。
当时收到了很多平时不太联系的同学,发来的询问信息,这也促使我想将我的备考经验写下来,希望真的可以帮助接下来备考的学弟学妹们!因为想要讲的话太多,所以这篇文章会比较长,希望各位能够一点点看完。
或许会从我的经验教训中找到自己的方向以及方法来面对考研。
在结尾处会奉上我的学习资料供大家下载。
四川大学物理学的初试科目为:(101)思想政治理论和(201)英语一(690)高等数学(微积分、级数)和(933)普通物理(光学、电磁学)参考书目为:1.四川大学《高等数学》2.贾起民《电磁学》3.郭永康《光学教程》先说说真题阅读的做法…第一遍,做十年真题【剩下的近三年的卷子考试前2个月再做】,因为真题要反复做,所以前几遍都是把自己的答案写在一张A4纸上,第一遍也就是让自己熟悉下真题的感觉,虐虐自己知道英语真题的大概难度,只做阅读理解,新题型完形填空啥的也不要忙着做,做完看看答案,错了几个在草稿纸上记下来就好了,也不需要研究哪里错了为什么会错…第一遍很快吧因为不需要仔细研究,14份的试卷,一天一份的话,半个月能做完吧,偷个懒一个月肯定能做完吧【第一遍作用就是练练手找到以前做题的感觉,千万不要记答案,分析答案…】ps:用书选择:木糖英语闪电单词+木糖英语真题。

至善川大考研网
往年四川大学高分子物理及化学考研真题收藏版共享
四川大学2007年攻读硕士学位研究生入学考试试题
考试科目:高分子物理及化学
科目代号:867
适用专业:材料加工工程、材料工程(专业学位)(详细资料至善川大考研网)
一、名词解释(每个2分,共10分)
1.高聚物的多分散性和分散指数
2.配位聚合和定向聚合
3.聚合反应程度和聚合度
4.自由基聚合物反应和逐步聚合反应
5.聚合物降解和解聚
二、简答题
1.请阐述各种自由基聚合反应方法的主要特点,说明各种方法制备的PVC树脂的主要用途和性能特点。
(30分)
2.写出合成两种单体的无规共聚物和嵌段共聚物的反应方程式(30分)
(1)苯乙烯和丁二烯
(2)丙烯和乙烯
(3)氯乙烯和醋酸乙烯酯
3.高分子熔体或者高分子溶液这种具有粘弹性的流体在流动时,由于其弹性的原因常会产生通常粘性流体所观察不到的现象,如Weissenberg现象和Barus效应,试着根据下图所示的两种情况进行分析,并从体系的弹性机理受到变形作用后的效果加以说明。
(25分)4.试着分析牛顿流体的流变行为,并绘出牛顿流体和非牛顿流体的流动曲线,并简单给出解释。
同时分析影响高聚物熔体剪切粘度的因素。
(25分)
5.与低分子物相比较,高分子材料的结晶行为有什么不同?为什么?在成型加工中可以利用那些场外条件来提高高分子材料的结晶度?(30)。

四 川 大 学2013年攻读硕士学位研究生入学考试试题考试科目:物理化学 考研鸟独家提供 一、选择题1、A,D2、C3、A考研鸟解析:理想气体的焓仅仅是温度的函数 4、C考研鸟解析:只有G 的偏摩尔量恰好是化学势 5、B考研鸟解析:BB B x RT p T p px RT T ln ),(ln)(*θ+=+=μμμθ),(*p T μ是纯气体B 在指定T ,p 时的化学势,显然这不是标准态。
6、B7、D考研鸟解析:Qp<0,表明焓变小于0,为放热反应 8、C 9、C10、B 11、A 12、B 考研鸟解析:13、B考研鸟解析:克拉贝龙方程(Clapegron eguation )VT HdT dp ∆∆=上式称克拉贝龙方程,即压力随温度的改变量与相变热及相变体积之间的关系。
适用:任何单组分的两相平衡体系。
14、B考研鸟解析:f=3-相数+1=4-相数 15、A 16、B考研鸟解析:科尔劳乌施根据实验结果发现,在浓度极稀时强电解质的Λm 与c 几乎成线性关系,且浓度在0.01mol·dm -3以下时, Λm 与c 之间有如下关系:)1( m c m β-ΛΛ∞=式中β在一定温度下,对于一定的电解质和溶剂来说是一个常数,将直线外推至与纵坐标相交处即得到溶液在无限稀释时的摩尔电导率m ∞Λ(又称为极限摩尔电导率)。
17、A考研鸟解析:注意A 和D 的区别,自己算一下,注意前面有价数乘积采用各种不同方法测定强电解质的离子平均活度系数γ± ,一般所得结果均能吻合得较好。
1921 年,Lewis 提出了“离子强度”的概念,并总结出了强电解质溶液γ± 与I 之间的经验关系。
离子强度的定义为2B BB12I mz =∑即可表述为离子强度I 等于溶液中每种离子i 的质量摩尔浓度(m i )乘以该离子的价数(z i )的平方所得诸项之和的一半。
Lewis 根据实验进一步指出,活度因子与离子强度的关系在稀溶液的范围内,符合如下经验式lg Iγ±=-常数Debye Huckel -理论所证实Debye Huckel -的极限定律:lg ||A z z γ±+-=-18、A 19、C 20、B 21、B考研鸟解析:'12h R gγρ=22、D 23、B 24、B 25、B二、填空题1、=;>2、=;<考研鸟解析:可逆过程熵变为0,实际气体由内压,绝热膨胀温度降低,类比范德华气体 3、>;< 4、>;<考研鸟解析:理想气体的内能和焓变仅仅是温度的函数,温度增加,内能和焓变增加,温度降低,内能和焓变降低 5、<,>考研鸟解析:Gibbs-Duhem公式—系统中偏摩尔量之间的关系如果在溶液中不按比例地添加各组分,则溶液浓度会发生改变,这时各组分的物质的量和偏摩尔量均会改变。

物理化学考研考试题及答案### 物理化学考研考试题及答案#### 一、选择题(每题2分,共20分)1. 热力学第一定律的数学表达式是:A. ΔU = Q - WB. ΔH = Q + WC. ΔS = Q/TD. ΔG = ΔH - TΔS2. 根据范特霍夫方程,反应的平衡常数K随温度变化的表达式是:A. dlnK/dT = ΔH/RB. dlnK/dT = ΔS/RC. dlnK/dT = -ΔH/RT^2D. dlnK/dT = -ΔS/RT^23. 以下哪个是理想气体状态方程?A. PV = nRTB. PV = nRT + aC. PV = nRT - aD. PV = nR(T + a)4. 阿伏伽德罗定律适用于:A. 所有气体B. 理想气体C. 固体和液体D. 所有物质5. 根据吉布斯自由能的定义,下列哪个表达式是正确的?A. ΔG = ΔH - TΔSB. ΔG = ΔU + PΔVC. ΔG= ΔU - TΔSD. ΔG = ΔH - PΔV6. 反应速率常数k与温度T的关系遵循:A. 阿累尼乌斯方程B. 范特霍夫方程C. 阿伏伽德罗定律D. 理想气体状态方程7. 以下哪个是热力学第二定律的表述?A. 能量守恒B. 热量不能自发地从低温物体传向高温物体C. 没有永动机D. 所有自发过程都伴随着熵的增加8. 根据化学平衡常数的定义,下列哪个表达式是正确的?A. K = [A][B]/[C][D]B. K = [C][D]/[A][B]C. K = [A]/[B]D. K = [B]/[A]9. 以下哪个是溶液的拉乌尔定律?A. P = XA * PAB. P = (XA * PA) + (XB * PB)C. P = (PA + PB) / 2D. P = (PA * PB)^0.510. 根据亨利定律,下列哪个表达式是正确的?A. P = kH * CB. P = kH * C^2C. P = kH / CD. P = kH * C^-1#### 二、简答题(每题10分,共30分)1. 简述热力学第二定律的两种表述方式,并说明它们之间的联系。

2014年四川大学887物理化学考研真题一、选择题(60分,每题2分)1.对于孤立体系中发生的实际过程,下列等式中不正确的是()。
A.W=0B.Q=0C.ΔU=0D.ΔH=02.对于一定量的单原子理想气体,当温度一定时,下列说法中不正确的是()。
A.内能的值一定B.焓的值一定C.熵的值一定D.热容的值一定3.对于封闭体系中发生的等压过程和等容过程,下列说法中不正确的是()。
A.等压过程有Q p=ΔHB.等容过程有Q V=ΔUC.Q p与Q V都是状态函数D.Q p与Q V都不是状态函数4.对于理想气体的绝热过程,下列说法中正确的是()。
A.绝热可逆膨胀过程有ΔU=0B.绝热可逆压缩过程有ΔS=0C.绝热可逆膨胀过程有ΔH=0D.绝热可逆压缩过程有ΔG=05.对于理想气体,其混合过程的热力学函数的变化为()。
A.Δmix H=0,Δmix V=0,Δmix G<0B.Δmix H<0,Δmix V=0,Δmix G=0C.Δmix G=0,Δmix S=0,Δmix H<0D.Δmix G=0,Δmix H=0,Δmix S>06.对于理想溶液,其混合过程的热力学函数的变化为()。
A.Δmix H=0,Δmix S=0,Δmix G<0B.Δmix H=0,Δmix G=0,Δmix S>0C.Δmix V=0,Δmix S=0,Δmix H<0D.Δmix V=0,Δmix H=0,Δmix S>07.关于逸度和逸度系数,下列说法中正确的是()。
A.逸度又称为校正压力B.逸度系数与温度无关C.逸度又称为实际压力D .逸度系数与压力无关8.关于活度和活度系数,下列等式中不正确的是( )。
A .a B =p B /p B * B .γB =a B /x B C .0lim 1B B x γ→=D .1lim B B x γγ→=9.关于Δr G m 和Δr G m ϴ,下列说法中正确的是( )。
A .在等温等压下,Δr G m >0的反应不能自发进行 B .Δr G m 是反应进度的函数C .在等温等压下,Δr G m ϴ=0时反应达到平衡D .Δr G m ϴ是温度和压力的函数10.关于反应平衡常数,下列说法中正确的是( )。

复习必备川大工科物理化学考试试题A 卷(2007-2008年2学期) 川大学子专用一 选择题 每小题2分,共40分。
1、在一抽空的器中放入过量的NH 4HCO 3(S ),加热时反应NH 4HCO 3(S )=NH3(g )+NH 3(g)+H 2O(g)+CO 2(g)达到平衡,则该系统的独立组分数C 和自由度数F 为,A .1,2B .2,1C .2,2 D1,12、物质A 与B 可形成低共沸混合物E 。
已知纯A 的沸点小于纯B 的沸点。
若将任意比例的A+B 混合物在一个精馏,在塔顶的馏出物是A .纯AB .纯BC .低共沸混合物D .都有可能3、二元液系相图中,共沸点的自由度数F 为A .0 B.1 C.2 D.34、当克拉佩龙-克劳修斯方程应用与液相变为气相时,则A .P 必随T 的升高而减小 B.P 不随T 的升高而改变C .P 必随T 的升高而变大 D.P 随T 的升高可变大或减小5、组分A 和B 可以形成以下几种化合物:A 2B (s )、AB (s )、AB 2(s )和AB 3(s ),则此A-B 系统的低共点最多有A .2个 B.3个 C.4个 D.5个6、电池在恒温、恒压下可逆放电2F 与以一定的电压放电2F ,二者相比不同的有:A .电池反应的r m H ∆B .电池反应的r m G ∆C .电池反应的r m S ∆D .对环境作的电功W7、已知Ti ++e →Ti 的3(1)0.34,3E V Ti e Ti θ+=-+→的(2)0.72E V θ=则32Ti e Ti +++→的(3)E θ是A .2.50VB .1.25VC .1.06VD .0.38V8、下列哪组电极的组合可计算AgC1的标准摩尔生成吉布斯函数?A .Ag +/Ag 和C1-/AgC1/AgB .Ag +/Ag 和Cl 2/C1-C .C1-/AgC1/Ag 和Cl 2/C1-D .三者都不可以9.已知121()50.1110,x x m m Na Sm mol OH Sm mol +-+∧=⨯∧=⨯ ()NaOH t OH ∞在无限稀的溶液是A .0.202 B. 0.253 C .0.798 D. 110.在下述电池中,电池电动势与氯离子活度无关的是:A 。
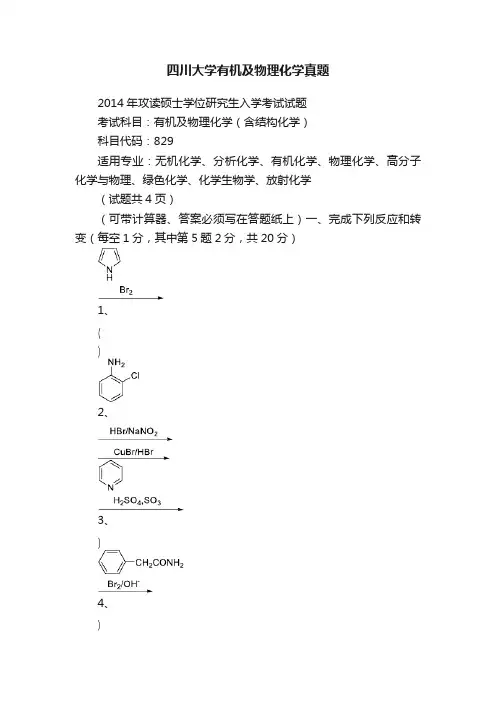
四川大学有机及物理化学真题2014年攻读硕士学位研究生入学考试试题考试科目:有机及物理化学(含结构化学)科目代码:829适用专业:无机化学、分析化学、有机化学、物理化学、高分子化学与物理、绿色化学、化学生物学、放射化学(试题共4页)(可带计算器、答案必须写在答题纸上)一、完成下列反应和转变(每空1分,其中第5题2分,共20分)1、2、3、4、5、6、7、8、9、10、111213、14二、(23分)由制定原料和必要试剂完成下列转变1、由苯出发合成1,3,5-三溴苯2、由苯胺制备对溴苯胺3、由β-甲基吡啶合成β-氨基吡啶4、由正溴丁烷为原料合成正丁胺,要求不含其它胺5、三、(10分)用化学方法鉴别下列物质,写出鉴别过程、现象1、D-麦芽糖,D-果糖,蔗糖,淀粉2、苯胺,苯酚,环己胺四、(10分)推测反应机理1、2、五、(10分)推测结构1、某化合物A 分子式为C 10H 15N 能溶于稀盐酸,与亚硝酸作用放出氮气得B ,B 与浓硫酸共热得C ,C 进行臭氧化得乙醛和一残留物D ,化合物D 在红外图谱的1900~1650cm -1范围内有一强特征吸收峰,且能发生碘仿反应,得苯甲酸。
写出A,B,C,D 的结构式,并用反应式说明推断过程。
2、两个具有旋光性的化合物A 和B ,与苯肼作用生成相同的糖脎。
A ,B 用硝酸氧化后,A 和B 都生成含有四个碳原子的二元酸,但A 氧化后得到的二元酸有旋光性,B 氧化后得到的二元酸没有旋光性,写出A ,B 的结构式,并用反应式说明推断过程。
六、(9分)如下图所示的绝热容器,用销钉固定的绝热隔板将容器分为两部分,隔板两边装有理想气体He 和N 2,初始状态如图。
若将隔板换成一块铝板(销钉仍保持固定),体系最终将达热平衡,求此过程的?U 、?H 和?S ,并判断过程是否自发?七、(14分)H 2O(A)-NaI(B)体系的固液平衡相图如右图所示:(1)、标出各区域的相态(2)、试绘出物系a 、b 冷却过程中的步冷曲线(3)、以0o C 纯水为标准态,求10%的NaI 水溶液温度降低至-10.7o C (此时冰与饱和溶液平衡共存)饱和溶液中水的活度,已知水的凝固热为-600.8-?1J mol八、(10分)298K 时测定0.001-?3mol dm 24Na SO 溶液的电导率κ--=??211 2.610S m ,已知∞+--Λ=321m (Na ) 5.010S m mol ,∞+--Λ=2321m 1(Ca ) 6.010S m mol 2,以上溶液可视为无限稀释。


第一章热力学第一定律练习题一、判断题(说法对否):1.道尔顿分压定律,对理想气体和实际混合气体来说关系式P B =n B (RT/V)都成立。
2.在两个封闭的容器中,装有同一种理想气体,若两个容器中压力、体积相同,那么温度也相同。
3.物质的温度越高,则热量越多;天气预报:天气很热。
其热的概念与热力学相同。
4.恒压过程也就是恒外压过程,恒外压过程也就是恒压过程。
5.实际气体在恒温膨胀时所做的功绝对值等于所吸收的热。
6.凡是温度升高的过程体系一定吸热;而恒温过程体系不吸热也不放热。
7.当系统的状态一定时,所有的状态函数都有一定的数值。
当系统的状态发生变化时,所有的状态函数的数值也随之发生变化。
8.在P ө、100℃下有lmol 的水和水蒸气共存的系统,该系统的状态完全确定。
9.一定量的理想气体,当热力学能与温度确定之后,则所有的状态函数也完全确定。
10.从同一始态经不同的过程到达同一终态,则Q 和W 的值一般不同,Q +W 的值一般也不相同。
11.因Q P =ΔH ,Q V =ΔU ,所以Q P 与Q V 都是状态函数。
12.封闭系统在压力恒定的过程中吸收的热等于该系统的焓。
13.对于一定量的理想气体,当温度一定时热力学能与焓的值一定,其差值也一定。
14.在101.325kPa 下,1mol l00℃的水等温蒸发为100℃的水蒸气。
若水蒸气可视为理想气体,那么由于过程等温,所以该过程ΔU =0。
15.1mol ,80.1℃、101.325kPa 的液态苯向真空蒸发为80.1℃、101.325kPa 的气态苯。
已知该过程的焓变为30.87kJ ,所以此过程的Q =30.87kJ 。
16.1mol 水在l01.325kPa 下由25℃升温至120℃,其ΔH =∑C P ,m d T 。
17.因焓是温度、压力的函数,即H =f (T ,p ),所以在恒温、恒压下发生相变时,由于d T =0,d p =0,故可得ΔH =0。

2017四川大学各院系专业考研专业课资料汇总_研途宝考研
川大2017考研复习也慢慢步入正轨,而市面上很多关于川大考研各专业复习资料参差不齐,考研备考的成果则是我们选择了使用什么样的复习资料,选对了复习资料无疑能让我们的备考工作事半功倍,因此,研途宝至善川大考研网整理了四川大学各院系专业的考研资料,给大家考研专业课真题资料的选择提供参考。
川大专业课考研辅导推荐:
对于考研辅导班,人云亦云。
但复习进度慢、基础比较低的同学,选择报考辅导班是非常有必要的。
目前,针对四川大学最实效的四大考研辅导班主要有:
2017四川大学考研VIP高辅班
2017四川大学考研专业课无忧通关班
2017四川大学考研专业课VIP全科班
2017四川大学考研专业课一对一全程班
更多四川大学考研参考书目、考研真题、考研报录比、考研大纲、考研录取分数线、考研招生简章、考研招生目录等考研信息,请直接去研途宝至善川大考研官网查看。
物理化学考研试题及答案一、选择题(每题5分,共20分)1. 下列关于理想气体状态方程的描述,正确的是()。
A. 只适用于理想气体B. 适用于所有气体C. 只适用于固态物质D. 只适用于液态物质答案:A2. 根据热力学第一定律,下列说法正确的是()。
A. 能量守恒B. 能量可以创造C. 能量可以消灭D. 能量可以转移,但总量不变答案:D3. 在电化学中,正极发生的反应是()。
A. 还原反应B. 氧化反应C. 还原反应和氧化反应D. 既不发生还原反应也不发生氧化反应答案:A4. 根据热力学第二定律,下列说法正确的是()。
A. 热量可以从低温物体自发地传递到高温物体B. 热量不能自发地从低温物体传递到高温物体C. 热量可以自发地从高温物体传递到低温物体D. 热量不能从低温物体传递到高温物体答案:B二、填空题(每题5分,共20分)1. 理想气体状态方程为:\( PV = nRT \),其中P代表______,V代表______,n代表______,R代表______,T代表______。
答案:压强;体积;摩尔数;气体常数;温度(开尔文)2. 根据热力学第一定律,系统内能的增加等于系统对外做的功加上系统吸收的热量,即\( \Delta U = W + Q \),其中\( \Delta U \)代表______,W代表______,Q代表______。
答案:内能的变化;做的功;吸收的热量3. 电化学中,原电池的正极是______发生的地方,负极是______发生的地方。
答案:还原反应;氧化反应4. 热力学第二定律的开尔文表述是:不可能从单一热源吸取热量,使之完全变为有用功而不产生其他影响。
这句话表明了______。
答案:热机效率不可能达到100%三、简答题(每题10分,共20分)1. 简述热力学第二定律的两种表述方式及其含义。
答案:热力学第二定律的两种表述方式是开尔文表述和克劳修斯表述。
开尔文表述指出,不可能从单一热源吸取热量,使之完全变为有用功而不产生其他影响,意味着热机效率不可能达到100%。
四川大学考研历年真题解析
——887物理化学
主编:弘毅考研
编者:Micro Chen
弘毅教育出品
【资料说明】
《四川大学887物理化学历年真题解析》是一份优秀的专业课历年试题及详细解析,是考取四川大学选考887物理化学必备的一份资料。
历年真题是除了参考教材之外的最重要的一份资料,其实,这也是我倾其心力,编撰此资料的原因所在。
历年真题除了能直接告诉我们历年考研试题中考了哪些内容、哪一年考试难、哪一年考试容易之外,还能告诉我们很多东西。
同时2012年的试题,我们将在真题公布以后将试题和答案发送给读者,保证你拿到手的是最新的资料。
1.命题风格与试题难易
川大887物理化学的命题难度较华南理工,中石油(北京)等高校的物理化学命题简单了不少,基本上是针对概念的小问题比较多。
所以同学们在复习时,一定要紧紧地抓住课本,牢记课本上的每一个细微的知识点。
回顾2011年与2012年的试题,可以发现均有50分的选填“<”、“>”、“=”类型的题,每空一分,看似随意,实则聚沙成塔。
成绩也就在不经意间拉开了。
同时,《物理化学教程》的课后习题要做熟做透,大题要做到出到必会。
2.考试题型与分值
大家要了解有哪些题型,每个题型的分值。
从最近五年看,川大的题目基本上为判断,选择,填空。
计算。
这两年新增了选填“<”、“>”、“=”类型的题。
小题的分值占到100分,大题一般为50分。
所以要两手抓,两手都要硬。
3.各章节的出题比重
川大的专业课没有考试大纲,因此没有重、难点的告知,但大家可以通过对历年真题的分析,掌握各个章节在整个考研中的重要地位。
例如,化学动力学以及多相热力学、反应热力学每年都要出到40-50分,相变热力学和电化学以及表面化学要出到50-60分,胶体每年都会涉及一些,一般在5-15分。
而量子力学和统计热力学则几乎没有出现,可以忽略。
(09年有一道1分的判断题)。
通过这些分析,就把握了复习的重点。
4.重要的已考知识点
考研专业课试卷中,很多考点会反复出现,一方面告诉大家这是重点,另一方面也可以帮助大家记忆重要知识点,灵活的掌握各种答题方法。
比如经常出现的液体的表面性质,相图,基元反应动力学方程等。
对于反复考查的知识点,一定要稔熟于心,考研
是选拔高层次人才的考试,因此对于灵活性的要求更高,需要大家养成良好的发散思维。
5.每隔几年出现原题
这是川大887物理化学出题的一大特点,有时候甚至数据都不变。
因此这些分数要是再抓不住,那就可以回家卖红薯了。
通过上述的分析,我们不难看出历年真题在备考中的重要性!真题不仅要好好研究,而且还要作为最重要的模拟题反复地训练,在模拟训练的时候,要掌握好时间,做到统筹规划,有条不紊。
同时也要注意02-05年的真题,时间远不代表它们没有价值。
资料编者前前后后花去了不少的时间和精力。
希望通过此书,能与大家相聚川大!
弘毅胜卷是迄今为止,唯一一套由弘毅教育联合本校在读优秀研究生、博士生联合编撰的考研辅导用书,希望通过此书,帮助读者成功考取自己理想中的高校。
由于时间、水平所限,资料中难免有不妥之处,尚需考生谅解,欢迎批评指正,资料内容问题请发邮件至xiugai@,在此深表感谢!
编者
目录
历年真题 (5)
2013年攻读硕士学位研究生入学考试试题 (5)
2012年攻读硕士学位研究生入学考试试题..................... 错误!未定义书签。
2011年攻读硕士学位研究生入学考试试题..................... 错误!未定义书签。
2010年攻读硕士学位研究生入学考试试题..................... 错误!未定义书签。
2009年攻读硕士学位研究生入学考试试题..................... 错误!未定义书签。
2008年攻读硕士学位研究生入学考试试题..................... 错误!未定义书签。
2007年攻读硕士学位研究生入学考试试题..................... 错误!未定义书签。
2006年攻读硕士学位研究生入学考试试题..................... 错误!未定义书签。
2005年攻读硕士学位研究生入学考试试题..................... 错误!未定义书签。
2004年攻读硕士学位研究生入学考试试题..................... 错误!未定义书签。
2003年攻读硕士学位研究生入学考试试题..................... 错误!未定义书签。
2002年攻读硕士学位研究生入学考试试题..................... 错误!未定义书签。
真题解析.................................................. 错误!未定义书签。
2012年攻读硕士学位研究生入学考试真题解析................. 错误!未定义书签。
2011年攻读硕士学位研究生入学考试真题解析................. 错误!未定义书签。
2010年攻读硕士学位研究生入学考试真题解析................. 错误!未定义书签。
2009年攻读硕士学位研究生入学考试真题解析................. 错误!未定义书签。
2008年攻读硕士学位研究生入学考试真题解析................. 错误!未定义书签。
2007年攻读硕士学位研究生入学考试真题解析................. 错误!未定义书签。
2006年攻读硕士学位研究生入学考试真题解析................. 错误!未定义书签。
2005年攻读硕士学位研究生入学考试真题解析................. 错误!未定义书签。
2004年攻读硕士学位研究生入学考试真题解析................. 错误!未定义书签。
2003年攻读硕士学位研究生入学考试真题解析................. 错误!未定义书签。
2002年攻读硕士学位研究生入学考试真题解析................. 错误!未定义书签。
历年真题
2013年攻读硕士学位研究生入学考试试题
一、选择题(50分,每题2分。
考生注意:只能用A,B,C,D答题)
1.1mol纯理想气体,要确定其它状态函数的值,必须首先确定()
A.P,V
B.T,U
C.P,U
D.T,P
2.以下叙述中不正确的是()
A.系统的不同状态可具有相同的温度
B.系统的不同状态可具有相同的体积
C.状态改变,系统所有状态函数都要变
D.状态改变,系统某些状态函数可以不变
3.在恒容下的一定量理想气体,当温度升高时,其焓将()
A.增大
B.减少
C.不变
D.不能确定
4.下列叙述中不正确的是()
A.广度性质的状态函数才有偏摩尔量
B.。