专题一:常见物质的颜色
- 格式:doc
- 大小:28.50 KB
- 文档页数:1
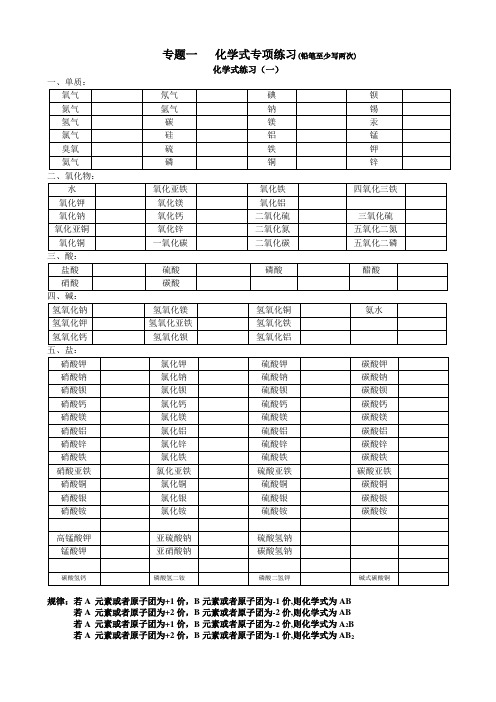
专题一化学式专项练习(铅笔至少写两次)
化学式练习(一)
一、单质:
规律:若A 元素或者原子团为+1价,B元素或者原子团为-1价,则化学式为AB 若A 元素或者原子团为+2价,B元素或者原子团为-2价,则化学式为AB 若A 元素或者原子团为+1价,B元素或者原子团为-2价,则化学式为A2B 若A 元素或者原子团为+2价,B元素或者原子团为-1价,则化学式为AB2
化学式练习(二)俗称
化学式练习(三)颜色、溶解性
专题一化学式专项练习答案
化学式练习(一)答案
一、单质:
规律:若A 元素或者原子团为+1价,B元素或者原子团为-1价,则化学式为AB 若A 元素或者原子团为+2价,B元素或者原子团为-2价,则化学式为AB 若A 元素或者原子团为+1价,B元素或者原子团为-2价,则化学式为A2B 若A 元素或者原子团为+2价,B元素或者原子团为-1价,则化学式为AB2
化学式练习(二)俗称参考答案。

化学中考专题:化学推断题常见物质的特性一、熟记常见物质的颜色:二、物质俗名及其对应的化学式和化学名:三、常见物质的用途①常用于金属除锈:稀硫酸、盐酸;②改良酸性土壤的物质:生石灰、熟石灰;③人体中的胃酸主要成分:盐酸;④常用的建筑材料:CaCO3、Ca(OH)2⑤制取肥皂、造纸、纺织、印染:NaOH⑥用于玻璃、造纸、纺织、洗涤剂生产:Na2CO3初中科学常用化学方程式CaO + H2O Ca(OH)2Ca(OH)2 + CO2CaCO3↓+ H2O2NaOH + CO2Na2CO3 + H2OCa(OH)2 + Na2CO3CaCO3↓+ NaOHNaOH + HCl NaCl + H2O (微观实质:氢离子和氢氧根离子反应生成水)C + O2点燃CO22CO + O2点燃2CO2C + CO2高温2COC + 2CuO 高温2Cu + CO2↑CO + CuO Cu + CO2H2 + 2CuO 点燃2Cu + H2OCaCO3高温CaO + CO2↑CaCO3 + 2HCl = CaCl2 + H2O + CO2↑2Cu + O2点燃2CuOCuO + H2SO4 = CuSO4 + H2OCuO + 2HCl = CuCl2 + H2OCuSO4 + BaCl2= CuCl2 + BaSO4↓CuSO4 + 2NaOH =Cu(OH)2↓+Na2SO4Cu(OH)2 + 2HCl =CuCl2 + 2H2OCu(OH)2 + H 2SO 4 =CuSO 4 + 2H 2O 3Fe + 2O 2 点燃 Fe 3O 4 Fe + 2HCl = FeCl 2 + H 2↑FeCl 3 + 3NaOH = Fe(OH)3↓+ 3NaCl3CO + Fe 2O 3 高温 2Fe + 3CO 2 (工业用赤铁矿炼铁的主要反应:红棕色固体变成黑色) Fe + CuSO 4 = FeSO 4 + Cu (铁的表面有红色固体生成,溶液由蓝色变成浅绿色) Fe 2O 3 + 6HCl = 2FeCl 3 + 3H 2O Fe 2O 3 + 3H 2SO 4 = 2Fe 2(SO 4)3 + 3H 2O 2KMnO 4 K 2MnO 4 + MnO 2 + O 2↑2H 2O 2 MnO 2 H 2O + O 2↑ 2H 2O 通电 2H 2 ↑ + O 2 ↑ 2H 2 + O 2 点燃 2H 2OAgNO 3 + HCl = AgCl ↓+ HNO 3 AgNO 3 + NaCl = AgCl ↓+NaNO 3 BaCl 2 + H 2SO 4 = BaSO 4↓+ 2HClMnO 2△2KCl + 3O 2↑2KClO 31.(2019.日照)甲、乙、丙三种物质的转化关系如固所示(“→”表示反应能一步实现,部分反应物、生成物和反应条件已略去)。

推断专题常见的突破口:(可能在题干中、框图中、问题中)一.常见沉淀的颜色白色沉淀: CaCO3 BaCO3 AgCl BaSO4 Mg(OH)2 Al(OH)3----….红褐色沉淀: Fe(OH)3蓝色沉淀: Cu(OH)2二. 常见固态物质的颜色:①红色固体:Cu(紫红色)、Fe2O3(红棕色)、红磷(一般不考虑)②黄色固体:S③白色固体:KClO3 KCl CaO P2O5 NaCl Na2CO3…………..④黑色固体:C、CuO、MnO2、Fe3O4铁粉(均不溶于水)⑤紫黑色固体:KMnO4三、常见的金属、金属氧化物、常见的气体Fe、Cu、Zn------ CuO、Fe2O3、CaO、Fe3O4------- O2、H2、N2、CO2、CO、CH4----- 四. 常见有色溶液的颜色:①含有铜离子(Cu2+)的溶液为: 蓝色如:CuSO4溶液、CuCl2溶液 Cu(NO3)2溶液②含有铁离子(Fe3+)的溶液为:黄色如:FeCl3 溶液、Fe2(SO4)3溶液③含有亚铁离子(Fe2+)的溶液为: 浅绿色如: FeCl2 、FeSO4溶液是浅绿色的五. 要熟记下列物质的、化学式或主要成分1、CaO 氧化钙生石灰Ca(OH)2氢氧化钙熟石灰、消石灰NaCl 氯化钠食盐NaOH 氢氧化钠火碱、烧碱、苛性钠Na2CO3碳酸钠纯碱、苏打、碱面(家中的)C2H5OH 乙醇酒精CO2 二氧化碳干冰(CO2固体)NaHCO3碳酸氢钠小苏打2、【主要成分】:CaCO3碳酸钙。
大理石、石灰石、水垢、蛋壳、贝壳、珍珠、钟乳石的主要成分CH4甲烷 (天然气、沼气、瓦斯气的主要成分)Fe2O3氧化铁(三氧化二铁)铁锈的主要成分,赤铁矿石的主要成分。
HCl 氯化氢气体(盐酸中的溶质)(钢、生铁的主要成份是铁)六.化学之最:1、天然存在最硬的物质:金刚石 2.、空气中含量最多的气体:氮气3.、空气中含量最多的元素:氮元素4.、地壳中含量最多的元素:氧元素5.、最轻的气体:氢气6.、最简单的有机物:甲烷7、生物细胞中含量最多的元素:氧元素 8、相对分子质量最小的氧化物:水9、最清洁的燃料是:氢气【金属之最】:①地壳中含量最多的金属元素:铝元素②人体中含量最多的金属元素:钙元素③.导电性最好的金属:银④.目前世界年产量最高的金属:铁⑤.熔点最高的金属是:钨⑥熔点最低的金属:汞七、常见的有毒的物质:聚氯乙烯八、溶于水放热的常见三大物质1、氧化钙和水反应放热: CaO+H 2O==Ca(OH)22、浓硫酸溶于水放热3、氢氧化钠溶于水放热 ★(溶于水吸热的是:硝酸铵----NH 4NO 3) 九、几个特别之处:1、具有还原性的三大物质:C 、CO 、 H 2 C + 2CuO 2Cu + CO 2↑ 3C + 2Fe 2O 34Fe + 3 CO 2↑ CO 2 + C2CO 3CO + Fe 2O 32Fe + 3CO 22、加热分解生成三种物质的化学反应 2KMnO 4 K 2MnO 4+MnO 2+O 2↑NH 4HCO 3 NH 3↑+ H 2O + CO 2↑ 3、特殊的分解反应4、组成元素相同的物质:CO 和CO 2 KMnO 4和K 2MnO 4、 Fe 3O 4和Fe 2O 3 H 2O 2和H 20 5、黑色物质间的转化:3Fe + 2 O 2Fe 3O 4 4CO + Fe 3O 43Fe + 4CO 26、红色变成黑色、黑色变成红色的转化: 2Cu + O 2 2CuO C + 2CuO2Cu + CO 2↑3CO + Fe 2O 32Fe + 3CO 2 铁生锈的过程:黑色变成红色7、两种物质反应生成三种物质的反应:⑴碳酸盐和酸反应:CaCO 3 + 2HCl= CaCl 2 + H 2O + CO 2↑ Na 2CO 3 + 2HCl =2NaCl + H 2O + CO 2↑⑵铵盐能和碱性物质反应: 2NH 4Cl+Ca(OH)2=CaCl 2+2NH 3↑+2H 2O典型例题一.突破口出现在题干中1. A 、B 、C 、D 都是九年级化学中的物质,它们存在右下图所示的关系(反应条件略去)。


初三化学物质推断题专题训练1、常见固体物质颜色红色铜(紫红色具有金属光泽) 三氧化二铁(红褐色粉末) 氢氧化铁(红褐色沉淀)高锰酸钾(紫黑色)黄色硫磺(黄色粉末)蓝色五水硫酸铜氢氧化铜黑色碳铁粉氧化铜二氧化锰氧化铜绿色碱式碳酸铜白色绝大多数固体2、常见溶液颜色淡黄红褐含铁离子的溶液: 氯化铁溶液硫酸铁溶液硝酸铁溶液淡绿含亚铁离的溶液:蓝色含铜离子的溶液:3、常见沉淀BaSO4、AgCl、CaCO3、BaCO3(白色);Cu(OH)2(蓝色);Fe(OH)3(红褐色)4、火焰颜色:S在O2中燃烧(蓝紫色);S、H2在空气中燃烧(淡蓝色);CO、CH4在空气中燃烧(蓝色).二、初中常见物质的特殊性质1、二氧化碳能使清石灰水变浑浊:注意二氧化碳中混有氯化氢时不行2、氨气能使湿润的红色石蕊试纸变蓝3、银离子和氯离子互检,钡离子和硫酸根离子互检。
4、碳酸根碳酸氢根和氢离子反应生成气体5、铵根离子和氢氧根反应生成氨气6、在初中阶段不溶于稀硝酸的白色固体只有氯化银和硫酸钡7、能使白色无水CuSO4粉末变蓝的气体是水蒸气8、在空气中燃烧生成CO2和H2O的物质是有机物,如CH4、C2H5OH等9、能使黑色CuO变红(或红色Fe2O3变黑)的气体是H2或CO,固体是C三、特殊反应CO2+NaOH CO2+Ca(OH)2 R Cl+AgNO3 R SO4+BaCl2 C+CO2四、熟悉酸碱盐之间的反应规律置换酸+金属金属+盐溶液复分解酸+碱酸+盐酸+金属氧化物可溶性碱+可溶性盐可溶性盐+可溶性盐其它:还原剂+金属氧化物碱+酸性氧化物氧气制法五、其它(1)地壳中含量最多的元素是O,含量最多的金属元素是Al。
(2)人体中含量最多的元素是O。
(3)空气中含量最多的元素是N.(4)形成化合物最多的元素是C。
(5)相对分子质量最小,密度最小的气体是H2。
(6)相对分子质量最小的氧化物是H2O。
(7)自然界中硬度最大的物质是金刚石。

专题06 光的传播、光的色散、物体的颜色一、光的传播与光速①光源:正在发光且能自身发光的物体。
太阳和所有的恒星都是光源。
②光的传播:光源发出的光能在空气、水、玻璃等物质里传播。
光在同一种均匀物质中是沿直线传播的。
光的直线传播的典型应用有:瞄准时的三点一线,小孔成像,影子的形成,日食、月食的产生等。
③阳光下树阴中的圆形光斑的形成:小孔成像(太阳的像),与小孔的大小、形状无关,只与小孔与地面的距离有关。
④光的速度:3x108m/s二、光的散射与光的颜色①光的色散:太阳光(白光)通过三棱镜后分解成红、橙、黄、绿、蓝、定、紫七种色光过程。
说明:在红光之外还有红外线,能使温度计温度上升。
在紫光之外还有紫外线,能使胶卷感光,它也能杀死微生物,常用来消毒灭菌。
透明物体:透明物体的颜色是由透过它的色光的颜色来决定,即物体的颜色与透过它的 ②物体的颜色 色光的颜色相同。
不透明物体:不透明物体颜色由它反射的物体颜色决定,即物体颜色与它反射的色光的颜色相同。
③三原色:红、绿、蓝一、光的传播及其应用1.如图所示,为了探究孔的大小对光斑形状的影响,小华设计了四种有不同形状孔的卡片甲,并用另一张卡片乙覆盖在甲上,然后从图示位置沿箭头方向水平移动乙,观察光斑形状的变化情况。
其中符合要求的是()A.B.C.D.【答案】A【解析】当探究孔的大小对光斑形状的影响时,应该控制小孔的形状相同而改变小孔的大小,故A 符合要求,而B、C、D不合要求。
故选A。
2.(2022七下·鄞州期中)下列属于光源的是()A.天空中的一轮明月B.发光的猫眼C.闪闪发光的红宝石D.点燃的蜡烛【答案】D【解析】天空中的一轮明月、发光的猫眼和闪闪发光的红宝石,都不是自己发光,只有点燃的蜡烛能够自己发光,因此只有蜡烛是光源,故D正确,而A、B、C错误。
故选D。
3.(2022七下·鄞州期中)关于光的传播过程,下列说法中错误的是()A.光的传播方向始终不变B.光在空气中的传播速度约为3×105千米/秒C.光在同种均匀介质中沿直线传播D.光在水中的速度小于在空气中的速度【答案】A【解析】A.当光遇到不透明的物体时会发生反射,从一种介质斜射入另一种介质时会发生折射,故A错误符合题意;B.光在空气中的传播速度约为3×105千米/秒,故B正确不合题意;C.光在同种均匀介质中沿直线传播,故C正确不合题意;D.光在水中的速度小于在空气中的速度,故D正确不合题意。
初中化学常见物质的颜色归纳在化学的学习中经常会学到许多的颜色,那么初中化学常见物质的颜色有哪些呢?一起来看看,以下是店铺分享给大家的初中化学常见物质的颜色,希望可以帮到你!初中化学常见物质的颜色(一)、固体的颜色1、红色固体:铜,氧化铁2、绿色固体:碱式碳酸铜3、蓝色固体:氢氧化铜,硫酸铜晶体4、紫黑色固体:高锰酸钾5、淡黄色固体:硫磺6、无色固体:冰,干冰,金刚石7、银白色固体:银,铁,镁,铝,汞等金属8、黑色固体:铁粉,木炭,氧化铜,二氧化锰,四氧化三铁,(碳黑,活性炭)9、红褐色固体:氢氧化铁10、白色固体:氯化钠,碳酸钠,氢氧化钠,氢氧化钙,碳酸钙,氧化钙,硫酸铜,五氧化二磷,氧化镁(二)、液体的颜色11、无色液体:水,双氧水12、蓝色溶液:硫酸铜溶液,氯化铜溶液,硝酸铜溶液13、浅绿色溶液:硫酸亚铁溶液,氯化亚铁溶液,硝酸亚铁溶液14、黄色溶液:硫酸铁溶液,氯化铁溶液,硝酸铁溶液15、紫红色溶液:高锰酸钾溶液16、紫色溶液:石蕊溶液(三)、气体的颜色17、红棕色气体:二氧化氮18、黄绿色气体:氯气19、无色气体:氧气,氮气,氢气,二氧化碳,一氧化碳,二氧化硫,氯化氢气体等大多数气体。
初中化学复习策略初中化学复习策略之夯实基础第一轮复习主要是按课本结构进行,次序可适当调整,着重抓章节过关,打好基础。
要通过这一轮的复习,使学生认真掌握各章节的基本内容和重点,加深理解知识的前后联系,克服遗忘现象,第一轮复习要稳扎稳打,不要追求快速度。
第二轮复习是以综合提高为目的,通常是按照化学基本概念和基本原理、元素及其化合物、化学计算和化学实验四个专题进行。
复习时要着重整理知识,形成知识网络,加强知识间的纵横联系,注意总结规律性的知识,进一步加深对基础知识的理解,在第二轮复习中还要通过对典型例题的讲解,以及对错题的分析,来帮助学生总结题型和解题规律,明确解题思路,掌握解题的方法和解题的规范性,提高学生分析问题和解决问题的能力。
重、难点考点07—框式推断题专题突破(一)框式推断题常见解题思路:一:根据物质的颜色对物质做出判定:常见物质的颜色:红色的固体——Cu、Fe2O3、P(红磷)黑色的固体——C、CuO、Fe3O4、FeO、MnO2、铁粉白色的固体——MgO、P2O5、P(白磷)、CuSO4(无水硫酸铜)、KCl、NaCl等黄色的固体—— S蓝色的固体——CuSO4•5H2O蓝色絮状沉淀——Cu(OH)2红褐色絮状沉淀——Fe(OH)3常见不溶于酸的白色沉淀——BaSO4、AgCl溶于酸并二氧化碳气体的白色沉淀——BaCO3、CaCO3等不溶性碳酸盐的沉淀溶于酸但不产生气体的白色沉淀——Mg(OH)2、Al(OH)3等不溶性碱的沉淀蓝色的溶液—— CuSO4、CuCl2、Cu(NO3)2等含Cu2+溶液浅绿色的溶液——FeSO4、FeCl2、Fe(NO3)2等含Fe2+溶液黄色的溶液——FeCl3、Fe2(SO4)3、Fe(NO3)3等含Fe3+溶液二:根据物质的状态进行推断:1:具有刺激性气体的气体:NH3、SO2、HCl(皆为无色)2:无色无味的气体:O2、H2、N2、CO2、CH4、CO(剧毒)三:根据物质的特点进行推断:1.使带火星木条复燃的气体是O22.使澄清石灰水变浑浊的气体是CO2,但通入CO2 后变浑浊的溶液不一定是澄清石灰水,也可以是Ba(OH)2溶液。
3.最简单的有机物是甲烷CH44.天然最硬的物质是金刚石(C)5.吸水后由白变蓝的是无水CuSO46.最常见的液态物质是H2O、相对分子质量最小的氧化物是H2O7.常用的食品干燥剂是生石灰CaO8.常用的食品脱氧剂是Fe 粉9.与酸反应有CO2产生的物质是碳酸盐(或NaHCO3)10.与碱反应(研磨)有NH3产生的物质是铵盐(铵态氮肥)11.常温下唯一有氨味的铵态氮肥是NH4HCO3(碳铵)四:根据物质的俗称及用途对物质进行推断:1:一些物质的俗称NaOH-烧碱、火碱、苛性钠;Na2CO3-纯碱、苏打;NaHCO3-小苏打;Hg-水银;CO2-干冰;CaO-生石灰;Ca(OH)2-熟石灰、消石灰;CaCO3-石灰石、大理石;CH4-沼气、瓦斯、天然气;C2H5OH-酒精:2:一些重要物质的主要用途:NaOH:是一种重要的化工原料:可用于造纸、纺织、印染等,生活上可用作炉具清洁剂,实验室中可用于做某些气体的干燥剂,其溶液可用于吸收CO2;可用于制作“叶脉书签”。
河北省2021年中考化学框图推断题解题方式及专题训练专题解读框图推断题是河北省中考的固定题型。
从近几年中考试题分析来看,框图推断题都出此刻填空及简答题中,而且固定出此刻试卷的第31题,分值维持在4分。
此类试题的综合性较强,考点涉及范围广,难度较高。
命题起点往往集中在气体、单质、氧化物、酸碱盐之间的转化。
解题步骤1. 审题:认真审读原理,弄清文意和图意,理出题给条件,深挖细找,反复推敲。
2. 分析抓住关键,找准解题的冲破口,并从冲破口动身,探求知识间的内在联系,应用多种思维方式,进行周密的分析和逻辑推理,推出符合题意的结果。
3. 解答:依照题目的要求,依照分析和推理的结果,认真而全面地解答。
4. 查验得出结论后切勿忘记验证。
其方式是将所得答案放回原题中查验,假设完全符合,那么说明答案正确。
假设显现不符,那么说明答案有误,需要另行试探,推出正确答案。
解题要领1.关于重点学习研究的物质,必然要做到心中有数初中化学的知识点比较多,而中考试卷又不可能把所有的内容都涵盖,因此出题者要考查的也确实是那些重点的内容,即一些在初中化学里重点学习的物质。
比如,咱们重点学习的单质有:O二、H二、C、Fe;重点学习的氧化物有:H2O CO2 CO Fe2O3 CaO CuO;重点学习的酸是盐酸和硫酸;重点学习的碱是NaOH和 Ca(OH) 2 ;重点学习的盐是NaCl、Na2CO3、CaCO3 、NaHCO3 ;有机物是CH4 、C2H5OH。
2.要擅长从题干中找到“题眼”(1)以物质的颜色为“题眼”①常见固体颜色:黄色──硫磺(S)暗紫色──高锰酸钾(KMnO4)红色──Cu黑色──Fe3O4、CuO、MnO二、C粉、Fe粉②沉淀的颜色:蓝色沉淀──-Cu(OH)2 红褐色沉淀──Fe(OH)3白色沉淀(可溶于酸)──CaCO3、BaCO3、Mg(OH)2 白色沉淀(不溶于酸)──BaSO4、AgCl③溶液的颜色:蓝色──(含Cu2+的溶液)如:CuSO4、Cu(NO3)2等。
专题一、常见物质的颜色
(一)、固体的颜色
1、红色固体:铜、氧化铁【 Fe2O3】、氧化汞【 HgO 】
2、绿色固体:碱式碳酸铜【 Cu2(OH)2CO3】
3、蓝色固体:五水硫酸铜(硫酸铜晶体)、氢氧化铜
4、紫黑色固体:高锰酸钾
5、淡黄色固体:硫磺
6、无色固体:冰、干冰、金刚石
7、银白色固体:银、镁、铝、锌、钠、铂等金属
8、黑色固体:铁粉、木炭、氧化铜、二氧化锰、四氧化三铁、炭黑、活性炭
9、红褐色固体:氢氧化铁
10、白色固体(了解):氯化钠、碳酸钠、氢氧化钠、氢氧化钙、碳酸钙、氧化钙、五氧化二磷、氧化镁、氯化银、硫酸钡、氢氧化镁、氢氧化钡等
(二)、液体的颜色
11、无色液体:水、双氧水、乙醇
12、蓝色溶液(含Cu2+的溶液):硫酸铜溶液,硝酸铜溶液氯化铜溶液
13、浅绿色溶液(含Fe2+的溶液):硫酸亚铁溶液,氯化亚铁溶液,
硝酸亚铁溶液
14、黄色溶液(含Fe3+的溶液):硫酸铁溶液,氯化铁溶液,硝酸铁溶液
15、紫红色溶液:高锰酸钾溶液 16、紫色溶液:石蕊试液
(三)、气体的颜色
17、红棕色气体:二氧化氮 18、黄绿色气体:氯气
19、无色气体:氧气、氮气、氢气、二氧化碳、一氧化碳、二氧化硫、氯化氢气体等大多数气体。
1。