孟鲁司特钠咀嚼片说明书
- 格式:docx
- 大小:34.87 KB
- 文档页数:9

孟鲁司特钠咀嚼片说明书请仔细阅读说明书并在医师指导下使用【药品名称】通用名称:孟鲁司特钠咀嚼片英文名称:Montelukast Sodium Chewable Tablets汉语拼音:Menglusitena Jujuepian【成份】本品主要成份为孟鲁司特钠。
化学名称:[R-(E)]-1-[[[1-[3-[2-(7-氯-2-喹啉)乙烯基]苯基-3-[2-(1-羟基-1-甲基乙基)苯基]丙基]硫]甲基]环丙烷乙酸钠化学结构式:分子式:C35H35ClNNaO3S分子量:608.18【性状】本品4mg为粉红色圆角方形片,一面刻有“4”字样;5mg为粉红色椭圆形片,一面刻有“5”字样。
【适应症】本品适用于2岁至14岁儿童哮喘的预防和长期治疗包括预防白天和夜间的哮喘症状治疗对阿司匹林敏感的哮喘患者以及预防运动诱发的支气管收缩。
本品适用于减轻过敏性鼻炎引起的症状(2岁至14岁儿童的季节性过敏性鼻炎和常年性过敏性鼻炎)。
【规格】4mg(以孟鲁司特计);5mg(以孟鲁司特计)。
【用法用量】每日一次。
哮喘病人应在睡前服用。
过敏性鼻炎病人可根据自身的情况在需要时间服药。
同时患有哮喘和过敏性鼻炎的病人应每晚用药一次。
6至14岁哮喘和/或过敏性鼻炎儿童患者每日一次,每次一片(5mg)。
2至5岁哮喘和/或过敏性鼻炎儿童患者每日一次,每次一片(4mg)。
一般建议以哮喘控制指标来评价治疗效果,本品的疗效在用药一天内即出现。
本品可与食物同服或另服。
应建议患者无论在哮喘控制还是恶化阶段都坚持服用。
肾功能不全患者、轻至中度肝损害的患者及不同性别的患者无需调整剂量。
孟鲁司特钠咀嚼片与其它哮喘治疗药物的关系本品可加入患者现有的治疗方案中。
减少合并用药的剂量:支气管扩张剂单用支气管扩张剂不能有效控制的哮喘患者,可在治疗方案中加入本品,一旦有临床疗效反应(一般出现在首剂用药后),根据患者的耐受情况,可将支气管扩张剂剂量减少。
吸入糖皮质激素对接受吸入糖皮质激素治疗的哮喘患者加用本品后,可根据患者的耐受情况适当减少糖皮质激素的剂量。

孟鲁司特钠咀嚼片【药品名称】通用名称:孟鲁司特钠咀嚼片英文名称:Montelukast Sodium Chewable Tablets【成份】主要成份为孟鲁司特钠。
【适应症】本品适用于2岁至14岁儿童哮喘的预防和长期治疗,包括预防白天和夜间的哮喘症状,治疗对阿司匹林敏感的哮喘患者以及预防运动诱发的支气管收缩。
本品适用于减轻过...【用法用量】1.每日一次。
哮喘病人应在睡前服用。
过敏性鼻炎病人可根据自身的情况在需要时间服药。
同时患有哮喘和过敏性鼻炎的病人应每晚用药一次。
6至14岁哮喘和/或过敏性鼻炎儿童患者每日一次,每次一片(5mg)。
2至5岁哮喘和/或过敏性鼻炎儿童患者每日一次,每次一片(4mg)。
一般建议以哮喘控制指标来评价治疗效果,本品的疗效在用药一天内即出现。
本品可与食物同服或另服。
应建议患者无论在哮喘控制还是恶化阶段都坚持服用。
对肾功能不全患者、轻至中度肝损害的患者及不同性别的患者无需调整剂量。
2.本品与其它哮喘治疗药物的关系本品可加入患者现有的治疗方案中。
减少合并用药物的剂量:支气管扩张剂:单用支气管扩张剂不能有效控制的哮喘患者,可在治疗方案中加入本品,一旦有临床治疗反应(一般出现在首剂用药后),根据患者的耐受情况,可将支气管扩张剂剂量减少。
吸入糖皮质激素:对接受吸入糖皮质激素治疗的哮喘患者加用本品后,可根据患者的耐受情况适当减少糖皮质激素的剂量。
应在医师指导下逐渐减量。
某些患者可逐渐减量直至完全停用吸入糖皮质激素。
但不应当用本品突然替代吸入糖皮质激素或遵医嘱。
【不良反应】1.本品一般耐受性良好,不良反应轻微.通常不需要终止治疗。
本品总的不良反应发生率与安慰剂相似。
6至14岁儿童哮喘患者已在大约475名6岁至14岁儿童患者中进行了临床研究,评价了本品的安全性。
总体上儿童患者使用本品的安全性与成人相似,并与安慰剂接近。
在一项安慰剂对照为期8周的临床研究中,本品治疗组中与药物相关,发生率>1%且比安慰剂组高的唯一不良事件是头痛。

药品名称】通用名称:孟鲁司特钠片商品名称:孟鲁司特钠片英文名称:Montelukast Sodium Tablets拼音全码:MengLuSiTeNaPian【主要成份】本品主要成份为孟鲁司特钠。
【成份】化学名:[R-(E)]-1-[[[1-[3-[2-(7-氯-2-喹啉)乙烯基]苯基-3-[2-(1-羟基-1-甲基乙基)苯基]丙基]硫]甲基]环丙烷乙酸钠。
【性状】本品为薄膜衣片,除去包衣后显白色或类白色。
【适应症/功能主治】本品适用于15岁及15岁以上成人哮喘的预防和长期治疗,包括预防白天和夜间的哮喘症状,治疗对阿司匹林敏感的哮喘患者以及预防运动诱发的支气管收缩。
适用于减轻过敏性鼻炎引起的症状。
【规格型号】 10mg*12s【用法用量】每日一次,每次一片(10mg)。
哮喘病人应在睡前服用。
过敏性鼻炎病人可根据自身的情况在需要时服药。
同时患有哮喘和过敏性鼻炎的病人应每晚用药一次。
15岁及15岁以上患有哮喘和/或过敏性鼻炎的成人患者每日一次,每次10mg。
一般建议,以哮喘控制指标来评价治疗效果,本品的疗效在用药一天内即出现。
本品可与食物同服或另服。
应建议患者无论在哮喘控制还是恶化阶段都坚持服用。
老年患者、肾功能不全患者、轻至中度肝损害的患者及不同性别的患者无需调整剂量。
孟鲁司特钠片与其它哮喘治疗药物的关系,本品可加入患者现有的治疗方案中。
减少合并用药的剂量:支气管扩张剂单用支气管扩张剂不能有效控制的哮喘患者,可在治疗方案中加入本品,一旦有明显的临床疗效反应(一般出现在首剂用药后),根据患者的耐受情况,可将支气管扩张剂的剂量减少。
吸入糖皮质激素对接受吸入糖皮质激素治疗的哮喘患者加用本品后,可根据患者的耐受情况适当减少糖皮质激素的剂量。
应在医师指导下逐渐减量。
某些患者可逐渐减量直至完全停用吸入糖皮质激素,但不应当用本品突然替代吸入糖皮质激素。
【不良反应】药的一般耐受性良好,副作用较轻微,通常不需中止治疗。

孟鲁司特钠咀嚼片(顺尔宁)的说明书现在每个孩子都是家长的掌中宝,孩子患上儿科疾病也是每个家庭最不愿意看到的,所以治疗儿科疾病是家长朋友刻不容缓要做的事情。
由于孩子的体质弱于常人,为了更好地保障孩子的健康,很多家庭都会选择药物治疗。
目前孟鲁司特钠咀嚼片(顺尔宁)是治疗儿科疾病最好的药物,下面我们来对孟鲁司特钠咀嚼片(顺尔宁)进行详细的了解吧。
【药品名称】通用名称:孟鲁司特钠咀嚼片商品名称:孟鲁司特钠咀嚼片(顺尔宁)拼音全码:MengLuSiTeNaJuJiaoPian(ShunErNing)【主要成份】孟鲁司特钠。
【性状】本品为粉红色椭圆形片。
【适应症/功能主治】本品适用于儿童哮喘的预防和长期治疗,包括预防白天和夜间的哮喘症状,治疗对阿司匹林敏感的哮喘患者以及预防运动引起的支气管收缩。
本品适用于减轻过敏性鼻炎引起的症状。
【规格型号】4mg*5s【用法用量】每日1次。
哮喘病人应在睡前服用。
季节性过敏性鼻炎可根据自身的情况在需要时间服药。
同时患有哮喘和季节性过敏性鼻炎的病人应每晚用药1次。
2-5岁哮喘和/或季节性过敏性鼻炎儿童患者每日1次,每次1片(4mg)。
一般建议:以哮喘控制指标来评价治疗效果,本品的疗效在用药一天内即出现。
本品可与食物同服或另服。
应建议患者无论在哮喘控制还是恶化阶段都坚持服用。
对肾功能不全患者、轻至中毒肝损害的患者及不同性别的患者无需调整剂量。
本品与其它哮喘治疗药物的关系:本品可加入患者现有的治疗方案中。
减少合并用药物的剂量:支气管扩张剂:单用支气管扩张剂不能有效控制的哮喘患者,可在治疗方案中加入本品,一旦有临床治疗反应(一般出现在首剂用药后),根据患者的耐受情况,可将支气管扩张剂剂量减少。
吸入糖皮质激素:对接受吸入糖皮质激素治疗的哮喘患者加用本品后,根据患者的耐受情况适当减少糖皮质激素的剂量。
应在医师指导下逐渐减量。
某些患者可逐渐减量直至完全停用吸入糖皮质激素。
但不应当用本品突然替代吸入糖皮质激素或遵医嘱。

孟鲁司特钠片的功效和作用孟鲁司特钠片是一种抗过敏药物,主要用于治疗过敏性鼻炎和过敏性结膜炎等过敏性疾病。
其主要成分为孟鲁司特钠,属于二代抗组胺药物。
孟鲁司特钠片的主要功效和作用包括以下几个方面:1. 抗组胺作用:孟鲁司特钠片通过阻断组胺的H1受体,抑制组胺的释放和作用,从而减轻过敏反应引起的症状,如鼻塞、流涕、喷嚏、刺痛等。
2. 抗炎作用:孟鲁司特钠片能够抑制炎症反应,减少过敏反应引起的局部炎症症状,如鼻黏膜充血和水肿等。
3. 免疫调节作用:孟鲁司特钠片能够抑制免疫细胞的活化和迁移,减少炎症介质的释放,从而调节免疫系统的功能,减轻过敏反应。
4. 长效稳定作用:孟鲁司特钠片具有长效稳定效应,即减少过敏反应引起的症状持续时间,并减少发作次数,从而提高患者的生活质量。
5. 对眼部症状的缓解作用:孟鲁司特钠片还可以减轻过敏性结膜炎引起的眼部刺痒、疼痛、泪水增多等症状,改善眼部不适感。
此外,孟鲁司特钠片还有一些其他的作用和效果,如改善睡眠质量、减轻头痛和改善远视等。
但是使用孟鲁司特钠片时需要注意以下几点:1. 孟鲁司特钠片应按照医生的指导和剂量进行使用,不宜随意增减剂量。
2. 孟鲁司特钠片可能会产生一定的副作用,如嗜睡、头晕、口干等,患者应密切观察自身反应,并及时告知医生。
3. 孟鲁司特钠片不适用于哮喘患者及严重肝肾功能不全患者,孕妇及哺乳期妇女慎用。
4. 孟鲁司特钠片与其他药物可能存在相互作用,患者在使用过程中应避免与其他药物同时使用,并告知医生已使用的其他药物。
总之,孟鲁司特钠片是一种常用的抗过敏药物,具有抗组胺、抗炎和免疫调节等多种作用,可以有效缓解过敏性疾病的症状,但使用时需要注意剂量和副作用的控制。
在使用过程中,建议在医生的指导下合理使用,以达到最佳的治疗效果。
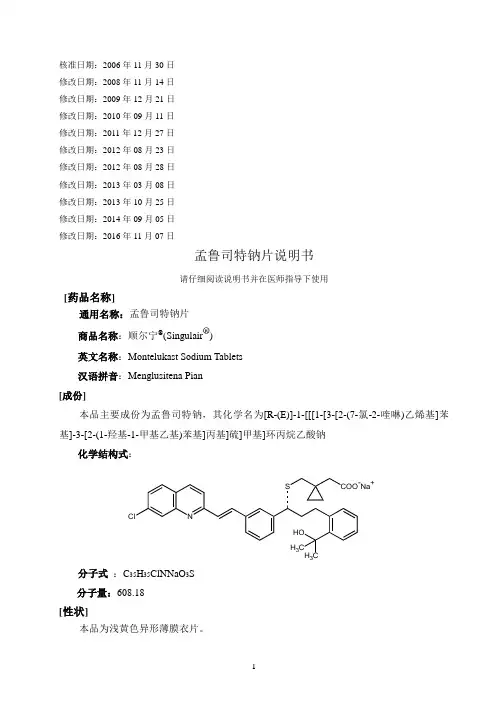
核准日期:2006年11月30日修改日期:2008年11月14日修改日期:2009年12月21日修改日期:2010年09月11日修改日期:2011年12月27日修改日期:2012年08月23日修改日期:2012年08月28日修改日期:2013年03月08日修改日期:2013年10月25日修改日期:2014年09月05日修改日期:2016年11月07日孟鲁司特钠片说明书请仔细阅读说明书并在医师指导下使用[药品名称]通用名称:孟鲁司特钠片商品名称:顺尔宁®(Singulair®)英文名称:Montelukast Sodium Tablets汉语拼音:Menglusitena Pian[成份]本品主要成份为孟鲁司特钠,其化学名为[R-(E)]-1-[[[1-[3-[2-(7-氯-2-喹啉)乙烯基]苯基]-3-[2-(1-羟基-1-甲基乙基)苯基]丙基]硫]甲基]环丙烷乙酸钠化学结构式:N Cl S COO-Na+ H3HOH3C分子式:C35H35ClNNaO3S分子量:608.18[性状]本品为浅黄色异形薄膜衣片。
[适应症]本品适用于15岁及15岁以上成人哮喘的预防和长期治疗,包括预防白天和夜间的哮喘症状,治疗对阿司匹林敏感的哮喘患者以及预防运动诱发的支气管收缩。
本品适用于减轻过敏性鼻炎引起的症状(15岁及15岁以上成人的季节性过敏性鼻炎和常年性过敏性鼻炎)。
[规格]10mg(以孟鲁司特计)。
[用法用量]每日一次,每次一片(10mg)。
哮喘病人应在睡前服用。
过敏性鼻炎病人可根据自身的情况在需要时服药。
同时患有哮喘和过敏性鼻炎的病人应每晚用药一次。
15岁及15岁以上患有哮喘和/或过敏性鼻炎的成人患者每日一次,每次10mg。
一般建议以哮喘控制指标来评价治疗效果,本品的疗效在用药一天内即出现。
本品可与食物同服或另服。
应建议患者无论在哮喘控制还是恶化阶段都坚持服用。
老年患者、肾功能不全患者、轻至中度肝损害的患者及不同性别的患者无需调整剂量。

药品名称:通用名称:孟鲁司特钠片英文名称:Montelukast Sodium Tablets商品名称:顺尔宁成份:孟鲁司特适应症:本品适用于15岁及15岁以上成人哮喘的预防和长期治疗,包括预防白天和夜间的哮喘症状,治疗对阿司匹林敏感的哮喘息者以及预防运动诱发的支气管收缩。
本品适用于减轻过敏性鼻炎引起的症状(15岁及15岁以上成人的季节性过敏性鼻炎和常年性过敏性鼻炎)。
规格:10mg(以孟鲁司特计)。
用法用量:每日一次,每次一片(10mg)。
哮喘病人应在睡前服用。
过敏性鼻炎病人可根据自身的情况在需要时服药。
同时患有哮喘和过敏性鼻炎的病人应每晚用药一次。
15岁及15岁以上患有哮喘和/或过敏性鼻炎的成人患者每日一次,每次10mg。
一般建议以哮喘控制指标来评价治疗效果,本品的疗效在用药一天内即出现。
本品可与食物同服或另服。
应建议患者无论在哮喘控制还是恶化阶段都坚持服用。
老年患者、肾功能不全患者、轻至中度肝损害的患者及不同性别的患者无需调整剂量。
孟鲁司特钠片与其它哮喘治疗药物的关系本品可加入患者现有的治疗方案中。
减少合并用药的剂量:支气管扩张剂单用支气管扩张剂不能有效控制的哮喘患者,可在治疗方案中加入本品,一旦有明显的临床疗效反应(一般出现在首剂用药后),根据患者的耐受情况,可将支气管扩张剂剂量减少。
吸入糖皮质激素对接受吸入糖皮质激素治疗的哮喘患者加用本品后,可根据患者的耐受情况适当减少糖皮质激素的剂量。
应在医师指导下逐渐减量。
某些患者可逐渐减量直至完全停用吸入糖皮质激素。
但不应当用本品突然替代吸入糖皮质激素。
不良反应:本品一般耐受性良好,不良反应轻微,通常不需要终止治疗。
本品总的不良反应发生率与安慰剂相似。
15岁及15岁以上哮喘患者已在大约2600名15岁及15岁以上的成年哮喘患者中进行了临床研究,评价了本品的安全性。
在两项设计相似,安慰剂对照的为期12周的临床研究中,本品治疗组中与药物相关的发生率≥1%且高于安慰剂组的不良事件是腹痛和头痛。

哮喘治疗神药孟鲁司特钠三兄弟,有这四大区别提起来孟鲁司特钠,想必大多数家长并不陌生。
它是一种白三烯受体拮抗剂,具有抗炎平喘的作用,临床上常用于治疗支气管哮喘,阿司匹林敏感性哮喘和过敏性鼻炎等呼吸科疾病。
细心的网友会发现,虽然是同一个名字,但是却有两种到三种不同的包装盒。
这其实是由于孟鲁司特钠有三种不同的剂型,分别是颗粒剂,咀嚼片和片剂。
那么,这三种剂型有哪些区别?使用时该如何选择呢?区别一:规格不同孟鲁司特钠颗粒剂:0.5g:4mg孟鲁司特钠咀嚼片:5mg和4mg两种规格孟鲁司特钠片:10mg区别二:适用人群不同孟鲁司特钠颗粒剂适用于1岁以上儿童哮喘的长期防治,以及2-5岁儿童季节性和常年性过敏性鼻炎的治疗。
孟鲁司特钠咀嚼片有4mg和5mg两种不同的规格。
前者适用于2-5岁哮喘和过敏性鼻炎患儿的治疗。
而后者适用于6-14岁患儿哮喘和过敏性鼻炎的治疗。
而10mg的孟鲁司特钠片剂则适用于15岁及以上患者哮喘和过敏性鼻炎的治疗。
区别三:储存条件不同需要注意的是,孟鲁司特钠对光、热、湿均不稳定。
会导致药物含量降低,杂质含量升高,进而影响药物的有效性和安全性。
因此,孟鲁司特钠片剂和咀嚼片需在避光,密封及25℃以下保存。
而孟鲁司特钠颗粒剂则需要在避光,密封及室温条件保存。
区别四:服用方法不同与片剂和咀嚼片不同的是,孟鲁司特钠颗粒剂由于与外界接触面积增大,药物稳定性更容易受到破坏。
因此,颗粒剂要求只有在服用时方可打开包装袋,打开后要在15分钟内服用全部药物。
此外,该药物不应溶解于除婴儿配方奶粉或母乳外的其他液体中服用,但是服药后可以饮水。

近日,随着全国天气断崖式降温,各医院门诊患者人数激增,其中不乏少数的哮喘患者及过敏性鼻炎患者。
谈及此处,今天我们就来了解一下,对于预防治疗哮喘和过敏性鼻炎的一个重要药物:孟鲁司特钠。
1.孟鲁司特钠的适应证是什么?适应证:哮喘的预防与长期治疗预防白天和夜间的哮喘症状治疗对阿司匹林敏感的哮喘患者预防运动诱发的支气管收缩减轻过敏性鼻炎引起的症状包括季节性过敏性鼻炎和常年性过敏性鼻炎2.孟鲁司特钠的作用机制是什么?孟鲁司特钠属于白三烯受体拮抗剂,白三烯是一种强效的炎症介质,其与受体结合后,会产生一系列与哮喘和过敏性鼻炎相关的生理效应,如支气管收缩、粘液分泌、血管通透性增加及嗜酸性粒细胞聚集,以及鼻部气道阻力增加等。
孟鲁司特钠对Ⅰ型半胱氨酰白三烯(CysLTi)受体有高度的亲和性和选择性,能有效地抑制半胱氨酰白三烯(LTC4、LTD4 和LTE4 )与CysLTi 受体结合从而发挥作用。
3.孟鲁司特钠有多种剂量和剂型,该如何选择?剂量剂型适用年龄备注4mg颗粒剂12个月-5岁的儿童国内医生一般也可参考FDA标准,将6个月作为儿童使用孟鲁司特钠的下限年龄。
咀嚼片2岁-5岁儿童4mg颗粒剂与4mg咀嚼片的区别在于,颗粒剂适用于还不会咀嚼的婴幼儿。
5mg咀嚼片6岁-14岁儿童10mg薄膜衣片15岁以上及成人4.服用孟鲁司特钠的注意事项①不应用于治疗哮喘急性发作。
②孟鲁司特钠耐受性好,不影响儿童生长速度,可长期服用。
③孟鲁司特钠稳定性差,应在15至30℃室温保存,并注意防潮和遮光。
需要服用时方可打开包装袋,打开包装袋后应立即服用(15分钟内)。
4mg孟鲁司特颗粒剂应与一勺室温或冷的软性实物(如苹果酱)混合服用,或溶于配方奶或母乳服用,不宜用水溶解送服。
④服药期间需要关注包括攻击性行为或敌对性的兴奋、易怒、烦躁不安、噩梦、幻觉、失眠、梦游、焦虑、抑郁等表现。
一旦出现可疑的不良反应时应停药并及时就医。
参考文献:1.儿童支气管哮喘诊断与防治指南2016年版[J].中华儿科杂志,2016,54(03):167-1812. 儿童过敏性疾病诊断及治疗专家共识[J].中华儿科杂志,2019,57(03):164-1713.中国过敏性哮喘诊疗指南(第一版,2019年)[J].中华内科杂志,2019,58(09):636-6554.儿童过敏性鼻炎诊断-临床实践指南[J].中国实用儿科杂志,2019,34(03):169-1755.儿童变应性鼻炎诊断和治疗的专家共识(2010年,重庆)[J].中华儿科杂志,2011,49(02):116-1176.孟鲁司特钠不同剂型药品说明书转载声明:本文转载自「临床药师网」,搜索「clinphar2007」即可关注,[阅读原文]。

顺尔宁说明书【通用名】孟鲁司特钠咀嚼片Montelukast【商品名】顺尔宁Singulair【化学名称】孟鲁司特钠,[R-(E)-1[[[1-[3[2-(7-氯-2-喹啉基)乙烯基]苯基]-3-(1-羟基-1-甲基乙基)苯基]丙基]硫代]甲基]环丙基乙酸,单纳盐]【理化性质】白色粉末,易溶于甲醇、乙醇和水,不溶于乙腈,对光敏感。
【药理作用】本品是一种强效的选择性的白三烯D4(LTD4,cysLT1)受体拮抗剂,是新一代非甾体抗炎药物。
能选择性抑制气道平滑肌中白三烯多肽的活性,并有效预防和抑制白三烯所导致的血管通透性增加、气道嗜酸粒细胞(EOS)浸润及支气管痉挛,能减少气道因变应原刺激引起的细胞和非细胞性炎症物质,能抑制变应原激发的气道高反应。
对二氧化硫、运动和冷空气等刺激及各种变应原如花粉、毛屑等引起的速发相和迟发相炎症反应均有抑制作用。
本品与人类气道中的cysLT受体能高度选择性结合,从而阻断白三烯的病理作用。
已经证明,吸入LTD4可引起较组胺强1000倍的剂量依赖性支气管收缩。
【适应证】本品适用于成人和儿童哮喘的预防和长期治疗,包括预防白天和夜间的哮喘症状,能够改善慢性气道炎症,改善肺功能,控制哮喘症状,减少必需的β2激动剂用量,治疗对阿司匹林敏感的哮喘患者以及预防运动引起的支气管收缩。
【用法与用量】15岁及15岁以上成人剂量为10mg,qd睡前服用。
6~14岁儿童剂量为5mg,qd,睡前服用。
该组患者不需再按年龄调整剂量。
6岁以下患儿的安全有剂量及用法尚未确定。
【不良反应】顺尔宁的一般耐受性良好,不良反应较轻微,通常不需中止治疗。
最常见的不良反应是头痛、偶有腹痛、咳嗽、流感样症状,儿童与成人的发生率相似。
【禁忌症】对本品的任何成分过敏者禁用。
【注意事项】①口服本药不应该用于治疗急性哮喘的发作,应劝告患者准备好必要的急救药品备用。
②虽然合用的吸入皮质类固醇制剂可在医师监督下逐渐减量,但不应骤然使用本品取代吸入或口服皮质类固醇制剂。

孟鲁司特片调研剂型:薄膜衣片规格:10mg申报类别:化药6类首家(进口: Merck Sharp & Dohme Ltd.)批准日期:1999年10月29日说明书:附后标准:附后新药保护:无专利情况:无1 01134866.6 孟鲁司特钠的制备方法及其制备中间体2 01136946.9 一种孟鲁司特钠的制备方法及其制备中间体3 02821212.6 孟鲁司特颗粒制剂4 200410057366.9 孟鲁司特钠的分散片剂型5 200510122973.3 孟鲁司特口腔崩解片制剂及其制备方法现生产厂家:四川大冢制药有限公司(片剂、咀嚼片)现申报厂家:孟鲁司特钠片孟鲁司特钠咀嚼片说明书[药品名称]通用名:孟鲁司特钠片/咀嚼片英文名:Montelukast Sodium Tablets/Chewable Tablets汉语拼音名:Menglusitena Pian/JuJue Pian化学名称:[R-(E)]-1-[[[1-[3-[2-[7-氯-2-喹啉]乙烯基]苯基-3-[2-(1-羟基-1-甲基乙基)苯基]丙基]硫]甲基]环丙烷乙酸单钠盐[性状]顺尔宁TM4mg和5mg为咀嚼片,10mg为薄膜包衣片。
[药理毒理]药理学半胱氨酰白三烯(LTC4、LTD4、LTE4)是由包括肥大细胞和嗜酸性粒细胞等多种细胞释放的具有强大炎性作用的二十烷类物质。
这些重要的哮喘前炎性介质能与在人类气道上发现的半胱氨酰白三烯受体(CysLT)结合,导致多种气道反应,包括支气管收缩、粘液分泌、血管通透性增加和嗜酸性粒细胞聚集。
孟鲁司特是一种能显著改善顺炎症指标的强效口服制剂。
生物化学和药理学的生物测定显示,孟鲁司特对CysLT1受体有高度的亲和性和选择性(与其它有药理学重要意义的气道受体如类前列腺素、胆碱能和β-肾上腺能受体相比)。
孟鲁司特能效地抑制LTC4、LTD4和LTE4与CysLT1受体结合所产生的生理效应而无任何受体激动活性。
孟鲁司特片调研剂型:薄膜衣片规格:10mg申报类别:化药6类首家(进口: Merck Sharp & Dohme Ltd.)批准日期:1999年10月29日说明书:附后标准:附后新药保护:无专利情况:无1 01134866.6 孟鲁司特钠的制备方法及其制备中间体2 01136946.9 一种孟鲁司特钠的制备方法及其制备中间体3 02821212.6 孟鲁司特颗粒制剂4 200410057366.9 孟鲁司特钠的分散片剂型5 200510122973.3 孟鲁司特口腔崩解片制剂及其制备方法现生产厂家:四川大冢制药有限公司(片剂、咀嚼片)现申报厂家:孟鲁司特钠片孟鲁司特钠咀嚼片说明书[药品名称]通用名:孟鲁司特钠片/咀嚼片英文名:Montelukast Sodium Tablets/Chewable Tablets汉语拼音名:Menglusitena Pian/JuJue Pian化学名称:[R-(E)]-1-[[[1-[3-[2-[7-氯-2-喹啉]乙烯基]苯基-3-[2-(1-羟基-1-甲基乙基)苯基]丙基]硫]甲基]环丙烷乙酸单钠盐[性状]顺尔宁TM4mg和5mg为咀嚼片,10mg为薄膜包衣片。
[药理毒理]药理学半胱氨酰白三烯(LTC4、LTD4、LTE4)是由包括肥大细胞和嗜酸性粒细胞等多种细胞释放的具有强大炎性作用的二十烷类物质。
这些重要的哮喘前炎性介质能与在人类气道上发现的半胱氨酰白三烯受体(CysLT)结合,导致多种气道反应,包括支气管收缩、粘液分泌、血管通透性增加和嗜酸性粒细胞聚集。
孟鲁司特是一种能显著改善顺炎症指标的强效口服制剂。
生物化学和药理学的生物测定显示,孟鲁司特对CysLT1受体有高度的亲和性和选择性(与其它有药理学重要意义的气道受体如类前列腺素、胆碱能和β-肾上腺能受体相比)。
孟鲁司特能效地抑制LTC4、LTD4和LTE4与CysLT1受体结合所产生的生理效应而无任何受体激动活性。
孟鲁司特钠咀嚼片(顺尔宁)的说明书关于《孟鲁司特钠咀嚼片(顺尔宁)的说明书》,是我们特意为大家整理的,希望对大家有所帮助。
如今每一个孩子全是父母的掌中宝,小孩得了儿科常见病也是每一个家中最不愿意见到的,因此医治儿科常见病是父母盆友势在必行要做的事儿。
因为小孩的身体素质弱于平常人,以便尽快确保小孩的身心健康,许多家中都是挑选用药治疗。
现阶段孟鲁司特钠咀嚼片(顺尔宁)是医治儿科常见病最好是的药品,下边我们来对孟鲁司特钠咀嚼片(顺尔宁)开展详尽的掌握吧。
生产药品名称疫苗通用性名字:孟鲁司特钠咀嚼片产品名称:孟鲁司特钠咀嚼片(顺尔宁)拼音字母全码:MengLuSiTeNaJuJiaoPian(ShunErNing)生产关键成分疫苗孟鲁司特钠。
生产性状疫苗本产品为淡粉色椭圆型片。
生产适用范围/功效与作用疫苗本产品适用儿童哮喘的防止和长期性医治,包含防止大白天和晚间的哮喘症状,医治对阿斯匹林比较敏感的哮喘病人及其防止健身运动造成的支气管炎收拢。
本产品适用缓解过敏性鼻炎造成的病症。
生产型号规格疫苗4mg*5s生产使用方法使用量疫苗每天1次。
哮喘病人应在临睡前用。
周期性过敏性鼻炎可依据本身的状况在需要時间吃药。
另外身患哮喘和周期性过敏性鼻炎的患者应每天晚上服药1次。
2-5岁哮喘和/或周期性过敏性鼻炎少年儿童病人每天1次,每一次1片(4mg)。
一般建议:以哮喘控制指标值来点评治疗效果,本产品的功效在服药一天内即出現。
本产品可与食材同屏或另服。
应建议病人不管在哮喘控制還是恶变环节都坚持不懈服食。
对肾功能不全病人、轻到中毒了肝损伤的病人及不一样性別的病人不用调节使用量。
本产品与其他哮喘治疗药品的关联:本产品可添加病人目前的治疗方案中。
降低合拼用药品的使用量:支气管炎扩张剂:单用支气管炎扩张剂不可以合理控制的哮喘病人,可在治疗方案中添加本产品,一旦有临床治疗反映(一般出現在首剂服药后),依据病人的承受状况,可将支气管炎扩张剂使用量降低。
孟鲁司特钠咀嚼片【通用名称】孟鲁司特钠咀嚼片【成份】主要成份为孟鲁司特钠。
化学名称:[R-(E)]-1-[[[1-[3-[2-(7-氯-2-喹啉)乙烯基]苯基]-3-[2-(1-羟基-1-甲基乙基)苯基]丙基]硫]甲基]环丙烷乙酸单钠。
【性状】本品为粉红色片。
【适应症】本品适用于2岁及2岁以上儿童和成人哮喘的预防和长期治疗,包括预防白天和夜间的哮喘症状,治疗对阿斯匹林敏感的哮喘患者以及预防运动诱发的支气管收缩。
本品适用于2岁及2岁以上儿童和成人以减轻季节性过敏性鼻炎引起的症状。
【规格】5mg*6片【用法用量】每日一次。
哮喘病人应在睡前服用。
季节性过敏性鼻炎病人可根据自身的情况在需要时服药。
同时患有哮喘和季节性过敏性鼻炎的病人应每晚用药一次。
15岁及15岁以上患有哮喘和/或季节性过敏性鼻炎的成人患者,每日一次,每次10mg。
6至14岁哮喘和/或季节性过敏性鼻炎儿童患者,每日一次,每次5mg。
一般建议以哮喘控制指标来评价治疗效果,本品的疗效在用药一天内即出现。
本品可与食物同服或另服。
应建议患者无论在哮喘控制还是恶化阶段都坚持服用。
【禁忌】对本品中的任何成份过敏者禁用。
【注意事项】口服本品治疗急性哮喘发作的疗效尚未确定。
因此,不应用于治疗急性哮喘发作。
虽然在医师的指导下可逐渐减少合并使用的吸入皮质类固醇剂量,但不应用本品突然取代吸入或口服皮质类固醇。
接受包括白三稀受体拮抗剂在内的抗哮喘药物治疗的患者,在减少全身皮质类固醇剂量时,极少病例发生以下一项或多项情况:嗜酸性粒细胞增多症、血管性皮疹、肺部症状恶化、心脏并发症和/或神经病变(有时诊断为Churg-Strauss综合症—一种系统性嗜酸细胞性血管炎)。
虽然尚未确定这些情况与白三稀受体拮抗剂的因果关系,但在接受本【特殊人群用药】妊娠与哺乳期注意事项:应在医师指导下使用。
【药物相互作用】本品可与其他一些常规用于哮喘预防和长期治疗及治疗季节性过敏性鼻炎的药物合用。
孟鲁司特钠药物机制、药物作用、超说明用药、不同制剂区别及用药注意事项孟鲁司特钠是治疗哮喘、过敏性鼻炎(AR)的常用药物,其用药安全性和临床疗效较满意。
肥大细胞、嗜酸性粒细胞、嗜碱性粒细胞内花生四烯酸通过5-脂氧酶途径生成半胱氨酰白三烯(CysLTs),使得LTC4、LTD4、LTE4 含量增高。
当LTC4、LTD4、LTE4 与CysLT1 受体作用,可致粒细胞趋化和气道炎症反应增加、支气管收缩。
图1 花生四烯酸代谢途径孟鲁司特钠是CysLT1 受体拮抗剂,可抑制LTC4、LTD4、LTE4 与CysLT1 受体的结合,减轻气道炎症反应。
具有抗炎、平喘的药理作用,适用于哮喘、AR 患者且对阿司匹林哮喘、运动性哮喘疗效较好。
超说明用药现状LTs 刺激 P 物质和速激肽的释放,与慢性咳嗽的发病关联密切。
孟鲁司特钠对上气道咳嗽综合征、鼻后滴流综合征所致慢性咳嗽具有一定临床疗效。
孟鲁司特可缩短咳嗽时间、降低咳嗽频率和严重程度;且用药者无严重药品不良反应发生。
哮喘、AR 和非哮喘性嗜酸性支气管炎者有受体上调表现,患者存在气道炎症反应,可减轻上述患者气道炎症、缓解临床症状。
孟鲁司特钠目前仅被批准用于哮喘、AR,用于UACS/PNDS,或者NAEB、PIC 患者,均属于超说明书用药。
目前国内医疗机构使用孟鲁司特钠多集中在慢性阻塞性肺疾病(COPD)、支气管炎、咳嗽等疾病。
推荐孟鲁司特钠用于咳嗽变异型哮喘引起的咳嗽可能有效,对于其他原因导致的咳嗽,未予推荐。
不同制剂区别咀嚼片中加入蔗糖、食用香料等辅料,可掩盖药物苦涩味,尤其适用于儿童等用药群体。
因此,孟鲁司特钠咀嚼片常用于咳嗽变异性哮喘(CVA)或AR 患儿。
咀嚼片需要在口腔嚼碎后再吞咽,对于崩解困难的片剂,制成咀嚼片可加快药物的崩解—溶解—吸收过程,缩短药物起效时间。
相比普通片剂,咀嚼片有一定剂型优势。
用药注意事项监护孟鲁司特钠的用药安全性。
孟鲁司特钠其耐受性良好、药品不良反应轻微。
孟鲁司特钠片服用方法孟鲁司特钠片是一种常用的降压药物,广泛应用于高血压、心绞痛等疾病的治疗。
正确的服用方法对药效的发挥起着至关重要的作用。
下面将介绍孟鲁司特钠片的正确服用方法,希望能够帮助患者正确使用这种药物,提高治疗效果。
1.服用时间。
孟鲁司特钠片通常建议在早晨服用,因为这个时间段对于降压药物的吸收和作用效果最好。
患者在服用孟鲁司特钠片时应该选择一个固定的时间,保持每天服药的时间一致,这样有助于提高药物的稳定性和疗效。
2.服用方式。
孟鲁司特钠片应该整片吞服,并且要搭配一定量的水一起服用。
患者在服用孟鲁司特钠片时应该避免将药片咀嚼或者压碎,以免影响药效的释放和吸收。
3.饮食注意。
在服用孟鲁司特钠片期间,患者应该避免食用高钠食物,如咸菜、腌制食品等,以免影响药效。
此外,应该避免饮酒,因为酒精会影响药物的代谢和吸收。
4.剂量调整。
患者在服用孟鲁司特钠片期间,应该严格按照医生的建议和处方来进行用药,不要随意增加或减少剂量,以免影响疗效和出现不良反应。
如果患者有任何不适或者疑问,应该及时咨询医生。
5.药物搭配。
在服用孟鲁司特钠片期间,患者应该避免与其他药物同时服用,特别是一些非处方药和保健品,以免发生药物相互作用,影响疗效。
总之,正确的服用方法对于孟鲁司特钠片的疗效至关重要。
患者在服用孟鲁司特钠片时应该严格按照医生的建议和处方来进行用药,避免随意更改剂量或者搭配其他药物。
同时,要注意饮食和生活习惯的调整,配合医生的治疗,才能达到最佳的治疗效果。
希望患者能够重视正确的用药方法,提高治疗效果,保障身体健康。
孟鲁司特钠片服用方法
孟鲁司特钠片是一种用于治疗高血压和心绞痛的药物,正确的
服用方法对于药效的发挥和身体健康都至关重要。
下面将为您详细
介绍孟鲁司特钠片的正确服用方法。
1. 服用时间,一般来说,孟鲁司特钠片建议在每天固定的时间
服用,最好是在早上或者晚上。
您可以根据自己的作息习惯来选择
一个固定的时间,以养成良好的服药习惯。
2. 服用方式,将孟鲁司特钠片整片吞服,并用一杯水送服。
如
果您对吞药有困难,可以将药片放在舌下,等待片剂溶解后再进行
吞咽。
3. 饭前或饭后,一般来说,孟鲁司特钠片可以饭前或饭后服用。
但是,为了最大限度地发挥药效,建议在饭后30分钟内服用,以减
少胃部不适的可能性。
4. 剂量调整,孟鲁司特钠片的剂量应根据医生的建议进行调整,切勿随意增减剂量。
如果您觉得当前的剂量无法控制病情,应及时
咨询医生,而不是自行调整剂量。
5. 持续服用,孟鲁司特钠片是一种长效药物,需要持续服用才
能发挥最佳的治疗效果。
即使症状好转或消失,也不应随意停药,
应按照医生的建议进行持续服用。
6. 注意事项,在服用孟鲁司特钠片期间,应避免饮酒和吸烟,
因为这些会影响药效。
同时,如果出现严重的副作用或者不良反应,应立即停药并就医。
总之,正确的孟鲁司特钠片服用方法对于治疗高血压和心绞痛
非常重要。
在服药期间,应严格按照医生的建议进行用药,并定期
复诊,以确保药物的疗效和身体的健康。
希望本文所介绍的内容能
够帮助您更好地使用孟鲁司特钠片,祝您早日康复!。
孟鲁司特钠咀嚼片说明书请仔细阅读说明书并在医师指导下使用药品名称】通用名称:孟鲁司特钠咀嚼片英文名称:Montelukast Sodium Chewable Tablets汉语拼音:Menglusitena Jujuepian【成份】本品主要成份为孟鲁司特钠。
化学名称:[R-(E)]-1-[[[1-[3-[2-(7- 氯-2-喹啉)乙烯基]苯基-3-[2-(1-羟基-1-甲基乙基)苯基]丙基]硫]甲基]环丙烷乙酸钠化学结构式:分子式:C35H35ClNNaO3S分子量:608.18【性状】本品4mg为粉红色圆角方形片,一面刻有“4字”样;5mg 为粉红色椭圆形片,一面刻有“5字”样。
【适应症】本品适用于2 岁至14 岁儿童哮喘的预防和长期治疗包括预防白天和夜间的哮喘症状治疗对阿司匹林敏感的哮喘患者以及预防运动诱发的支气管收缩。
本品适用于减轻过敏性鼻炎引起的症状(2 岁至14 岁儿童的季节性过敏性鼻炎和常年性过敏性鼻炎)。
规格】4mg(以孟鲁司特计);5mg(以孟鲁司特计)用法用量】每日一次。
哮喘病人应在睡前服用。
过敏性鼻炎病人可根据自身的情况在需要时间服药。
同时患有哮喘和过敏性鼻炎的病人应每晚用药一次。
6至14岁哮喘和/或过敏性鼻炎儿童患者每日一次,每次一片(5mg)。
2至5岁哮喘和/或过敏性鼻炎儿童患者每日一次,每次一片(4mg)。
一般建议以哮喘控制指标来评价治疗效果,本品的疗效在用药一天内即出现。
本品可与食物同服或另服。
应建议患者无论在哮喘控制还是恶化阶段都坚持服用。
肾功能不全患者、轻至中度肝损害的患者及不同性别的患者无需调整剂量。
孟鲁司特钠咀嚼片与其它哮喘治疗药物的关系本品可加入患者现有的治疗方案中。
减少合并用药的剂量:支气管扩张剂单用支气管扩张剂不能有效控制的哮喘患者,可在治疗方案中加入本品,一旦有临床疗效反应(一般出现在首剂用药后) ,根据患者的耐受情况,可将支气管扩张剂剂量减少。
吸入糖皮质激素对接受吸入糖皮质激素治疗的哮喘患者加用本品后,可根据患者的耐受情况适当减少糖皮质激素的剂量。
应在医师指导下逐渐减量。
某些患者可逐渐减量直至完全停用吸入糖皮质激素。
但不应当用本品突然替代吸入糖皮质激素或遵医嘱。
【不良反应】本品一般耐受性良好,不良反应轻微,通常不需要终止治疗。
原研孟鲁司特钠咀嚼片总的不良反应发生率与安慰剂相似。
6 至14 岁儿童哮喘患者已在大约475名6 岁至14岁儿童患者中进行了临床研究,评价了原研孟鲁司特钠咀嚼片的安全性。
总体上儿童患者使用原研孟鲁司特钠咀嚼片的安全性与成人相似,并与安慰剂接近。
在一项安慰剂对照为期8 周的临床研究中,原研孟鲁司特钠咀嚼片治疗组中与药物相关,发生率>1%且比安慰剂组高的唯一不良事件是头痛。
但头痛发生率在两组间无显著差异。
在评价对生长速率的影响的临床研究中,原研孟鲁司特钠咀嚼片所表现出儿童用药的安全性特征与以前的描述一致。
累积已有263 名6 岁至14 岁儿童患者使用原研孟鲁司特钠咀嚼片治疗至少3 个月、164名患者治疗6 个月或更长。
随着使用原研孟鲁司特钠咀嚼片治疗时间的延长,不良事件发生的情况无改变。
2 至5 岁儿童哮喘患者已在大约573 名2 岁至5 岁的儿童患者中评价了原研孟鲁司特钠咀嚼片的安全性。
在一项安慰剂对照为期12 周的临床研究中,原研孟鲁司特钠咀嚼片治疗组中与药物相关,发生率>1%且比安慰剂组高的唯一不良事件是口渴。
但口渴的发生率在两组间无显著差异。
累积已有426名2岁至5岁儿童患者使用原研孟鲁司特钠咀嚼片治疗至少3 个月,230名患者治疗6个月或更长,63名患者用药12个月或更长。
随着使用原研孟鲁司特钠咀嚼片治疗时间的延长,不良事件发生的情况无改变。
2 至14 岁季节性过敏性鼻炎儿童患者在一项为期2周的安慰剂对照临床研究中,已在280名2至14岁季节性过敏性鼻炎患者中评价了原研孟鲁司特钠咀嚼片的安全性。
每天晚间服用原研孟鲁司特钠咀嚼片一次的耐受性良好,不良反应发生率与安慰剂组类似。
在这项研究中,原研孟鲁司特钠咀嚼片治疗组的不良反应发生率低于1%,且未发现有与药物相关,发生率高于安慰剂组的不良反应。
临床实践的合并分析使用有效的自杀行为评估方法对41项安慰剂对照临床研究(35 项研究针对15 岁及以上患者;6 项研究针对6-14岁儿童患者)进行了合并分析。
在9929例服用原研孟鲁司特钠咀嚼片的患者和7780 例服用安慰剂的患者中,一例有自杀意念的患者服用了原研孟鲁司特钠咀嚼片。
任何一组均未出现完成自杀、自杀企图或针对自杀行为的预备行动。
针对46 项安慰剂对照临床研究(35 项研究针对15岁及以上的患者;11项研究针对3 个月至14 岁的儿童患者)进行了独立的合并分析,评估行为相关性不良事件。
在11,673 例服用原研孟鲁司特钠咀嚼片的患者和8827例服用安慰剂的患者中,行为相关性不良事件的发生率分别为2.73%和2.27%;比值比为1.12 (95% CI [0.93;1.36])。
这些合并分析中包含的临床试验没有特定设计自杀率或行为相关性不良事件的检查。
上市后的经验原研孟鲁司特钠咀嚼片上市使用后有以下不良反应报告:感染和传染:上呼吸道感染。
血液和淋巴系统紊乱:出血倾向增加、血小板减少症。
免疫系统紊乱:包括过敏反应的超敏反应、十分罕见的肝脏嗜酸性粒细胞浸润。
精神系统紊乱:包括攻击性行为或敌对性的兴奋、焦虑、抑郁、方向知觉丧失、注意力不集中、夜梦异常、幻觉、失眠、记忆损伤、精神运动过激(包括易激惹、烦躁不安和震颤)、梦游、自杀的想法和行为(自杀)、抽搐。
神经系统紊乱:眩晕、嗜睡、感觉异常/ 触觉减退及十分罕见的癫痫发作。
心脏紊乱:心悸。
呼吸,胸腔和纵隔系统紊乱:鼻衄;肺嗜酸性粒细胞增多症。
胃肠道紊乱:腹泻、消化不良、恶心、胰腺炎、呕吐。
肝胆紊乱:ALT和AST升高、十分罕见的肝炎(包括胆汁淤积性,肝细胞和混合型肝损害)。
皮肤和皮下组织紊乱:血管性水肿、挫伤、多形性红斑、结节性红斑、瘙痒、皮疹、史蒂文斯—约翰逊综合征/ 中毒性表皮坏死松解症、荨麻疹。
肌肉骨骼和结缔组织紊乱:关节痛、包括肌肉痉挛的肌痛。
肾和泌尿系统紊乱:儿童遗尿症(偶见)。
其他紊乱和给药部位情况:衰弱/ 疲劳,水肿,发热。
禁忌】对本品中任何成份过敏者禁用【注意事项】口服本品治疗急性哮喘发作的疗效尚未确定。
因此,不应用于治疗急性哮喘发作。
应告知患者准备适当的抢救用药。
虽然在医师的指导下可逐渐减少合并使用的吸入糖皮质激素剂量,但不应用本品突然替代吸入或口服糖皮质激素。
接受包括白三烯受体拮抗剂在内的抗哮喘药物治疗的患者,极少病例发生以下一项或多项情况:嗜酸性粒细胞增多症、血管性皮疹、肺部症状恶化、心脏并发症和/ 或神经病变(有时诊断为Churg-Strauss综合征——一种全身性嗜酸细胞性血管炎)。
这些情况有时与减少或停用口服糖皮质激素治疗有关。
虽然这些情况与白三烯受体拮抗剂的因果关系尚未确定,但建议对服用本品本品的患者加以注意并作适当的临床监控。
应告知苯丙酮尿症患者,4 mg和5 mg咀嚼片分别含有0.674和0.842 mg苯丙氨酸(阿斯巴甜的组分)。
孟鲁司特可能对驾驶和操纵机器的能力无影响或存在微小的影响。
然而,有个别嗜睡和头晕的报道。
据报道,服用原研孟鲁司特钠咀嚼片的成人、青少年和儿童患者可出现神经精神事件。
服用原研孟鲁司特钠咀嚼片的上市后报告包括兴奋、攻击行为或敌意、焦虑、抑郁症、定向力障碍、注意力障碍、梦境异常、幻觉、失眠、易怒、记忆缺陷、不安、梦游症、自杀念头和行为(包括自杀)、抽搐和震颤。
有关原研孟鲁司特钠咀嚼片的一些上市后报告的临床细节似乎与药物引起的效应一致。
服用原研孟鲁司特钠咀嚼片的患者有精神神经事件的报道(见不良反应)。
由于其他因素也可能导致这些事件,因此不能确认是否与原研孟鲁司特钠咀嚼片相关。
医生应与患者和/ 或护理人员探讨这些不良事件。
患者和/ 或护理人员应被告知,如果发生这些情况,应通知医生。
已知对阿司匹林敏感的患者在服用本品时应继续避免使用阿司匹林或非甾体抗炎药。
【孕妇及哺乳期妇女用药】无妊娠妇女研究资料,除非明确需要服药,孕妇应避免服用本品。
全球上市后经验显示,妊娠期间使用原研孟鲁司特钠咀嚼片后有罕见的新生儿先天性肢体缺陷的报道。
这些妇女中绝大部分在怀孕期间还使用了其他哮喘治疗药物。
本品的使用与这些事件的因果关系尚未建立。
尚不明确本品是否能从乳汁分泌。
由于许多药物均可从乳汁分泌,哺乳期妇女应慎用本品。
【儿童用药】已在6 个月至14 岁儿童中进行了安全性和有效性研究。
6 个月以下儿童患者的安全性和有效性尚未研究。
研究表明孟鲁司特钠咀嚼片不会影响儿童的生长速率。
【老年用药】不适用。
【药物相互作用】本品可与其它一些常规用于哮喘的预防和长期治疗及治疗过敏性鼻炎的药物合用。
在药物相互作用研究中,推荐剂量的本品不对下列药物产生有临床意义的药代动力学影响:茶碱、泼尼松、泼尼松龙、口服避孕药(乙炔雌二醇/炔诺酮35/1)、特非那定、地高辛和华法林。
甲状腺激素、镇静类安眠药、非甾体类抗炎药、苯二氮卓类药物和减充血剂:虽然没有进行额外的特定的相互作用研究,但原研孟鲁司特钠咀嚼片与临床研究中广泛使用的常见处方药物联用,没有临床不良相互作用的证据。
这些药物包括甲状腺激素、镇静类安眠药、非甾体类抗炎药、苯二氮卓类药物和减充血剂。
在合并使用苯巴比妥的患者中,孟鲁司特的血浆浓度-时间曲线下面积(AUC)减少大约40%。
由于孟鲁司特通过CYP 3A4、2C8和2C9代谢,因此孟鲁司特应谨慎与CYP、3A4、2C8 和2C9诱导剂(如苯妥英钠、苯巴比妥、利福平)同时服用,特别是儿童。
但是不推荐调整本品的使用剂量。
体外试验表明孟鲁司特是CYP2C8 的抑制剂。
然而,一项关于孟鲁司特和罗格列酮(一种主要通过CYP2C8 代谢的典型探测底物)药物相互作用的临床研究数据表明,孟鲁司特在体内对CYP2C8 没有抑制作用。
因此认为孟鲁司特不会对通过这种酶代谢的药物(例如:紫杉醇、罗格列酮、瑞格列奈)产生影响。
体外研究表明,孟鲁司特是CYP2C8、2C9和3A4 的底物。
一项涉及孟鲁司特和吉非贝齐(CYP2C8和2C8的抑制剂)药物间相互作用的临床研究证明,吉非贝齐能使孟鲁司特的全身暴露水平增加4.4倍,CYP3A4 的强效抑制剂——伊曲康唑,与吉非贝齐和孟鲁司特同时给药后不会进一步增加孟鲁司特的全身暴露水平。
在临床安全性研究中,使用了大于在成人中批准的10mg 剂量(例如连续22 周给予成人患者200mg/天的剂量,以及连续大约1 周给予患者量高为900mg/ 天的剂量),没有观察到有临床意义的不良事件,基于这样的数据,吉非贝齐对孟鲁司特全身暴露水平的影响被认为是不具有临床意义的。