高二化学有机化合物分类(1)
- 格式:ppt
- 大小:453.00 KB
- 文档页数:8


第三章认识有机化合物第一节有机化合物的分类(学案)【模块要求】1.从结构上认识有机化学、有机物的结构特点及含义。
2.初步了解有机物从结构上的两种分类方法3.掌握常见官能团的结构和名称。
【复习回顾】1.烷烃结构的特点:、、2.烃和烃的衍生物(1)烃:组成的有机化合物总称为烃(也叫碳氢化合物)。
(2)烃的衍生物:烃分子中的氢原子被所取代而生成的一系列化合物。
3.官能团:有机化合物中,化合物特殊性质的原子或原子团......。
4.碳架:在有机化合物中,碳原子互相连结成的链或环是分子的骨架,又称碳架。
5.杂原子:在有机化合物中,除C、H 原子以外的原子如N、O、S、P等称为杂原子。
6.我们学过的分类法有哪些?【学习过程】:一、按碳的骨架分类1.烃的分类:链状烃():烃分子中碳和碳之间的连接呈链状。
烃:分子中含有碳环的环状烃烃:分子中含有一个或多个苯环的一类碳氢化合物。
【温故知新】如何用树状分类法,给链烃分类?2.有机化合物分类:状化合物:化合物:化合物:①CH2=CH-CH=CH2②③④CH3CH2CHO ⑤⑥⑦CH3-CH2-CH2OH ⑧⑨⑩⑾⑿⒀烃【思考】下列合成过程:CH3CH3CH3CH2Cl CH3CH2OH CH3COOH其中CH3CH2Cl、CH3CH2OH、CH3COOH以上三者衍生物的性质各不相同的原因是什么呢?二、按官能团分类【思考】1.醇和酚的区别:(1)醇:羟基和基直接相连。
官能团:(2)酚:羟基和直接相连。
官能团:如: CH 3CH 2OH( ) ( ) ( ) ( )2.具有复合官能团的复杂有机物:官能团具有各自的独立性,在不同条件下所发生的化学性质可分别从各官能团讨论。
如: 具有三个官能团: ,所以这个化合物可看作 类, 类和 类。
【练习】1.下列说法正确的是( ) A .羟基跟链烃基直接相连的化合物属于醇类 B .含有羟基的化合物属于醇类C .酚类和醇类具有相同的官能团, 因而具有相同的化学性质D .分子内含有苯环和羟基的化合物都属于酚类 2.下列物质中不属于有机物的是( )A .氰化钠(NaCN )B .醋酸(CH 3COOH )C .乙炔D .碳化硅(SiC ) 3.按官能团的不同对下列有机物进行分类:( ) ( ) ( )( ) ( ) ( )4、请同学们根据官能团的不同对下列有机物进行分类。
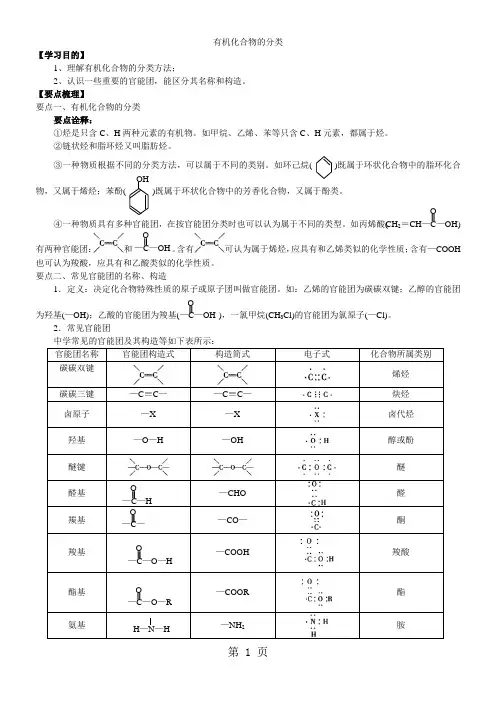
有机化合物的分类【学习目的】1、理解有机化合物的分类方法;2、认识一些重要的官能团,能区分其名称和构造。
【要点梳理】要点一、有机化合物的分类要点诠释:①烃是只含C 、H 两种元素的有机物。
如甲烷、乙烯、苯等只含C 、H 元素,都属于烃。
②链状烃和脂环烃又叫脂肪烃。
③一种物质根据不同的分类方法,可以属于不同的类别。
如环己烷 )既属于环状化合物中的脂环化合物,又属于烯烃;苯酚 )既属于环状化合物中的芳香化合物,又属于酚类。
④一种物质具有多种官能团,在按官能团分类时也可以认为属于不同的类型。
如丙烯酸( )有两种官能团:和 。
含有可认为属于烯烃,应具有和乙烯类似的化学性质;含有—COOH 也可认为羧酸,应具有和乙酸类似的化学性质。
要点二、常见官能团的名称、构造1.定义:决定化合物特殊性质的原子或原子团叫做官能团。
如:乙烯的官能团为碳碳双键;乙醇的官能团 为羟基(—OH);乙酸的官能团为羧基( ),一氯甲烷(CH 3Cl)的官能团为氯原子(—Cl)。
2.常见官能团中学常见的官能团及其构造等如下表所示:官能团名称 官能团构造式构造简式电子式化合物所属类别碳碳双键烯烃 碳碳三键 —C ≡C — —C ≡C —炔烃 卤原子 —X —X 卤代烃 羟基 —O —H—OH醇或酚 醚键醚 醛基 —CHO醛羰基—CO —酮羧基 —COOH羧酸酯基—COOR酯氨基—NH 2胺OHCH 2=CH —C —OHO—C —OH O —C —OH O—C —H O —C — O—C —O —HO—C —O —R OH —N —H要点诠释:①官能团是中性基团,不带电荷。
②官能团决定有机物的主要化学性质,但一样的官能团连接的方式和位置不同,化学性质也有所不同。
③分子中含有两种或两种以上的官能团时,该分子可能具有多方面的性质,假设多种官能团之间互相影响,又可能表现出特殊性质,如羟基与链烃相连时形成的是醇,而直接与苯环相连时形成的是酚。




高二化学有机化合物按官能团分类有机物可分为烯烃、醇、酚、醚、醛、酮等。
按官能团分类:醇、酚:羟基(-OH);伯醇羟基可以消除碳双键,酚羟基可以与NaOH反应产生水,与反应产生水NaHCO3.两者都能与金属钠反应产生氢气醛:醛基(-CHO);银镜反应可与斐林试剂反应氧化成羧基.加氢产生羟基.酮:基础(>C=O);它可以与氢加成形成羟基羧酸:羧基(-COOH);酸性,与NaoH反应产生水NaHCO3.反应产生二氧化碳硝基化合物:硝基(-NO2);胺:氨基(-NH2).弱碱性烯烃:双键(>C=C加成反应.炔烃:三键(-C≡C-)加成反应醚:醚键(-O-)醇羟基脱水可由醇羟基脱水形成磺酸:磺基(-)酸性,可替代浓硫酸腈:氰基(-CN)酯:酯(-COO-)羧基和羟基的水解产生,醇、酚和羧酸的反应产生注:苯环不是官能团,但苯基(-)在芳香烃中具有官能团的性质.苯基是过去的提法,但现在不认为苯基是官能团官能团:指决定化合物化学特性的原子或原子团.或称功能团.卤素原子、羟基、醛基、羧基、硝基以及不饱和烃中碳碳双键和碳碳三键都是官能团。
官能团在有机化学中起着以下五个作用.1.决定有机物的类型有机物的分类依据包括组成、碳链、官能团和同系物.烃类和烃类衍生物的分类依据不同,从以下两表可以看出.烃类分类方法:烃类衍生物分类方法:2.位置异构和类型异构产生官能团中学化学中有机物的同分异构有三种类型:碳链异构、官能团位置异构和官能团.对于类似的有机物,由于官能团的位置不同,同分异构是由官能团的位置异构引起的。
例如,以下8种氯乙烯异构反映了碳双键和氯原子的不同位置.对于相同的原子组成,形成不同的官能团,从而形成不同的有机物类别,即官能团的异构类型.例如,相同碳原子数的醛和酮、相同碳原子数的羧酸和酯都是由不同类型的异构引起的,由不同的官能团形成.3.决定一种或几种有机物的化学性质官能团决定了有机物的性质,-X、-OH、-CHO、-COOH、-NO2、-、-NH2、RCO-,这些官能团决定了卤代烃、醇或酚、醛、羧酸、硝基化合物或亚硝酸酯、磺酸、胺和酰胺的化学性质.因此,学习有机物的性质实际上是学习官能团的性质,含有官能团的有机物应具有官能团的化学性质,不含官能团的有机物不具有官能团的化学性质,这是学习有机化学时应该认识到的一点.例如,醛可以发生银镜反应,或被新的氢氧化铜悬浮浊度液氧化,可以认为这是醛的特征反应;但这不是醛的特性,而是醛的特性,因此,所有含有醛基的物质,如葡萄糖、甲酸和甲酸酯,都可以发生银镜反应,或被新制的氢氧化铜悬浮液氧化.4.影响其他基团的性质有机物分子中的基团之间存在相互影响,包括官能团对烃基的影响、烃基对官能团的影响以及含有多官能团的物质中官能团的相互影响.①醇、苯酚和羧酸的分子都含有羟基,所以氢可以通过钠释放,但由于连接的基团不同,酸性也不同.R-OH中性,不能和NaOH、反应;-OH酸性极弱,比碳酸弱,不能使指示变色,能与NaOH反应,不能反应;R-COOH弱酸性,具有酸的通性,能与酸相匹配NaOH、反应.很明显,羧酸中羧基中的碱的影响使羟基中的氢容易电离.②醛和酮都有基础(>C=O),然而,醛中的碱基碳原子与氢原子相连,酮中的氢原子与烃基相连,因此前者具有还原性,后者相对稳定,不被弱氧化剂氧化.③同一分子中的原子团也相互影响.如苯酚,-OH苯环容易取代(致活),苯基使用-OH显示酸性(即电离出H ).多羟基影响果糖中的碱基,可发生银镜反应.从上面可以看出,我们不仅可以通过有机物中所含的官能团来决定有机物的化学性质,还可以通过物质的化学性质来判断其所含的官能团.如果葡萄糖能发生银镜反应,加氢还原成六元醇,可以看出它有醛基;葡萄糖五乙酸酯可以酯化成酸,说明它有五个羟基,所以是多羟基醛.5.有机物的许多性质发生在官能团上有机化学反应主要发生在官能团上,所以要注意反应发生在什么键上,以便正确书写化学方程式.如果醛的加氢发生在醛基碳氧键上,氧化发生在醛基碳氢键上;卤代烃的替代发生在碳卤键上,消除发生在碳卤键和相邻碳原子的碳氢键上;醇的酯化是羟基中的O—H键断裂,取代就是C—O 键断裂;加聚反应是含碳双键(>C=C。


高二化学知识点大全有机物在高中化学中,有机物是化学知识中的一个重要部分。
有机物主要由碳元素构成,可以分为多个类型,如碳氢化合物、醇类、酮类等等。
下面将介绍一些高二化学中的有机物知识点。
一、碳氢化合物(烃类)碳氢化合物是由碳和氢元素构成的化合物,是有机化合物的基础。
根据碳原子之间的连接方式,碳氢化合物可以分为脂肪烃、环烃和烯烃等几种类型。
1. 脂肪烃:由碳原子形成直链或支链结构。
常见的脂肪烃有甲烷、乙烷、丙烷等。
脂肪烃是石油和天然气的主要组成部分,也是常见的燃料。
2. 环烃:由碳原子形成环状结构。
常见的环烃有环己烷、环丁烷等。
环烃在化学工业中广泛应用,如用于合成塑料和橡胶等。
3. 烯烃:含有至少一个碳-碳双键的烃类化合物。
例如乙烯是一种重要的烯烃,广泛应用于化学工业中。
二、醇类醇类是由氧原子连接到一个或多个碳原子上的有机化合物,通式为R-OH。
醇可以分为一元醇、二元醇、三元醇等多个类型。
1. 一元醇:醇分子中只有一个羟基(-OH)存在。
例如乙醇、甲醇等。
2. 二元醇:醇分子中有两个羟基存在。
例如乙二醇。
三、酮类酮类是由碳原子形成一个羰基(C=O)的有机化合物。
酮类的通式为R1-CO-R2,其中R1和R2可以是不同的有机基团。
四、醛类醛类是由碳原子形成一个羰基(C=O)和一个氢原子的有机化合物。
醛类的通式为R-CHO,其中R可以是不同的有机基团。
五、有机酸有机酸是由碳原子形成羧基(-COOH)的有机化合物。
常见的有机酸包括甲酸、乙酸等。
六、酯类酯类是由醇和有机酸反应生成的化合物。
酯类的通式为R-COO-R',其中R和R'可以是不同的有机基团。
七、氨基酸氨基酸是由一个氨基和一个羧基(-COOH)组成的化合物。
氨基酸是生物体内合成蛋白质的基本单位。
以上是一些高二化学中的有机物知识点介绍,有机物在日常生活中广泛存在,了解有机物的性质和应用对于学生学习化学和理解化学现象非常重要。
希望本文能为您提供有机物方面的基础知识,以便更好地理解和应用化学知识。


化学有机化合物化学有机化合物是由碳原子与氢原子和其他原子(通常是氧、氮、硫、磷等)通过共价键连接而成的化合物。
有机化合物是化学中一类重要的物质,广泛存在于生物体、石油和煤炭中。
一、有机化合物的分类有机化合物可以根据它们的结构特征和功能进行分类。
最常见的分类方法是根据碳原子的数目和结构类型。
1. 根据碳原子的数目,有机化合物可分为以下几类:a) 甲烷类化合物:只包含一个碳原子。
例如,甲烷(CH4)是最简单的有机化合物。
b) 乙烷类化合物:包含两个碳原子。
例如,乙烷(C2H6)是一种常见的有机化合物。
c) 烷烃类化合物:含有多个碳原子,所有碳原子通过单键连接。
例如,丙烷(C3H8)和正戊烷(C5H12)。
d) 烯烃类化合物:含有一个或多个碳-碳双键。
例如,乙烯(C2H4)是一种常见的烯烃。
e) 炔烃类化合物:含有一个或多个碳-碳三键。
例如,乙炔(C2H2)是一种常见的炔烃。
2. 根据结构类型,有机化合物可分为以下几类:a) 饱和化合物:所有碳原子都通过单键连接,没有含有双键或三键的碳原子。
例如,烷烃类化合物属于饱和化合物。
b) 不饱和化合物:至少有一个碳原子通过双键或三键连接。
例如,烯烃类和炔烃类化合物属于不饱和化合物。
c) 环状化合物:分子中存在一个或多个环状结构。
例如,环己烷(C6H12)是一种常见的环状化合物。
二、有机化合物的性质有机化合物具有许多独特的性质,包括物理性质和化学性质。
1. 物理性质:a) 沸点和熔点:有机化合物的沸点和熔点通常较低,因为它们之间的相互作用较弱。
但是,随着分子量的增加,这些性质也会增加。
b) 溶解性:许多有机化合物在非极性溶剂中较容易溶解,而在极性溶剂中溶解性较差。
例如,烷烃类化合物在非极性溶剂如正己烷中溶解度较高。
2. 化学性质:a) 燃烧:有机化合物通常是可燃的,可以与氧气反应生成二氧化碳和水。
例如,烷烃类化合物燃烧时会产生大量的热和光。
b) 氧化还原反应:许多有机化合物具有良好的氧化还原性质。