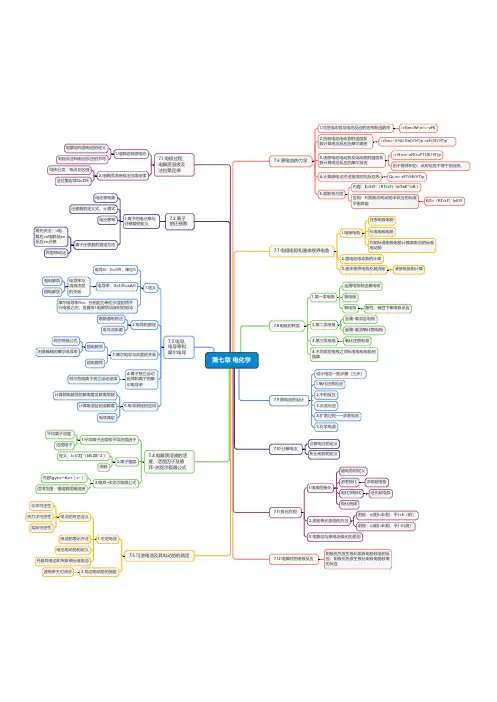
电化学原理和方法(张祖训,汪尔康著)思维导图
- 格式:xmin
- 大小:8.54 KB
- 文档页数:1





电毛细曲线的左支上dσ/dφ<0,故q>0,即电极表面荷正电。
右支上>0,故q<0,即电极表面荷负电。
在曲线最高点处有d
=0,相应的电势称为“零电荷电势”(φ0)。
用汞电极在不同无机盐溶液中测得的电毛细曲线在较负电势区基本重合,表示当电极表面荷负电时界面结构基本相同.但在较正电势区各曲线相差较大,表示当电极荷正电时界面结构与阴离子的特性有关。
零电荷电势的位置与所选用的阴离子有关
Cs分别等于电解池等效阻抗的电阻部分与电容部分时,整个电桥处于平衡状态.
用摘汞电极在不同无机盐溶液中测得的微分电容曲线见图。
与用电毛细曲线测得的结果相似,在电极电势较正的区域内界面微分电容的数值强烈依赖于阴离子的特性。
在无机盐稀溶液中测得的微分电容曲线上有一明显的极小值,其位置与稀溶液中的零电荷电势吻合。
1. 0.0001; 2.
0.001; 3. 0.01; 4. 0.1; 5. 1 (mol/L KCl)
的实验结果表明:分散层电容在总的双电层电容所
占的分量较小,特别是在那些远离零电荷电位的区间。
当电极表面电荷密度q和溶液浓度c都很小时,双电层中的
静电作用能远小于离子热运动能,即|ψ1|F<<RT。
所
由式可知,当相间电位| φa|的绝对值增大时,|ψ1| 也会增大,但
电极表面荷正电时,构成双电层溶液一例剩余电荷的阴离子水化程度较低.又能进行特性吸附,因而阴离子的水化膜遭到破
12
6r B r A U r +−
=exp(Ze U ψ=静电。




《电化学测试技术》课程教学大纲课程英文名称:Electrochemical Measurement Technology一、大纲使用说明(一)课程的地位及教学目标《电化学测试技术》是应用化学专业的一门核心专业基础课,其上承《物理化学》、《电化学原理》,下接《腐蚀与防护研究方法》、《化学电源》等课程。
通过《电化学测试技术》课程理论部分的学习,学生应该较为熟练地掌握电化学测试的基础知识、基本技能、方法,再通过实验课使学生加深电化学测试基本操作的理解和运用,为学生后续课程的学习、创新实验的进行及毕业设计打下基础。
(二)知识、能力及技能方面的基本要求1.知识方面的基本要求掌握三电极体系、电位测量的误差来源及精确测量的要求;掌握稳态研究方法、稳态过程的含义、特点,极化的种类及影响因素、控制电流法与控制电位法、稳态极化曲线测定、旋转圆盘电极及应用;掌握暂态过程的特点、等效电路的构成及其简化、控制电流与控制电位暂态测量方法;掌握线性电位扫描测试技术;掌握交流阻抗测试及阻抗谱分析技术。
2.能力方面的基本要求具备利用电化学测试手段研究、分析并解决涉及电化学工程与技术(如化学电源、腐蚀与防护等)等方面的实际问题的能力,如电化学方法测定金属材料在介质中的腐蚀速度、化学电源中粉末电极的电化学活性、涂料、涂层的耐腐蚀能力评价等。
3.技能方面的基本要求能够根据科研或生产实际要求,进行电化学测试设计、会使用电化学方法对所得结果进行分析与计算,掌握常规电化学测试仪器的使用方法。
(三)实施说明本教学大纲依据专业指导性教学计划制定,指导教学环节。
1.理论教学环节教学以课堂讲授为主,多媒体辅助教学。
对课程中的重点、难点问题着重讲解。
采用启发式、案例式教学,培养学生思考问题、分析问题和解决问题的能力;结合科研生产中的电化学测试实际例子对课程进行讲解,通过课堂讲解,加强学生对电化学原理基础知识与基本理论的理解。
通过少量作业调动学生学习的主观能动性,培养学生的自学能力。
模块复习一、《化学反应原理》核心知识结构图键能/kJ·mol—1436 946 393 298K时氮气跟氢气反应的热化学方程式正确的是A.N2(g)+3H2(g)===2NH3(g) △H=—104kJ·mol—1B.N2+3H2===2NH3△H=—104kJ·mol—1C.N2(g)+H2(g)===NH3(g) △H=+989kJ·mol—1D.N2(g)+3H2(g)===2NH3(g) △H=+989kJ·mol—1(二)盖斯定律的应用2.100g C不完全燃烧所得产物中,CO所占体积为1/3,CO2为2/3,且:C(s)+ 12O2(g)═ CO(g)△H = -110.35 k J·mol-1CO(g)+ 12O2(g)═ CO2(g)△H = -282.57 k J·mol-1与这些碳完全燃烧相比,损失的热量为A.39.292 kJ B.3274.3 kJ C.784.92 kJ D.2489.44 kJ(三)原电池的工作原理,书写化学电源的电极反应式,金属的电化学腐蚀3.关于原电池的叙述中,错误的是A.构成原电池正极和负极的必须是两种不同的金属B.原电池是将化学能转化为电能的装置C.在原电池中,电子流出的一极是负极,发生氧化反应D.原电池放电时,电流的方向是从负极到正极4.右图是2004年批量生产的笔记本电脑所用甲醇燃料电池的结构示意图。
甲醇在催化剂作用下提供质子(H+)和电子,电子经外电路、质子经内电路到达另一极与氧气反应,电池总反应为2CH3OH +3O2 =2CO2 +4H2O 。
下列说法正确的是:A.左电极为电池的负极,a处通入的物质是甲醇B.右电极为电池的负极,b处通入的物质是空气C.负极反应式为:CH3OH +H2O-6e—=CO2 +6H+D.正极反应式为:O2 +2H2O +4e—=4OH―5.以下现象与电化腐蚀无关的是A.黄铜(铜锌合金)制作的铜锣不易产生铜绿B.生铁比软铁芯(几乎为纯铁)容易生锈C.铁质器件附有铜质配件,在接触处易生铁锈D.银质奖牌长期放置后在其奖牌的表面变暗(四)电解原理及电极反应式的书写6.用铂作电极电解一定浓度的下列物质的水溶液。