宽城三中 课题2溶解度导学案
- 格式:docx
- 大小:105.84 KB
- 文档页数:4

第九单元课题2 溶解度(2)主备人:姚娟娟审核人:邱芳玉、马瑞丽班级姓名【学习目标】1、知道固体溶解度的概念及涵义;2、能根据固体溶解度的计算公式进行简单计算。
【自主学习】知识点:固体溶解度的概念及涵义【阅读】课本P36第一段文字,完成下列习题。
固体溶解度是指:在下,某固体物质在里达到状态时所溶解的质量。
通常所说的溶解度是指物质在里的溶解度。
强调:应用固体溶解度的概念时,必须注意“四要素”:①一个条件;②一个标准;③一个状态;④一个单位。
【讨论】在20℃时,硝酸钾的溶解度是31.6g,这句话的涵义。
【练习】氯化钾在30℃时的溶解度是37g,则此温度下配制得的饱和溶液中,溶质、溶剂、溶液三者间的质量比为________________。
【小结】在一定温度下,溶质在100g溶剂中形成的饱和溶液中,溶质的质(填“大于”、“等于”或“小于”)此时的溶解度(用S表示),此时饱和溶液的质量为。
【讨论】通过溶解度(S)可得知:此温度下该物质的饱和溶液中,溶质、溶剂和饱和溶液间的质量关系,即溶质、溶剂和饱和溶液三者的质量比为:(用S表示)。
【阅读】课本P36“资料”,回答:溶解性的大小跟溶质和溶剂的、、等有关。
【当堂训练】1、在60℃时,氯化钾的溶解度是45.5g。
此时氯化钾溶液中溶质质量g,溶剂质量g,溶液质量g,该溶液为(填“饱和”或“不饱和”)溶液。
2、下列关于溶解度的说法正确的是()A.100g水中溶解20gNaCl达到饱和状态,则NaCl的溶解度为20gB.在20℃时,把20gNaCl溶解在100g水中,所以20℃时,NaCl的溶解度为20g C.在20℃时,把20gNaCl溶解在水里制成饱和溶液,所以20℃时,NaCl的溶解度为20g D.在30℃时,100g水中最多能溶解37gNaCl恰好饱和,则30℃时NaCl的溶解度为37g 3、在60℃时,硝酸钾的溶解度为110g。
该温度下硝酸钾饱和溶液中有关质量关系正确的是()A.溶质质量:溶剂质量=1:10B.溶质质量:溶液质量=10:21C.溶剂质量:溶液质量=10:21D.溶液质量:溶质质量=21:104、60℃时,将某物质的饱和溶液12.5克,蒸干得到2.5克固体,则60℃时该物质溶解度为()A.25克B.20克C.20D.255、已知60℃时硝酸钾的溶解度为110g,60℃时将70g硝酸钾放入50g水中充分搅拌后,所得溶液的质量是()A.120g B.110g C.105g D.100g6、A、B、C、D四个烧杯分别盛有50g水,在相同的温度下,向四个烧杯中依次加入27g、9g、36g、18g的同种物质,充分溶解后的情况如图所示。

课题2 溶解度导学案(第二课时)〖情境导入、生成问题〗1. 复习提问:什么叫饱和溶液与不饱和溶液? 怎样区分?饱和溶液与不饱和溶液的相互转换?2.创设情境:我国有许多盐碱湖,湖水中溶有大量的氯化钠和纯碱,那里的农民冬天捞碱,夏天晒盐,你知道为什么吗?3.明确学习目标,解读目标。
为了准确表示一种物质在另一种物质里的溶解能力大小,定量地描述KNO3与NaCl在水中的溶解性强弱,我们可以用“溶解度”来表示。
〖自主探究、生成能力〗一、饱和溶液阅读课本P36理解溶解度概念的四个要素:①_________________;②_________________;③______________________;④________________________。
[交流讨论]“在20 ℃时,NaCl的溶解度为36.0 g。
”这句话所表达的含义是什么呢?。
[小结]1.;2.[活动与探究]:根据表9-1所提供的数据绘制几种物质在不同温度时的溶解度,即溶解度曲线[讨论交流]:教材中图9-121.溶解度曲线有何特点?2.从溶解度曲线图上找出上述几种物质在10℃、65℃时的溶解度?3.从图9-12中,你能比较出50℃时KCl、KNO3的溶解度大小吗?4.从溶解度曲线中,你能获得哪些信息?【小结】:通过溶解度曲线,(1)可以判断固体物质的溶解度受温度影响的变化情况;①;②;③。
(2)可以比较不同物质在时溶解度的大小;(3)也可以查出同一种物质在时的溶解度。
【交流讨论】课本P 381.打开汽水盖,汽水会自动喷出来。
说明气体在水中的溶解度与_________有关;2.喝了汽水后,常常会打嗝。
说明气体在水中的溶解度与____________有关;3.说汽水中冒出的气体为CO 2,你能用实验方法将其检验出来吗?【归纳总结】气体的溶解度受 和 的影响。
压强增大,气体溶解度 ,压强减小,溶解度 ;温度升高,气体的溶解度 。
【自主学习】阅读课本P 38“气体的溶解度”及P 39“资料”,了解气体物质的溶解度及在生活中的应用。

《课题2 溶解度》教案【教学目标】1.知识与技能(1)理解饱和溶液的涵义。
(2)了解溶解度涵义,初步学习绘制溶解度曲线和查阅溶解度曲线。
2.过程与方法(1)学习观察、分析实验现象,并能归纳出相应的概念。
(2)学习通过实验解决问题。
3.情感态度与价值观(1)认识矛盾的双方在一定条件下可以相互转化的辩证唯物主义思想。
(2)树立做任何事情都要实事求是的观点。
【教学重点】理解饱和溶液和溶解度的概念。
【教学难点】1.理解饱和溶液和溶解度的概念。
2.正确理解固体物质溶解度的概念。
【教学方法】实验、对比,归纳,练习、联系实际。
【教具准备】教师用具;投影仪。
学生用具;仪器:烧杯、玻璃棒、酒精灯、蒸发皿、药匙,天平、砝码、量筒、石棉网、铁架台、坐标纸。
药品;氯化钠、硝酸钾。
【课时安排】2课时【教学过程】第一课时[复习提问]什么叫溶液?溶液由什么组成?[学生活动][引入]我们知道食盐易溶于水而形成溶液,但在一杯水里能否无限地溶解食盐呢?[学生发言]1.能 2.不能[过渡]下面我们就以氯化钠和硝酸钾为例探讨这个问题。
[投影]活动与探究1.取装有20mL水的烧杯2.用硝酸钾代替氯化钠[学生活动,教师巡视][互相交流](由一组同学描述现象、结论,其他各组提出异议)[结论]1.在一定条件下,氯化钠不能无限溶解,当不能溶解时,加入水,又能继续溶解。
2.在一定条件下,硝酸钾也不能无限制溶解,当不能溶解时,升高温度,又能继续溶解。
[提问]上述活动的“一定条件”是什么?[学生讨论、总结]1.一定温度2.一定量的溶剂[追问]如果不指明这两个条件。
能否说某物质的溶解量是有限的?[学生讨论、回答]不能。
因为我们可以改变温度。
改变溶剂的量,使溶质无限制地熔解。
[引导]我们把一定条件下不能继续溶解溶质的溶液叫饱和溶液,相反。
还能继续溶解溶质的溶液叫不饱和溶液。
[思考]请大家根据刚才的分析,总结饱和溶液与不饱和溶液的科学概念。
[学生发言][投影板书]一、饱和溶液1.饱和溶液和不饱和溶液①饱和溶液:在一定温度下,在一定量的溶剂里,不能继续溶解溶质的溶液叫做(这种溶质的)饱和溶液。

课题2 溶解度(第1课时)【学习目标】1、饱和溶液与不饱和溶液概念在一定下,一定量的里,不能再溶解某种物质时,叫作这种物质....的溶液。
上述条件下,还能继续溶解某种物质的溶液,叫作这种物质....的溶液。
【特别提醒】某温度下,A物质的饱和溶液不能再溶解A物质,但却可以继续溶解B物质。
2、饱和溶液与不饱和溶液的转化3、结晶:晶体在溶液中形成的过程称为结晶。
(1)结晶方法:一般为两种,一种是结晶,另一种是结晶。
(2)结晶所经历的过程:不饱和溶液→饱和溶液→结晶(析出晶体)★受温度影响大.的物质采用降温结晶,受温度影响小.的物质采用蒸发结晶。
【特别提醒】★不饱和溶液一般降低温度可变成饱和溶液,但熟石灰是升高温度变成饱和溶液。
★不饱和溶液不一定是稀溶液,饱和溶液不一定是浓溶液。
★同一温度下,同一溶质的饱和溶液一定比不饱和溶液浓。
【当堂训练】1、饱和溶液是( )A.在一定量溶剂里,不能再溶解任何物质的溶液B.很浓的溶液C.不是稀溶液,也不是浓溶液D.一定温度下,在一定量的溶剂里,不能再溶解某种溶质的溶液2、一杯20℃的硝酸钾溶液,能证明它是饱和溶液的方法是( )A.蒸发5g水有固体析出B.加入少许的硝酸钾固体,不溶C.把溶液降温到10℃有固体析出D.以上方法都行3、把60℃的饱和硝酸钾溶液降温到20℃,下列说法中正确的是( )①溶液的质量不变②溶质的质量不变③溶剂的质量不变④仍是饱和状态A.①和②B.③和④C.①和③D.②和④4、(多选)欲使任意一种不饱和溶液转变为饱和溶液,最可靠的方法是( )A.升高温度B.降低温度C.加溶质D.蒸发5、将60℃的硝酸钾溶液降温至20℃,有晶体析出.有关该过程的说法错误的是()A.60℃时的溶液一定是硝酸钾的饱和溶液B.20℃时的溶液一定是硝酸钾的饱和溶液C.温度越高,硝酸钾在水中溶解得越多D.硝酸钾的晶体可采用降温结晶的方法得到6、保持温度不变,向一接近饱和的硝酸钾溶液中加入硝酸钾晶体,下列图像所反映的关系正确的是( )A. B. C. D.7、20℃时,50g水中溶解了18g氯化钠恰好成为饱和溶液。
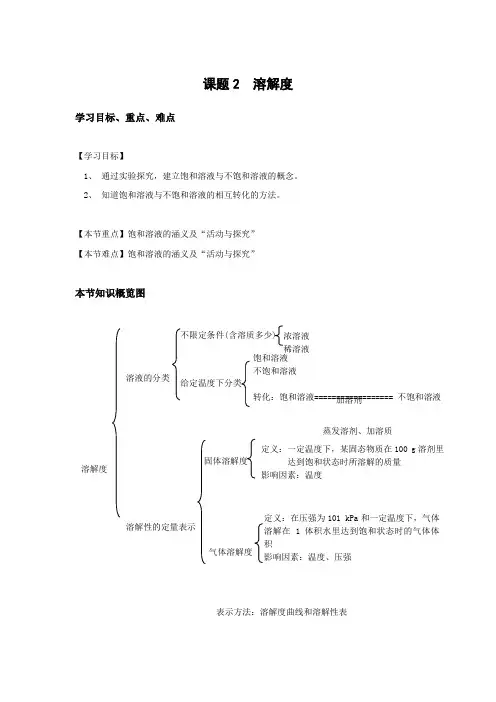
课题2 溶解度学习目标、重点、难点【学习目标】1、通过实验探究,建立饱和溶液与不饱和溶液的概念。
2、知道饱和溶液与不饱和溶液的相互转化的方法。
【本节重点】饱和溶液的涵义及“活动与探究”【本节难点】饱和溶液的涵义及“活动与探究”本节知识概览图溶解度溶液的分类不限定条件(含溶质多少) 浓溶液稀溶液给定温度下分类饱和溶液不饱和溶液转化:饱和溶液================== 不饱和溶液加溶剂蒸发溶剂、加溶质溶解性的定量表示固体溶解度定义:一定温度下,某固态物质在100 g溶剂里达到饱和状态时所溶解的质量影响因素:温度气体溶解度定义:在压强为101 kPa和一定温度下,气体溶解在 1体积水里达到饱和状态时的气体体积影响因素:温度、压强表示方法:溶解度曲线和溶解性表新课导引有这样一则谜语:“生在大海,走在岸边,太附一晒,身体全白.”请猜一生活用品.我们很容易猜到:食盐.为什么海水经太阳一晒,就变成食盐了呢?原来,海洋是一个巨大的宝库,海水里溶有大量的食盐、氯化钙、氯化镁等许许多多的物质.食盐这种物质的溶解度受温度的影响很小,所以,当水分蒸发的时候,它很容易从溶液中析出.这就是分离混合物的一种方法——蒸发结晶.不论是用海水晒盐,还是用盐湖水、盐井水来煮盐,都是利用食盐的溶解度受温度影响不大的性质,采用蒸发的方法得到食盐的.但是,这种方法得到的食盐含有许多杂质,叫做粗盐.粗盐经过溶解、过滤、蒸发、洗涤等步骤,就可以制得精盐了.你知道分离混合物的方法吗?物质能无限地溶解在水里吗?像食盐水这样的物质可采用蒸发溶剂法获得食盐,而KNO3溶液则应采用冷却热饱和溶液法使KNO3结晶出来;物质不能无限地溶解在水里,当温度不变时,一定量的水中所能溶解的某种物质的量是一定的.教材精华知识点1 饱和溶液√物质在水中的溶解物质不能无限地溶解在一定量的水中.探究实验【提出问题】物质能无限地溶解在一定量的水中吗?【设计实验】向盛有一定量水的烧杯中加入一定量氯化钠,搅拌,直至氯化钠溶解后,再加入氯化钠,搅拌,观察现象.然后再加入少量水,搅拌,观察现象.根据现象得出结论.【实验用品】烧杯、玻璃棒、药匙、蒸馏水、食盐等.【实验过程】向装有20mL水的烧杯中加入5 g氯化钠,搅拌,等氯化钠溶解后,再加5 g氯化钠,搅拌,观察现象,然后再加入10 mL水,观察现象(如图9-8所示).【解释与结论】 如下表所示.操 作加入5 g NaCl ,搅拌 再加入5 g NaCl ,搅拌再加入10 mL 水,搅拌现 象溶解部分溶解,烧杯底有未溶解的NaCl剩余NaCl 固体溶解 结 论溶解现象与溶质和溶剂的量有关,物质不能无限地溶解在一定量的水里探究实验【提出问题】 20 mL 水中加入一定量硝酸钾固体,固体未完全溶解,之后加热,硝酸钾能完全溶解吗?【设计实验】 硝酸钾能溶解于水中,向盛有一定量水的烧杯中分几次加入一定量硝酸钾,观察现象.待烧杯中有硝酸钾固体时,加热该烧杯,观察未溶解的硝酸钾是否溶解,冷却后再观察现象.根据现象得出结论.【实验用品】 带铁圈的铁架台、烧杯、酒精灯、玻璃棒、石棉网、硝酸钾固体、蒸馏水等.【实验过程】 用硝酸钾代替氯化钠进行上述探究实验,每次加入5 g 硝酸钾,看加几次后才使烧杯中的硝酸钾固体有剩余而不再继续溶解,然后加热烧杯,如图9-9所示,观察剩余固体有什么变化.再加入5 g 硝酸钾,搅拌,观察现象,待溶液冷却后,观察现象.【解释与结论】 如下表所示.操 作现 象结 论加入5 g 硝酸钾,搅拌 溶解①溶解的最大量与溶质的性质有关②溶解的最大量与温度有关再加5 g 硝酸钾,搅拌 溶解,但有硝酸钾固体剩余加热剩余的硝酸钾固体溶解再加5 g 硝酸钾,搅拌 硝酸钾固体有剩余冷却剩余的硝酸钾固体增多√饱和溶液与不饱和溶液的概念在一定温度下,向一定量溶剂里加入某种溶质,当溶质不能继续溶解时,所得到的溶液叫做饱和溶液;还能继续溶解的溶液,叫做不饱和溶液.√不饱和溶液与饱和溶液的转化某种溶质的饱和溶液与不饱和溶液之间可以相互转化,其过程可表示如下:不饱和溶液============饱和溶液√浓溶液与稀溶液为了粗略地表示溶液中溶质含量的多少,通常把溶液分为浓溶液和稀溶液,在一定量的溶液中,含溶质的量相对较多的叫浓溶液,含溶质的量相对较少的叫稀溶液. 网hslx3y3h √结晶的方法 (1)结晶.热的溶液冷却或溶剂的量减少后,已溶解在溶液中的溶质从溶液中以晶体的形式析出,这一过程叫做结晶. (2)结晶的两种方法. ①蒸发溶剂结晶.一般适用于在一定量水中溶解的最大量受温度影响变化不大的物质,如从海水中提取食盐,大致过程如下:②冷却热饱和溶液结晶.适用于在一定量水中溶解的最大量受温度影响变化较大的物质,如从KNO 3饱和溶液中得到KNO 3晶体,就可以用冷却热饱和溶液结晶的方法.知识点2 溶解度 √溶解度的概念溶解度表示在一定温度下,某固态物质在100 g 溶剂里达到饱和状态时所溶解的质量.如果不指明溶剂,通常所说的溶解度是指物质在水里的溶解度.增加溶质或降低温度增加溶剂或升高温度√准确理解溶解度概念的四要素(1)条件:“在一定温度下”.影响固体物质的溶解度的内因是溶剂和溶质的性质,而外因则是温度,如果温度改变,则固体物质的溶解度也会改变,因此,只有指明温度,溶解度才有意义.(2)标准:“在100 g溶剂里”.为了确定标准,人们规定“在100 g溶剂里”.需要强调和注意的是:100 g是溶剂的质量而不是溶液的质量,只有准确理解这个标准,才能正确应用溶解度的概念.(3)状态:“达到饱和状态”.溶解度表示的是同一条件下的某种物质的溶解能力的大小,只有达到该条件下溶解的最大值,才可知其溶解度,因此必须要求“达到饱和状态”.(4)单位:“溶解度表示……所溶解的质量”,通常用“克”作为单位.√溶解度的相对大小溶解度的相对大小,即固体溶解度与溶解性的关系如下表所示.表中的溶解度是指在20℃时的溶解度.√绘制溶解度曲线用纵坐标表示溶解度,横坐标表示温度,把一种或几种物质在不同温度时的溶解度标在图上,得到物质溶解度随温度变化的曲线,称为溶解度曲线(如图9-10和图 9-ll所示).√气体的溶解度(1)气体的溶解度的定义.气体的溶解度是指在压强为101 kPa和一定温度时,气体溶解在1体积水里达到饱和状态时的气体体积.如:压强为101 kPa和温度为0℃时,1体积水里最多能溶解0.024体积氮气,则在0℃时,氮气的溶解度为0.024.(2)气体溶解度的影响因素.①内因:气体和水的性质.②外因:温度和压强.课堂检测1.下列关于饱和溶液的说法正确的是()A.饱和溶液是不能再溶解溶质的溶液B. 饱和溶液不能再溶解任何溶质C.饱和溶液不能转化为不饱和溶液D.饱和溶液是指在一定温度下,一定量溶剂中,不能再溶解某种溶质的溶液2.室温下,向一定质量的NaCl溶液中加入l0 g NaCl固体,充分搅拌后,尚有部分固体未溶解,再加入10 g水后,剩余固体全部溶解.下列判断正确的是 ( )A.加水前一定是饱和溶液B.加水前可能是饱和溶液C.加水后一定是饱和溶液D.加水后可能是饱和溶液3.要使一杯氯化铵不饱和溶液变为饱和溶液,可采用的方法是()A.加水B.不断搅拌C. 升高温度D.加氯化铵晶体4.根据如图9—12所示信息判断,下列叙述不正确的是()A. 硝酸钾的溶解度随温度升高而增大B.t l℃时,氯化钠和硝酸钾的溶解度相同C. 将t2℃时的硝酸钾饱和溶液降温到t l℃,有晶体析出D.t2℃时,80 g硝酸钾溶于100 g水中可制得饱和溶液5. 喝了汽水以后常常要打嗝,如图9—13所示的曲线中能正确解释这一现象的是()6.图9-14是甲、乙两物质的溶解度曲线,以下说法正确的是()A.t1℃时甲、乙两物质的溶解度均为30 gB.甲物质的溶解度大于乙物质的溶解度C. 甲、乙两物质的溶解度受温度影响的程度相同D.t2℃时50 g的乙物质能完全溶解在100 g水中7.如图9-15所示的是甲、乙两物质的溶解度曲线,下列说法中错误的是()A.t1℃时,甲的溶解度小于乙的溶解度B.t2℃时,甲和乙的饱和溶液中含有溶质的质量相等C. 将t3℃的甲、乙两物质的饱和溶液降温到t2℃时都会析出D. 当甲中混有少量乙时,可采用冷却热饱和溶液的方法提纯甲8 .如图9—16L所示为甲、乙两物质的溶解度曲线.t1℃时,分别将20克甲、乙两种固体物质加入到盛有100克水的两个烧杯中,恰好完全溶解,升温到t2℃时出现Ⅱ所示的现象.则t2℃时烧杯中甲物质溶液的质量是克.体验中考1.图9-26是甲、乙两种固体物质的溶解度曲线.据此判断下列说法不正确的是()A.t2℃时,甲、乙的溶解度相等B.t3℃时,将60 g乙加入100 g水中可得160 g溶液C. 乙的溶解度受温度影响很小D.t1℃时,乙的溶解度大于甲的溶解度2 .图9-27是a、b两种固体物质的溶解度曲线.t1℃时,在两个烧杯中分别加入a、b两种物质各60 g后,再分别加入100 g水,充分搅拌.下列叙述正确的是 ( )A.在t1℃时,所得a、b两种物质的溶液均为饱和溶液B.在t2℃时,a、b两种物质的溶解度都是60C. 当温度由t1℃升高到t2℃时,两烧杯中的溶液所含溶质的质量相等D.当温度由t1℃升高到t2℃时,b物质的溶液中一定有固体析出3 .根据如图9-28所示的溶解度曲线判断,下列说法中正确的是()A. 甲物质的溶解度小于乙物质的溶解度B.t2℃时,甲物质的饱和溶液和乙物质的饱和溶液中含有溶质的质量相等C.将t3℃时的甲、乙两物质的饱和溶液降温到t2℃时都会析出晶体D.当甲物质中混有少量乙物质时,可采用冷却热饱和溶液的方法提纯甲4.图9-29是某实验小组的同学绘制的两种固体物质的溶解度曲线图.请你根据图示回答问题:(1)t1℃时,a物质的溶解度 b物质的溶解度 (填“>”、“<”或“=”).(2)将t2℃时a、b两种物质相同质量的饱和溶液,分别冷却到t1℃,析出晶体最多的是物质.(3)溶解度曲线图中的任何一点都表示溶液的一种特定状态.图中A、B两个状态中,溶液属于不饱和状态的是,状态最不稳定的是 .学后反思附:课堂检测及体验中考答案课堂检测1.答案: D2.答案: AD3.答案: D.4.答案: D.5.答案: B.6.答案: A.7.答案: B.8.答案:115体验中考1.答案: B.2.答案: C.3.答案: CD.4.答案:(1)< (2)a (3)B;A。

因素有和。
5.溶解度曲线表示,大部分物质的溶解度曲线
;少部分物质的溶解度曲线
课后练习
1.一杯20℃的氯化钠溶液,能证明它是饱和溶液的是()
A.蒸发10g水,有氯化钠晶体析出
B.降低温度,有氯化钠晶体析出
C.加入10g氯化钠晶体,仍有氯化钠晶体
D.在该温度下,加入少许氯化钠晶体,晶体质量不再减少
2..如图是甲、乙两种物质的溶解度曲线,下列说法不平确的是()
A.t1℃时,甲、乙两种物质的溶解度相等
B.甲物质的溶解度随温度的升高而增大
C.将t2℃时甲、乙两种物质的饱和溶液降温到t1℃,溶液仍然饱和
D.t1℃时,将50g甲物质加入100g水中,充分搅拌,能得到甲物质的饱和溶液
3.如图是甲、乙、丙三种物质的溶解度曲线,下列分析错误的是()
A.30 ℃时,把10 g丙溶解在50 g水中,得到丙的饱和溶液
B.50 ℃时,把甲、乙、丙三种溶液降温至10 ℃,析出晶体的质量由大
到小的顺序为:甲>丙>乙
C.将甲的饱和溶液变为不饱和溶液,可采用升高温度的方法
D. 30 ℃时,甲的饱和溶液的溶质质量分数约为23.1%。
课题2 溶解度(第1课时)导学案1.能从溶液形成的角度区分饱和溶液与不饱和溶液。
2.通过演示实验帮助学生理解饱和溶液与不饱和溶液相互转化的方法。
3.了解晶体及晶体的形成过程,理解海水晒盐的流程图及其原理。
4.通过学生的自主学习和教师分析使学生理解固体溶解度的概念并会解决一些简单问题。
5.知道溶解度与溶解性的关系。
学习重、难点:1.饱和溶液与不饱和溶液的概念及相互转化。
2.固体溶解度的概念、溶解度曲线的绘制及其主要外界影响因素。
学习过程:一 [知识链接]:通过上表你能回忆出什么叫溶液吗?它有哪些基本特征?2.现有6.5g锌与100g稀硫酸恰好完全反应。
(1)在100g稀硫酸中,溶质的化学式为,其质量为 g;溶剂的化学式为,其质量为 g.(2)完全反应后,所得溶液的质量为 g,其中溶质的化学式为,其质量为g;溶剂的化学式为,其质量为 g.二 [自主学习]:1. 在一定温度下,向一定量的溶剂里加入某种溶质,当溶质溶解时,所得到的溶液叫做这种溶质的饱和溶液;的溶液,叫做不饱和溶液。
2.饱和溶液和不饱和溶液的相互转化:()不饱和溶液饱和溶液()3.判断一种溶液是否饱和的方法:。
4.固体溶解度是指在下,某固态物质在 g溶剂里达到状态时所溶解溶质的。
5.固体溶解度的大小与溶解性的关系你的饭量有多大?一次能能无限制的吃饭吗?俗话说:“饭前喝汤,苗条漂亮;饭后喝汤,肥胖晃晃。
”妈妈在家为小槐同学准备了一碗汤,小槐一尝淡了,要妈妈加 (盐);小槐一尝还说淡了,又要妈妈加 (盐);小槐一尝还是说淡了,再要妈妈加 (盐)……食盐是我们熟悉的物质,它是否无限制地溶解在一定量的水中呢?[活动探究一]:在常温下,向装有20mL水的烧杯中加入5g氯化钠,搅拌,等氯化钠溶解后,再加5g,搅拌,观察现象。
然后再加入10mL水,搅拌,观察现象。
请同学们参阅33—34页并观察教师演示实验完成下列表格:用硝酸钾代替氯化钠进行上述实验,每次加入5 g:加了几次后才使烧杯中硝酸钾固体有剩余而不再继续溶解?然后加热烧杯,观察剩余固体有什么变化。

课题2 溶解度饱和溶液(第1课时)导学案班级姓名【预习】1、在一定下,向溶剂里加入某种溶质,当溶质继续溶解时,所得到的溶液叫做该溶质的饱和溶液,继续溶解的溶液,叫做该溶质的不饱和溶液。
2、饱和溶液与不饱和溶液在一定条件下是可以相互转化的,不饱和溶液通过、、方法可以转化为饱和溶液;饱和溶液通过、方法可以转化为不饱和溶液。
(对于大多数物质)3、溶质从溶液中以的形式析出得过程叫做结晶。
当晶体从饱和溶液中析出后,剩余的液体被称为母液,它通常是(填饱和溶液或不饱和溶液)。
从硝酸钾和氯化钠的结晶过程可以看出,结晶有两种方法即结晶和结晶。
4、生活中人们常根据溶液中溶质的多少,又可把溶液粗略地分为和。
【预习交流】(课前5分钟同桌互查并识记预习内容,找出问题集中处理)【学习目标】1、记住饱和溶液与不饱和溶液以及结晶的定义。
(重点)2、通过实验探究理解并记住饱和溶液与不饱和溶液相互转化得方法、结晶的方法(重难点)3、能说出饱和溶液与不饱和溶液的判断方法以及结晶现象。
【学习过程】实验探究:(动手做一做,以小组为单位做好记录)1、在常温下,向装有20ml水的烧杯中进行如下操作:2、32搅拌后静置,观察。
问题1:在描述饱和溶液与不饱和溶液时,你认为要明确哪些关键点?应如何判断一溶液为饱和溶液或不饱和溶液?问题2:对于大多数物质来讲,欲将不饱和溶液变为饱和溶液,你可采取哪些方法?你认为其中最可靠得方法有哪些?【讨论交流】(先自己独立完成,再与组内成员相互交流讨论)1、除去泥沙的粗盐中还含有氯化钙、氯化镁等杂质,可采用氯化钠得饱和溶液反复冲洗粗盐颗粒得方法来除去这些杂质,你能说说其中得道理吗?2、本节课我们学习得饱和溶液与不饱和溶液跟生活中常说得浓溶液与稀溶液有必然得联系吗?【达标检测】溶液在20℃时已达到饱和状态的叙述是()1、能证明某KNO3A. 温度不变时,向该溶液中加入少量水,溶质的质量分数变小晶体析出B. 取少量该溶液,降温到10℃时,有KNO3C. 取少量该溶液,升温后无KNO晶体析出3D. 温度不变时,向该溶液中加入少量KNO晶体,晶体不再溶解32、将某温度下的KNO3饱和溶液转化为不饱和溶液,下列方法可行的是()A.加入KNO3晶体 B.加水 C.降温 D.恒温蒸发水分3、下列关于饱和溶液的说法中,错误的是()A.在温度不变时,KNO3饱和溶液不能再溶解KNO3晶体B.改变条件可以使不饱和溶液变成饱和溶液C.室温下,与固体溶质共存的溶液一定是这种溶质的饱和溶液D.在温度升高时,某物质的饱和溶液一定能继续溶解该物质4、在20℃时,100g某溶液真发掉15g随后,析出晶体1g。

课题2 溶解度教学目标1.知识与技术(1).了解饱和溶液的涵义。
(2).了解溶解度的涵义,初步学会绘制和查阅溶解度曲线。
2.进程与方式:运用科学探讨的方式理解饱和溶液与不饱和溶液的涵义,并通过实验探讨了解“饱和”与“不饱和”的相对性。
3.情感态度与价值观通过溶解度的学习,让学生关注与溶解度有关的日常现象,如:鱼池缺氧和增氧等,感受化学对改善生活和增进社会发展的踊跃作用。
教学重难点重点:成立饱和溶液和溶解度的概念难点:溶解度概念的形成。
教学准备:药品:NaCl(s)、KNO3(s)、H2O(l)仪器:烧杯、玻璃棒、药匙、量筒相关课件及幻灯片教学方式:讲解法、讨论法、探讨学习法、合作学习法课时建议:2课时教学进程:板书设计课题二溶解度第一课时一、饱和溶液1.饱和溶液:在必然温度下,向必然量的溶剂里加入某种物质,当溶质不能继续溶解时,所取得的溶液叫饱和溶液。
2.饱和溶液和不饱和溶液的彼此转化:增加溶质或降低温度或蒸发溶剂不饱和溶液饱和溶液增加溶剂或升高温度第二课时二、溶解度1.概念:在必然温度下,某固态物质在100g溶剂里达到饱和状态时所能溶解的质量。
必然温度下100g水中2.溶解度四要素:达到饱和状态时溶解的质量3.解度曲线的意义:(1).溶解度的三种情况:A.大多数物质的溶解度随温度的升高而增大,如:KNO3。
B.少数物质的溶解度受温度的影响不大,如:NaCl。
C.极少数物质的溶解度随温度的升高而减小,如:Ca(OH)2(2).交点P表示:在该温度下,A、B两种物质的溶解度相等。
(3).影响固体物质的溶解度的因素是:温度。
4.气体的溶解度:气体的溶解度是指在压强为101KPA和必然温度时,气体溶解在1体积水里达到饱和状态时的气体体积。
影响气体溶解度的因素是:温度和压强。
附:课堂练习1.要使一瓶接近饱和的溶液转变成饱和溶液,最靠得住的方式是()A.升温B.降温C.加溶质D.倒出一些溶液2.下列因素中,固体物质的溶解度与其无关的是()A.溶质的性质B.溶剂的性质C.温度高低D.溶液的质量3.从冰箱里掏出含有蔗糖固体的溶液A,放置一段时间后,固体慢慢消失,形成溶液B。

课题2溶解度〔第3课时〕教学案班级:初三〔〕姓名:学科:化学课型:新授编者:备课组【学习目标】1、学会使用溶解度曲线。
2、知道结晶有蒸发结晶、降温结晶和升温结晶三种途径。
3、理解气体溶解度的概念,知道影响气体溶解度的因素【学习重点】学会使用溶解度曲线。
【学习难点】合理选择结晶方法。
【学习过程】一、复习〔检查自我,我沉着!〕1、7.“20℃时KClO3的溶解度为〞,它表示〔〕A.20℃时100g KClO3饱和溶液中含KClO3gB.20℃时,KClO3在水中溶解,溶液到达饱和状态C.100g水最多溶解KClO3D.20℃时,100g水溶解KClO3时,溶液到达饱和状态2、以下说法中正确的选项是〔〕A.在100g水里最多能溶解36g食盐,所以食盐的溶解度为36gB.所有固体物质的溶解度都随着温度的升高而增大C.有过剩溶质存在于其中的溶液,一定是这种物质在该温度时的饱和溶液D.20℃时100g水里溶解了30gKNO3,所以KNO3的溶解度是30g3、在20℃时,食盐的溶解度是36g。
在20℃时,向50g水中参加20g食盐,形成的溶液是溶液〔填“饱和〞或“不饱和〞〕,溶质质量是 g,溶液质量是 g。
二、先学〔充实自我,我自强!〕〔六〕气体溶解度1、讨论:①为什么汽水翻开后产生气泡,而不翻开时没有?②为什么烧开水时,水未开时就看到水中冒气泡?③夏天,阵雨来临之前,鱼塘里的鱼常会出现“浮头〞现象,你知道为什么吗?假设你承包了这个鱼塘,你将采取哪些措施?2、知识架构:〔1〕气体溶解度:某气体在千帕,一定时,溶解在体积水里到达状态时的气体。
[例2]在0 ℃时,氮气的溶解度为0.024,那么在千帕, ℃时,1升水中最多能溶解氮气。
〔2〕影响因素:气体溶解度随压强的增大而,随温度的升高而。
三、后教〔完善自我,我能行!〕结合教材中图9-12的溶解度曲线,海水晒盐和课题1中硝酸钾的实验进行讨论:⑴利用溶解度曲线,试分析对应的结晶方法。
课题2 溶解度第一课时导学目标知识点:1.饱和溶液与不饱和溶液的概念2.饱和溶液与不饱和溶液相互转化方法3.结晶的概念4.判断溶液是饱和溶液的方法课时:2课时导学方法:学生阅读→教师总结→问题讨论→讲解总结→随堂练习→稳固提高导学过程:一、课前导学:学生预习并完成相关概念:饱和溶液:不饱和溶液:二、课堂导学:1.提问:物质能不能无限制地溶解在一定量的水中呢?2.活动与探究〔1〕取装有20ml水的烧杯〔2〕用硝酸钠代替氯化钠〔学生根据实验现象进行讨论〕归纳总结:叫做饱和溶液,叫做不饱和溶液。
结晶:3.判断某溶液是否饱和的方法:在一定条件下,溶质是否继续溶解4.饱和溶液与不饱和溶液的相互转化增加溶质或降低温度不饱和溶液饱和溶液增加溶质或升高温度[随堂练习]1.如何判断某一蔗糖溶液是否饱和?2.在一定温度下,向100g食盐饱和溶液中参加3g食盐,充分搅拌后,溶液的质量变为103g,此说法是否正确,为什么?3.“在一定量的氯化钠溶液中,参加少量硝酸钾固体,发现硝酸钾固体消失,那么说明原氯化钠溶液不饱和〞,这句话是否正确?教师引导,学生自我小结:课堂练习:1.要使一杯氯化铵不饱和溶液变为饱和溶液,可采取的方法是〔〕A.加水 B.不断搅拌C.升高温度 D.加氯化铵晶体2.在其他条件不变的情况下,将不饱和溶液变为饱和溶液,最简便且可靠的方法是〔〕A.升高温度 B.降低温度C.参加溶质 D.减少溶剂课外练习:1.在其他条件不变的情况下,向一定量的饱和溶液中参加少量硝酸钾晶体,那么此饱和溶液的质量〔〕A.增加 B.不变 C.减小 D.无法确定2.以下有关溶液的说法错误的选项是〔〕A.碘酒中的溶质是酒精B.改变条件,饱和溶液与不饱和溶液可相互转化C.氢氧化钙的饱和溶液一定是浓溶液D.析出晶体后的溶液是该温度下的饱和溶液3.天热的时候把半杯糖水〔蔗糖已全部溶解〕放进冰箱的冷藏室,过一段时间后发现杯底出现了局部蔗糖晶体。
宽城三中九年级化学导学案主备人:周建华审核人:裴庆敏课题2 溶解度第1课时饱和溶液与不饱和溶液学习目标:1.能区分饱和溶液与不饱和溶液。
2.理解饱和溶液与不饱和溶液相互转化的方法。
3.了解晶体及晶体的形成过程,理解海水晒盐的流程图及其原理。
自主学习一、饱和溶液与不饱和溶液1、定义:在一定________下,向一定量的_________里加入某种溶质,当溶质_______继续溶解时,所得到的溶液叫做这种溶质的___________溶液,________继续溶解的溶液,叫做这种溶质的_________溶液。
注意:(1)描述饱和溶液、不饱和溶液时,必须注明_____________、_____________(2)饱和溶液是指条件不变时(填“能”或“不能”)继续溶解该溶质,而(填“可能”或“不可能”)继续溶解其他溶质。
如某温度下的氯化钠的饱和溶液只是不能继续溶解________,还可以溶解______________等溶质。
2、判断方法:(1)观察法:当溶液底部有剩余溶质存在,且溶质的量不在减少时,表面溶液已经饱和。
(2)实验法:向该溶液中加入_______________________,搅拌后,若能溶解,是______溶液,若_____ 溶解,是_______溶液。
3、相互转化:()不饱和溶液饱和溶液()注:①Ca(OH)2和气体等除外,它的溶解度随温度升高而降低②最可靠的方法是:加溶质、蒸发溶剂4、饱和溶液与浓溶液:饱和溶液_________是浓溶液,不饱和溶液_________是稀溶液,如饱和的石灰水溶液就是稀溶液。
在一定温度时,同一种溶质的饱和溶液要比它的不饱和溶液______.练习:1.在一定的和里还(填“能”或“不能”)继续溶解某种溶质的溶液叫做不饱和溶液,而在一定的和里还(填“能”或“不能”)继续溶解某种溶质的溶液叫做饱和溶液。
2.在一个大萝卜上挖个坑,向其中注入饱和食盐水,一定时间后将食盐水倒出,在相同的温度下,发现倒出的溶液还能溶解少量的食盐,这说明倒出的溶液()A.是饱和溶液B.是不饱和溶液C.氯化钠溶解度升高D.氯化钠溶解度降低3.t℃时,有一杯接近饱和的硝酸钾溶液,下列做法一定不能使其变为饱和溶液的是()A.蒸发溶剂B.降低溶液的温度C.向溶液中加入硝酸钾D.向溶液中加入t℃的饱和溶液4如图所示,在室温下的饱和食盐水中放了一个塑料小球。
(1)现加入少量食盐晶体,充分搅拌和静置后,在温度不变的情况下,小球在液面沉浮情况有何变化,并简叙原因:_______________________________________________________。
(2)若要在不用外力的情况下使小球略上浮,你准备采取的具体方法是:______________________________________________________。
6.A、B、C、D四个烧杯中分别盛有相等质量的水,在温度相同的条件下,向四个烧杯中分别加入20 g、15 g、10 g、5 g某物质,充分溶解后观察到如图所示的现象.请完成下列问题:(1)在A、B、C、D四个烧杯中,_________中一定是饱和溶液,_________中的可能是饱和溶液,_________中的一定不是饱和溶液.(2)四个烧杯中的溶液的溶质质量分数(浓度)最大的是_________.(3)若固体是KNO3,对盛有一定是饱和溶液的烧杯加热,随着温度升高,先变成不饱和溶液的是_________.(4)在一定温度下,往A、B中加入相同质量的水,B中固体刚好溶解,A中固体能否全部溶解?_________.(填能或不能)二、结晶1、定义:饱和溶液中的_______以_______的形式析出,这一过程叫做结晶。
这一过程属于变化(填“物理”或“化学”),而析出的固体叫做。
结晶后的溶液一定是_________溶液。
2、方法:(1)________________,如海水晒盐。
(2)___________________________________,如饱和的硝酸钾溶液中有晶体析出。
3、海水晒盐(1)通过该流程图你能分析出海水晒盐的原理是,该过程属于变化(填“物理”或“化学”)。
(2)根据生产过程推断,①、②分别是池和池。
(3下列说法中,错误的是( )A.在甲步骤中,海水的成分基本不变B.①中,氯化钠溶液由不饱和逐渐变为饱和溶液C.进入②后,继续蒸发水,有结晶现象发生D.析出食盐晶体后的母液是不饱和溶液练习:1、利用海水来制盐的原理是()A.通过化学反应,产生沉淀而制食盐B.升高温度,降低食盐在水中的溶解度C.利用阳光、风力蒸发水分使食盐析出D.降低温度,减小食盐的溶解度2、如图是对20℃一定质量的甲的溶液进行恒温蒸发的结晶实验过程,请回答:(1)蒸发前原溶液是________(填“饱和”或“不饱和”)溶液,n的数值是________.(2)依据实验,你认为甲的溶解度随温度变化的趋势是________(填字母)的.(A)随温度升高而增大(B)随温度升高而减小(C)无法判断.第2课时 溶解度学习目标:1、了解溶解度的含义。
2、初步学会绘制和分析溶解度曲线。
自主学习一、 固体溶解度1. 定义:在_____________下,某固态物质在_________溶剂里达到__________时所溶解的_________. 注意:固体溶解度四要素:(1)一定_________下。
(2)__________溶剂中。
(3)达到____________。
(4)单位是___________。
★ 说明:(1)如果不指明溶剂,溶剂就是水。
固体物质的溶解度实际上是某温度下 水中最多能溶解的 的质量。
(2)比较溶解必须在同一温度下。
练习:(1)20℃时,氯化钠的溶解度为36g .对这句话理解错误的是( )A. 20℃时,100g 水中最多能溶解氯化钠36gB. 20℃时,100g 氯化钠饱和溶液中含氯化钠36gC. 20℃时,氯化钠饱和溶液中水与氯化钠的质量比为100:36D. 20℃时,将36g 氯化钠溶解于100g 水中,所得溶液为该温度下氯化钠的饱和溶液(2)10℃时,50g 水里最多溶解甲物质10g ,20℃时,100g 水里最多溶解乙物质20g ,则甲乙两物质的溶解度是 ( ) A.甲大于乙 B.甲等于乙 C.甲小于乙 D.无法比较2. 含义: 如20℃时NaCl 的溶液度为36g 含义____________________________________________________3.影响因素:①____________________ ②_______________(1)大多数固体物的溶解度随温度升高而升高;如KNO 3(2)少数固体物质的溶解度受温度的影响很小;(3)极少数物质溶解度随温度升高而降低。
如Ca(OH)25.(1)点:溶解度曲线上的任何一点所表示的都是某溶质在该温度下的溶解度,其溶液为饱和状态。
(2)交点:不同溶解度曲线的交点所表示的是不同的溶质在该温度下的溶解度相同。
(3)线:溶解度曲线的走势表示的是某溶质的溶解度受温度变化的情况;曲线的陡度可判断溶解度受温度影响的大小。
(4)面:曲线下方面积上的任何一点表示在某温度下该溶液处于不饱和状态;曲线上方面积上的任何一点表示在某温度下该溶液处于饱和状态(即有未溶解的溶质)。
《解度曲线的应用》(1)t3℃时A的溶解度为_________, P点的的含义________________________________________________ (2)通过该曲线你发现固体溶解度受温度响的趋势有:A:B:C:(3)N点为t3℃时A的__________溶液,可通过_______________________________方法使它变为饱和.(4)t1℃时A、B、C、溶解度由大到小的顺序___________________。
大A溶解度的方法是,增大C溶解度的方法是。
(5)从A溶液中获取A晶体可用__________________的方法获取晶体。
(6)从B的溶液中获取晶体,适宜采用_________________ 的方法获取晶体(7)t2℃时A、B、C的饱和溶液各W克,降温到t1℃会析出晶体的有_____________,无晶体析出的有_______________.(8)除去A中的泥沙用____________法;分离A与B(含量少)的混合物,用___________法.(9) t3℃时配置等质量的三种饱和溶液_______需要的水最少,______需要的水最多。
(10)在t3℃时,将38克、40克、42克a物质分别放入50克水中搅拌形成溶液的质量分别为克,克,克;溶液饱和情况分别为,,。
(11)为了使A物质的不饱和溶液转化为饱和溶液可采用的方法是;而为了使C物质的不饱和溶液转化为饱和溶液可采法是 ______ 。
二、气体溶解度1、定义:指该气体在压强为__________和一定________时,在_________水里溶解达到_______状态时的气体_________.2、含义:例如:0℃时,氧气的溶解度为0.049的含义是___________________________________________3、影响因素:(1)__________(气体的溶解度随______的升高而_______)(2)__________(气体的溶解度随______的增大而_______)练习:1、加热冷水时,当温度尚未达到沸点时,为什么水中常有气泡冒出?天气闷热时,鱼塘的鱼为什么总是接近水面?2、气体的溶解度也有一定的变化规律.(1)打开可乐瓶,逸出大量气泡.由此可见,压强越小,CO2的溶解度越_________.为增大CO2的溶解度,可采用的一种方法是___________________________.(2)不同温度下,氧气的溶解度随压强的变化如图所示,图2中t j对应的温度为40℃,则t2对应的温度____ (填编号).a.大于50℃b.小于50℃c.无法确定.。