“硫在氧气中燃烧”实验的改进
- 格式:ppt
- 大小:219.50 KB
- 文档页数:9

硫在氧气中燃烧实验改进的探究南宁市邕宁区那楼中学玉小艳一、实验目的硫在氧气中燃烧实验是氧气重要性质的实验之一。
但是硫燃烧生成二氧化硫是污染物,课本上的教师演示实验是需要在通风橱内进行的。
我们农村学校没有见过通风橱,为了减少演示实验时二氧化硫的污染,特别是在空气中燃烧所产生的二氧化硫。
所以才对这个实验进行了微改进。
网络上已经有很多对该实验的改进,有的改进为密闭容器中进行,但是装置变得复杂,操作也不简便,成功率很低。
所以我本次改进试着从实验的微型化入手,以图减少对环境的污染,同时也可以利用身边的废物进行再利用。
二、实验仪器及试剂1.实验仪器集气瓶、橡胶塞、废旧饮用水瓶、燃烧匙、酒精灯、火柴、滤纸、大烧杯、药匙。
2.实验药品硫粉、NaOH溶液、氧气、水。
三、实验仪器装置图及仪器的组装说明1.仪器装置图(见附图)2. 组装说明先将废旧的1.555升的饮用纯净水瓶按比例从瓶口下部分剪开(瓶口到裁剪处要比集气瓶高出2-3厘米)。
找出一个合适该瓶口的橡胶塞,打孔,插入燃烧匙。
调整高度(滤纸要放置在集气瓶口),再拿出燃烧匙在燃烧匙杆上插入3-5层的厚滤纸(滤纸先按瓶子大小裁剪好)。
最后把燃烧匙组装在已经剪好的废旧瓶口上。
为了方便加入药品,可在燃烧匙药勺处剪开塑料瓶,等加入药品后再封上。
四、实验操作部分(教学过程)1.收集一瓶氧气,注意先在集气瓶内加入少量氢氧化钠溶液(约占集气瓶总体积的1/8)。
2、在大烧杯中加入少量的水,同时把收集好氧气的集气瓶放在大烧杯中。
往滤纸中滴加氢氧化钠溶液(要加入足够的氢氧化钠溶液,使之能更好的吸收二氧化硫)3、将塑料瓶剪开处打开,加入药品,封好。
点燃酒精灯加热药品,等硫燃烧后观察现象。
再慢慢的伸入氧气瓶中,观察现象并与氧气中现象相比较。
4、最后液封起来,防止二氧化硫泄露污染空气。
五、装置改进的意义装置简单,并且实验中现象明显,并用NaOH溶液吸收生成的二氧化硫气体,使在空气中燃烧反应生成的二氧化硫尽可能的被吸收。


硫在氧气中燃烧的结论硫在氧气中燃烧,这可是一个令人惊奇又让人咋舌的实验。
想象一下,拿出一小块硫,看起来不起眼,但它却能引发一场热烈的化学“派对”。
硫在空气中慢慢发热,跟一位小明星似的,开始吸引所有的目光。
然后,嗖的一声,氧气来了,硫立刻就变得活跃起来,像是打了鸡血,瞬间燃烧起来。
这一刻,简直像是在看一场炫目的烟花秀,红色、蓝色的火焰在空气中跳动,宛如梦幻般的舞蹈。
硫燃烧的过程中,它释放出的热量和光芒,简直能让人眼前一亮,仿佛生活中的一切烦恼都被这耀眼的光辉驱散了。
说到硫燃烧的结果,那可是很有意思的哦!燃烧后,硫会跟氧气反应,生成一种叫做二氧化硫的气体。
这个气体可不是一般的气体,它可酸了。
想象一下,就像你吃了一块特别酸的柠檬,立马让你眉头紧皱。
二氧化硫溶于水后,能形成硫酸,哇,这可不是闹着玩的,硫酸可是一种非常强烈的酸,处理不当可是会让人感到“头痛”的。
这个反应就是告诉我们,虽然燃烧的过程那么美丽,但背后的化学变化可一点都不简单。
就像人们常说的,表面光鲜,内里复杂,真是一点不假。
硫在燃烧过程中释放的二氧化硫可不仅仅是个“酸”,它在空气中还会带来一些环境问题,真是让人哭笑不得。
比如,二氧化硫在空气中和水分结合,形成酸雨,这对植物、动物和建筑物都造成了困扰。
植物大哥在雨水里遭殃,建筑小弟也受不了这种腐蚀,真是叫苦不迭。
科学家们可不止一次警告大家,注意环境保护,别让这场化学“派对”变成了环境的悲剧。
我们都希望这个星球能更美好,不是吗?硫的燃烧还有个小秘密,那就是它的颜色。
你知道吗,燃烧时发出的火焰是蓝色的,这可不是开玩笑。
蓝色火焰的出现是因为反应中产生的温度非常高,这火焰不仅让人感到神秘,还让人忍不住想去探索它背后的科学原理。
难怪有人说,科学就像一块神秘的拼图,越拼越有趣。
说到这里,有些朋友可能会问,为什么我们要研究硫燃烧呢?硫在我们的日常生活中并不陌生。
它出现在化肥、药品、甚至某些食品中,可以说是我们的“老朋友”。

2021年(人教)中考化学:第2单元 我们周围的空气附答案 人教第2单元 我们周围的空气一、选择题1、电工师傅使用的“试电笔”中常充入一种稀有气体,它通电时发出红光.则该气体是( )A.氧气B.氮气C.氖气D.二氧化碳2、以下不属于上海市空气质量监测内容的是( )A. 二氧化碳B. 二氧化硫C. 氮氧化物D. 可吸入可粒物3、下列关于氧气的说法中,错误的是( )A .氧气是空气的主要成分之一B .氧气可用于医疗急救C .燃料燃烧一般离不开氧D .氧气可用于食品保鲜4、下列反应属于分解反应的是( )A .水――→通电氢气+氧气B .铜+氧气+二氧化碳+水―→碱式碳酸铜C .甲烷+氧气――→点燃二氧化碳+水D .氢氧化钠+硫酸铜―→氢氧化铜+硫酸钠5、空气中能使食物变质的主要气体是( )A. 氮气B. 氧气C. 二氧化碳D. 稀有气体6、今年春季以来,我国许多城市雾霾天气频发,PM2.5是造成雾霾天气的“元凶”之一.PM2.5是用来监测空气中下列哪项含量的( )A. 可吸入颗粒物B. 二氧化氮C. 二氧化碳D. 一氧化碳7、氧气是我们身边常见的物质,以下有关氧气的叙述正确的是( ) A .氧气具有可燃性.B .空气成分中氧气约占空气质量的21%C .氧气能作燃料.D .某些物质在空气中不能燃烧,但在氧气中能燃烧.8、现有a 、b 两支试管,a 试管内有少量二氧化锰,同时在两支试管内滴加相同的过氧化氢溶液,能正确表示a 、b 两支试管放出氧气质量(纵坐标)与反应时间(横坐标)关系的图像是()9、实验室加热高锰酸钾制氧气,可直接采用的发生装置是()A. B. C. D.10、空气的成分中,体积分数约占21%的是( )A. 氮气B. 氧气C. 二氧化碳D. 稀有气体11、以下关于燃烧现象的描述,正确的是( )A.硫在氧气中燃烧发出淡蓝色火焰B.铁丝在氧气中燃烧火星四射C.蜡烛在氧气中燃烧产生大量白烟D.碳在空气中燃烧生成二氧化碳12、下列关于催化剂的说法正确的是()A.化学反应前后催化剂的质量不变B.化学反应前后催化剂的性质不变C.催化剂只能加快化学反应速率D.没有催化剂化学反应不能发生13、育才中学化学兴趣小组的同学准备用下图装置在实验室制取并收集氧气,下列说法错误的是()A.小伟认为装置A加热前试管内的物质是纯净物B.小明认为若将装置B 中的长颈漏斗换成分液漏斗就可以控制反应的速率C.小芳认为装置D收集到的氧气比装置C收集到的氧气更纯净D.小华用图2中的装置来代替装置C收集氧气时,应将带火星的小木条放在导气管b处进行验满二、非选择题14、根据空气的成分填空。

硫燃烧的创新实验
一、实验目的
硫在空气和氧气中燃烧的实验对比是学习氧气性质的关键性实验,实验的成功与否直接影响到能否得出氧气支持燃烧的主要性质。
但是,此实验难免会有大量的二氧化硫气体排放
到教室里,严重危害学生的健康,为此,我对这一实验进行了改进,完全避免了这一现象的
发生,而且操作简单,现象明显,师生不在身受其害。
二、实验仪器及试剂
集气瓶、胶塞、燃烧匙、导线、钨丝、注射器一支、学生电源、药匙、硫粉、5%过氧化
氢溶液、二氧化锰
三、实验仪器装置图
组装说明;大集气瓶做发生装置,双孔橡皮塞上分别是燃烧匙和两根金属丝,注射器里装入的是5%的双氧水溶液。
四、实验操作
1、硫在空气中燃烧。
连接好装置,在集气瓶中加入少量二氧化锰,向燃烧匙中加入适量硫粉,塞紧瓶塞。
然后,打开电源开关,待到钨丝发红,便会点燃硫粉,此时关闭电源,出现微弱的淡蓝色火焰。
2、硫在氧气中燃烧。
缓慢推动注射器,让双氧水与二氧化锰接触并产生氧气,硫剧烈燃烧,发出蓝紫色火焰。
3、吸收处理污染物
待装置冷却后,取下注射器,在注射器中再注入氢氧化钠溶液,再向瓶中推入氢氧化钠溶液以吸收处理二氧化硫污染产物。
五、创新的意义
首先,这个实验最大的特点就是将硫的点燃、给硫提供氧气和实验结束后对空气污染物的处理三位一体有机的结合,大大激发了学生的大胆创新思维意识和学习兴趣。
其次,在操作简单、比较环保的基础上实现了与普通实验过程中一样明显的实验现象,起到了很好的对比效果。
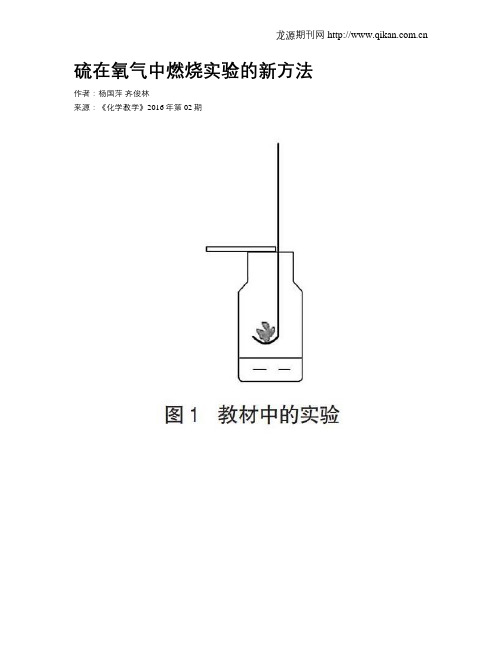
硫在氧气中燃烧实验的新方法作者:杨国萍齐俊林来源:《化学教学》2016年第02期摘要:现行化学教材中“硫在氧气中燃烧”实验,会产生有毒气体二氧化硫,污染室内空气,不符合对现代教学环境的要求。
利用吸滤瓶、电烙铁、燃烧匙、气球等器材设计了一套封闭式实验装置,很好地解决了实验过程中二氧化硫的污染问题。
通过实验改进培养了学生的创新能力和环保意识,提高了教学效果。
关键词:硫;燃烧;二氧化硫;实验改进文章编号:1005 6629(2016)2-0069-04中图分类号:G633.8文献标识码:B1 问题的提出硫在氧气中燃烧实验是现行九年级化学教材中的一个经典实验(如图1所示),它能够说明硫能在氧气中燃烧并产生蓝紫色火焰的实验事实。
教材中的该实验方法尽管现象明显,便于操作,易于观察,能起到增强学生感性认识、培养学生观察能力、提高教学质量之目的,但由于此实验方法是在空气中点燃硫粉,然后放入盛有氧气的集气瓶内燃烧。
因此,实验过程中有毒的二氧化硫气体,不仅在集气瓶外产生,而且在集气瓶内燃烧时还会从玻璃片与瓶口之间的缝隙中大量外逸,污染室内空气,影响师生健康,不利于培养学生的环境意识,更不适应当前社会保护环境、保证教学环境空气质量的要求。
另外,在集气瓶内制备氧气,还需一套较为复杂的氧气制备系统(如图2所示),这不仅增加了工作量,而且浪费教学时间,影响了教学效率。
多年来,尽管一些教师试图对该实验方法进行改进,以解决生成物二氧化硫对教学环境的污染问题,但收效甚微:有的改进方法没有彻底解决二氧化硫的污染问题,即点燃硫粉还是在室内进行,仍会对教学环境造成—定的污染(如图3所示);有的实验方法不仅需要一个复杂的氧气制备系统,而且用电炉丝加热,方法较为笨拙,难于固定盛放硫粉的瓷片,给实验操作带来诸多不便(如图4所示);还有的实验方法虽然对教材中实验方法进行了大胆改进,并有一定的创意,即用注射器直接将氧气吹到石棉网上燃烧的硫粉内,但是该方法会造成更为严重的室内环境污染问题。
硫在空气及氧气中燃烧实验绿色化改进作者:吴正兴来源:《教育信息化论坛》2018年第03期摘要:硫在空气及氧气中燃烧实验是初中化学中常见的并且经常操作的化学实验,但课本中所描述的及传统教学中常用的实验都或多或少存在问题,如对人体、环境的危害。
为此,需要不断改进和创新“硫在空气及氧气中的燃烧实验”。
本文简介了硫在空气及氧气中的燃烧实验,分析其存在的问题和绿色化改进的意义,并结合课堂教学和绿色理念提出改进措施,提升化学对环境、对学生的有益影响。
关键词:初中化学;硫燃烧实验;绿色化学一、硫在空气及氧气中燃烧实验硫在空气及氧气中燃烧实验是沪教版九年级化学教学中的重点,并且根据教学要求一般化学老师都会在教学过程中穿插化学实验,其目的是通过实验来让学生观察硫在空气及氧气中燃烧的现象。
硫在空气中燃烧,会产生淡蓝色的火焰并伴随燃烧产生刺激性气味的气体;在氧气中燃烧则会产生出蓝紫色的火焰,并产生带刺激性气味的气体,这种气体即为二氧化硫,其反应形式为硫通过燃烧与氧气结合,形成二氧化硫,其化学反应方程式为:S+O2 =SO2。
二、硫在空气及氧气中燃烧实验存在问题及绿色化改进的意义课本中介绍的传统操作方法即先把硫放入到燃烧匙中,然后放在酒精灯外焰加热至其燃烧,观察实验现象。
此种实验操作方式燃烧产生的二氧化硫等有毒有害气体,漂浮在室内空气中,影响教室内师生的身体健康。
所以在实验过程中教师一般采用开窗通风的方式将反应产生的有毒有害气体吹散到外界环境中,既增加了实验步骤与工作量,又难免对教师及学生的身体健康产生一定影响。
排放到自然环境中,虽然一个班级一次实验所产生的二氧化硫和有毒有害气体对自然环境的影响远没有达到破坏的程度,但多个班级、多个地区、多次实验的排放量综合到一起,足够对自然环境产生影响。
当过多的二氧化硫溶于水中,形成亚硫酸,当亚硫酸在恶劣的自然环境中进一步氧化后,便会迅速形成酸雨,也会对人类生活及健康带来影响。
另外,实验中为使燃烧现象明显,会适量增加硫的用量,导致化学原料使用量增多,课堂教学成本增加。
硫在氧气中燃烧的改进实验
绿色化学是可持续发展的需要,是现代化学的新发展和重要特点。
化学实验绿色化是社会发展的需要,是学生身心健康发展的需要,是进行环境教育的需要,也是了解现代化学发展和趋势的需要。
中学化学教学过程中,无论是演示实验还是学生实验,常常是有毒的物质参加反应,若处理不当,对环境会造成污染。
针对这一问题,而引导学生积极思维,进行创新,对实险进行绿色化设计。
例如,硫在氧气中燃烧的实验,由于生成的SO2是有毒气体,所以在进行实验的时候就要充分考虑其污染性,所以我对此实验作了以下改进,并且将在这个实验中模拟酸雨的危害。
该实验集几个实验于一体,既验证了氧气的性质和酸雨的成因及危害,又消除了实验中SO2对空气的污染。
具体操作如下:
【一】实验原理
【二】实验用品
盛满氧气的集气瓶,橡皮塞,燃烧匙,酒精灯,浅黄色的硫粉,锌粒,大理石,树叶。
【三】实验步骤
1.把一个小燃烧匙的柄固定在橡皮塞上,在集满氧气的集气瓶里倒入少量的水,放入一粒锌、一小块大理石和一片树叶。
2.用角匙取少量浅黄色的硫粉,放入燃烧匙中。
3.点燃酒精灯,加热燃烧匙中的硫粉,硫粉先融化,后起火燃烧,发出微弱的淡蓝色火焰。
4.把盛有燃着硫的燃烧匙伸入盛有氧气的集气瓶中,塞上橡皮塞,燃烧匙中立刻发出明亮的蓝紫色火焰。
5.待硫熄灭后振荡,一会儿,就可以看见锌和大理石表明有少量气泡冒出,树叶发黄。
【四】问题讨论
根据实验结果出现的现象,举例说明SO2对人类的生产生活具有什么危害?
(SO2能够造成酸雨危害,不仅会腐蚀建筑物,还会腐蚀树木,使森林遭到破坏。
)。
利用魔棒点灯原理改进化学实验摘要:利用魔棒点灯原理,使用医疗中的废弃物和实验室中的常备物品,改进化学实验,不但可以避免环境污染,还能取得良好的教学效果。
关键词:环境污染魔棒点灯原理变废为宝人教版义务教育课程标准实验教科书化学九年级上册第27页【实验2-1】《测定空气里氧气含量》和第34页【实验2-3】《硫在氧气里燃烧》这两个实验都存在一个共同的致命弱点:实验开始时,反应物硫和磷均需在空气中用酒精灯点燃,如此一来,产物五氧化二磷和二氧化硫就会散发在空气中,造成严重的环境污染,危害师生健康。
很多老师改用白磷来引燃,因白磷有剧毒,同样存在不安全因素。
那么,引燃过程能否在密闭的反应容器中进行,从而避免污染呢?由此我想到了魔棒点灯的原理:浓硫酸遇到氯酸钾、过氧化钠、高锰酸钾等强氧化剂时,立即放出大量的热量,使局部温度迅速升高,达到酒精的着火点;与此同时,反应产生的氧气又起到助燃的作用,于是酒精灯就被点燃了。
这种方法能不能引燃红磷和硫磺呢?为此,我进行了如下实验:在通风良好的室外,在两块碎瓷片上各放适量的红磷和硫磺,再在上面各放几粒氯酸钾或过氧化钠或高锰酸钾晶体,然后滴加几滴浓硫酸,发现红磷和硫磺都迅速燃烧起来。
而且所加氯酸钾、过氧化钠、高锰酸钾等晶体的量越多,燃烧的速度越快、越剧烈。
但加高锰酸钾时,燃烧过程中有紫色烟产生,开始时根本就看不见红磷燃烧所产生的白烟和硫磺燃烧产生的淡蓝色火焰。
实践证明,用这一反应原理来引燃红磷和硫磺是可行的。
但由于燃烧比较剧烈,如果在密闭容器中进行引燃,很可能发生爆炸事故,所以,如果要在密闭容器中进行引燃,考虑到实验的安全性,实验装置中应增加缓冲由于燃烧而引起的气体体积膨胀的装置,比如气球等;同时,如果用高锰酸钾和浓硫酸反应来进行引燃,则燃烧过程中产生的紫色烟分散在容器内,观察不到红磷燃烧所产生的白烟和硫磺燃烧产生的淡蓝色火焰,从而影响学生对实验现象的观察。
所以应该用氯酸钾或过氧化钠和浓硫酸反应来进行引燃,并且氯酸钾或过氧化钠的用量一定要少。