核磁共振氢谱 解析图谱的步骤
- 格式:doc
- 大小:18.50 KB
- 文档页数:3






聚合物核磁共振氢谱分析一、目的与要求1. 学习核磁共振的基本原理和实验方法;2. 学习液体核磁共振样品的制备方法;3. 掌握核磁共振谱的解析方法。
二、基本原理1H NMR可提供三方面的信息:化学位移值、耦合常数和裂分峰形以及各峰面积的积分线,根据这三方面的信息可以推测有机物的结构。
化学位移值主要用于推测基团类型以及所处化学环境。
化学位移值与核外电子云密度有关,因此凡是影响电子云密度的因素都将影响基团的化学位移。
这些因素包括与1H相邻元素的种类和基团的电负性、非球形对称电子云所产生的磁各向异性、氢键以及溶剂效应等。
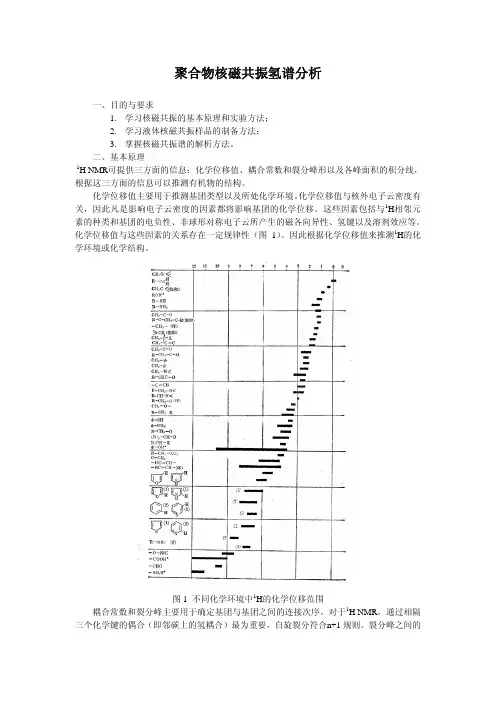
化学位移值与这些因素的关系存在一定规律性(图1)。
因此根据化学位移值来推测1H的化学环境或化学结构。
图1 不同化学环境中1H的化学位移范围耦合常数和裂分峰主要用于确定基团与基团之间的连接次序。
对于1H NMR,通过相隔三个化学键的偶合(即邻碳上的氢耦合)最为重要,自旋裂分符合n+1规则。
裂分峰之间的裂距表示磁核之间相互作用的程度,称作耦合常数,用J表示,单位为Hz。
耦合常数是一个重要结构参数,可以从谱图中测量裂分峰的裂距得到。
但应注意从谱图上测得的裂距是以化学位移值表示的数据,将其乘以标准物质的共振频率(通常以仪器的频率代替)才能得到以Hz为单位的耦合常数。
积分曲线的高度代表相应峰的面积,反映了各种共振信号的相对强度。
因此与相应基团中氢原子数目成正比。
通过对积分线的测量和计算可以推测化合物中各种不同基团所含的氢原子数和总的氢原子数。
核磁共振谱图的解析就是综合利用上述三种信息推测有机物的结构。
核磁共振波谱测定时,通常是用适当的溶剂将试样溶解,参考物TMS作为内标加入其中。
为了避免溶剂中的1H干扰,通常使用氘代溶剂或四氯化碳等不含氢的溶剂。
所谓氘代溶剂是指溶剂分子中的氢原子被重氢,即氘(D)所取代,常用的氘代试剂有氘代氯仿(CDCl3)、氘代丙酮(CD3COCD3)、重水(氘代水,D2O)和氘代二甲基亚砜(CD3SOCD3)等。
谱图的解析NMR谱法一般经历如下的步骤进行谱图的解析:★与IR法相同,首先尽可能了解清楚样品的一些自然情况,以便对样品有一些大概的认识;通过元素分析获得化合物的化学式,计算不饱和度Ω;★根据化学位移值确认可能的基团,一般先辨认孤立的,未偶合裂分的基团,即单峰,即不同基团的1H之间距离大于三个单键的基团及一些活泼氢基团,如甲基醚、甲基酮()、甲基叔胺()、甲基取代的苯等中的甲基质子及苯环上的质子,活泼氢为―O―H,,-SH等;然后再确认偶合的基团。
从有关图或表中的δ可以确认可能存在的基团,这时应注意考虑影响δ的各种因素如电负性原子或基团的诱导效应、共轭效应、磁的各向异性效应及形成氢键的影响等;★根据偶合裂分峰的重数、偶合常数,判断基团的连接关系。
先解析一级光谱,然后复杂光谱。
进行复杂光谱解析时,应先进行简化;★根据积分高度确定出各基团中质子数比,印证偶合裂分多重峰所判断的基团连接关系;★通过以上几个程序,一般可以初步推断出可能的一种或几种结构式。
然后,反过来,从可能的结构式按照一般规律预测可能产生的NMR谱,与实际谱图对照,看其是否符合,从而可以推断出某种最可能的结构式。
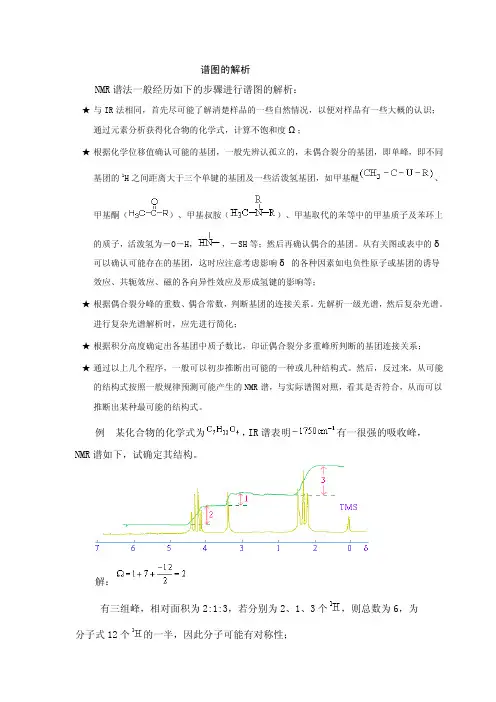
例某化合物的化学式为,IR谱表明有一很强的吸收峰,NMR谱如下,试确定其结构。
解:有三组峰,相对面积为2:1:3,若分别为2、1、3个,则总数为6,为分子式12个的一半,因此分子可能有对称性;IR显示~1750cm-1有一强峰,应有存在,且分子中有4个O,则可能有2个;处有一组三重峰,可能为-CH3,且受裂分,而处有一组四重峰,与是典型的组分;而δ较大,可能为的组分;处有一单峰,相对面积为1,则是一个与碳基相连的孤立(不偶合)的,可能为所以可能有的结合。
而此结合的、O的数目为分子式的一半,而C原子数一半多半个原子。
因此可以推测出整个分子的中间C原子为对称的结构,可能为验证:以炔可能结构,推测其NMR谱,与实验谱图比较,结果相符合。

核磁一般氢谱和碳谱的解析步骤分析氢谱有如下的步骤。
(1) 区分出杂质峰、溶剂峰、旋转边带。
杂质含量较低,其峰面积较样品峰小很多,样品和杂质峰面积之间也无简单的整数比关系。
据此可将杂质峰区别出来。
氘代试剂不可能100%氘代,其微量氢会有相应的峰,如CDCl3中的微量CHCl3在约7.27ppm处出峰。
边带峰的区别请阅6.2.1。
(2) 计算不饱和度。
不饱和度即环加双键数。
当不饱和度大于等于4时,应考虑到该化合物可能存在一个苯环(或吡啶环)。
(3) 确定谱图中各峰组所对应的氢原子数目,对氢原子进行分配。
根据积分曲线,找出各峰组之间氢原子数的简单整数比,再根据分子式中氢的数目,对各峰组的氢原子数进行分配。
(4) 对每个峰的δ、J都进行分析。
根据每个峰组氢原子数目及δ值,可对该基团进行推断,并估计其相邻基团。
对每个峰组的峰形应仔细地分析。
分析时最关键之处为寻找峰组中的等间距。
每一种间距相应于一个耦合关系。
一般情况下,某一峰组内的间距会在另一峰组中反映出来。
通过此途径可找出邻碳氢原子的数目。
当从裂分间距计算J值时,应注意谱图是多少兆周的仪器作出的,有了仪器的工作频率才能从化学位移之差Δδ(ppm)算出Δν(Hz)。
当谱图显示烷基链3J耦合裂分时,其间距(相应6-7Hz)也可以作为计算其它裂分间距所对应的赫兹数的基准。
(5) 根据对各峰组化学位移和耦合常数的分析,推出若干结构单元,最后组合为几种可能的结构式。
每一可能的结构式不能和谱图有大的矛盾。
(6) 对推出的结构进行指认。
每个官能团均应在谱图上找到相应的峰组,峰组的δ值及耦合裂分(峰形和J值大小)都应该和结构式相符。
如存在较大矛盾,则说明所设结构式是不合理的,应予以去除。
通过指认校核所有可能的结构式,进而找出最合理的结构式。
必须强调:指认是推结构的一个必不可少的环节。
如果未知物的结构稍复杂,在推导其结构时就需应用碳谱。
在一般情况下,解析碳谱和解析氢谱应结合进行。

核磁氢谱峰的裂分核磁共振氢谱之氢谱解析步骤:由分子式计算其不饱和数。
Ω=C+1-(^+φ-^)4Λ/ /O其中:H:化合物中质子的数目。
X:化合物中卤素原子数目。
N:化合物中三价氮原子数目。
由各组峰面积积分比,计算各组峰代表的相对氢核数目。
若氢谱积分不正确(积分面积比不是整数或者峰的个数不对),则可能:噪声的积分可能被计算了。
饱和效应:由于各类质子的弛豫时间不一致,饱和程度不同,会引起误差,积分面积很难严格的与质子数目成正比。
附近含H少的H弛豫时间长,所以积分小,若将其面积定为1,则附近含H少的H 由于弛豫时间短而积分大导致积分大于整数,所以要选择适当的H的面积定为1同位素卫星峰:例如氢谱里出现"C同位素卫星峰。
有互变异构(醛与烯醇之间的互变异构)、旋转(船式和椅式)等,使得H峰个数变多,物质易出现互变异构的话,可以换溶剂、做低温。
溶剂峰出现使峰个数增多。
若分子对称,则面积比成比例减少。
左右一般有水峰,若没有,则可能物质中有活泼H,与水发生了化学交换。
3.由化学位移识别各组峰所代表氢核的性质(即连在什么上的氢):活泼氢可通过其特征化学位移或增宽的信号进行识别(证实活泼氢:对活泼氢可用重水(气代试剂)交换予以证实(会发生H,D交换使检测物质OH峰消失)或变温(消除化学交换))。
根据化学位移、自旋分裂和偶合常数,详细分析分子中各结构单元的关系(即连起来得到合理结构式,带回去看能否解释所有峰):一张谱图经常有一级类型部分和高级谱图部分,可以由易到难,逐步解析。
对高级图谱,应根据谱图特点识别自旋系统,测量和计算化学位移和偶合常数,画出图解。
根据裂分成几重峰,决定两边连的什么类型的C e形成一个环也是一个饱和度。
氢键作用和化学交换作用要一起考虑,共同对谱图产生影响(存在竞争):OH峰尖,则OH对CH:有裂分。
OH峰宽(H键),则OH对CH2无裂分。
取代苯环:(1)单取代苯环(在苯环区内有5个H时):(II)-CHCH「、-CH--Ch-CH=CHR等使邻间、对位氢的值(相对未取代苯)位移均不大的基团。

核磁共振氢谱分析流程下载温馨提示:该文档是我店铺精心编制而成,希望大家下载以后,能够帮助大家解决实际的问题。
文档下载后可定制随意修改,请根据实际需要进行相应的调整和使用,谢谢!并且,本店铺为大家提供各种各样类型的实用资料,如教育随笔、日记赏析、句子摘抄、古诗大全、经典美文、话题作文、工作总结、词语解析、文案摘录、其他资料等等,如想了解不同资料格式和写法,敬请关注!Download tips: This document is carefully compiled by theeditor. I hope that after you download them,they can help yousolve practical problems. The document can be customized andmodified after downloading,please adjust and use it according toactual needs, thank you!In addition, our shop provides you with various types ofpractical materials,such as educational essays, diaryappreciation,sentence excerpts,ancient poems,classic articles,topic composition,work summary,word parsing,copy excerpts,other materials and so on,want to know different data formats andwriting methods,please pay attention!1. 样品制备:选择合适的溶剂:根据样品的溶解性选择合适的氘代溶剂,如 CDCl3、DMSO-d6 等。
核磁共振氢谱的操作方法核磁共振氢谱(Proton Nuclear Magnetic Resonance,简称1H NMR)是一种常用的分析技术,用于确定化合物的结构和分析样品的组成。
下面是1H NMR的操作方法,包括样品制备、仪器设置和数据分析等步骤。
1. 样品制备:a. 准备适量的待测化合物,通常为液体样品。
确保样品纯度高,无杂质干扰。
b. 使用干燥剂(例如无水氯化钙或无水硫酸铜)除去样品中的水分。
c. 将样品溶解在适当的溶剂中,常用的溶剂包括氯仿、二氯甲烷、二甲基甲酰胺等。
溶剂选择要避免与待测化合物相互作用或干扰信号。
2. 仪器设置:a. 打开核磁共振仪,确保仪器处于正常工作状态。
b. 调节仪器的温度控制,一般选择室温或其他适当的温度。
c. 选择适当的核磁共振频率,通常为300 MHz至800 MHz,具体取决于仪器性能和需求。
3. 样品装填:a. 使用适当的样品管(通常为NMR试管)装填样品。
确保样品管干净,无杂质。
b. 使用移液器将样品转移至样品管中,通常需要10-15毫升样品。
c. 安装样品管到核磁共振仪的样品槽中,确保样品正确安装并固定。
4. 参数设置:a. 打开核磁共振软件,设置相关参数。
包括扫描数目、扫描时间、脉冲宽度等。
b. 设置核磁共振仪的基线校正,确保仪器的信号稳定和准确。
5. 数据采集:a. 点击软件中的"开始"按钮,启动数据采集过程。
b. 仪器会发送一系列脉冲和信号来激发样品中的氢原子。
c. 接收到的信号将被转换为频谱图,并在计算机屏幕上显示。
6. 数据分析:a. 在频谱图上观察峰的位置和强度。
每个峰对应于样品中的不同氢原子环境。
b. 使用参考物质(例如三氯甲烷或二氯乙烷)作为内部标准,可以确定峰的化学位移(chemical shift)。
c. 使用积分曲线测量峰的面积,可以确定不同类型氢原子的相对数量。
d. 通过与已知化合物进行比较,可以确定待测化合物的结构和组成。
核磁共振氢谱详解核磁共振谱仪被公认为是一种非常重要的研究和测试工具,它的许多功能是其它手段无法代替的。
1945年Bloch和Purcell分别领导两个小组同时独立地观察到核磁共振(NMR),二人因此荣获1952年诺贝尔物理奖。
历经半个多世纪,NMR已从最初发现到最终发展成为成熟的医用的MRI影像学检测手段,期间6次被授予诺贝尔奖(物理、化学、生理/医学),堪称史上获奖次数最多的技术。
自1953年出现第一台核磁共振商品仪器以来,核磁共振在仪器、实验方法、理论和应用等方面有着飞跃的进步。
谱仪频率已从30MHz发展到1100MHz。
谱图已从一维谱到二维谱、三维谱甚至更高维谱。
所应用的学科已从化学、物理扩展到生物、医学等多个学科。
总而言之,核磁共振已成为最重要的仪器分析手段之一。
核磁共振技术发展较早,20世纪70年代以前,主要是核磁共振氢谱的研究和应用。
70年代以后,随着傅里叶变换波谱仪的诞生,13C—NMR的研究迅速开展。
由于1H—NMR的灵敏度高,而且积累的研究资料丰富,因此在结构解析方面1H—NMR的重要性仍强于13C—NMR。
解析图谱的步骤1.先观察图谱是否符合要求;①四甲基硅烷的信号是否正常;②杂音大不大;③基线是否平;④积分曲线中没有吸收信号的地方是否平整。
如果有问题,解析时要引起注意,最好重新测试图谱。
2.区分杂质峰、溶剂峰、旋转边峰(spinningsidebands)、13C 卫星峰(13Csatellitepeaks)(1)杂质峰:杂质含量相对样品比例很小,因此杂质峰的峰面积很小,且杂质峰与样品峰之间没有简单整数比的关系,容易区别。
(2)溶剂峰:氘代试剂不可能达到100%的同位素纯度(大部分试剂的氘代率为99-99.8%),因此谱图中往往呈现相应的溶剂峰,如CDCL3中的溶剂峰的δ值约为7.27ppm处。
(3)旋转边峰:在测试样品时,样品管在1H-NMR仪中快速旋转,当仪器调节未达到良好工作状态时,会出现旋转边带,即以强谱线为中心,呈现出一对对称的弱峰,称为旋转边峰。
核磁共振氢谱解析
核磁共振氢谱(NMR)是一种分析有机分子结构的技术。
在该技术中,核磁共振仪会对样品中的氢原子进行激发,使其产生共振信号,然后测量该信号的频率和强度。
利用核磁共振氢谱技术可以确定分子中不同类型氢原子的相对数量和结构。
每种氢原子所产生的信号的位置、强度和形状均有所不同,可以通过与已知的标准进行比较,从而确定分子结构中每个氢原子的位置和数目。
在解析核磁共振氢谱时,可以通过以下步骤进行:
1. 确定信号的化学位移:信号的化学位移是指共振信号在谱图中所处位置的数值。
该数值可以通过将信号的频率与参考化合物的信号频率进行比较得出。
2. 确定信号的数量:每种不同类型的氢原子所产生的信号数量是确定的,可以通过比较谱图中各个信号的峰的面积或积分来确定每种氢原子的相对数量。
3. 确定信号的形状:不同类型氢原子产生的信号的形状可以有所不同,可能是单峰、双峰或多峰。
该信号形状可以提供分子结构的信息。
4. 确定化合物的结构:通过确定化学位移、数量和形状,可以确定化合物中氢原子的位置和数目,从而确定化合物的结构。
总之,核磁共振氢谱解析是一种能够确定有机分子结构的技术,对有机化学和药物化学等领域具有重要的应用价值。
核磁共振氢谱解析图谱的步骤
核磁共振氢谱
核磁共振技术发展较早,20世纪70年代以前,主要是核磁共振氢谱的研究和应用。
70年代以后,随着傅里叶变换波谱仪的诞生,13C—NMR的研究迅速开展。
由于1H—NMR的灵敏度高,而且积累的研究资料丰富,因此在结构解析方面1H—NMR的重要性仍强于13C—NMR。
解析图谱的步骤
1.先观察图谱是否符合要求;①四甲基硅烷的信号是否正常;②杂音大不大;③基线是否平;④积分曲线中没有吸收信号的地方是否平整。
如果有问题,解析时要引起注意,最好重新测试图谱。
2.区分杂质峰、溶剂峰、旋转边峰(spinning side bands)、13C卫星峰(13C satellite peaks)
(1)杂质峰:杂质含量相对样品比例很小,因此杂质峰的峰面积很小,且杂质峰与样品峰之间没有简单整数比的关系,容易区别。
(2)溶剂峰:氘代试剂不可能达到100%的同位素纯度(大部分试剂的氘代率为99-99.8%),因此谱图中往往呈现相应的溶剂峰,如CDCL3中的溶剂峰的δ值约为7.27 ppm处。
(3)旋转边峰:在测试样品时,样品管在1H-NMR仪中快速旋转,当仪器调节未达到良好工作状态时,会出现旋转边带,即以强谱线为中心,呈现出一对对称的弱峰,称为旋转边峰。
(4)13C卫星峰:13C具有磁距,可以与1H偶合产生裂分,称之为13C卫星峰,但由13C的天然丰度只为1.1%,只有氢的强峰才能观察到,一般不会对氢的谱图造成干扰。
3.根据积分曲线,观察各信号的相对高度,计算样品化合物分子式中的氢原子数目。
可利用可靠的甲基信号或孤立的次甲基信号为标准计算各信号峰的质子数目。
4.先解析图中CH3O、CH3N、、CH3C=O、CH3C=C、CH3-C等孤立的甲基质子信号,然后再解析偶合的甲基质子信号。
5.解析羧基、醛基、分子内氢键等低磁场的质子信号。
6.解析芳香核上的质子信号。
7.比较滴加重水前后测定的图谱,观察有无信号峰消失的现象,了解分子结
构中所连活泼氢官能团。
8.根据图谱提供信号峰数目、化学位移和偶合常数,解析一级类型图谱。
9.解析高级类型图谱峰信号,如黄酮类化合物B环仅4,-位取代时,呈现AA,BB,系统峰信号,二氢黄酮则呈现ABX系统峰信号。
10. 如果一维1H-NMR难以解析分子结构,可考虑测试二维核磁共振谱配合解析结构。
11. 组合可能的结构式,根据图谱的解析,组合几种可能的结构式。
12. 对推出的结构进行指认,即每个官能团上的氢在图谱中都应有相应的归属信号。
四. 核磁共振碳谱(13C—NMR)
解析图谱的步骤
1.鉴别谱图中的非真实信号峰
(1)溶剂峰:虽然碳谱不受溶剂中氢的干扰,但为兼顾氢谱的测定及磁场需要,仍常采用氘代试剂作为溶剂,氘代试剂中的碳原子均有相应的峰。
(2)杂质峰:杂质含量相对于样品少得多,其峰面积极小,与样品化合物中的碳呈现的峰不成比例。
(3)测试条件的影响:测试条件会对所测谱图有较大影响。
如脉冲倾斜角较大而脉冲间隔不够长时,往往导致季碳不出峰;扫描宽度不够大时,扫描宽度以外的谱线会折叠到图谱中来;等等,均造成解析图谱的困难。
2.不饱和度的计算
根据分子式计算的不饱和度,推测图谱烯碳的情况。
3.分子对称性的分析
若谱线数目等于分子式中碳原子数目,说明分子结构无对称性;若谱线数目小于分子式中碳原子数目,说明分子结构有一定的对称性。
此外,化合物中碳原子数目较多时,有些核的化学环境相似,可能δ值产生重叠现象,应予以注意。
4.碳原子δ值的分区
碳原子大致可分为三个区
(1)高δ值区δ>165ppm,属于羰基和叠烯区:①分子结构中,如存在叠峰,除叠烯中有高δ值信号峰外,叠烯两端碳在双键区域还应有信号峰,两种峰同时存在才说明叠烯存在;②δ>200 ppm的信号,只能属于醛、酮类化合物;③160-180ppm的信号峰,则归属于酸、酯、酸酐等类化合物的羰基。
(2)中δ值区δ90-160ppm(一般情况δ为100-150ppm)烯、芳环、除叠烯中央碳原子外的其他SP2杂化碳原子、碳氮三键碳原子都在这个区域出峰。
(3)低δ值区δ<100ppm,主要脂肪链碳原子区:①不与氧、氮、氟等杂原子相连的饱和的δ值小于55ppm;②炔碳原子δ值在70-100ppm,这是不饱和碳原子的特例。
5.碳原子级数的确定
由低核磁共振或APT(attached proton test)、DEPT(distortionless enhancement by polarization transfer)等技术可确定碳原子的级数,由此可计算化合物中与碳原子相连的氢原子数。
若此数目小于分子式中的氢原子数,二者之差值为化合物中活泼氢的原子数。
6.推导可能的结构式
先推导出结构单元,并进一步组合成若干可能的结构式。
7.对碳谱的指认
将核磁共振碳谱中各信号峰在推出的可能结构式上进行指认,找出各碳谱信号相应的归属,从而在被推导的可能结构式中找出最合理的结构式,即正确的结构式。