高中化学第一轮复习化学计量及其应用
- 格式:ppt
- 大小:1.70 MB
- 文档页数:76

高考化学一轮复习化学常用计量教学案 "教学目标知识技能:掌握物质的量及其单位——摩尔、摩尔质量、气体摩尔体积的涵义。
掌握物质的量与微粒(原子、分子、离子等)数目、气体体积(标准状态下)之间的相互关系。
能力培养:通过基本计算问题的讨论,培养学生的计算思维能力。
科学思想:在阿伏加德罗定律的应用上,着重掌握有关比例的数学思想。
科学方法:演绎推理法。
重点、难点物质的量与微粒(原子、分子、离子等)数目、气体体积(标准状况下)之间的相互关系是重点,气体摩尔体积的应用条件是难点。
教学过程设计教师活动【引入】今天我们复习化学常用计量。
【提问】科学家引入物质的量这个物理量的意义是什么?【再问】谁来说说物质的量是怎样联系宏观和微观的?学生活动回答:把质量、体积等宏观物理量和微观的微粒个数联系起来。
回答:主要通过以物质的量为核心物理量建立的下列关系图,把微粒数、物质质量、气体标准状况下的体积、溶液的物质的量浓度等相互关联起来。
归纳:小结:物质的量及其单位摩尔的作用实际是联系宏观和微观的桥梁。
【提问】下列叙述是否正确?(1)摩尔是物质的量的单位,1mol任何物质都含有6.02×1023个分子。
(2)1mol氢的质量为1g,它含有阿伏加德罗常数个氢分子。
(3)氧气的摩尔质量为 32g,氧气的分子量也为32g。
(4)12g碳-12所含的碳原子数是阿伏加德罗常数,每摩物质含有阿伏加德罗常数个微粒。
思考,回答:(1)不正确,并非所有物质均含有分子。
(2)不正确,不能说 1mol氢,应指明微粒名称。
(3)不正确,摩尔质量的单位为g·mol-1,分子量没有单位。
(4)正确【提问】在应用摩尔这个单位时,应注意什么?回答:(1)摩尔只能用来表示微粒的集体数目;(2)必须指明微粒的具体名称。
【讲解】微粒可以是真实的,如:1mol水分子;也可以是假想的,如:1mol NaCl,表示1molNa+和1mol Cl- 的特定组合。

专题一化学计量及其应用考点1:物质的量、阿伏加德罗常数考点2物质的量浓度一、物质的量和阿伏加德罗常数:1、重要概念辨析:(1)物质的量及其单位:物质的量是国际单位制中的七个基本物理量之一,符号为“n”,单位是“mol”(2)阿伏加德罗常数与6.02×1023阿伏加德罗常数:符号为N A。
定义为:0.012Kg12C所含碳原子的准确数目,是一个精确值。
在现有条件下,测得其数值约为6.02×1023注意:6.02×1023只是其近似值。
(3) 摩尔质量与相对分子质量的关系:摩尔质量是单位物质的量的物质所具有的质量,摩尔质量在数值上等于相对分子质量,单位是g/mol。
(4)气体摩尔体积与22.4L/mol.气体摩尔体积是单位物质的量的气体所占的体积,单位是L/mol,符号为Vm。
由于气体体积与温度、压强有关,故Vm也随温度压强的变化而变化,在标况下(0℃,101千帕):Vm=22.4L/mol2、阿伏加德罗定律及其推论:(1)、阿伏加德罗定律:同温同压下,相同体积的任何气体都具有相同的分子数(物质的量)。
(2)阿伏加德罗定律的推论:用理想气体的状态方程推:PV=nRT(R为常数)①压强之比:P1/P2=n1/n2=N1/ N2;(同温同体积时,任何气体的压强之比等于其物质的量之比,也等于其分子数之比)②体积之比:V1/V2=n1/n2=N1/N2(同温同压时,任何气体的体积之比等于其物质的量之比,也等于其分子数之比)③质量之比:m1/m2=M1/M2(同温同压同体积的任何气体的质量之比等于其摩尔质量之比)④密度之比:ρ1/ρ2 =M1/M2(同温同压同体积的任何气体的密度之比等于其摩尔质量之比,其比值叫相对密度(用D表示))。
二、物质的量浓度:1、定义:以单位体积的溶液里含有溶质B的物质的量来表示溶液组成的物理量叫溶质B的物质的量浓度。
表达式:C B=n B/V(单位:mol/L)注意:(1)V规定为溶液的体积,不是水的体积。

第一章从实验学化学一、化学计量①物质的量定义:表示一定数目微粒的集合体符号n 单位摩尔符号 molN公式:n=NA②摩尔质量:单位物质的量的物质所具有的质量用M表示单位:g/mol 数值上等于该物质的分子量质量与物质的量m公式:n=M③物质的体积决定:①微粒的数目②微粒的大小③微粒间的距离微粒的数目一定固体液体主要决定②微粒的大小气体主要决定③微粒间的距离体积与物质的量V公式:n=Vm标准状况下,1mol任何气体的体积都约为22.4L④阿伏加德罗定律:同温同压下,相同体积的任何气体都含有相同的分子数⑤物质的量浓度:单位体积溶液中所含溶质B的物质的量。
符号 C 单位:mol/l 公式:C B=n B/V n B=C B×V V=n B/C B溶液稀释规律 C(浓)×V(浓)=C(稀)×V(稀)⑥溶液的配置(l)配制溶质质量分数一定的溶液计算:算出所需溶质和水的质量。
把水的质量换算成体积。
如溶质是液体时,要算出液体的体积。
称量:用天平称取固体溶质的质量;用量简量取所需液体、水的体积。
溶解:将固体或液体溶质倒入烧杯里,加入所需的水,用玻璃棒搅拌使溶质完全溶解.(2)配制一定物质的量浓度的溶液(配制前要检查容量瓶是否漏水)计算:算出固体溶质的质量或液体溶质的体积。
称量:用托盘天平称取固体溶质质量,用量简量取所需液体溶质的体积。
溶解:将固体或液体溶质倒入烧杯中,加入适量的蒸馏水(约为所配溶液体积的1/6),用玻璃棒搅拌使之溶解,冷却到室温后,将溶液引流注入容量瓶里。
洗涤(转移):用适量蒸馏水将烧杯及玻璃棒洗涤2-3次,将洗涤液注入容量瓶。
振荡,使溶液混合均匀。
定容:继续往容量瓶中小心地加水,直到液面接近刻度2-3mm处,改用胶头滴管加水,使溶液凹面恰好与刻度相切。
把容量瓶盖紧,再振荡摇匀。
5、过滤过滤是除去溶液里混有不溶于溶剂的杂质的方法。
过滤时应注意:①一贴:将滤纸折叠好放入漏斗,加少量蒸馏水润湿,使滤纸紧贴漏斗内壁。

第一章 化学计量及其应用 一、物质的量〔n 〕1.物质的量是表示含有一定数目粒子的集合体的物理量,单位是摩尔〔mol 〕。
2.摩尔:规定1mol 粒子集合体所含的粒子数=kg 12C 中含有的碳原子数约为6.02×1023 。
3.阿伏伽德罗常数:1mol 粒子集合体所含的粒子数。
数值约为6.02×1023,常用N A 表示,单位mol −1。
公式:n NN A 。
4.“物质的量〞的表示方法: x mol H 2SO 4〔数值〕 〔单位〕 〔指定化学式或微粒符号〕二、摩尔质量〔M 〕第一课 物质的量 气体摩尔体积 知识结构考点1:物质的量 摩尔质量知识全梳理概念符号单位g·mol −1为单位时,任何粒子的摩尔质量在数值上Mg·mol−1单位物质的量的物质所具有的质量诊断辨析例1.以下说法不正确的选项是〔〕A.铜的摩尔质量在数值上等于它的相对原子质量B.kg碳所含的碳原子数,其数值约等于6.02×1023C.1molH2SO4约含有1.204×1024个氢原子D.常温常压下,1molCO2气体的质量为44g【答案】B【解析】kg所含的碳原子数为阿伏伽德罗常数,该项说法没有指明哪种碳原子,错误;C项,根据H2SO4分子式,1molH2SO4含有2mol氢原子,约为1.024×1024个,正确;D项,CO2摩尔质量为44g/mol,故1molCO2气体的质量为44g,正确。
例2.以下表达中错误的选项是〔〕A.1mol任何物质都含有6.02×1023个分子B.12C中约含有6.02×1023个碳原子C.1mol H2O中含有2mol H和1mol OD.1mol C中约含有3.612×1024个电子【答案】A【解析】A.不是任何物质都是由分子构成的,构成物质的微粒还有原子和离子,A项错误;B.0.012kg 12C的物质的量为1mol,约含有6.02×1023个碳原子,B项正确;C.一个水分子中含两个氢原子和一个氧原子,因此1mol H2O中含有2mol H和1mol O,C项正确;D.1个C原子有6个电子,1mol C就有6mol电子,所以1mol C中约含有3.612×1024个电子,D项正确;应选A。
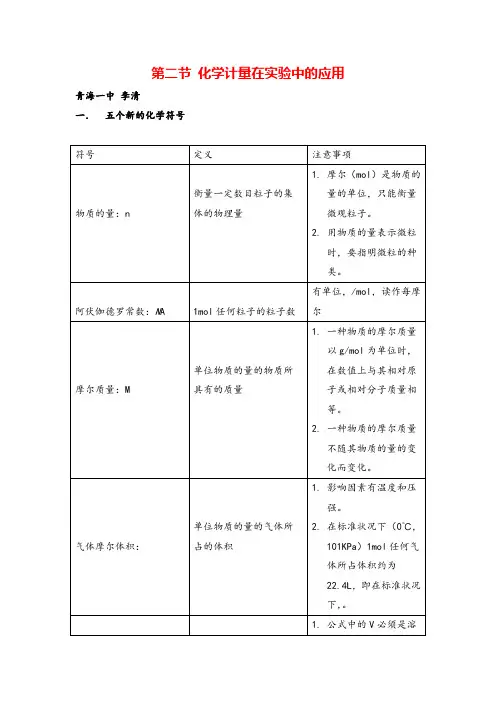
第二节化学计量在实验中的应用青海一中李清一.五个新的化学符号二.各个量之间的关系:公式: n=三.溶液稀释规律:C(浓)×V(浓)=C(稀)×V(稀)【练习1】(2017春•汪清县校级期末)下列对于“摩尔”的理解正确的是()A.摩尔是国际单位制的七个物理量之一B.摩尔是物质的量的单位,简称摩,符号为molC.摩尔是表示物质质量的单位D.1mol氧含6.02×个【考点】物质的量的单位--摩尔.化学计量【专题】化学用语专题.【分析】A.摩尔是单位,不是物理量;B.物质的量单位为摩尔,简称摩,符号为mol;C.物质的量单位为摩尔;D.1mol氧指代不明确.【解答】解:A.物质的量是国际单位制的七个物理量之一,其单位为摩尔,故A错误;B.物质的量单位为摩尔,简称摩,符号为mol,故B正确;C.摩尔是表示物质的量的单位,质量单位为克,故C错误;D.1mol氧指代不明确,故D错误;故选:B。
【练习2】(2012秋•历下区校级月考)下列说法中不正确的是()A.物质的量是一个物理量,物质的量的单位是摩尔B.2 mol水的摩尔质量是1 mol水的摩尔质量的2倍C.利用物质的量可以把物质的宏观数量与微观粒子的数量联系起来D.每摩质含有阿伏加德常数个基本微粒【考点】物质的量与其浓度和气体摩尔体积的综合应用.【专题】化学用语专题.【分析】A.物质的量是国际基本物理量,其单位是摩尔;B.摩尔质量不随物质的物质的量多少变化;C.从物质的量的作用分析;D.根据N=nNA判断.【解答】解:A.物质的量是国际7个基本物理量之一,其单位是mol,故A正确;B.水的摩尔质量是18g/mol,物质的摩尔质量不随物质的物质的量多少变化,故B错误;C.物质的量的作用就是把物质的宏观数量与微观粒子的数量联系起来,起到一个桥梁用,故C正确D.根据N=nNA知,每摩尔含有阿伏加德罗常数个基本微粒,故D正确;故选:B。

化学计量及其的应用1.(2020年河北示范性高中高三联考)已知AG=lg c (H +)c (O H -)。
室温下用0.01 mol ·L -1的NH 3·H 2O 滴定20.00 mL 0.01 mol ·L -1某一元酸HQ 的结果如图所示,下列说法中正确的是( )。
A.HQ 属于弱酸B.整个过程中,C 点时水的电离程度最大C.E 点对应溶液中c (OH -)+c (NH 3·H 2O)=c (N H 4+)+c (H +) D.K b (NH 3·H 2O)的数量级为10-51.D 解析 由A 点可知0.01 mol ·L -1 HQ 溶液中c (H +)=0.01 mol ·L -1,所以HQ 属于强酸,故A 项错误;整个过程中,当酸碱恰好完全反应生成盐时,水的电离程度最大,由于生成的盐是强酸弱碱盐,此时溶液显酸性,而C 点溶液呈中性,故B 项错误;E 点溶液为等浓度NH 4Q 和NH 3·H 2O的混合液,根据电荷守恒有c (OH -)+c (Q -)=c (N H 4+)+c (H +),根据物料守恒有2c (Q -)=c (N H 4+)+c (NH 3·H 2O),所以E 点对应液中2c (OH -)+c (NH 3·H 2O)=c (N H 4+)+2c (H +),故C 项错误;E 点溶液为等浓度NH 4Q 和NH 3·H 2O 的混合液,由于电离和水解都很微弱,c (NH 3·H 2O)≈c (N H 4+),NH 3·H 2O N H 4++OH -,K b (NH 3·H 2O)= c (N H 4+)·c (O H -)c (N H 3·H 2O)≈c (OH -),由图像可知,E 点时AG=lg c (H +)c (O H -)=-4.5,再根据水的离子积K w =c (H +)·c (OH -)=1×10-14,解得c (OH -)=10-4.75,所以K b (NH 3·H 2O)的数量级为10-5,故D 项正确。

第1课时 化学入门——化学常用计量知识点一 物质的量、摩尔质量1.物质的量、阿伏加德罗常数 (1)基本概念间的关系[提醒] “物质的量”的计量对象是微观粒子(如:分子、原子、离子、原子团、质子、中子、电子等),而不是宏观物质。
(2)“物质的量”的表示方法如:1 mol Fe 、1 mol O 2、1 mol Na +。
[提醒] 物质的量(n )、粒子数(N )、阿伏加德罗常数(N A )之间的关系:n =NN A。
2.摩尔质量(1)概念:单位物质的量的物质所具有的质量。
符号:M ,单位:g·mol -1。
(2)数值:当粒子的摩尔质量以g·mol -1为单位时,在数值上等于该粒子的相对分子(或原子)质量。
(3)关系:物质的量(n )、质量(m )与摩尔质量(M )之间的关系为n =m M 。
(4)计算方法①根据标准状况下气体的密度(ρ):M =ρ×22.4 L·mol -1。
如:标准状况下某气体的密度为1.429 g·L -1,则该气体的M =32_g·mol -1。
②根据气体的相对密度⎝⎛⎭⎫D =ρ1ρ2:M1M 2=D 。
如:某气体对甲烷的相对密度为4,则该气体的M =64_g·mol -1。
③根据物质的质量(m )和物质的量(n ):M =mn 。
如:0.5 mol 某气体的质量是22 g ,则该气体的M =44_g·mol -1。
④根据一定质量(m )的物质中粒子数目(N )和阿伏加德罗常数(N A ):M =N A · mN 。
如:45 g乳酸中含乳酸的分子数为3.01×1023,则乳酸的摩尔质量为90_g·mol -1。
[对点训练]1.判断正误(正确的打“√”,错误的打“×”)。
(1)0.012 kg 12C 中含有的碳原子数约为6.02×1023个(√) (2)7.8 g Na 2O 2中含有的阴离子数为0.2N A (×) (3)1 mol NaCl 和1 mol HCl 含有相同的粒子数目(×) (4)1 mol OH -的质量是17 g·mol -1(×)(5)22 g CO 2中含有的氧原子数为N A (√)(6)常温常压下,14 g 乙烯和丙烯的混合物中含有的氢原子数目为2N A (√) 2.在0.5 mol Na 2SO 4中含有的离子的个数和氧原子的质量分别是( ) A .1.5N A 2 mol B .1.5N A 32 g C .3.01×1023 4 molD .N A 64 g解析:选B 0.5 mol Na 2SO 4中含有的离子数为0.5×3N A =1.5N A ,含氧原子的物质的量为0.5 mol ×4=2 mol ,质量为2 mol ×16 g·mol -1=32 g 。



2022年高三一轮复习化学教案第1章化学计量在实验中的应用第一课时物质的量与阿伏伽德罗常的应用复习目标:1、把握物质的量、摩尔质量、阿伏伽德罗常等概念。
2、把握以物质的量为中心,相互之间的转化关系。
3、能够把握考查N A题型的解答方法及技巧。
基础知识:一、物质的量(1)物质的量是七个差不多物理量之一,其意义是表示含有一定量数目的粒子的集体。
符号为:n ,单位为:摩尔(mol)。
〖说明〗物质的量是用来描述微观粒子,如分子、原子、离子、电子、质子、中子等。
在描述的时候应该标明微观粒子的特定组合。
如1molH,或1mol氢原子。
(2)物质的量的基准(N A):以0.012kg12C所含的碳原子数即阿伏加德罗常数作为物质的量的基准。
阿伏加德罗常数能够表示为N A,其近似值为6.02×1023 mol-1二、摩尔质量(M)摩尔质量是单位物质的量的物质所具有的质量,单位是g/mol 。
假如g/mol作为单位,其数字上等于相对原子(分子)质量或式量。
三、物质的量为中心的转化关系【解题指导】阿佛加德罗常数考点命题陷阱归类分析阿佛加德罗常数(用N A表示)涉及的知识面广,灵活性强,是高考的热点之一,要紧以选择题的形式(选择正确的或错误的)进行考查。
分析近几年的高考试题,此类题型常以选择题形式显现,容易引起学生错误的有以下几点:1、温度和压强:22.4L/mol是在标准状况(0 ℃,1.01×105Pa)下的气体摩尔体积。
命题者有意在题目中设置非标准状况下的气体体积,让考生与22.4L/mol进行转换,从而误入陷阱。
2、物质状态:22.4L/mol使用的对象是气体(包括混合气体)。
命题者常把一些容易忽视的液态或固态物质作为气体来命题,让考生落入陷阱。
如SO3:常温下是固态;水:常温下是液态。
戊烷,辛烷常温下是液态等。
3、物质变化:一些物质间的变化具有一定的隐藏性,有时需要借助方程式分析才能挖掘出隐含的变化情形。

常用化学计量一、物质的量及其单位——摩尔1.定义物质的量是一个物理量,它表示含有一定数目粒子的集合体,符号为n,单位为摩尔。
1 mol粒子集体所含的粒子数与0.012 kg 12C中所含的碳原子数相同,约为6.02×1023。
以摩尔为单位表示物质的量时,必须要指明粒子的种类(原子、分子、离子或它们的特定组合,一般写化学式)。
在试题中如果涉及粒子数或粒子数目比时,应考虑求该粒子的物质的量,计算物质的量的公式有:n=N/N A、n=m/M、n=V/V m、n=cV。
2.阿伏加德罗常数1 mol任何粒子的粒子数叫阿伏加德罗常数,符号为N A,单位mol-1。
阿伏加德罗常数就是0.012 kg 12C中所含的碳原子数,通常用近似值6.02×1023 mol-1表示,N A=N/n。
二、摩尔质量摩尔质量是单位物质的量的物质所具有的质量,符号为M,M=m/n。
常用的单位为g/mol (或g·mol-1)。
某物质的摩尔质量在数值上等于该物质的相对原子质量或相对分子质量。
在试题中涉及求某物质相对分子质量时,应该考虑求该物质的摩尔质量。
应用摩尔质量时必须指明对象,M B=m B /n B.,对于同一物质规定的基本单元不同,摩尔质量就不同。
如O2中O的摩尔质量为16 g/mol,而O2的摩尔质量为32 g/mol。
三、气体摩尔体积1.定义单位物质的量的气体所占的体积叫做气体摩尔体积,符号V m,常用单位L/mol。
定义公式V m=V/n。
在标准状况下(0℃、101kPa,简称标况)1 mol任何气体所占的体积都约为22.4 L,即在标准状况下,气体的摩尔体积约为22.4 L/mol。
2.对于V m =22.4 L/mol概念的理解(1)决定1 mol物质体积大小的因素:物质体积的大小取决于构成这种物质的粒子数目、粒子的大小和粒子之间的距离。
1 mol不同的固态物质或液态物质所含有的粒子数相同,而粒子之间的距离很小,这就使得固态物质或液态物质的体积主要决定于粒子的大小。
章末质检卷(一)化学计量在实验中的应用一、选择题:本题包括12小题,每小题4分,共48分。
每小题只有一个选项符合题意。
1.实验室配制250 mL 0.1 mol·L-1的Na2CO3溶液,无需用到的仪器是()2.混合气体由N2和CH4组成,测得混合气体在标准状况下的密度为0.821 g·L-1,则混合气体中N2和CH4的体积比为()A.1∶1B.1∶4C.4∶1D.1∶23.体积相同的甲、乙两容器中,一个充满C2H4,另一个充满C2H2和C2H6。
在同温同压下,两个容器内的气体一定具有相同的()A.原子总数B.碳原子总数C.质量D.密度4.实验室有一瓶溶液,标签上标有“BaCl2 0.2 mol·L-1”的字样,下面是某同学对该溶液的叙述,其中正确的是()A.配制500 mL该溶液,可将0.1 mol BaCl2溶于500 mL水中B.Ba2+和Cl-的物质的量浓度均为0.2 mol·L-1C.将该瓶溶液稀释一倍,则所得溶液中c(Cl-)为0.2 mol·L-1D.从试剂瓶中取出该溶液的一半,则所取溶液的物质的量浓度为0.1 mol·L-15.如图为配制450 mL 1.00 mol·L-1 NaOH溶液的示意图,下列说法正确的是()A.图①中应称得NaOH 18.0 gB.未进行④和⑤的操作,所配溶液浓度将偏大C.定容后把容量瓶倒置摇匀,发现液面低于刻度线不必再加水至刻度线D.步骤②后应将溶液立即转移到容量瓶中,防止药品变质6.(2021广西南宁三中三模)用次氯酸钠处理氨氮废水的主要化学方程式为3NaClO+2NH3·H2O3NaCl+N2↑+5H2O。
设N A为阿伏加德罗常数的值。
下列说法正确的是()A.1 L 1 mol·L-1的NaClO溶液中,ClO-的数目小于N AB.若反应转移电子6N A,则生成22.4 L N2C.1 mol 氮气中含有共价键数为2N AD.1 mol 重水中含有中子数为12N A7.某溶液中,忽略水的电离,只含有下表中所示的四种离子,推测X离子及其物质的量b可能为()A.OH-、8aB.I-、8aC.S O42-、4aD.S O42-、8a8.(2021新疆乌鲁木齐一模)设N A为阿伏加德罗常数的值,下列有关叙述正确的是()A.12 g石墨烯和12 g金刚石均含有N A个碳原子B.300 mL 2 mol·L-1蔗糖溶液中所含分子数为0.6N AC.在高温、高压和催化剂的条件下,密闭容器中2 g H2与足量N2反应,转移电子数为2N AD.1 mol OD-和17 g—OH所含的质子与中子均为9N A9.(2021辽宁丹东一模)常温下,100 mL 1.0 mol·L-1 Na2C2O4溶液中加入足量pH=1的稀硫酸,再加入20 mL KMnO4溶液恰好完全反应。
高考化学一轮复习目录第一章化学计量在实验中的应用第1 讲物质的量、气体摩尔体积第2 讲物质的量浓度第二章化学物质及其变化第1 讲物质的组成、性质及分类第2 讲离子反响离子方程式第3 讲氧化复原反响的根本概念第4 讲氧化复原反响的规律和应用第三章金属及其化合物第1 讲碱金属元素——钠第2 讲铁及其化合物第3 讲镁及其化合物第4 讲铝及其化合物第四章常见的非金属及其化合物第1 讲无机非金属材料的主角——硅第2 讲富集在海水中的元素——氯第3 讲硫及其化合物第4 讲氮的氧化物和硝酸第5 讲氨和铵盐第五章物质结构与元素周期律第1 讲元素周期表第2 讲元素周期律第3 讲化学键第六章化学反响中的能量变化电化学第1 讲化学反响中的能量变化实验探究:中和热的测定第2 讲原电池化学电源第3 讲电解池金属的电化学腐蚀与防护第七章化学反响速率和化学平衡第1 讲化学反响速率第2 讲化学反响的方向和限度第3 讲化学平衡移动第八章水溶液中的离子平衡第1 讲弱电解质的电离平衡第2 讲水的电离和溶液的酸碱性第3 讲盐类的水解第4 讲难溶电解质的溶解平衡第九章认识有机化合物第1 讲有机物的结构特点和分类第2 讲研究有机化合物的方法第十章烃第1 讲脂肪烃第2 讲芳香烃第十一章烃的衍生物第1 讲卤代烃第2 讲醇酚第3 讲醛羧酸酯第十二章根本营养物质、高分子化合物第1 讲根本营养物质第2 讲进入合成有机高分子化合物的时代第十三章化学实验根底第1 讲化学实验根底知识实验探究:“仪器改造〞与“一器多用〞第2 讲物质的检验、别离和提纯第3 讲实验方案的设计与评价第4 讲探究性化学实验。
【一. 教学内容:化学计量在试验中的应用二、教学目标驾驭摩尔、摩尔质量、气体摩尔体积、物质的量浓度和阿伏加德罗常数的含义;依据物质的量与微粒(原子、分子、离子、电子等)数目、气体体积(标准状况)之间的关系进行计算;了解配制肯定物质的量浓度、肯定质量分数的溶液的方法。
三、教学重点、难点有关摩尔、摩尔质量、气体摩尔体积、物质的量浓度、阿伏加德罗常数的基本计算;有关物质的量浓度、质量分数和溶解度之间的困难计算;配制肯定物质的量浓度溶液的方法及误差分析。
四、教学过程:(一)相关概念:物质的量是描述肯定数目的微粒集体的物理量。
符号用n表示,它的单位是摩尔,符号为mol;摩尔是物质的量的单位,每摩尔物质含有阿伏加德罗常数个微粒;化学上把0.012kg12C所含碳原子数称为阿伏加德罗常数,符号为N A,数值为6.02×1023,单位为mol-1摩尔质量是指单位物质的量的物质所具有的质量。
用符号M表示,单位为g/mol。
在标准状况下,1mol的任何气体所占的体积都约是22.4L,这个体积叫做气体摩尔体积,符号:V m,单位:L·mol-1。
以1L溶液里含有多少摩溶质来表示溶液组成的物理量,叫做物质的量浓度。
符号:C 单位:mol·L-1。
说明:1、物质的量是国际单位制中七个基本物理量之一,科学上采纳“物质的量”这个物理量把肯定数目的原子、分子或离子等微观粒子与可称量的物质联系起来。
它是一个口头上或书面表达上都不行分割的专用名词,不行随意添减字,既是物质的质量,也是物质的数量。
2、运用摩尔做单位时,应当用化学式符号指明粒子种类,而不能用名称。
否则,概念模糊,意义不清。
3、应用阿伏加德罗常数N A时,必需留意以下几点:①状态问题:如:水在标准状态下为液态,SO3在标准状态下为固态,在常温常压下为液态,碳原子数大于4的烃,在标准状况下为固态或液态;②特殊物质的摩尔质量:如:D2O、T2O、18O2等;③分子中的原子数、电子数、中子数的计算;④一些物质中化学键的数目;⑤一些较困难的反应中转移的电子数目。