初中化学重点复习系列7-化学转换三角及推断
- 格式:doc
- 大小:101.50 KB
- 文档页数:4

化学三角转化关系一、酸碱中的中和反应酸碱中的中和反应是一种常见的化学转化关系。
当酸和碱混合时,产生盐和水的反应称为中和反应。
例如,将盐酸和氢氧化钠混合,会生成氯化钠和水。
这个反应过程中,酸和碱分别失去了H+离子和OH-离子,生成了水分子。
这种反应在我们日常生活中很常见,比如当我们喝柠檬汁时,柠檬汁中的酸会与口腔中的碱性物质中和,产生水和盐。
二、氧化还原反应氧化还原反应是化学反应中的重要类型之一。
在氧化还原反应中,物质中的原子氧化态和还原态发生变化,同时伴随着电子的转移。
例如,金属与非金属氧化物反应生成盐的过程中,金属原子失去电子变成阳离子,非金属氧化物原子得到电子变成阴离子。
这种反应在燃烧、腐蚀等过程中都有应用。
例如,当铁与氧气反应时,铁原子氧化成铁离子,氧气还原成氧离子,生成了氧化铁。
三、酯化反应酯化反应是一种酸催化的化学反应,常用于合成酯。
酯是一类含有酯基的有机化合物,其分子中含有羰基和氧原子。
酯化反应一般是酸催化的醇和酸反应生成酯和水。
例如,乙醇和乙酸反应生成乙酸乙酯和水。
酯化反应在食品、香料、涂料等领域有广泛的应用。
比如,水果中的香味主要来自于酯类物质。
四、聚合反应聚合反应是一种将小分子单体通过共价键连接起来形成高分子化合物的反应。
在聚合反应中,单体分子中的双键或三键被打开,形成新的共价键,从而形成高分子链。
例如,乙烯分子经过聚合反应可以形成聚乙烯链。
聚合反应在合成塑料、纤维等材料中起着重要作用。
五、水解反应水解反应是一种化合物与水反应生成两个或多个新的化合物的反应。
在水解反应中,水分子中的氢离子和水解物中的某个原子或基团发生置换,生成新的化合物。
例如,脂肪酸与水反应生成酸和醇。
水解反应在生物体内的消化过程中起着重要作用。
通过以上几种常见的化学转化关系,我们可以看到化学在物质变化中起着重要的作用。
通过不同的反应类型,我们可以合成新的化合物,改变物质的性质和用途。
化学转化关系的研究对于我们理解物质的本质和改进化学工艺具有重要的意义。


初三化学三角转换关系
初三化学中的三角转换关系通常指的是物质之间的转化关系。
这种关系通常可以用图形来表示,其中每个物质都是一个顶点,而箭头表示转化方向。
例如,钙三角表示的是钙元素的不同化合物之间的转化关系。
包括碳酸钙(CaCO₃)、氧化钙(CaO)和水(H₂O)之间相互转化的关系。
氧化钙可以与水反应生成氢氧化钙,而氢氧化钙又可以与二氧化碳反应重新生成碳酸钙。
另一个例子是碳三角,它表示的是碳、一氧化碳和二氧化碳之间的相互转化关系。
碳可以在氧气中燃烧生成二氧化碳,一氧化碳可以与氧气发生反应生成二氧化碳,二氧化碳也可以通过植物的光合作用重新转化为碳。
在化学中,还有很多其他的三角转换关系,这些关系可以帮助我们理解物质的性质和变化规律,从而更好地掌握化学知识。

①②③H 2O2H 2O 2O 2O u C Cu4O S u C ①②⑤④③C COCO 2①②④③CaOCa(OH)2CaCO 3①②③①②⑤④③FeFe 2O 3FeCl 3FeFe 3O 4FeCl 2①②⑤④③初中化学 化学转换三角及推断一、三角转换1、氧三角 ①2H 2O 2MnO22H 2O+O 2↑ ②2H 2O通电2H 2↑+O 2↑ ③2H 2+O 2点燃2H 2O2、碳三角 ①2C+O 2点燃2CO②C+O 2点燃CO 2③2CO+O 2点燃2CO 2④C+CO 2高温2CO3、钙(石灰)三角及转化:石灰石、生石灰、熟石灰 ①CaCO 3高温CaO+CO 2↑②CaO+H 2O==Ca(OH)2 ③Ca(OH)2+CO 2==CaCO 3↓+H 2O 4、铜三角 ①2Cu+O 2 △2CuO②H 2+CuO△Cu+H 2O③CuO+H 2SO 4==CuSO 4+H 2O ④Fe+CuSO 4==FeSO 4+Cu ⑤Cu+Ag 2SO 4==CuSO 4+2Ag 5、铁三角1 ①2H 2O+4Fe+3O 2 缓慢氧化2Fe 2O 3·H 2O②Fe 2O 3+3CO高温2Fe+3CO 2③Fe 2O 3+6HCl==2FeCl 3+3H 2O ④Al+FeCl 3==AlCl 3+Fe ⑤2Fe+3Cl 2点燃2FeCl 36、铁三角2(Fe 3O 4可以写成Fe 2O 3 •FeO ) ①3Fe+2O 2点燃Fe 3O 4 ② Fe 3O 4+4CO高温3Fe+4CO 2③Zn+FeCl 2==ZnCl 2+Fe ④Fe+2HCl==FeCl 2+H 2↑⑤Fe 3O 4+8HCl==2FeCl 3+FeCl 2+4H 2OH 2SO 4HClHNO 3/CO 2①②④③Ca(OH)2NaOH Cu(OH)2/NH 3①②④③Na 2CO 3Na 2SO 4NaCl/NaNO 3CaCO 3CaCl 2Ca(NO 3)2①②③7、酸三角①H 2SO 4+BaCl 2==BaSO 4↓+2HCl ②HCl+AgNO 3==AgCl ↓+HNO 3③H 2SO 4+Ba(NO 3)2==BaSO 4↓+2HNO 3 ④Na 2CO 3+H 2SO 4==Na 2SO 4+H 2O+CO 2↑ 8、碱三角①Ca(OH)2+Na 2CO 3==CaCO 3↓+2NaOH ②2NaOH+CuSO 4==Cu(OH)2↓+Na 2SO 4 ③Ca(OH)2+CuSO 4==Cu(OH)2↓+CaSO 4 ④Ca(OH)2+(NH 4)2SO 4==CaSO 4+2H 2O+2NH 3↑ 9、盐三角1①Na 2CO 3+H 2SO 4==Na 2SO 4+H 2O+CO 2↑ ②Na 2SO 4+BaCl 2==BaSO 4↓+2NaCl ③Na 2CO 3+2HCl==2NaCl+H 2O+CO 2↑ ④Na 2CO 3+2HNO==2NaNO 3+H 2O+CO 2↑ 10、盐三角2①CaCO 3+2HCl==CaCl 2+H 2O+CO 2↑ ②CaCl 2+2AgNO 3==2AgCl ↓+Ca(NO 3)2 ③CaCO 3+2HNO 3==Ca(NO 3)2+H 2O+CO 2↑ 外一:我们身边 的物质总转变② ① ⑧ ⑨ ⑥ ⒀⒁③ ④ ⑦ ⒂⑤ ⑩ ⑾⑿①2KMnO 4 △K 2MnO 4+MnO 2+O 2↑ ②2H 2O 2MnO22H 2O+O 2↑ ③2H 2O通电2H 2↑+O 2↑④2H 2+O 2点燃2H 2O⑤3Fe+2O 点燃Fe 3O 4 ⑥C+O 点燃CO 2⑦6CO 2+6H 2O 叶绿素光照C 6H 12O 6+6O 2 ⑧H 2CO 3△H 2O+CO 2↑⑨CO 2+H 2O==H 2CO 3⑩Ca(OH)2+CO 2=CaCO 3↓+H 2OO 2Fe 3O 4 H 2CO 3 COCO 2 CaCO 3H 2OH 2O 2KMnO4⑿CaCO3+2HCl=CaCl2+H2O+CO2↑⒀3CO+Fe2O3高温2Fe+3CO2 ⒁2CO+O点燃2CO2⒂C+CO2高温2CO⑾CaCO3高温CaO+CO2↑二、推断题解题思路1、阅读题目:要求通阅全题,统领大局。
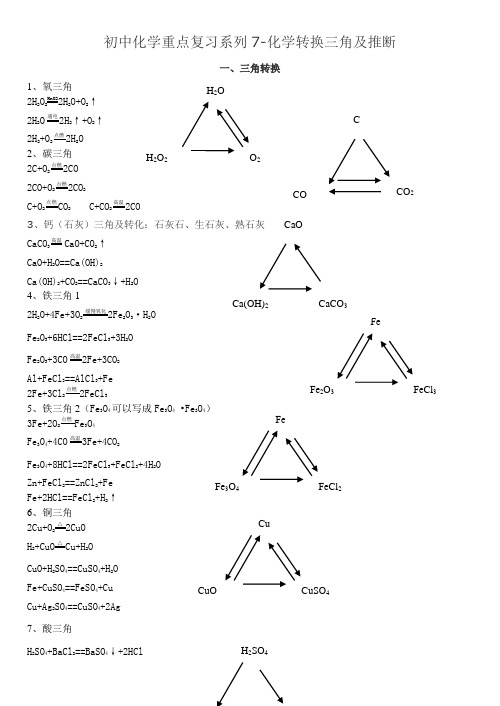
初中化学重点复习系列7-化学转换三角及推断一、三角转换1、氧三角2H 2O 2MnO22H 2O+O 2↑ 2H 2O通电2H 2↑+O 2↑2H 2+O 点燃2H 2O 2、碳三角2C+O 2点燃2CO 2CO+O 2点燃2CO 2C+O 2点燃CO 2 C+CO 2高温2CO3、钙(石灰)三角及转化:石灰石、生石灰、熟石灰 CaCO 3高温CaO+CO 2↑CaO+H 2O==Ca(OH)2 Ca(OH)2+CO 2==CaCO 3↓+H 2O 4、铁三角1 2H 2O+4Fe+3O 2缓慢氧化2Fe 2O 3·H 2OFe 2O 3+6HCl==2FeCl 3+3H 2O Fe 2O 3+3CO高温2Fe+3CO 2Al+FeCl 3==AlCl 3+Fe2Fe+3Cl 2点燃2FeCl 35、铁三角2(Fe 3O 4可以写成Fe 3O 4 •Fe 3O 4)3Fe+2O 2点燃Fe 3O 4 Fe 3O 4+4CO高温3Fe+4CO 2Fe 3O 4+8HCl==2FeCl 3+FeCl 2+4H 2O Zn+FeCl 2==ZnCl 2+Fe Fe+2HCl==FeCl 2+H 2↑ 6、铜三角2Cu+O 2 △2CuO H 2+CuO△Cu+H 2OCuO+H 2SO 4==CuSO 4+H 2O Fe+CuSO 4==FeSO 4+Cu Cu+Ag 2SO 4==CuSO 4+2Ag 7、酸三角H 2SO 4+BaCl 2==BaSO 4↓+2HClCCOCO 2H 2OH 2O 2O 2FeFe 2O 3FeCl 3CuCuOCuSO 4H 2SO 4CaOCa(OH)2 CaCO 3FeFe 3O 4FeCl 2HCl+AgNO 3==AgCl ↓+HNO 3 H 2SO 4+Ba(NO 3)2==BaSO 4↓+2HNO 3 Na 2CO 3+H 2SO 4==Na 2SO 4+H 2O+CO 2↑ 8、碱三角Ca(OH)2+Na 2CO 3==CaCO 3↓+2NaOH 2NaOH+CuSO 4==Cu(OH)2↓+Na 2SO 4 Ca(OH)2+CuSO 4==Cu(OH)2↓+CaSO 4 Ca(OH)2+(NH 4)2SO 4==CaSO 4+2H 2O+2NH 3↑ 9、盐三角1Na 2CO 3+H 2SO 4==Na 2SO 4+H 2O+CO 2↑ Na 2SO 4+BaCl 2==BaSO 4↓+2NaCl Na 2CO 3+2HCl==2NaCl+H 2O+CO 2↑ Na 2CO 3+2HNO==2NaNO 3+H 2O+CO 2↑ 10、盐三角2CaCO 3+2HCl==CaCl 2+H 2O+CO 2↑ CaCl 2+2AgNO 3==2AgCl ↓+Ca(NO 3)2CaCO 3+2HNO 3==Ca(NO 3)2+H 2O+CO 2↑ 外一:我们身边的物质总转变 ② ① ⑧ ⑨ ⑥ ⒀⒁③④ ⑦ ⒂⑤ ⑩ ⑾⑿①2KMnO 4 △ K 2MnO 4+MnO 2+O 2↑ ②2H 2O 2MnO22H 2O+O 2↑ ③2H 2O通电2H 2↑+O 2↑ ④2H 2+O 2点燃2H 2O⑤3Fe+2O 2点燃Fe 3O 4⑥C+O 2点燃CO 2⑦6CO 2+6H 2O 叶绿素光照C 6H 12O 6+6O 2⑧H 2CO 3△H 2O+CO 2↑ ⑨CO 2+H 2O==H 2CO 3⑩Ca(OH)2+CO 2=CaCO 3↓+H 2O⑾CaCO 3高温CaO+CO 2↑⑿CaCO 3+2HCl=CaCl 2+H 2O+CO 2↑⒀3CO+Fe 2O 3高温2Fe+3CO 2 ⒁2CO+O 2点燃2CO 2⒂C+CO 2高温2CO二、推断题解题思路1、 阅读题目:要求通阅全题,统领大局。
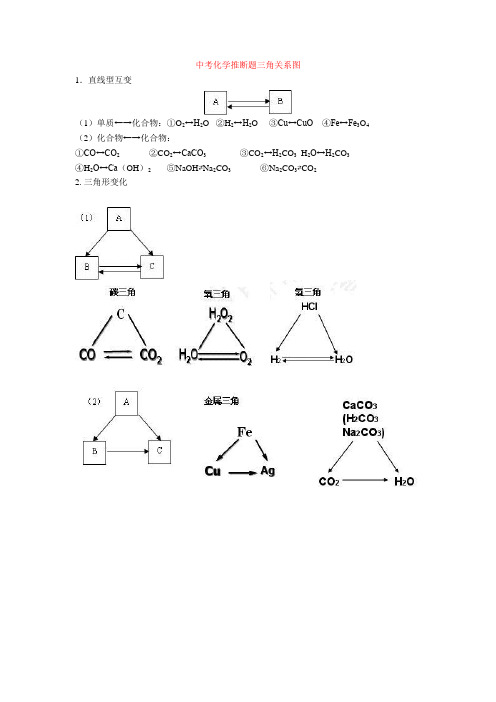
中考化学推断题三角关系图1.直线型互变(1)单质←→化合物:①O2↔H2O ②H2↔H2O ③Cu↔CuO④Fe↔Fe3O4(2)化合物←→化合物:①CO↔CO2 ②CO2↔CaCO3 ③CO2↔H2CO3 H2O↔H2CO3④H2O↔Ca(OH)2 ⑤NaOH⇄Na2CO3 ⑥Na2CO3⇄CO22. 三角形变化(4)其它:3. 四边形关系:二、中考化学推断题2.A-F 分别代表初中化学中常见的七种物质,且它们都含有—种相同元素,该元素为地壳中含量第一位的元素。
同时,A 由一种元素组成,B、C、D 都由二种元素组成, E、F、G 都由三种元素组成。
(图中的“—”表示相连两物质之间可以发生反应,“→”表示一种物质可以一步转化为另一种物质,反应条件、部分反应物和生成物已略去)。
(1)A 的化学式:________。
(2)写出 B 与 E 反应的化学方程式:________。
【答案】O 2 2442=CuO+H SO CuSO +H O【解析】【分析】地壳中含量第一位的元素为氧元素,A 由一种元素组成,则A 为O 2;B 、C 、D 都由二种元素组成,且A 可以转化成B 、C 、D ,B 可以转化成C 、D ,D 可以转化成C ,则B 为CuO ;D 为CO 2;C 为H 2O ;E 、F 、G 都由三种元素组成,且B 与E 可以发生反应,D 可以转化为G ,C 可以转化为F ,E 、G 可以反应,G 、F 可以反应,F 、E 可以反应,则E 为H 2SO 4;F 为Ca(OH)2;G 为Na 2CO 3;代入转化关系图,验证正确。
【详解】(1)根据推断过程,A 为氧气,故填:O 2(2)B 与E 反应是氧化铜和硫酸的反应,生成硫酸铜和水,故填:2442=CuO+H SO CuSO +H O3.小慧同学在学习中构建了“硫及其化合物的价、类关系图”。
(1)X 和Y 分别表示:________、_________。
中考化学专项总复习:物质转化与推断1、图中的A、B、C、D、E、F、G都是初中化学中的常见物质。
其中A是盐,常用做建筑材料,B是人体胃液中所含有的一种酸,C是植物光合作用的一种原料,E是盐,广泛用于玻璃、造纸、纺织和洗涤剂的生产等,F、G是碱。
它们之间存在以下转化关系(图中部分生成物已略去)。
(1)写出物质A、B的化学式:A B;(2)写出反应的化学方程式:(3)写出物质G在实验室必需密封保存的原因:。
【答案】解:(1)A、B、C、D、E、F、G都是初中化学中的常见物质,A是一种盐,常用作建筑材料,所以A是碳酸钙,B是人体胃液中所含的一种酸,所以B是盐酸,C是植物光合作用的一种原料,碳酸钙和盐酸反应生成无色溶液D和C,C和碱F反应会生成碳酸钙,所以C 是二氧化碳,E是盐,广泛用于玻璃、造纸、纺织和洗涤剂的生产等,所以E是碳酸钠,二氧化碳和G反应会生成碳酸钠,所以G是氢氧化钠,二氧化碳和碱F会生成碳酸钙,所以F是氢氧化钙,经过验证,推出的各种物质均满足题中的转化关系,推导正确,所以A 是CaCO3,B是HCl;(2)碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,化学方程式为:Na2CO3+Ca (OH)2=CaCO3↓+2NaOH;(3)物质G在实验室必需密封保存的原因是:吸水潮解,与CO2反应。
故答案为:(1)CaCO3,HCl;(2)Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;(3)吸水潮解,与CO2反应。
2、如图是一些常见物质间互相转化的关系图(部分反应条件已省略)。
A、B均为无色气体,X为固体,Y为能使澄清石灰水变浑浊的无色气体,E、F为常见金属,试推断:(1)乙、戊物质的化学式分别为。
(2)写出下列转化的化学方程式(丙+X→F+Y):。
【答案】解:(1)A、B均为无色气体,X为固体,Y为能使澄清石灰水变浑浊的无色气体,所以Y 是二氧化碳E、F为常见金属,无色液体甲通电会生成无色气体A、B,所以甲是水,A、B 是氢气或氧气中的一种,戊是浅绿色溶液,所以戊中含有亚铁离子,金属E和稀硫酸反应会生成戊和气体单质A,所以E是铁,A是氢气,B就是氧气,戊是硫酸亚铁,溶液丁是蓝色,所以丁中含有铜离子,丁和铁会生成硫酸亚铁,所以丁是硫酸铜,黑色固体丙和硫酸反应会生成硫酸铜,所以丙是氧化铜,金属F和氧气反应会生成氧化铜,所以F是铜,氧气和金属E反应会生成黑色固体乙,黑色固体乙又会转化成铁,所以E是铁,乙是四氧化三铁,四氧化三铁和气体X反应会生成铁和二氧化碳,所以X是一氧化碳,经过验证,推导正确,所以乙、戊物质的化学式分别为Fe3O4、FeSO4;(2)丙+X→F+Y的转化是氧化铜和一氧化碳在加热的条件下生成铜和二氧化碳,化学方程式为:CO+CuO Cu+CO2。
物质的转化与推断一概念:物质的推断是根据物质的特征性质,利用已知的(实验现象)或(相互转化关系)进行判断推理,确定物质的(名称或成分)。
二、解题思路:原理——明显条件、隐含条件----物质特征、现象特征、反应特征-------结论------验证三、物质推断的一般方法:1、一点击破,顺逆推断:抓住“突破口”,直接得出结论,然后顺向、逆向或者两边向中间推断,逐一得出其他结论。
2、相遇组合,对比推断:利用图表列出各物质,再由各物质的性质及反应规律列出物质间反应间的现象,然后对号入座推断出各物质。
3、提出假设,讨论推断:在分析题目所个条件的基础上,提出假设后进行反复验证,逐步缩小范围,排除不符合题意的结论。
推断题注意事项:审题时要注意题目中的关键字、词所表达的意思。
一般情况下,与试题叙述的现象完全吻合的是“一定存在”;与现象不吻合或者有某种物质的存在使现象不正确的物质是“一定不存在”;有某种物质的存在不影响其他反应的现象或自始至终没有参加任何反应的物质是“可能存在”。
推理分析要紧扣实验现象,思考时要层次分明。
判断的结论要准确,既要明确的肯定能,又要明确的否定。
四、储备:1、基础知识(六大突破口: 特殊颜色、特殊状态或者特殊气味、特征反应条件、特征反应现象、元素或物质之最、物质的特殊用途或存在状态)2.重点难点常见的六大突破口反应特征(H+、OH_,CL-,SO42-,CO32-,Cu2-,Fe3+)常见的离子对及反应特征:H+OH、H+CO3、NH4++OH、Ag+CL-,Ba+SO4,Ba+CO3,Ca+CO3 ,Cu+OH/,Fe+OH,Mg+OH化学反应的基本类型特征:常见的能分解反应的物质、常见的置换反应类型(C/H2+金属氧化物、活泼金属+酸、金属+盐)、常见的有两种相同元素组成的物质:H2O2与H2O,CO2与CO,FeCl3与FeCl2物质的俗名和主要成分的化学式常见物质间的相互转化关系:O2,CO2,H2O,Fe,C u,酸碱,盐五、题型精讲1、框图推断题现有一包固体粉末,可能由碳酸钠,硫酸钠,碳酸钙和氯化钠中的一种或几种组成,某同学想确定其组成成分,按如图所示步骤进行了如下实验(各步骤中加入的试剂均为足量):请回答:(1)固体粉末中肯定存在的物质是________,用化学方程式表示白色沉淀部分溶解的原因是________;(2)如何判断固体粉末中是否有“可能存在的物质”,简述实验操作步骤,现象和结论________.2、表格类推断题。
初中化学物质三角转换编辑整理:尊敬的读者朋友们:这里是精品文档编辑中心,本文档内容是由我和我的同事精心编辑整理后发布的,发布之前我们对文中内容进行仔细校对,但是难免会有疏漏的地方,但是任然希望(初中化学物质三角转换)的内容能够给您的工作和学习带来便利。
同时也真诚的希望收到您的建议和反馈,这将是我们进步的源泉,前进的动力。
本文可编辑可修改,如果觉得对您有帮助请收藏以便随时查阅,最后祝您生活愉快业绩进步,以下为初中化学物质三角转换的全部内容。
初中化学物质转化关系归纳———三角转换石灰三角及转化:石灰石、生石灰、熟石灰CaCO3高温CaO+CO2↑CaO+H2O==Ca(OH)2Ca(OH)2+CO2==CaCO3↓+H2O氧三角2H2O2MnO22H2O+O2↑2H2O通电2H2↑+O2↑2H2+O2点燃2H2O碳三角2C+O2点燃2CO2CO+O2点燃2CO2C+O2点燃CO2C+CO2高温2CO铁三角2H2O+2Fe+3O2缓慢氧化2Fe2O3·H2OFe2O3+6HCl==2FeCl3+3H2OAl+FeCl3==AlCl3+Fe2Fe+2Cl3点燃2FeCl3铜三角2Cu+O2加热2CuOH2+CuO△Cu+H2OCuO+H2SO4==CuSO4+H2OCu+HgSO4==CuSO4+Hg酸三角H2SO4+BaCl2==BaSO4↓+2HClHCl+AgNO3==AgCl↓+HNO3H2SO4+Ba(NO3)2==BaSO4↓+2HNO3Na2CO3+H2SO4==Na2SO4+H2O+CO2↑碱三角Ca(OH)2+Na2CO3==CaCO3↓+2NaOH 2NaOH+CuSO4==Cu(OH)2↓+Na2SO4 Ca(OH)2+CuSO4==Cu(OH)2↓+CaSO4 Ca(OH)2+(NH4)SO4==CaSO4+2H2O+2NH3↑2盐三角1Na2CO3+H2SO4==Na2SO4+H2O+CO2↑Na2SO4+BaCl2==BaSO4↓+2NaClNa2CO3+2HCl===2NaCl+H2O+CO2↑盐三角2CaCO3+2HCl==CaCl2+H2O+CO2↑CaCl2+2AgNO3==2AgCl↓+Ca(NO3)2 CaCO3+2HNO3==Ca(NO3)2+H2O+CO2↑。
初中化学重点复习系列7-化学转换三角及推断一、三角转换1、氧三角2H 2O 2MnO22H 2O+O 2↑ 2H 2O通电2H 2↑+O 2↑2H 2+O 点燃2H 2O 2、碳三角2C+O 2点燃2CO 2CO+O 2点燃2CO 2C+O 2点燃CO 2 C+CO 2高温2CO3、钙(石灰)三角及转化:石灰石、生石灰、熟石灰 CaCO 3高温CaO+CO 2↑CaO+H 2O==Ca(OH)2 Ca(OH)2+CO 2==CaCO 3↓+H 2O 4、铁三角1 2H 2O+4Fe+3O 2缓慢氧化2Fe 2O 3·H 2OFe 2O 3+6HCl==2FeCl 3+3H 2O Fe 2O 3+3CO高温2Fe+3CO 2Al+FeCl 3==AlCl 3+Fe2Fe+3Cl 2点燃2FeCl 35、铁三角2(Fe 3O 4可以写成Fe 3O 4 •Fe 3O 4)3Fe+2O 2点燃Fe 3O 4 Fe 3O 4+4CO高温3Fe+4CO 2Fe 3O 4+8HCl==2FeCl 3+FeCl 2+4H 2O Zn+FeCl 2==ZnCl 2+Fe Fe+2HCl==FeCl 2+H 2↑ 6、铜三角2Cu+O 2 △2CuO H 2+CuO△Cu+H 2OCuO+H 2SO 4==CuSO 4+H 2O Fe+CuSO 4==FeSO 4+Cu Cu+Ag 2SO 4==CuSO 4+2Ag 7、酸三角CCOCO 2H 2OH 2O 2O 2FeFe 2O 3FeCl 3CuCuOCuSO 4CaOCa(OH)2 CaCO 3FeFe 3O 4FeCl 2H 2SO 4+BaCl 2==BaSO 4↓+2HCl HCl+AgNO 3==AgCl ↓+HNO 3 H 2SO 4+Ba(NO 3)2==BaSO 4↓+2HNO 3 Na 2CO 3+H 2SO 4==Na 2SO 4+H 2O+CO 2↑ 8、碱三角Ca(OH)2+Na 2CO 3==CaCO 3↓+2NaOH 2NaOH+CuSO 4==Cu(OH)2↓+Na 2SO 4 Ca(OH)2+CuSO 4==Cu(OH)2↓+CaSO 4 Ca(OH)2+(NH 4)2SO 4==CaSO 4+2H 2O+2NH 3↑ 9、盐三角1Na 2CO 3+H 2SO 4==Na 2SO 4+H 2O+CO 2↑ Na 2SO 4+BaCl 2==BaSO 4↓+2NaCl Na 2CO 3+2HCl==2NaCl+H 2O+CO 2↑ Na 2CO 3+2HNO==2NaNO 3+H 2O+CO 2↑ 10、盐三角2CaCO 3+2HCl==CaCl 2+H 2O+CO 2↑ CaCl 2+2AgNO 3==2AgCl ↓+Ca(NO 3)2CaCO 3+2HNO 3==Ca(NO 3)2+H 2O+CO 2↑ 外一:我们身边的物质总转变 ② ① ⑧ ⑨ ⑥ ⒀⒁③④ ⑦ ⒂⑤ ⑩ ⑾⑿①2KMnO 4 △ K 2MnO 4+MnO 2+O 2↑ ②2H 2O 2MnO22H 2O+O 2↑ ③2H 2O通电2H 2↑+O 2↑ ④2H 2+O 点燃2H 2O⑤3Fe+2O 2点燃Fe 3O 4⑥C+O 2点燃CO 2⑦6CO 2+6H 2O 叶绿素光照C 6H 12O 6+6O 2⑧H 2CO 3△H 2O+CO 2↑ ⑨CO 2+H 2O==H 2CO 3⑩Ca(OH)2+CO 2=CaCO 3↓+H 2O⑾CaCO 高温CaO+CO 2↑⑿CaCO 3+2HCl=CaCl 2+H 2O+CO 2↑⒀3CO+Fe 2O 高温2Fe+3CO 2 ⒁2CO+O 2点燃2CO 2⒂C+CO 2高温2COH 2SO 4HClHNO 3/H 2CO 3Ca(OH)2NaOHCu(OH)2/NH 3·H 2ONa 2CO 3Na 2SO 4NaCl/NaNO 3CaCO 3CaCl 2 Ca(NO 3)2O 2 Fe 3O 4H 2CO 3COCO 2 CaCO 3 H 2O H 2O 2KMnO 4二、推断题解题思路1、阅读题目:要求通阅全题,统领大局。
关键点要反复读,读得它“原形毕露,真相大白”。
2、寻找突破:要求在读题的过程中找出明显条件,挖掘隐含条件,寻找解题的突破口。
3、正确推断:要求从突破口入手将明显与隐含条件相结合,运用合理的方法正确推断。
4、验证答案:要求将推出的结果代入题中逐步检验。
三、推断题解题方法1、顺推法:通常以题首为突破口,按照物质的性质,以及物质间的相互反应为依托逐步深入下去,直至顺利解题。
逆推法:通常以题给的结论或实验现象为突破口,从题尾入手依次向前逆推,从而获得问题的答案。
分层法:将整个推断过程分层进行,先得出每层的结论,再统摄整理。
2、剥离法:根据已知条件把推断过程中存在的有明显特征的未知物质先剥离出来,再将其作为已知条件来逐个推断其他物质。
四、寻找突破1、以物质的特征颜色为突破口黑色的物质:按思考选择的顺序依次为氧化铜、碳、四氧化三铁、二氧化锰、铁粉;红色的单质:铜、红磷、氧化铁绿色的物质:碱式碳酸铜(铜绿);蓝色的溶液:含有Cu2+的溶液(如:硫酸铜、氯化铜、硝酸铜溶液);蓝色的物质:胆矾(蓝矾CuSO4•5H2O);黄色的单质:硫磺(S);黄色的溶液:含有Fe3+的溶液(如:氯化铁、硫酸铁、硝酸铁);浅绿色的溶液:含有Fe2+的溶液(如:氯化亚铁、硫酸亚铁、硝酸亚铁);紫红色溶液:高锰酸钾溶液;蓝色沉淀:氢氧化铜;红褐色沉淀:氢氧化铁。
常见的白色沉淀:碳酸钙、碳酸钡、氢氧化镁、氢氧化铝、硫酸钡、氯化银。
2、以物质的用途为突破口3、以物质的特征组成为突破口4、以典型反应条件为突破口5、以物质的典型性质为突破口6、以化学反应的特殊现象为突破口7、以元素或物质之最为突破口常见的元素或物质之最如下:地壳中含量最多的元素是O,含量最多的金属元素是Al;人体中含量最多的元素是O,最多的金属元素是Ca;空气中含量最多的元素是N;形成化合物最多的元素是C;质子数最少的元素是H;相对分子质量最小、密度也最小的气体是H2;相对分子质量最小的氧化物是H2O;自然界中硬度最大的物质是金刚石;空气中含量最多的气体是N2;最简单的有机物是CH4;最常用的溶剂是H2O;人体中含量最多的物质是H2O。
五、练习1、画出石灰三角并写出化学反应方程式。
2、A-F和X都是初中化学中的常见物质,其中A、C是无色气体,B、F是红色固体,它们的转化关系如下图所示(部分生成物已省略):⑪写出反应①的化学方程。
⑫写出反应②的化学方程式,该反应属于(填写基本反应类型)反应。
⑬含D的生产、生活用品腐蚀的过程,实际上是D与空气中的发生化学反应的过程。
3.用化学方程式表示下列转变② ① ⑧ ⑨ ⑥ ⒀⒁③④ ⑦ ⒂⑤ ⑩ ⑾⑿①______________________________ ②______________________________ ③______________________________ ④______________________________ ⑤______________________________ ⑥______________________________ ⑦______________________________ ⑧______________________________⑨______________________________⑩______________________________ ⑾______________________________ ⑿______________________________ ⒀______________________________ ⒁______________________________ ⒂______________________________ 4、A 、B 、C 、D 、E 为初中化学中不同类别的物质,它们的变化关系如下图所示,其中棕红色物质A 在一定条件下可以转化为单质B ,“ ”表示相连的两种物质能发生反应。
则: (1)D 的化学式为 。
(2)A 转化为B 的化学方程式是 。
(3)C 与E 反应的化学方程式是 。
5、下图是初中化学中常见物质间的转化关系,其中甲、乙、丙为单质;A 、B 、C 、D 、E 为化合物,且A 与B 的组成元素相同,D 与E 的组成元素也相同。
已知C 、丙均为黑色粉末,C 和E 在高温条件下可生成丙和D ,D 能使澄清的石灰水变浑浊。
其余反应条件、部分反应物和生成物均已略去。
试推断:(1) D 物质的化学式______;(2)写出下列化学方程式:A→甲+B :______ _____;甲→E :_____ ___________; 甲→C :__________ ___________。
6、下图是初中化学中常见物质间的转化关系,其中,在通常情况下,F 、G 是组成元素相同的两种气体,Q 、R 都是黑色固体(部分反应条件略去),试回答下列问题: (1)D 、G 的化学式为:______、______。
(2)若E 是生活中常用的调味剂、防腐剂, 则C 的化学式为______,反应①的化学方程式为:______________。
(3)图中标出的九种物质按单质、氧化物、酸、碱、盐进行分类,一定没有的物质类别是________。
(4)反应①~⑤中没有涉及的基本反应类型是______。
O 2 Fe 3O 4H 2CO 3COCO 2 CaCO 3 H 2O H 2O 2KMnO 4。