常用纯溶剂截止波长
- 格式:xls
- 大小:25.50 KB
- 文档页数:1

甲醇的截止吸收波长甲醇是一种常见的有机化合物,化学式为CH3OH。
它是一种无色、挥发性液体,具有特殊的气味。
甲醇在工业生产和日常生活中具有广泛的应用,例如作为溶剂、燃料和化工原料等。
本文将着重介绍甲醇的截止吸收波长及其相关特性。
甲醇的截止吸收波长是指在紫外-可见光谱范围内,甲醇吸收光线的最大波长。
根据文献资料,甲醇的截止吸收波长约为205 nm。
这意味着在较短波长的紫外光下,甲醇会吸收光线,而在较长波长的可见光下,甲醇几乎不吸收光线。
甲醇的截止吸收波长与其分子结构和能级有关。
甲醇分子中的氧原子与氢原子结合,形成一个羟基(OH)官能团。
这个羟基官能团的存在使得甲醇分子具有一定的极性,从而影响了甲醇的光学性质。
甲醇的截止吸收波长对于许多应用具有重要意义。
例如,在紫外-可见分光光度法中,研究物质的吸收特性是常用的分析方法之一。
通过测量甲醇溶液在不同波长下的吸光度,可以确定甲醇的截止吸收波长,并进一步研究甲醇与其他物质的相互作用。
甲醇的截止吸收波长还与其在光催化反应中的应用有关。
光催化反应是一种利用光能催化化学反应的方法,可以实现一些传统方法难以达到的反应条件。
甲醇作为一种常用的光催化反应底物,在特定波长的光照下,可以发生一系列有机合成反应,例如醇的氧化、醚的合成等。
除了甲醇本身的截止吸收波长,甲醇溶液中其他物质的存在也可能影响其吸收特性。
例如,某些金属离子可以与甲醇分子形成络合物,改变甲醇的分子结构和电子能级,从而影响甲醇的吸收波长。
这种效应在分析化学和催化反应中具有重要意义。
甲醇的截止吸收波长为205 nm。
这一特性与甲醇分子的结构和能级密切相关,影响了甲醇在分析化学和光催化反应中的应用。
进一步研究甲醇的截止吸收波长及其影响因素,有助于深入理解甲醇的光学性质和化学反应机理,为相关领域的研究提供指导和依据。
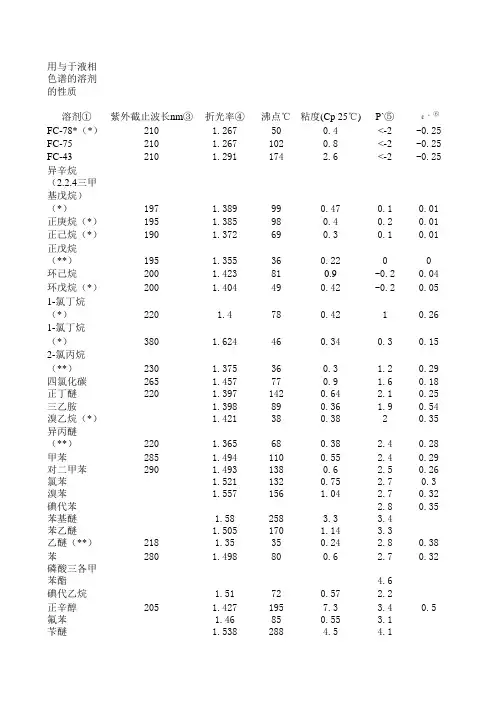
用与于液相色谱的溶剂的性质溶剂①紫外截止波长nm③折光率④沸点℃粘度(Cp 25℃)P`⑤FC-78*(*)210 1.267500.4<-2 FC-75210 1.2671020.8<-2 FC-43210 1.291174 2.6<-2197 1.389990.470.1异辛烷(2.2.4三甲基戊烷)(*)正庚烷(*)195 1.385980.40.2正己烷(*)190 1.372690.30.1正戊烷(**)195 1.355360.220环己烷200 1.423810.9-0.2环戊烷(*)200 1.404490.42-0.2 1-氯丁烷(*)220 1.4780.421 1-氯丁烷(*)380 1.624460.340.3 2-氯丙烷(**)230 1.375360.3 1.2四氯化碳265 1.457770.9 1.6正丁醚220 1.3971420.64 2.1三乙胺 1.398890.36 1.9溴乙烷(*) 1.421380.382异丙醚(**)220 1.365680.38 2.4甲苯285 1.4941100.55 2.4对二甲苯290 1.4931380.6 2.5氯苯 1.5211320.75 2.7溴苯 1.557156 1.04 2.7碘代苯 2.8苯基醚 1.58258 3.3 3.4苯乙醚 1.505170 1.14 3.3乙醚(**)218 1.35350.24 2.8苯280 1.498800.6 2.7磷酸三各甲苯酯 4.6碘代乙烷 1.51720.57 2.2正辛醇205 1.4271957.3 3.4氟苯 1.46850.55 3.1苄醚 1.538288 4.5 4.1二氯甲烷(**)233 1.421400.41 3.1苯甲醚 1.5141540.9 3.8异戊醇 1.405130 3.5 3.7 1.2-二氯乙烷228 1.442830.78 3.5叔丁醇 1.38582 3.6 4.1正丁醇210 1.397118 2.6 3.9正丙醇240 1.38597 1.94四氢呋喃(*)212 1.405660.464丙胺(*) 1.385480.35 4.2乙酸乙酯(*)256 1.37770.43 4.4异丙醇205 1.38482 1.9 3.9氯仿(*)245 1.443610.53 4.1苯乙酮 1.532202 1.64 4.8甲乙酮(*)329 1.376800.38 4.7环己酮 1.451562 4.7硝基苯 1.55211 1.8 4.4苯乙腈 1.526191 1.2 4.8二恶烷215 1.42101 1.2 4.8四甲基脲265 1.4491756喹啉 1.625237 3.45吡啶 1.5071150.88 5.3硝基乙烷380 1.391140.64 5.2丙酮(*)330 1.356560.3 5.1苄醇 1.538205 5.5 5.7四甲基胍 6.1甲氧基乙醇210 1.4125 1.6 5.5丙烯碳酸酯 6.1乙醇210 1.35978 1.08 4.3氧二丙腈 6.8苯胺 1.584184 3.77 6.3乙酸 1.37118 1.16乙腈190 1.341820.34 5.8N,N-二甲基乙酰胺268 1.4361660.78 6.5二甲基甲酰胺268 1.4281530.8 6.4二甲基硫酰268 1.47718927.2N-甲基-2-吡咯烷酮285 1.468202 1.67 6.7六甲基磷酸三酰胺 1.45723337.4甲醇(*)205 1.326650.54 5.1硝基甲烷380 1.381010.616间甲酚 1.54202147.4N-甲基甲酰胺 1.447182 1.656乙二醇 1.43118216.5 1.11甲酰胺 1.447210 3.39.6水 1.3381000.8910.2①(*)表示低粘度(〈0.5cp)、沸点适当(〉45℃)的溶剂;(**)表示粘度很小,沸点也很底的溶③指近似截止波长,低于该值时溶剂不透明。

测定紫外光谱时溶剂的选择(常用的溶
剂的波长极限)
令狐采学
由于溶剂对电子光谱图的影响很大,因此在吸收光谱图上或数据表中必须注明所用溶剂;对已知化合物作紫外光谱比较时,也应注意所用溶剂是否相同。
紫外-可见分光光度法中如何正确选择溶剂?
溶剂极性除了对最大吸收峰波长有影响外,还影响吸收光谱的精细结构。
当物质处于蒸气状态时,由于分子间的相互作用力减小到最低程度,电子光谱的精细结构(振转光谱)清晰可见;当物质处于非极性溶剂中时,由于溶质分子和溶剂分子间的相互碰撞,使精细结构部分消失;当物质处于极性溶剂中时,由于溶剂化作用,限制了分子的振动和转动,使精细结构完全消失,分子的电子光谱只呈现宽的谱线包封。
测定化合物的紫外吸收光谱时选择溶剂的原则是:
(1)样品在溶剂中溶解良好,能达到必要的浓度以得到吸光度适中的吸收曲线;
(2)溶剂不影响样品的吸收光谱,因此在测定的波长范围内溶剂应当是紫外透明的,即溶解本身没有吸收。
透明范围的最短波长称为透明界限,测试时应根据溶剂的透明界限选择合适
的溶剂;(3)为了降低溶剂与溶质分子间的作用力,减少溶剂对吸收光谱的影响,应尽量采用低极性溶剂;
(4)溶剂挥发性小、不易燃、无毒性、价格便宜;
(5)所选用的溶剂应与待测组分不发生化学反应。

液相截止波长
Document number:WTWYT-WYWY-BTGTT-YTTYU-2018GT
1、溶剂
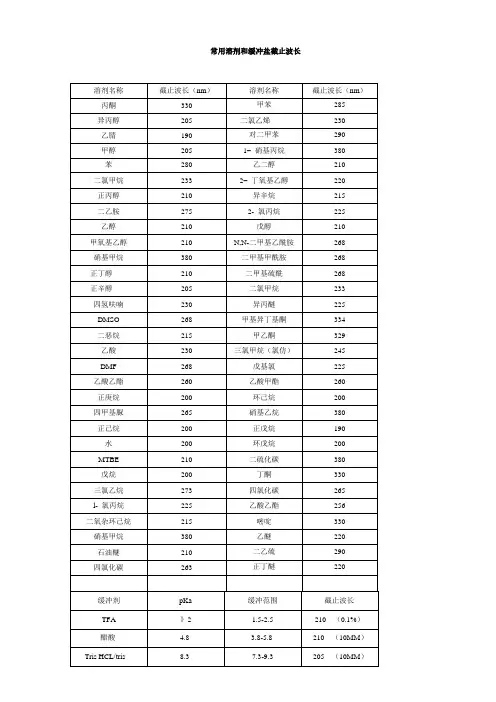
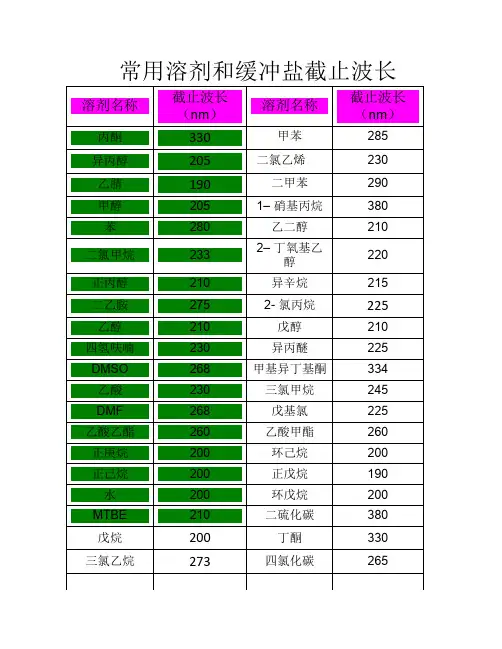
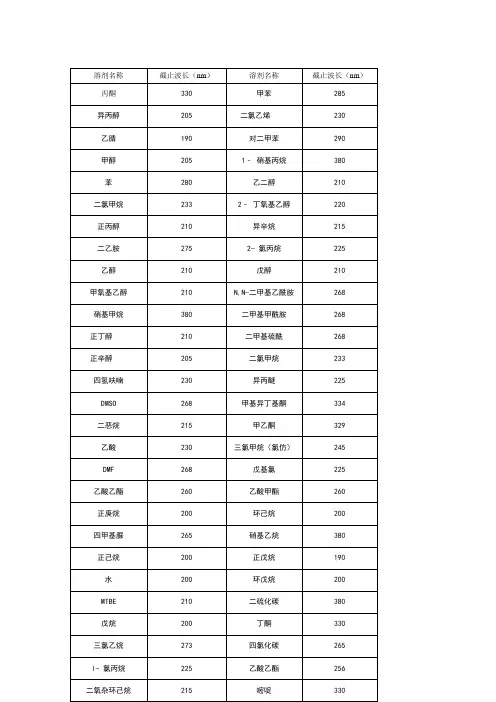
溶剂名称截止波长(nm)溶剂名称截止波长(nm)丙酮330 甲苯285
异丙醇205 二氯乙烯230
乙腈190 二甲苯290
甲醇205 1–硝基丙烷380
苯280 乙二醇210
二氯甲烷233 2–丁氧基乙醇220
正丙醇210 异辛烷215
二乙胺275 2-氯丙烷225
乙醇210 戊醇210
四氢呋喃230 异丙醚225
DMSO 268 甲基异丁基酮334
乙酸230 三氯甲烷245
DMF 268 戊基氯225
乙酸乙酯260 乙酸甲酯260
正庚烷200 环己烷200
正己烷200 正戊烷190
水200 环戊烷200
MTBE 210 二硫化碳380
戊烷200 丁酮330
三氯乙烷273 四氯化碳265
l-氯丙烷225 乙酸乙酯256
二氧杂环己烷215 嘧啶330
硝基甲烷380 乙醚220
石油醚210 二乙硫290
四氯化碳263
缓冲盐
缓冲剂pKa Bufferrange截止波长
TFA 》2 (%)
醋酸(10MM)TrisHCL/tris (10MM)氯化铵(10MM)
磷酸< <200%) 磷酸二氢钾(10MM)
磷酸氢二钾(10MM)
bistrisHCl (10MM)bistris (10MM)三乙胺
柠檬酸钠(10MM)。

测定紫外光谱时溶剂的选择(常用的溶剂的波长极限)由于溶剂对电子光谱图的影响很大,因此在吸收光谱图上或数据表中必须注明所用溶剂;对已知化合物作紫外光谱比较时,也应注意所用溶剂是否相同。
紫外-可见分光光度法中如何正确选择溶剂?
溶剂极性除了对最大吸收峰波长有影响外,还影响吸收光谱的精细结构。
当物质处于蒸气状态时,由于分子间的相互作用力减小到最低程度,电子光谱的精细结构(振转光谱)清晰可见;当物质处于非极性溶剂中时,由于溶质分子和溶剂分子间的相互碰撞,使精细结构部分消失;当物质处于极性溶剂中时,由于溶剂化作用,限制了分子的振动和转动,使精细结构完全消失,分子的电子光谱只呈现宽的谱线包封。
测定化合物的紫外吸收光谱时选择溶剂的原则是:
(1)样品在溶剂中溶解良好,能达到必要的浓度以得到吸光度适中的吸收曲线;
(2)溶剂不影响样品的吸收光谱,因此在测定的波长范围内溶剂应当是紫外透明的,即溶解本身没有吸收。
透明范围的最短波长称为透明界限,测试时应根据溶剂的透明界限选择合适的溶剂;
(3)为了降低溶剂与溶质分子间的作用力,减少溶剂对吸收光谱的影响,应尽量采用低极性溶剂;
(4)溶剂挥发性小、不易燃、无毒性、价格便宜;
(5)所选用的溶剂应与待测组分不发生化学反应。

.测定紫外光谱时溶剂的选择(常用的溶剂的波长极限)由于溶剂对电子光谱图的影响很大,因此在吸收光谱图上或数据表中必须注明所用溶剂;对已知化合物作紫外光谱比较时,也应注意所用溶剂是否相同。
紫外-可见分光光度法中如何正确选择溶剂?溶剂极性除了对最大吸收峰波长有影响外,还影响吸收光谱的精细结构。
当物质处于蒸气状态时,由于分子间的相互作用力减小到最低程度,电子光谱的精细结构(振转光谱)清晰可见;当物质处于非极性溶剂中时,由于溶质分子和溶剂分子间的相互碰撞,使精细结构部分消失;当物质处于极性溶剂中时,由于溶剂化作用,限制了分子的振动和转动,使精细结构完全消失,分子的电子光谱只呈现宽的谱线包封。
测定化合物的紫外吸收光谱时选择溶剂的原则是:(1)样品在溶剂中溶解良好,能达到必要的浓度以得到吸光度适中的吸收曲线;(2)溶剂不影响样品的吸收光谱,因此在测定的波长范围内溶剂应当是紫外透明的,即溶解本身没有吸收。
透明范围的最短波长称为透明界限,测试时应根据溶剂的透明界限选择合适的溶剂;(3)为了降低溶剂与溶质分子间的作用力,减少溶剂对吸收光谱的影响,应尽量采用低极性溶剂;1 / 3.(4)溶剂挥发性小、不易燃、无毒性、价格便宜;(5)所选用的溶剂应与待测组分不发生化学反应。
常用溶剂的波长极限(nm)溶剂极限波长溶剂极限波长正戊烷戊基氯190225二烷基硫酸钠柠檬酸钠,10 mM 225190四氢呋喃乙腈230190碳酸氢铵10 mM 乙酸,1% 190 230甲酸钠,10 mM 二氯乙烯200230环戊烷二氯甲烷200 235环己烷1% 三乙胺,200235醋酸铵,10 mM 三氯甲烷205 245 异丙乙酸甲2026甲四氯化202651 氯化钠二乙20275石油21280乙甲2128乙二甲2129乙二二乙2129丁2133二氧杂环己丙21332 / 3.3 / 3。

乙腈的截止波长乙腈是一种有机化合物,化学式为CH3CN。
它是一种无色液体,在常温常压下具有刺激性的气味。
乙腈广泛应用于有机合成、溶剂、电子工业、化工和医药等领域。
乙腈的截止波长是指乙腈在紫外-可见光谱中吸收较强的波长。
根据文献资料,乙腈的截止波长约为190-200纳米。
这意味着乙腈在低于190纳米的紫外光区域有较强的吸收能力。
乙腈的截止波长对于许多领域的研究和应用都非常重要。
例如,在生物医学研究中,乙腈的截止波长可以用于测定蛋白质和核酸的浓度。
通过测量乙腈在特定波长下的吸光度,可以计算样品中蛋白质和核酸的含量。
这对于研究生物大分子的结构和功能具有重要意义。
乙腈的截止波长还可以用于光谱分析和荧光测量。
在光谱分析中,乙腈可以作为溶剂,用于将样品溶解并测量其吸光度。
乙腈的截止波长可以帮助确定合适的测量范围,避免光谱信号受到乙腈的吸收影响。
在荧光测量中,乙腈的截止波长可以用于选择合适的激发光源,以提高荧光测量的准确性和灵敏度。
乙腈的截止波长还与其分子结构密切相关。
乙腈分子由碳、氢和氮原子组成,其中氮原子上带有一个孤对电子。
这个孤对电子可以参与分子间的氢键形成,从而影响乙腈的结构和性质。
乙腈的截止波长可以反映其分子间相互作用的强度和类型。
因此,通过测量乙腈的截止波长,可以进一步研究其分子结构和相互作用。
乙腈的截止波长还与其在有机合成中的应用有关。
乙腈是一种常用的有机溶剂,广泛应用于有机合成反应中。
乙腈的截止波长可以用于选择合适的光源和滤光片,以避免光敏反应的发生。
此外,乙腈的截止波长还可以用于监测反应进程中的吸收变化,从而控制反应的进行。
乙腈的截止波长是乙腈在紫外-可见光谱中吸收较强的波长。
它在生物医学研究、光谱分析、荧光测量和有机合成中具有重要的应用价值。
通过测量乙腈的截止波长,可以研究其分子结构和相互作用,进一步推动相关领域的发展和应用。
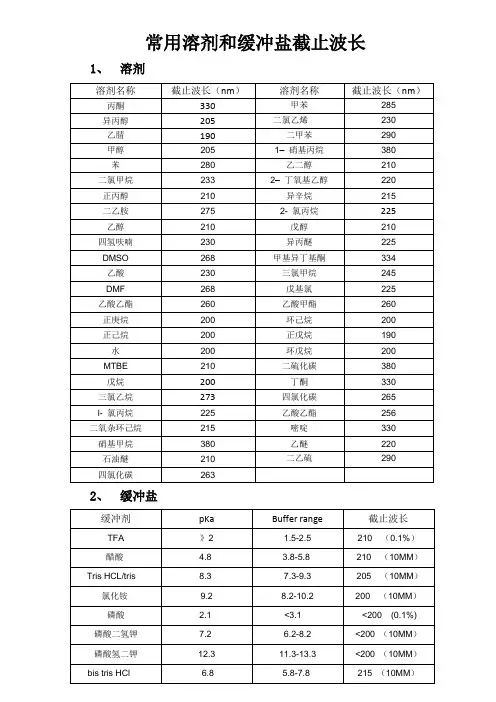
三氯甲烷的紫外截止波长是245nm提供给楼主一下信息:常见色谱溶剂的UV 截止波长:(后面数字表示截止波长)1–硝基丙烷380 乙二醇2102–丁氧基乙醇220 异辛烷215丙酮330 异丙醇205乙腈190 2- 氯丙烷225戊醇210 异丙醚220戊基氯225 甲醇205苯280 乙酸甲酯260二硫化碳380 丁酮330四氯化碳265 甲基异丁基酮334三氯甲烷245 二氯甲烷233环己烷200 正戊烷190环戊烷200 正丙醇210二乙胺275 l- 氯丙烷225二氧杂环己烷215 硝基甲烷380乙醇210 石油醚210乙酸乙酯256 嘧啶330乙醚220 四氢呋喃230二乙硫290 甲苯285二氯乙烯230 二甲苯290乙酸,1% 230 氯化钠, 1 M 207醋酸铵,10 mM 205 柠檬酸钠,10 mM 225 碳酸氢铵,10 mM 190 十二烷基硫酸钠190 BRIJ 35,0.1% 190 甲酸钠,10 mM 200 CHAPS,0.1% 215 三乙胺,1% 235磷酸氢二铵,50 mM 205 三氟醋酸,0.1% 190 EDTA,二钠盐,1 mM 190 TRIS HCl,20 mM,pH 7.0 202,pH 8.0 212 HEPES,10 mM,pH 7.6 225 Triton-X 1000.1% 240 盐酸,0.1% 190 200 磷酸钾,一元碱,10 mM 190 二元碱,10 mM 190,乙酸钠10 mM 205以上信息由waters提供。
EDTA,二钠盐,1 mM 190 TRIS HCl,20 mM,pH 7.0 202,pH 8.0 212 HEPES,10 mM,pH 7.6 225 Triton-X 100,0.1% 240盐酸,0.1% 190 200 磷酸钾,一元碱,10 mM 190 二元碱,10 mM190乙酸钠,10 mM 205以上信息由waters提供。
对于紫外吸收检测器,应注意选用检测器波长比溶剂的紫外截止波长要长。
所谓溶剂的紫外截止波长指当小于截止波长的辐射通过溶剂时,溶剂对此辐射产生强烈吸收,此时溶剂被看作是光学不透明的,它严重干扰组分的吸收测量。
出了一些常用溶剂的紫外截止波长。
甲醇205nm 水187nm 乙腈190nm 四氢呋喃212nm 丙酮330nm 二氯甲烷233nm 氯仿245nm 苯210nm 正几烷190nm也就是说你用上述溶剂时,检测波长不要低于所列数值,否则可能出现溶剂峰,但是在210-230之间,离190nm乙腈的截至波长远,不会产生吸收,倒是甲醇在210nm容易产生吸收,在色谱图最前面出现2-3个小峰。
但不是倒峰。
我建议你直接进几针流动相,看有没有峰出现,一般在210nm以上,乙腈是不会有溶剂峰的,除非你的乙腈污染,或者质量不好(建议买fisher色谱纯,国产的一般不行),进乙腈也可以,看是不是流动相或乙腈的问题柱高压1.颗粒物积聚在烧结物或者树脂床上(它们都会使背压增高)。
如果柱压增高了,将柱子与进样器断开,运行泵,以验证背压的来源确实是来自柱子的颗粒污染(样品、洗脱液和系统)。
倒转柱子,以反向的流动来冲洗柱子。
如果这样不能解决问题,更换进口过滤器或者筛板。
2.微生物在洗脱液中生长。
倒转柱子,尝试以反向的流动来将污染物冲洗出柱子。
更换进口过滤器或者筛板。
3.有蛋白质脂肪,油脂污染或者极性化合物等污染。
再生柱子。
再生1.再生反相色谱柱a.首先倒转柱子。
b.以大约最佳流速的40%的流速冲洗柱子大约45-60分钟,使用的溶剂的顺序要按照水—甲醇—异丙醇—二氯甲烷—异丙醇—甲醇—水进行。
c.柱子转回正常方向,使用分析所用洗脱液平衡。
注意:在使用另外的淋洗方法的时候,一定要先用水开始冲洗以去除缓冲液,保证其后的洗脱液可以混溶。
测定紫外光谱时溶剂的选择(常用的溶剂的波长极限)由于溶剂对电子光谱图的影响很大,因此在吸收光谱图上或数据表中必须注明所用溶剂;对已知化合物作紫外光谱比较时,也应注意所用溶剂是否相同。
紫外-可见分光光度法中如何正确选择溶剂?溶剂极性除了对最大吸收峰波长有影响外,还影响吸收光谱的精细结构。
当物质处于蒸气状态时,由于分子间的相互作用力减小到最低程度,电子光谱的精细结构(振转光谱)清晰可见;当物质处于非极性溶剂中时,由于溶质分子和溶剂分子间的相互碰撞,使精细结构部分消失;当物质处于极性溶剂中时,由于溶剂化作用,限制了分子的振动和转动,使精细结构完全消失,分子的电子光谱只呈现宽的谱线包封。
测定化合物的紫外吸收光谱时选择溶剂的原则是:(1)样品在溶剂中溶解良好,能达到必要的浓度以得到吸光度适中的吸收曲线;(2)溶剂不影响样品的吸收光谱,因此在测定的波长范围内溶剂应当是紫外透明的,即溶解本身没有吸收。
透明范围的最短波长称为透明界限,测试时应根据溶剂的透明界限选择合适的溶剂;(3)为了降低溶剂与溶质分子间的作用力,减少溶剂对吸收光谱的影响,应尽量采用低极性溶剂;(4)溶剂挥发性小、不易燃、无毒性、价格便宜;(5)所选用的溶剂应与待测组分不发生化学反应。
常用溶剂的波长极限(nm)溶剂极限波长溶剂极限波长正戊烷190戊基氯225二烷基硫酸钠190柠檬酸钠,10mM225乙腈190四氢呋喃230碳酸氢铵10mM190乙酸,1%230甲酸钠,10mM200二氯乙烯230环戊烷200二氯甲烷235环己烷200三乙胺,1%235醋酸铵,10mM205三氯甲烷245异丙醇205乙酸甲酯260甲醇205四氯化碳265氯化钠,1M207二乙胺275石油醚210苯280乙醇210甲苯285乙醚210二甲苯290乙二醇210二乙硫290水210丁酮330二氧杂环己烷215丙酮330异辛烷215嘧啶330 2-氯丙烷225甲基异丁基酮334 2–丁氧基乙醇220二硫化碳380 1,4-二氧六环2201–硝基丙烷380异丙醚220硝基甲烷380。
二氯甲烷截止波长二氯甲烷(CH2Cl2),也称为亚氯甲烷,是一种常见的有机化学试剂和溶剂。
它是一种无色液体,在常温下具有刺激性气味。
二氯甲烷是由一个碳原子和两个氯原子与两个氢原子相连形成的,化学式为CH2Cl2。
在光学领域,截止波长是指物理系统中的波长上限,该波长以上的光波将无法透过该系统或被完全吸收。
对于二氯甲烷而言,其截止波长是指在该波长以下,其分子中的能级与光子能量差距足够大,从而使得光子可以激发分子内部的电子跃迁。
以下是对二氯甲烷截止波长的详细探讨。
二氯甲烷的分子结构中存在着氯原子和碳原子,因此它具有较高的电负性。
由于氯原子的存在,二氯甲烷分子极性增大,使得它在化学反应中具有较高的反应性。
此外,二氯甲烷也具有较高的沸点和较低的凝固点,使其成为许多化学和工业应用中的理想选择。
二氯甲烷在紫外-可见区域的吸收特性主要来自于分子中碳原子周围的σ*轨道与π*轨道的相互作用。
这两个轨道分别属于反键和非键电子,它们之间的能量差距与分子的π电子能级结构有关。
在UV-Vis 光谱中,这种分子内电子的跃迁将会引起可见光波长下的吸收峰。
根据现有的文献和研究,二氯甲烷的截止波长主要集中在紫外光区域(200-400纳米)。
具体来说,在实验室条件下,使用紫外-可见分光光度计或其他相关仪器,可以测量出二氯甲烷在此波长范围内的吸光度值。
通过绘制吸光度和波长之间的关系曲线,可以确定截止波长的位置。
除了实验测量,理论计算也可以用于确定二氯甲烷的截止波长。
使用量子力学方法,可以计算出分子内部能级间的能量差值,并根据这些能量差值确定截止波长的位置。
这样的计算方法需要依赖于大量的计算资源和精确的量子力学计算模型。
需要注意的是,二氯甲烷在紫外光区域的吸收峰并不是一个单一的波长,而是一个宽广的范围。
这是因为分子内部的电子能级结构以及分子之间的相互作用会导致吸收峰的位置发生变化。
因此,截止波长实际上是一个特定范围内的波长,而不是一个精确的数值。