热分析实验教程
- 格式:ppt
- 大小:15.37 MB
- 文档页数:53

实验四:综合热分析仪实验实验四:综合热分析仪实验一、实验目的1. 了解综合热分析仪的组成及各部分的功能。
要求学生认识综合热分析仪的各部件,掌握各部件的基本功能。
2. 加深理解综合热分析仪的原理和应用。
要求学生利用课堂所学的综合热分析仪的基本原理,结合实验仪器有更进一步的了解,并能够应用到实践中去。
3. 掌握利用综合热分析仪研究材料热稳定性的方法。
掌握综合热分析仪测试材料的步骤以及方法,并能够对测得的曲线进行正确的分析。
二、实验原理1.热重分析基本原理热重法是对试样的质量随以恒定速度变化的温度或在等温条件下随时间变化而发生的改变量进行测量的一种动态技术,在热分析技术中热重法使用最为广泛,这种研究是在静止的或流动着的活性或惰性气体环境中进行的。
热重法通常有下列两种类型:等温热重法——在恒温下测定物质质量变化与时间的关系;非等温热重法——在程序升温下测定物质质量变化与温度的关系。
热重法所用仪器称为热重分析仪或热天平,其基本构造是由精密天平和线性程序控温的加热炉所组成,热天平是根据天平梁的倾斜与重量变化的关系进行测定的,通常测定重量变化的方法有变位法和零位法两种。
?变位法,主要利用质量变化与天平梁的倾斜成正比关系,当天平处于零位时位移检测器输出的电讯号为零,而当样品发生重量变化时,天平梁产生位移,此时检测器相应的输出电讯号,该讯号可通过放大后输入记录仪进行记录。
零位法,由重量变化引起天平梁的倾斜,靠电磁作用力使天平梁恢复到原来的平衡位置,所施加的力与重量变化成正比。
当样品质量发生变化时,天平梁产生倾斜,此时位移检测器所输出的讯号通过调节器向磁力补偿器中的线圈输入一个相应的电流,从而产生一个正比于质量变化的力,使天平梁复位到零。
输入线圈的电流可转换成电压讯号输入记录仪进行记录。
2.示差扫描量热分析法示差扫描量热分析法(DSC)是在程序控制温度下,测量输入到试样和参比物的功率差与温度之间关系的一种技术,试样和参比物分别由单独控制的电热丝加热,根据试样中的热效应,可连续调节这些电热丝的功率,用这种方法使试样和参比物处于相同的温度下,达到这个条件所需的功率差作为纵坐标,系统的温度参数作为横坐标,一起由记录仪进行记录。

热分析实验热分析实验(演示试验)一、实验意义和目的材料组成的热分析方法是当前材料研究中普遍使用的一种试验手段,合理正确使用热分析方法能快速高效分析混合物中组成成分的性质和含量。
如果能合理进行实验设计,则能有效追踪材料结构形成或材料性能劣化过程中的反应物、生成物的定量变化。
鉴于材料热分析方法是材料科学研究广泛使用的测试仪器,已广泛运用于科研、工业生产中。
因而,掌握其基本工作原料,了解试样制备方法,掌握仪器的基本操作方法等具有重要的意义。
本实验目的是通过材料差式扫描量热分析试验的演示操作;试样制备,测试、结果分析。
让学生了解差热分析仪的基本构造及其工作原理,并掌握差热分析仪的基本操作方法,学会利用该设备对材料进行定性分析。
二、实验原理(一)差式扫描量热分析仪的基本原理物质加热后发生化学的或物理的变比时,会表现出吸热、放热等能量的转变,或重量、体积等的变化。
不同的物质有不同的组成和结构,加热后有特定的热效应。
当物质发生相变化时,就会在特定热效应中反应出来。
因此,可以用对物质加热的方法进行相分析。
材料热分析技术主要包括差热分析(DTA)、热重分析(TG)和差式扫描量热分析仪(DSC)。
本试验主要是采用DSC进行试验操作,DSC的基本原理是在加热过程中,测量被测物质与参比物之间的能量差与温度之间的关系。
通常有热通量式和热流式、功率补偿式。
功率补偿式是在试样和参比样下装置补偿加热丝。
在量测回路中增加一个功率补偿放大器。
加热丝各自独立。
给参比样加热电流为I R,试佯下的加热电流为I S。
当试样加热时,热电偶量测试样温度比参比样温度高,产生温差电势U△T,经过差热放大器和功率补偿放大器后,使I S减小,I R增大。
产生相反的电势-U△T,补偿原来的U△T,使试样和参比样之间温差△T等于0。
从补偿的功率可以求出试样的热流率(焰变)。
相比与DTA而言,仪器灵敏度高、测量准确、重现性好、且能直接测量反应热,计算方便,已成为现代仪器分析的主要手段之一。

综合同步热分析(T G A-D S C)实验讲义一、实验目的:用热分析仪对进行TG和DSC分析,并对热分析谱图进行定性和定量分析。
二、预习要求1、了解热分析仪的工作原理和操作方法;2、了解TG和DSC分析的基本原理及热分析谱图的意义。
三、原理1、热分析的定义:热分析(thermal analysis):顾名思义,可以解释为以热进行分析的一种方法。
1977年在日本京都召开的国际热分析协会(ICTA)第七次会议上,给热分析下了如下定义:即热分析是在程序控制温度下,测量物质的物理、化学性质与温度的关系的一类技术。
通俗来说,热分析是通过测定物质加热或冷却过程中物理性质(目前主要是重量和能量)的变化来研究物质性质及其变化,或者对物质进行分析鉴别的一种技术。
程序控制温度:一般是指线性升温或线性降温,当然也包括恒温、循环或非线性升温、降温。
也就是把温度看作是时间的函数:T=φ(t); t:时间。
常见的物理变化:熔化、沸腾、升华、结晶转变等;常见的化学变化:脱水、降解、分解、氧化,还原、化合反应等。
这两类变化,常伴有焓变,质量、机械性能和力学性能等的变化。
2、热分析存在的客观物质基础在目前热分析可以达到的温度范围内,从-150℃到1500℃(或2400℃),任何两种物质的所有物理、化学性质是不会完全相同的。
因此,热分析的各种曲线具有物质“指纹图”的性质。
3、热分析的起源及发展1899 年英国罗伯特-奥斯汀(Roberts-Austen)第一次使用了差示热电偶和参比物,大大提高了测定的灵敏度,正式发明了差热分析(DTA)技术。
1915 年日本东北大学本多光太郎,在分析天平的基础上研制了“热天平”即热重法(TG),后来法国人也研制了热天平技术。
1964 年美国瓦特逊(Watson)和奥尼尔(O’Neill)在DTA技术的基础上发明了差示扫描量热法(DSC)。
美国P-E公司最先生产了差示扫描量热仪,为热分析热量的定量作出了贡献。

综合热分析仪热重分析法试验步骤分析仪器工要懂得仪器的日常维护和对重要技术指标的简易测试方法,自身常常对仪器进行维护和测试,以保证仪器工作在较佳状态。
一、温度和湿度是影响仪器性能的紧要因素。
他们可以引起机械部件的锈蚀,使金属镜面的干净度下降,引起仪器机械部分的误差或性能下降;造成光学部件如光栅、反射镜、聚焦镜等的铝膜锈蚀,产生光能不足、杂散光、噪声等,甚至仪器停止工作,从而影响仪器寿命。
维护保养时应定期加以校正。
应具备四季恒湿的仪器室,配置恒温设备,特别是地处南方地区的试验室。
二、环境中的灰尘和腐蚀性气体亦可以影响机械系统的快捷性、降低各种限位开关、按键、光电偶合器的牢靠性,也是造成必须学部件铝膜锈蚀的原因之一、因此必须定期清洁,保障环境和仪器室内卫生条件,防尘。
三、仪器使用肯定周期后,内部会积累肯定量的灰尘,可以由维护和修理工程师或在工程师引导下定期开启仪器外罩对内部进行除尘工作,同时将各发热元件的散热器重新紧固,对光学盒的密封窗口进行清洁,必须时对光路进行校准,对机械部分进行清洁和必须的润滑,最后,恢复原状,再进行一些必须的检测、调校与记录。
注意事项1.该仪器应放在干燥的房间内,使用时放置在坚固平稳的工作台上,室内照明不宜太强。
热天时不能用电扇直接向仪器吹风,防止电灯泡灯丝发亮不稳定。
2.使用本仪器前,使用者应当首先了解本仪器的结构和工作原理,以及各个控制旋钮之功能。
在未按通电源之前,应当对仪器的安全性能进行检查,电源接线应坚固,通电也要良好,各个调整旋钮的起始位置应当正确,然后再按通电源开关。
3.在仪器尚未接通电源时,电表指针必须于“0”刻线上,若不是这种情况,则可以用电表上的校正螺丝进行调整。
综合热分析仪热重分析法试验步骤综合热分析仪重要测量与热量有关的物理、化学变更,如物质的熔点、熔化热、结晶与结晶热、相变反应热、热稳定性(氧化诱导期)、玻璃化变更温度、吸附与解吸、成分的含量分析、分解、化合、脱水、添加剂等变更进行讨论。

一、实验目的1. 了解热分析的基本原理和方法;2. 掌握热重分析(TG)和差热分析(DTA)的操作方法;3. 通过实验,分析样品的热性质变化,并探讨其与物质结构、组成的关系。
二、实验原理热分析是一种基于物质在加热或冷却过程中物理性质和化学性质变化的测试方法。
主要方法包括热重分析(TG)、差热分析(DTA)、差示扫描量热法(DSC)等。
本实验主要涉及TG和DTA两种方法。
1. 热重分析(TG):在程序控制温度下,测量物质的质量与温度或时间的关系。
通过TG曲线,可以分析样品的热稳定性、分解温度、相变温度等热性质。
2. 差热分析(DTA):在程序控制温度下,比较样品与参比物的温度差。
当样品发生相变、分解等热效应时,其温度差会发生变化,从而得到DTA曲线。
三、实验器材1. 热重分析仪2. 差热分析仪3. 样品支架4. 样品5. 计算机及数据采集软件四、实验操作步骤1. 样品准备:将样品研磨成粉末,过筛,取适量放入样品支架。
2. 热重分析(TG)实验:a. 打开热重分析仪,预热至设定温度;b. 将样品支架放入炉内,设置加热程序;c. 记录样品质量随温度的变化曲线。
3. 差热分析(DTA)实验:a. 打开差热分析仪,预热至设定温度;b. 将样品支架放入炉内,设置加热程序;c. 同时记录样品与参比物的温度差随时间的变化曲线。
4. 数据处理与分析:将实验数据导入计算机,使用数据采集软件进行曲线拟合、峰面积计算等分析。
五、实验结果与分析1. 热重分析(TG)结果:通过TG曲线,可以看出样品在加热过程中质量的变化。
分析样品的分解温度、相变温度等热性质。
2. 差热分析(DTA)结果:通过DTA曲线,可以看出样品在加热过程中温度差的变化。
分析样品的相变温度、分解温度等热性质。
3. 结果比较:对比TG和DTA结果,分析样品的热性质变化,探讨其与物质结构、组成的关系。
六、实验结论通过本次实验,我们掌握了热重分析(TG)和差热分析(DTA)的操作方法,分析了样品的热性质变化,并探讨了其与物质结构、组成的关系。

热分析实验报告(二)引言概述:本文旨在对热分析实验进行详细的报告,旨在介绍实验的目的、方法、结果和讨论。
通过热分析实验,我们可以了解样品的热性能以及固态化学反应的热效应。
本次实验采用差示扫描量热法(DSC)和热重分析法(TGA)来分析样品的热性质和热分解行为。
正文:1. 实验目的1.1 熟悉差示扫描量热法和热重分析法的原理和操作方法1.2 分析样品的热性能,探究可能的相变和热效应1.3 研究样品的热分解行为,了解其稳定性和热稳定性2. 实验方法2.1 样品的制备和处理2.1.1 样品的选择和准备2.1.2 样品的称量和粉碎2.1.3 样品的处理和预处理2.2 差示扫描量热法(DSC)的操作步骤2.2.1 DSC仪器的准备和参数设置2.2.2 样品的装填和测量2.2.3 实验过程的记录和数据处理2.3 热重分析法(TGA)的操作步骤2.3.1 TGA仪器的准备和参数设置 2.3.2 样品的装填和测量2.3.3 实验过程的记录和数据处理3. 实验结果3.1 DSC曲线分析结果3.1.1 样品在升温过程中的热峰分析 3.1.2 样品在降温过程中的热峰分析 3.2 TGA曲线分析结果3.2.1 样品的失重过程分析3.2.2 样品的热分解过程分析3.3 结果的数值分析和对比4. 讨论4.1 样品的热性能分析4.1.1 样品的相变行为和热效应4.1.2 样品的热容量和热传导性能 4.2 样品的热分解行为分析4.2.1 样品的失重过程的解释和分析 4.2.2 样品的热分解动力学分析4.3 结果与理论的对比和讨论5. 结论5.1 通过DSC和TGA分析,我们获得了样品的热性能和热分解行为的有用信息5.2 样品的相变行为和热效应与其化学成分和结构密切相关5.3 样品的热分解行为显示了其热稳定性和可能的降解途径5.4 本实验为今后的相关研究和工业应用提供了有价值的参考依据总结:本文对热分析实验进行了详细的报告,介绍了实验的目的、方法、结果以及讨论。

热分析的实验报告实验名称:热分析实验报告实验目的:1. 掌握热分析仪器的基本操作方法;2. 了解样品在不同温度条件下的热变化过程;3. 通过热分析实验,分析样品的热稳定性和热分解特性。
实验仪器和试剂:1. 热重仪(TG);2. 差热扫描量热仪(DSC);3. 微量天平;4. 铝样品盘;5. 分析样品。
实验步骤:1. 开启热重仪和差热扫描量热仪的电源,预热30分钟;2. 准备分析样品,取适量的样品放在铝样品盘中,并称重记录样品质量;3. 将铝样品盘放入热重仪或差热扫描量热仪的样品舱中,并用卡扣固定好;4. 设置实验参数,如升温速率、起始和终止温度等;5. 开始实验,记录样品在不同温度下的质量变化情况和热量变化曲线;6. 实验结束后,关闭仪器,整理实验数据。
实验结果及分析:根据实验数据绘制样品质量随温度变化的曲线图和热量变化曲线图,并根据曲线特征进行分析。
1. 样品质量随温度变化的曲线图:从曲线图中观察样品在不同温度下的质量变化情况,可以看出样品在一定温度范围内存在质量损失或增加的现象。
这些质量的变化可能是由于样品发生了挥发、热分解、燃烧等热化学反应引起的。
通过观察曲线的变化趋势和峰值的位置,可以初步判断样品的热稳定性和热分解特性。
2. 热量变化曲线图:根据热量变化曲线图,可以得到样品在不同温度下吸热或放热的情况。
曲线中的峰值表示了样品发生热化学反应时吸热或放热的最大峰值。
通过观察峰值的位置、面积和形状,可以推测样品的热分解峰温、热分解焓变等参数。
结论:通过对实验结果的分析,可以得出样品的热稳定性、热分解特性等信息。
例如,样品在一定温度范围内质量的损失或增加,表明样品可能存在挥发或热分解的反应。
热量变化曲线中的峰值位置、形状和面积可以初步判断样品的热分解特性。
需要注意的是,实验结果仅为初步判断,具体分析还需要进一步的实验和数据处理。
同时,在进行热分析实验时,应确保实验仪器的准确性和可靠性,并控制实验参数的合理性,以获得可重复的实验结果。

实验六 热分析实验一、目的与要求1.了解热重分析的仪器装置及实验技术。
2.了解差热分析的仪器装置及实验技术。
3熟悉综合热分析的特点,掌握综合热曲线的分析方法。
4.测绘矿物的热重曲线和差热分析曲线,解释曲线变化的原因。
二、原理1 热重分析的仪器结构与分析方法热重分析法是在程序控制温度下,测量物质的质量随温度变化的一种实验技术。
热重分析通常有静态法和动态法两种类型。
静态法又称等温热重法,是在恒温下测定物质质量变化与温度的关系,通常把试样在各给定温度加热至恒重。
该法比较准确,常用来研究固相物质热分解的反应速度和测定反应速度常数。
动态法又称非等温热重法,是在程序升温下测定物质质量变化与温度的关系,采用连续升温连续称重的方式。
该法简便,易于与其他热分析法组合在一起,实际中采用较多。
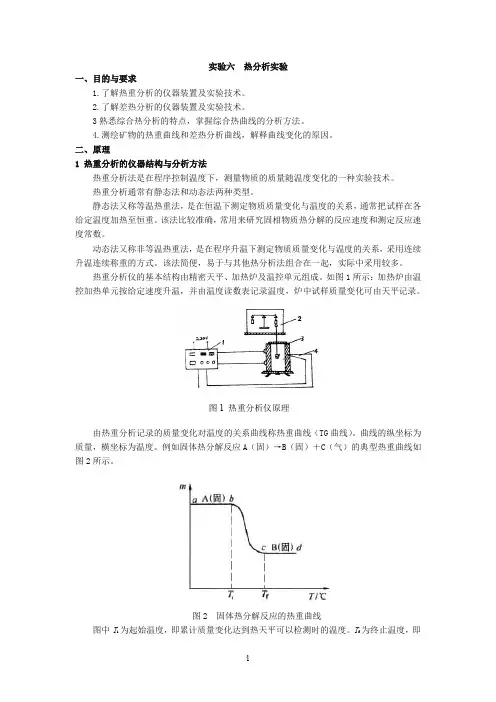
热重分析仪的基本结构由精密天平、加热炉及温控单元组成。
如图1所示:加热炉由温控加热单元按给定速度升温,并由温度读数表记录温度,炉中试样质量变化可由天平记录。
由热重分析记录的质量变化对温度的关系曲线称热重曲线(TG 曲线)。
曲线的纵坐标为质量,横坐标为温度。
例如固体热分解反应A (固)→B (固)+C (气)的典型热重曲线如图2所示。
图2 固体热分解反应的热重曲线图中T i 为起始温度,即累计质量变化达到热天平可以检测时的温度。
T f 为终止温度,即图1 热重分析仪原理累计质量变化达到最大值时的温度。
热重曲线上质量基本不变的部分称为基线或平台,如图2中ab 、cd 部分。
若试样初始质量为W 0,失重后试样质量为W 1,则失重百分数为(W 0-W 1)/W 0×100%。
许多物质在加热过程中会在某温度发生分解、脱水、氧化、还原和升华等物理化学变化而出现质量变化,发生质量变化的温度及质量变化百分数随着物质的结构及组成而异,因而可以利用物质的热重曲线来研究物质的热变化过程,如试样的组成、热稳定性、热分解温度、热分解产物和热分解动力学等。


实验一同步热分析实验一、综合热分析一、实验目的1.了解热失重(TG),差热分析(DTA)和差动热分析(DSC)的基本原理和应用,及相互间的差别。
2.了解STA449F3同步热分析仪的构造原理和基本操作。
3.熟练掌握使用STA449F3同步热分析仪分别测量TG-DTA和TG-DSC曲线4.掌握分析实验数据的步骤,并解释相关现象。
二、实验原理热分析是测量在受控程序温度条件下,物质本身的质量或热量变化与温度的函数关系的一组技术。
目前热分析已经发展成为系统的分析方法,它包括热失重分析TG、差热分析DTA和差动热分析DSC,是材料领域研究工作的重要工具,特别是在高聚合物的分析测定方面应用非常广泛。
它不仅能获得结构方面的信息,而且还能测定多种性能,是材料测试实验室必备的仪器。
热重分析(TG)是指在程序控制升温条件下,测量物质的质量与温度变化的函数关系,或者测定试样在恒定的高温下质量随时间变化的一种分析技术。
热重分析的谱图一般是以质量W对温度T的曲线或者试样的质量变化速度dw/dt对温度T的曲线来表示。
后者称为微分热重曲线(DTG)。
TG主要用来研究样品在空气中或惰性气体中热稳定性和分解过程,除此之外,还可研究固相反应,测定水分挥发物或者吸收、吸附和解吸附过程,气化速率、气化热、升华温度、升华热、氧化降解、增塑剂挥发性、水解和吸湿性、塑料和复合材料的组分等。
差热分析(DTA)是测定试样在受热(或冷却)过程中,由于物理变化或化学变化所产生的热效应来研究物质转化及化学反应的一种分析方法,简称DTA(Differential Thermal Analysis)。
物质发生相变、分解、化合、凝固、脱水、蒸发等过程时都伴有热效应发生,DTA可用于测定物质发生热反应时的特征温度及吸收或放出的热量。
DTA的工作原理为,在进行DTA测试时,所选用的参比物为空坩埚,加热炉以一定的速率升温,若试样没有热反应,则它的温度和参比坩埚温度之间的温差ΔT=0,差热曲线为一条直线,与基线一致;当试样发生了物理或化学变化而吸入或放出热量时,ΔT≠0,在热谱图上会出现吸热或放热峰,形成ΔT随温度变化的差热曲线(热谱图),在习惯上通常以温度差ΔT作纵坐标,吸热峰向下,放热峰向上,温度T作横坐标,自左向右增加。
热量分析实验技术使用教程引言在科学研究和工程技术中,热量的测量和分析是非常重要的。
热量分析实验技术是一种通过实验手段测量、分析和计算物体所包含的热量的方法。
本文将介绍热量分析实验技术的使用方法,帮助读者了解如何正确使用这一实验技术进行热量相关的研究和实践。
一、实验前准备进行热量分析实验时,首先需要准备实验室所需的设备和材料。
主要的设备包括热量计、温度计、电子天平等。
而材料则根据实验需求而定,可以是各种物体、液体或气体。
此外,还需要准备记录实验数据的笔记本和实验报告的撰写材料。
二、实验操作步骤1. 实验器材校准在进行热量实验前,需要确保实验器材的准确性和稳定性。
首先,使用温度计对热量计的温度进行校准,确保其准确反映环境温度。
接下来,使用电子天平对物体的质量进行准确测量,避免实验结果的误差。
2. 测量实验物体的初始温度和质量在实验开始之前,需要测量待测物体的初始温度和质量。
通过温度计可以得知物体的初始温度,而电子天平则可以准确测量物体的质量。
3. 将物体放入热量计中将待测物体放入热量计中,确保物体与热量计的热交换通道畅通。
待测物体的特性和实验需求决定了热量计中的介质选择,可以是水、油或者其他液体。
4. 测量物体的最终温度将热量计放置在恒温水浴中,保持恒定的环境温度。
然后观察待测物体的温度变化,待其达到热平衡状态后,记录下物体的最终温度。
通过计算待测物体的温度变化,可以得到物体吸收或释放的热量。
5. 计算热量根据热量计的性质和待测物体的特性,使用合适的公式计算热量。
例如,对于液体物体,可以使用热量公式Q = mcΔT(其中Q为热量,m为物体质量,c为液体的比热容,ΔT为物体的温度变化)进行计算。
6. 数据分析和结果讨论将实验所得数据进行整理和分析,并进行结果的讨论。
通过比较实验数据和理论值,可以评估实验的准确性和可靠性。
对于实验结果的不确定性,可以使用统计方法进行分析和讨论。
三、实验技巧和注意事项在进行热量分析实验时,需要注意以下几个技巧和事项:1. 控制环境温度的稳定性,避免外界因素对实验结果的干扰。
一、实验目的1.了解热分析法的种类、仪器装置及使用方法。
2.掌握几种热分析法的基本原理、测试技术及影响测量准确性的因素。
3.掌握热分析法在聚合物结晶中的分析原理,并能对实验结果做出解释。
二、方法简介:1. 热重分析法热重分析法( TG )是在程序温度控制下,测量物质的质量随温度变化的一种实验技术。
一般有静态法和动态法两种类型:静态法是在恒温下测定物质质量变化与温度的关系,将试样在各给定温度加热至恒重,该法用来研究固相物质热分解的反应速率和测定反应速度常数。
动态法是在程序升温下测定物质质量变化与温度的关系,采用连续升温连续称重的方式。
由热重分析记录的质量变化对温度的关系曲线称为热重曲线( TG 曲线)。
曲线横坐标为温度,纵坐标为质量,如热分解反应 A(s) → B(s)+ C(g) 的热重曲线如图 1 所示。
图中 T i 为起始温度,即累积质量变化达到热天平可检测的温度;Tf 为终止温度,即累积质量变化达到最大值时的温度;热重曲线上质量基本不变的部分称为基线或平台。
若试样初始质量为 W0 ,失重后试样质量为 W1 ,测失重百分数为2.差示扫描量热法(DSC)DSC的技术方法是按照程序改变温度,使试样与标样之间的温度差为零。
测量两者单位时间的热能输入差。
就是说,使物转移过程中的温度和热量能够加以定量物质在加热过程中会在某温度下发生分解、脱水、氧化、还原和升华等一系列的物理化学变化而出现质量变化,发生质量变化的温度及质量变化百分数随物质的结构和组成而异,因此可以利用物质的热重曲线来研究物质的热变化过程,推测反应机理及产物。
将实验以一定的升温速度加热至熔点以上,恒温一定时间,以充分消除试样的热历史,然后,迅速降温至测试温度进行等温结晶。
由于结晶时放出结晶潜热,所以出现一个放热峰,见图。
基线开始向放热方向偏离时,作为开始结晶的时间(t0),重新回到基线时,作为结晶结束的时间(t=t∞),则t时刻的结晶程度为式中 xt、x∞是结晶时间为t及无限大时非晶态转变为晶态的分数;At、A∞为0~t时间及0~∞时间DSC曲线所包含的面积。
实验二综合热分析实验一.实验目的1.了解热分析技术适用范围与测试对象2.了解综合热分析仪STA 449C的结构和测试原理3.观察热分析仪的操作方法和测试结果分析。
二.实验原理热分析是指在程序温度的控制下测量物质的物理性能与温度关系的一类技术。
在热分析法中,物质在一定温度范围内发生变化,包括与周围环境作用而经历的物理变化和化学变化,如释放出结晶水和挥发性物质的碎片、热量的吸收或释放,某些变化还涉及到物质的质量增加或质量损失,发生热化学变化和热物理性质及电学性质变化等。
热分析法的核心就是研究物质在受热或冷却时产生的物理和化学的变迁速率和温度以及所涉及的能量和质量变化。
总之,热分析技术是建立在物质热行为上的一类分析方法。
就固体物质而言受热后物理性质将发生变化。
如导热系数、热膨胀系数、热辐射性质、热容等都会发生变化。
当金属材料从一个相转变为另一个相的过程中会吸收或放出热量,如固态相变潜热、固液熔融相变潜热,发生相变所对应的温度称为临界点。
热分析方法就是测出发生相变的临界点温度。
对于金属合金材料,可以通过测出一系列不同成份配比的合金的临界点,并将同一物性的点连起来而得到合金的相图,这也是测定相图的最常用的方法。
常用的热分析方法有三种:差热分析法(DTA)、差示扫描量热分析法(DSC)和热重分析法(TG)。
1.差热分析法(DTA)差热分析是在温度程序的控制下,测量物质的温度与参比物的温度差和温度关系的一种技术。
其原理是:在相同的加热条件下对试样加热或冷却,若试样中不发生任何热效应,试样的温度和参比物的温度相等,两者温差为零。
若试样发生吸热效应,试样的温度将滞后于参比物的温度,此时两者的温差不为零,并在DTA曲线上出现一个吸热峰;若试样发生放热效应,试样的温度将超前于参比物的温度,此时两者的温差也不为零,并在DTA曲线上出现一个放热峰。
根据记录的曲线,就可以测出反应开始的起始温度,反应峰所对应的温度(峰位置),峰的面积就和产生的热效应值对应。