2020中考复习 化学基础知识演练——专题五十八:溶液
- 格式:doc
- 大小:187.00 KB
- 文档页数:10

2020中考化学临考抢分专题:溶液(含答案)一、选择题(本大题共12道小题)1.下列物质不属于溶液的是()A.生理盐水B.白醋C.医用酒精D.冰水混合物2.下列有关溶液的叙述错误的是()A.长期放置后不会分层的液体一定是溶液B.衣服上的油污用汽油或用加了洗涤剂的水可除去C.一瓶合格的生理盐水密封一段时间,不会出现浑浊D.实验室常将固体药品配制成溶液进行化学反应,以提高反应速率3.下列物质溶解或稀释过程中,溶液温度没有明显改变的是()A.NaOHB.NH4NO3C.浓硫酸D.NaCl4. 氢氧化钙的溶解度随温度的升高而减小。
要把一瓶接近饱和的石灰水变饱和,具体措施有:①加入氢氧化钙;②升高温度;③降低温度;④加入水;⑤蒸发水。
其中措施正确的是()A.①②④B.①③④C.①③⑤D.①②⑤5. 20 ℃时,把36 g氯化钠放入64 g水中,使其充分溶解(20 ℃时氯化钠的溶解度为36 g)。
对所得溶液的有关说法错误的是()A.该溶液是饱和溶液B.溶液中Na+和Cl-个数一定相等C.溶液质量为100 gD.溶质与溶剂质量比为9∶256. 按下列方法配制的溶液,其溶质质量分数为5%的是()A.称取5.0 g氯化钾,溶解在95 mL水中,充分搅拌B.称取5.0 g生石灰,放入95 mL水中,充分搅拌C.量取5.0 mL浓盐酸,倒入95 mL水中,充分搅拌D.称取5.0 g二氧化锰,放入95 mL水中,充分搅拌7. 20 ℃时氯化钾的溶解度为34 g。
下列是四位同学在20 ℃时配制的氯化钾溶液,其中一定达到饱和的是()8. KCl和KNO3的溶解度曲线如图所示。
下列说法正确的是()A.10 ℃时,KNO3的溶解度比KCl的大B.KNO3的溶解度受温度的影响比KCl的大C.随着温度的升高,KCl的溶解度逐渐减小D.40 ℃时KNO3的饱和溶液,升温至60 ℃时仍是饱和溶液(忽略水分挥发)9.在t1℃时,将等质量的硝酸钾和氯化钾分别加入到各盛有100 g水的两个烧杯中,充分搅拌后现象如图甲所示,硝酸钾和氯化钾的溶解度曲线如图乙所示。

2020中考化学(人教)溶液复习练习附答案复习:溶液一、选择题1、下列有关溶液的叙述正确的是()A.稀溶液一定是不饱和溶液B.饱和溶液就是不能再溶解如何物质的溶液C.溶质的溶解度都随温度的升高而增大D.溶质在溶解的过程中,有的放出热量,有的吸收热量【参考答案】D2、下列物质中不能与水形成溶液的是()A. 白糖B. 食盐C. 氢氧化钠D. 植物油【参考答案】D3、关于饱和溶液和不饱和溶液的说法中正确的是()A.饱和溶液一定是浓溶液B.不饱和溶液一定是稀溶液C.饱和溶液一定比不饱和溶液浓D.在相同温度下,同种溶质的饱和溶液一定比不饱和溶液浓一些【参考答案】D【解析】A项,饱和溶液不一定是浓溶液,错误;B项,不饱和溶液不一定是稀溶液,错误;C项,饱和溶液不一定比不饱和溶液浓,错误;D项,在相同温度下,同种溶质的饱和溶液一定比不饱和溶液浓一些,正确。
故选D。
4、在《基础实验5:配制一定溶质质量分数的氯化钠溶液》和《基础实验6:粗盐的初步提纯》两个实验中都应使用到的仪器是()A.烧杯、玻璃棒、托盘天平、量筒B.烧杯、玻璃棒、量筒、试管C.托盘天平、量筒、烧杯、漏斗D.蒸发皿、酒精灯、烧杯、铁架台【答案】A5、已知硫酸的浓度越大,密度越大,现将等体积质量分数为90%和10%的硫酸溶液混合,所得溶液的溶质质量分数为()A.>50% B.=50% C.<50% D.不能确定【参考答案】A6、下列关于溶液的说法中,正确的是()A. 溶液一定是无色透明的B. 均一、稳定的液体一定是溶液C. 饱和的氢氧化钠溶液中不能再溶解任何物质D. 相同温度下,同种溶质在同种溶剂里的饱和溶液一定比不饱和溶液浓【参考答案】D7、甲、乙两种固体物质的溶解度曲线如图所示,下列说法正确的是()A.甲物质的溶解度大于乙物质的溶解度B.两种物质的溶解度都随着温度的升高而增大C.t1℃时,60 g甲加入到100 g水中,充分溶解,得到160 g 溶液D.甲、乙的饱和溶液从t2℃降温到t1℃,析出晶体的质量:甲一定小于乙【参考答案】B【解析】A项,在比较物质的溶解度时,需要指明温度,错误;B项,通过分析溶解度曲线可知,两种物质的溶解度都随着温度的升高而增大,正确;C项,t1℃时,甲物质的溶解度是30 g,60 g甲加入到100 g水中,充分溶解,得到130 g溶液,错误;D项,甲、乙的饱和溶液的质量不能确定,所以从t2℃降温到t1℃,析出晶体的质量不确定,错误。

2020中考人教化学第一轮复习:溶液及答案*专题:溶液*1、推理是学习化学的一种方法,以下推理正确的是A.氧气由氧元素组成,所以制取氧气的反应物一定含有氧元素B.质子数决定元素种类,所以质子数相同的粒子一定属于同种元素C.溶液是均一稳定的,所以均一稳定的物质一定是溶液D.催化剂可以加快化学反应速率,所以任何化学反应都需要催化剂【答案】A2、推理是研究和学习化学的重要方法。
以下说法正确的是()A.甲烷和乙醇的燃烧产物都是二氧化碳和水,则甲烷和乙醇都是由碳、氢两种元素组成的碳氢化合物B.洗涤剂除去衣服上的油污是利用了乳化作用,则汽油除去衣服上的油污也是利用了乳化作用C.二氧化碳使饱和石灰水变浑浊是化学变化,则升温使饱和石灰水变浑浊也是化学变化D.元素的种类是由质子数决定的,则质子数相同的原子属于同种元素【答案】D3、下列判断正确的是()A.合金至少有两种金属熔合而成B.不同种元素最本质的区别是质子数不同C.饱和溶液变为不饱和溶液,其溶质质量分数一定变小D.两种化合物相互作用生成另外两种化合物的反应一定是复分解反应【答案】B4、20℃时,取四份一定质量的饱和硝酸钾溶液分别进行如下实验后,所得结论正确的是()A. 保持温度不变,减少10g溶剂后,溶液中溶质的质量分数增大B. 保持温度不变,加入10g溶质后,溶液中溶质的质量分数增大C. 保持温度不变,减少10g溶剂后,溶质的溶解度减小D. 降低至10℃后,溶质的溶解度减小【答案】D5、实验室配制100g 10%的氯化钠溶液,有关实验操作不正确的是( ) A.用托盘天平称取10.0g氯化钠B.用量筒量取90.0mL的水C.将称取的氯化钠倒入量筒中溶解D.将配制的溶液装入试剂瓶中,贴上标签【答案】C6、下列物质放入水中,能形成溶液的是()A. 牛奶B. 面粉C. 蔗糖D. 花生油【答案】C7、如图是甲、乙两种物质的溶解度曲线,下列说法不正确的是()A.t1℃时,甲、乙两种物质的溶解度相等B.甲物质的溶解度随温度的升高而增大C.将t2℃时甲、乙两种物质的饱和溶液降温到t1℃,溶液仍然饱和D.t1℃时,将50g甲物质加入100g水中,充分搅拌,能得到甲物质的饱和溶液【答案】C8、下列实验符合如图所示变化趋势的是( )序号实验横坐标纵坐标A 向一定量氢氧化钠溶液中滴加稀硫酸稀硫酸的质量水的质量B 加热一定量高锰酸钾固体加热时间剩余固体中氧元素的质量C 向一定量饱和硝酸钾溶液中加水加水的质量溶质的质量分数D 向一定量锌粒中加入稀盐酸稀盐酸的质量锌粒的质量A.AB.BC.CD.D【答案】D9、配制100g 6%的NaCl溶液,不需要的仪器是( )【答案】A10、下列常见的医用溶液中,溶剂不是水的是()A. 葡萄糖注射液B. 生理盐水C. 75%消毒酒精D. 碘酒【答案】D11、许多化学反应都是在溶液中进行的,关于溶液理解正确的是()A.通过加热蒸发的方法提高75%酒精的浓度B.将氧化钙溶于水,可以形成氧化钙溶液C. 5gCuSO4▪5H2O溶于95g水中配制CuSO4溶液,此溶液溶质的质量分数小于5%D.将50℃下的饱和KNO3溶液冷却至室温,硝酸钾固体析出,过滤后可得纯水和硝酸钾固体【答案】C12、甲、乙两种物质的溶解度曲线如右图所示。

《溶液》专题检测一、单选题1.对“溶质的质量分数为20%的NaCl溶液”的含义,解释正确的是A.在该溶液中,溶质和溶剂的质量比为1:5 B.100克水中含有20克NaClC.在该溶液中,溶质与溶液的质量比为1:6 D.50克该溶液中含有NaCl为10克2.下列对事实的解释正确的是A.A B.B C.C D.D3.下列说法正确的是A.原子通过得失电子形成离子,离子一定不能形成原子B.不饱和溶液转化为饱和溶液,溶质的质量分数一定增大C.中和反应生成盐和水,有盐和水生成的反应一定是中和反应D.某溶液中滴入无色酚酞试液后变红,该溶液一定是碱性溶液4.下列实验数据合理的是()A.用10 ml量筒量了6.53 ml水 B.20g食盐溶于100g水,溶质质量分数为20% C.用托盘天平称得纯碱的质量为10.57g D.用pH试纸测得某地雨水的pH为5 5.甲、乙、丙三种固体的溶解度曲线如图所示,下列说法正确的是A.三种物质的溶解度:甲>乙>丙℃时,溶质的质量分数:甲=乙B.t1℃时,乙、丙的饱和溶液降温均有溶质析出C.t2D.甲中混有少量乙时,可通过溶解、加热浓缩、冷却结晶的方法提纯6.右图是甲、乙、丙三种物质的溶解度曲线.下列说法正确的是℃时,三种物质的溶解度由大到水的顺序是甲>乙>丙A.在t1B.在t℃时,甲、乙两物质的溶解度相等2C.甲、乙、丙三种物质的饱和溶液升温都会转化为不饱和溶液D.当乙的饱和溶液中混有少量丙时,可采用降温结晶的方法析出丙7.下列四个图象,分别对应四种操作过程,其中正确的是()A.①某温度下,向一定质量的饱和氯化钠溶液中加入氯化钠固体B.②浓盐酸敞口放置C.③室温下向一定体积的NaOH溶液中加入稀盐酸D.④向HCl和CuCl混合液中滴加KOH溶液28.现有20℃的KNO3饱和溶液100克,要改变此溶液的溶质质量分数,可采用的方法是在温度不变的情况下()A.蒸发掉l0克水B.加5克KNO3晶体C.倒出5克溶液D.加10克水9.下列4个图像能正确反映对应变化关系的是()A.A B.B C.C D.D10.下列变化吸收热量的是()A.硝酸铵溶于水B.食盐溶于水C.硫在空气中燃烧D.动物的新陈代谢11.下列实验方法错误的是()A.用稀硝酸除去NaCl中混有的Na2CO3B.用带火星的木条区别空气和O2C.用水区分NH4NO3和固体NaOH 两种固体 D.用湿润的石蕊试纸区别CO和CO212.“结构决定性质,性质决定用途”是学习化学的重要思想方法,下列说法不正确的是( ) A.洗涤剂具有乳化作用,所以可去除油污B.金刚石和石墨原子构成不同,所以物理性质差异很大C.焊锡的熔点比其组分金属低,所以可用于焊接金属D.一氧化碳和二氧化碳分子构成不同,所以化学性质不同13.色拉油、食盐、酱油、醋等都是我们家庭的常见的调味品。

溶液考点一:溶解度1.下图为硫酸钠和氯化钠的溶解度曲线。
下列说法正确的是( )A.温度升高,两种物质的溶解度都增大B.50 ℃的Na2SO4饱和溶液降到40 ℃时有晶体析出C.40 ℃时,75 g饱和Na2SO4溶液中含25 g Na2SO4D.可用降温结晶的方法提纯含少量Na2SO4的NaCl2.能证实20 ℃时原KNO3的溶液是饱和溶液的事实是( )A.降温到10 ℃时有KNO3晶体析出B.蒸发掉10克水,有KNO3晶体析出C.加热到30 ℃后,再加入KNO3晶体仍能继续溶解D.在20 ℃时,向上述KNO3溶液中加入少量KNO3晶体,溶液的质量不变。
3.下图是甲、乙、丙三种物质的溶解度曲线。
下列说法不正确的是( )A.t2℃时,三种物质的溶解度大小依次为甲>乙>丙B.若乙中含有少量杂质甲,可用蒸发结晶的方法进行提纯C.等质量的甲、乙两种溶液,由t2℃降到t1℃时,析出甲的质量多D.三种不饱和溶液都可以通过增加其溶质的方法变成饱和溶液4.如图是三种固体物质的溶解度曲线,下列说法正确的是( )A.物质c的溶解度随温度的升高而增大B.物质a的溶解度大于物质c的溶解度C.t2℃时,60 g物质a与100 g水充分混合后所得溶液的总质量为160 gD.将t1℃b、c两种物质的饱和溶液升温至t2℃,溶液中溶质质量分数不变的是b溶液5.甲、乙两物质的溶解度曲线如图所示,下列说法不正确的是( )A.t1℃时,甲和乙的溶解度相等B.甲和乙的溶解度都随温度的升高而增大C.t1℃时,甲和乙各30 g分别加入90 g水中,均能完全溶解D.t2℃时,在100 g水中放入60 g甲,形成饱和溶液6.水和以水为溶剂制成的溶液与人们的生活有着密切的关系。
(1)市售的一种罐装饮料,在饮料罐的夹层中分别装入一种固体物质和水,饮用前摇动饮料罐使它们混合,饮料温度就会降低,这种固体物质可能是________(填字母)。
A.烧碱B.食盐C.硝酸铵D.生石灰(2)如图是常见固体物质的溶解度曲线,根据图示回答:①对A物质来说,a点的意义是________________________________________________。
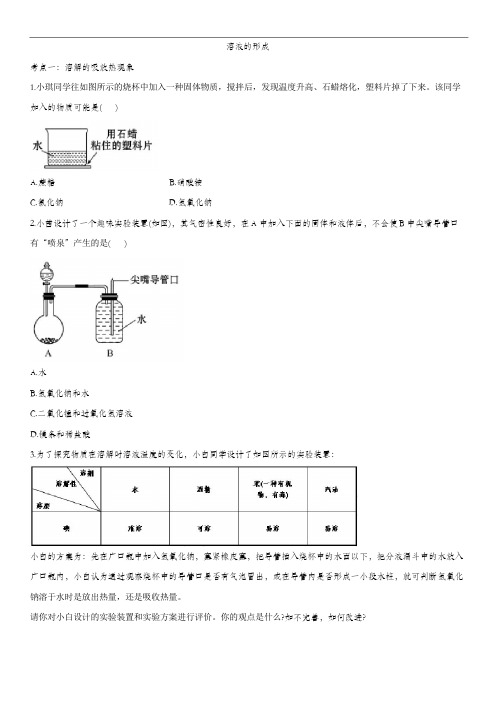
溶液的形成考点一:溶解的吸放热现象1.小琪同学往如图所示的烧杯中加入一种固体物质,搅拌后,发现温度升高、石蜡熔化,塑料片掉了下来。
该同学加入的物质可能是()A.蔗糖B.硝酸铵C.氯化钠D.氢氧化钠2.小茜设计了一个趣味实验装置(如图),其气密性良好,在A中加入下面的固体和液体后,不会使B中尖嘴导管口有“喷泉”产生的是()A.水B.氢氧化钠和水C.二氧化锰和过氧化氢溶液D.镁条和稀盐酸3.为了探究物质在溶解时溶液温度的变化,小白同学设计了如图所示的实验装置:小白的方案为:先在广口瓶中加入氢氧化钠,塞紧橡皮塞,把导管插入烧杯中的水面以下,把分液漏斗中的水放入广口瓶内,小白认为通过观察烧杯中的导管口是否有气泡冒出,或在导管内是否形成一小段水柱,就可判断氢氧化钠溶于水时是放出热量,还是吸收热量。
请你对小白设计的实验装置和实验方案进行评价。
你的观点是什么?如不完善,如何改进?4.用如图所示装置研究“活性炭吸附能力与温度变化的关系”。
将NH NO固体加入到水中搅拌,观察到两侧玻璃管43中液面上升的高度不同。
(1)由于试管内气体的压强_____________(选填“增大”或“减小”),使得玻璃管内液面上升。
(2)NH NO固体溶于水_____________(选填“放出”或“吸收”)热量。
43(3)活性炭吸附气体的能力随温度_____________而增强。
考点二:溶液的组成1.下列有关溶液的说法中正确的是()A.溶液都是无色、澄清、透明的B.固体物质的水溶液下层比上层密度大C.一种溶液中各部分的浓度和性质都是一样的D.静置后有沉淀析出的混合物一定是溶液2.铁和足量稀硫酸充分反应后,所得溶液中的溶质是()A.只有硫酸亚铁B.只有铁C.只有硫酸铁D.有硫酸亚铁和硫酸3.下列物质中,含有自由移动离子的是()A.氯化钠溶液B.氯化钠晶体C.蔗糖D.铜4.关于溶液有如下说法:①溶质只能是固体;②溶剂一定是水;③一种溶液中只含一种溶质;④溶质一定是以离子的形式存在于溶剂中。
溶液考点一:饱和溶液与不饱和溶液1.30 ℃时将等质量的两份饱和石灰水,一份冷却到20 ℃,另一份加入少量生石灰,温度仍保持在30 ℃,则两种情况下均不改变的是( )A.溶剂的质量B.溶质的质量C.溶质的溶解度D.溶液中溶质的质量分数2.一杯70 ℃的硝酸钾饱和溶液,冷却后有晶体析出(晶体不含结晶水),若不考虑溶剂的蒸发,则剩余溶液与原溶液相比( )A.由饱和溶液变为不饱和溶液B.溶质质量不变C.溶液质量不变D.溶质的质量分数减小3.对于大多数固体溶质的不饱和溶液,要使之变为饱和溶液,可采取的方法有:①降低温度;②升高温度;③加入含相同溶质的浓溶液;④加入该固体溶质;⑤增大压强。
其中正确的方法有( )A.①②③B.②③④C.③④⑤D.①④4.如图所示,一物体悬挂在饱和氯化钠溶液中,在恒温条件下向烧杯内溶液中分别加入下列物质(悬挂物不参与反应)。
说明弹簧秤读数变化情况(填“变大”“不变”或“变小”)。
(1)如果加入氯化钠晶体,弹簧秤读数____。
(2)如果加入蒸馏水,弹簧秤读数____。
(3)如果加入KNO3晶体,弹簧秤读数____。
5.如表是NaCl、KNO3的部分溶解度,请回答下列问题:温度/℃10 20 30 40 50 60 NaCl的溶解度/g 35.8 36.0 36.63 36.6 37.0 37.3KNO3的溶解度/g 20.9 31.6 45.8 63.6 85.5 110.0(1)NaCl、KNO3的溶解度受温度变化影响大的是____。
(2)20 ℃时,氯化钠的溶解度为____,取20 g氯化钠放入50 g水里,充分搅拌,可得到溶液____g。
(3)如图所示进行操作(每步均充分溶解),可得到饱和溶液的有____(填字母),溶质质量分数最大的是____(填字母)。
考点二:溶液的形成1.指出下列溶液中的溶质和溶剂。
(1)澄清石灰水中,溶质是____,溶剂是____。
(2)医用酒精溶液中,溶质是____,溶剂是____。
2020中考化学章节强化训练——溶液考点一:溶液的形成1.向下列物质中分别加入适量的水,充分搅拌,不能得到溶液的是A.豆油B.硝酸钙C.蔗糖D.酒精2.下列物质放入水中,能形成溶液的是()A.泥沙B.食盐C.植物油D.粉笔灰3.下列说法正确的是()A.溶质都是固体B.乳化能增强乳浊液的稳定性C.均一、稳定的液体都是溶液D.搅拌可增大物质的溶解度4.下列说法正确的是A.植物油与水混合一定形成溶液B.将100g10%的氯化钠溶液倒掉一半,剩余溶液的质量分数变为5%C.饱和溶液一定是浓溶液D.生活中利用洗涤剂清洗油污属于乳化现象5.下列说法正确的是()A.洗涤剂去油污属于乳化现象B.硝酸铵固体溶于水会出现放热现象C.化学反应前后催化剂质量发生变化D.自来水经过活性炭吸附可得到蒸馏水6.把少量的下列物质分别放入水中,充分搅拌,能形成溶液的是A.面粉B.蔗糖C.花生油D.泥土7.把少量下列物质分别放入水中,充分搅拌,不能得到溶液的是()A.纯碱B.蔗糖C.酒精D.面粉8.下列说法正确的是A.气体的溶解度随压强增大而减小B.洗洁精能使餐具上的油污乳化C.降低饱和溶液的温度,一定有晶体析出D.配制好的6%的NaCl溶液,装入试剂瓶中时不慎撒漏一部分,浓度减小考点二:溶解度1.下列有关溶液的说法中,正确的是A.溶液由溶质和溶剂组成,溶质必须是固体,溶剂必须是液体B.饱和溶液一定是浓溶液,不饱和溶液一定是稀溶液C.通过振荡、搅拌等方法可以增大固体物质在水中的溶解度D.要从溶液中获得晶体,可以采用蒸发溶剂或冷却热饱和溶液的方法2.海水淡化可采用膜分离技术,如图所示,对淡化膜右侧的海水加压,水分子可以通过淡化膜进入左侧淡水池,而海水中的各种离子不能通过淡化膜,从而得到淡水。
下列对加压后右侧海水成分变化的分析中,正确的是A.溶剂质量减少B.溶质质量增加C.溶液质量不变D.溶质的质量分数不变3.欲使一瓶接近饱和的氢氧化钙溶液变为饱和溶液,不能达到目的的方法是A.向其中加入氧化钙B.通入二氧化碳C.恒温蒸发水分D.升高温度4.如图所示,将液体X加入集气瓶中与固体Y作用,观察到气球逐渐变大,下表中液体X和固体Y的组合,符合题意的是A.①②⑤B.①③④C.①②④D.②③⑤5.KCl是一种常用的钾肥,其溶解度如下表所示。
2020中考人教化学:溶液编题含答案*专题:溶液*1、甲、乙两种物质的溶解度曲线如图所示.下列说法不正确的是()A.t2℃时,甲的溶解度大于乙的溶解度B.t2℃时,将30g甲物质加入50g水中充分溶解后得到75g饱和溶液C.t1℃时,甲、乙两种饱和溶液的溶质质量分数相等D.t2℃时甲、乙的饱和溶液降温到t1℃时,析出晶体的质量甲一定大于乙【答案】D【解析】A、根据溶解度曲线,t2℃时,甲的溶解度大于乙的溶解度,正确;B、t2℃时,甲的溶解度是50g,t2℃时,100g的水中最多溶解50g的甲,将30g甲放入50g水中,只能够溶解25g,得到溶液的质量为75g,正确;C、一定温度下饱和溶液的溶质质量分数=×100%。
t1℃时,甲、乙两种物质的溶解度相等,饱和溶液的溶质质量分数相等,正确;D、t2℃时,甲、乙饱和溶液的质量不能确定,降低温度后,析出晶体的质量也不能确定,错误。
2、下列物质中,属于溶液的是()A. 牛奶B. 糖水C. 蒸馏水D. 果酱【答案】B3、实验操作后的溶液一定是不饱和溶液的是()A. B. C. D.【答案】C4、一定温度下,将少量氧化钙固体加入到一定量的饱和石灰水中,甲、乙、丙三位同学分别作出图象甲、乙和丙,则其中图象丙中反映的情况是()A. 溶质的质量与时间的关系B. 溶剂的质量与时间的关系C. 溶质的溶解度与时间的关系D. 溶质的质量分数与时间的关系【答案】A5、实验操作错误的是()A.酒精灯失火用湿抹布扑盖B.将倒入量筒中配制溶液C.分离溶液中析出的晶体D.检查气密性【答案】B【详解】A、酒精灯失火要用湿抹布盖灭,选项正确;B、量筒是用来量取液体体积的,不能用来配制溶液,选项错误;C、分离固液混合物可采用过滤操作,选项正确;D、检查装置气密性可用手握住试管底部,观察有气泡冒出气密性良好,选项正确。
6、下列物质中不能与水形成溶液的是()A. 白糖B. 食盐C. 氢氧化钠D. 植物油【答案】D7、一定温度下,向饱和澄清石灰水中加入少量氧化钙,充分反应后恢复到原来的温度,反应后的溶液与原饱和澄清石灰水相比,下列说法正确的是( )A. 溶质的质量不变B. 溶质的质量减少C. 溶质的质量分数变大D. 溶质的质量分数减小【答案】B8、如图是NaCl、MgSO4的溶解度曲线。
2020中考人教版化学:溶液附答案*溶液*1、在工农业生产中,许多化学反应都在溶液中进行的主要原因是( )A.便于观察现象B.溶液间的反应不需要加热C.水是反应的催化剂D.溶液中分子或离子接触充分,反应速率快【答案】D。
2、把少量下列物质分别放入水中,充分搅拌,可以得到溶液的是()A.沙子B.食盐C.面粉D.橄榄油【【答案】】B3、下面关于饱和溶液的说法中,正确的是( )A.含有溶质很多的溶液B.还能继续溶解某种溶质的溶液C.不能继续溶解某种溶质的溶液D.在一定温度下,一定量的溶剂中,不能再溶解某种溶质的溶液【答案】D。
4、t℃时,向硝酸钠饱和溶液中加入一定量的水后,下列有关该溶液的叙述正确的是()A.仍为饱和溶液B.溶质的质量变小C.溶质的溶解度不变D.溶质的质量分数不变【答案】C5、为达到预期的目的,下列操作中不正确的是A.按溶解、过滤、蒸发的操作顺序可以分离CaCO3、CaCl2的混合物B.用磷在密闭容器中燃烧,除去密闭容器内空气中的氧气C.生活中为了降低水的硬度往往采用加热煮沸的方法D.某同学将pH试纸润湿后,用玻璃棒蘸取食用白醋滴在试纸上,测定其pH 【答案】D6、下列选项属于溶液的是()A.泥水B.白糖水C.玉米粥D.蒸馏水【答案】B7、室温时,有两瓶硝酸钾溶液,已知一瓶为饱和溶液,另一瓶为不饱和溶液,分别取样(如图),则一定无法区分这两种溶液的实验操作是( )A.加一定量的水B.加入少量该晶体C.略降低温度D.恒温蒸发少量水【答案】A。
8、某同学要配制50g质量分数为14%的氯化钠溶液,下列关于配制该溶液的说法不正确的是()①若用氯化钠固体配制,需称取氯化钠固体7.0g②选用200ml量筒量取所需水的体积③实验中用到的玻璃仪器有烧杯、量筒、玻璃棒和胶头滴管④用量筒量取水时,俯视读数,配得溶液的溶质质量分数偏小A.①③B.②④C.①②D.②【答案】B9、配制100 g 10%的氯化钠溶液,下列仪器选用不当的是( )A.10 mL量筒 B.电子天平 C.玻璃棒 D.烧杯【答案】A10、下列有关溶液的叙述错误..的是()A.长期放置后不会分层的液体一定是溶液B.衣服上的油污用汽油或用加了洗涤剂的水可除去C.一瓶合格的生理盐水密封一段时间,不会出现浑浊D.实验室常将固体药品配制成溶液进行化学反应,以提高反应速率【答案】A11、下列有关溶液的说法中,错误的是( )A.外界条件不改变,溶质不会从溶液中分离出来B.物质的溶解过程通常会伴随着能量的变化C.溶液中的溶质以分子或离子的形式均匀分散在溶剂中保持静止不动,所以溶液具有均一性和稳定性D.改变条件,能够使饱和溶液与不饱和溶液相互转化【答案】C。
1 2020中考复习 化学基础知识演练——专题五十八:溶液 考点一:溶液的形成 1.化学知识中有很多的“相等”。请你判断下列说法中不正确的是( ) A.溶液稀释前后,溶质的质量相等 B.在中性原子中,质子数等于核外电子数 C.50mL的水和50mL的酒精混合,所得溶液的体积等于100mL D.50g水和50g酒精混合,所得溶液的质量等于100g 2.下列物质分别加入适量水中,充分搅拌,能够得到溶液的是( ) A.蔗糖 B.花生油 C.面粉 D.冰块 3.下列说法错误的是( ) A.洗涤剂具有乳化功能,能洗去餐具上的油污 B.武德合金熔点低,可以作保险丝 C.二氧化锰可以作任何反应的催化剂 D.空气中体积分数最大的气体是氮气 4.下列物质溶于水的过程中,溶液温度会明显降低的是( ) A.氯化钠 B.硝酸铵 C.浓硫酸 D.氢氧化钠 5.洗洁精是家庭必备的清洁用品,可迅速分解油腻、去污、除菌, 有 味道淡雅、洁净温和、泡沫柔细、低残留的优点。洗洁精的有效成分是表面 活性剂,还含有泡沫剂、香精、水、色素等多种成分。请回答:
(1)洗洁精去除油污的有效成分是 ; (2)洗洁精去除油污的原理是 。 考点二:饱和溶液与不饱和溶液 1.从海水中提取食盐的流程如下,下列说法错误的是( )
A.经过第①步操作,海水中的成分基本不变 2
B.蒸发池中,氯化钠溶液逐渐变浓 C.经过第③步的操作,进入结晶池后,继续蒸发水,有④发生 D.析出食盐晶体后的母液是氯化钠的不饱和溶液 2.对“20℃时,硝酸钾溶解度为31.6g”这句话解释正确的是( ) A.20℃时,100g硝酸钾溶液中含有31.6g硝酸钾 B.在100g水中溶解31.6g硝酸钾就达到饱和状态 C.20℃时,100g水中最多能溶解31.6g硝酸钾 D.20℃时,溶解31.6g硝酸钾最多需要100g水 3.2017年《科学报告》一篇文章称,只需在普通口罩上添加氯化钠涂层,就能将其转化为“特效口罩”。口罩使用过程中,涂层中的氯化钠会溶解于病毒自身携带的水中,形成溶液,杀死病毒;杀死病毒后,水分蒸发,一段时间后,氯化钠再次析出。 (1)钠原子转化为钠离子,其核外电子数 (填“变大”或“变小”),常温下,氯化钠的饱和溶液中,氯化钠与水的质量比为 (已知:常温下,氯化钠的溶解度为36 g)。 (2)构成氯化钠的阳离子符号为 ,口罩使用过程中,氯化钠溶液中溶质质量分数一直保持不变,此判断 。(填“正确”或“错误”)。 4.小王同学用某固体物质进行了如图所示的实验(实验中水的损失忽略不计,操作M过程中未发生化学变化且温度没有变化),请回答下列问题:
(1)在10℃~40℃时,该物质的溶解度随温度的升高而(填“増大”或“减小”)。 (2)实验所得的溶液中肯定不饱和的有 (填溶液编号) (3)实验所得的溶液中溶质质量分数相同的有 和 、 和(均填溶液编号)。 (4)溶液c到溶液d的转化过程中,最多可能析出晶体(不带结晶水) g。 (5)操作M的名称是 。 考点三:溶解度曲线 1.甲、乙两种物质(不含结晶水)的溶解度曲线如图所示,下列叙述正确的是( ) 3
A.甲和乙的溶解度相等且均为30g B.甲物质的溶解度随温度的升高而减小 C.a1℃时,乙的饱和溶液中溶质与溶剂的质量比为3:7 D.将a2℃150g甲的饱和溶液降温到t1℃,有20g固体析出 2.如图是甲,乙、丙三种固体物质的溶解度曲线,据图回答下列问题:
(1)P点的含义是 。 (2)t2℃时,把50g甲中加入到200g水中充分搅拌,静置,形成的是 溶液(填“饱和”或“不饱和”)。 (3)稍微加热丙的饱和溶液即出现浑浊现象,其原因是 。 (4)除去甲中混有的少量乙,步骤是:加水溶解、加热浓缩、 、 过滤、洗涤、干燥。 (5)将t2℃时等质量的甲、乙两物质的饱和溶液分别降温至t1℃,对所得溶液的叙述正确的是 (填字母序号) A.溶剂质量:甲>乙 B.析出晶体质量:甲>乙 C.溶质质量分数:甲<乙 考点四:溶质的质量分数 1.向200g40%的氢氧化钠溶液中加入200g水,稀释后溶液中溶质的质量分数是( ) A.10% B.20% C.40% D.5% 2.高氯酸钾(KClO4)可用作火箭推进剂,其溶解度如下表。下列说法不正确的是( ) 4
A.高氯酸钾的溶解度随温度降低而减小 B.80℃的高氯酸钾饱和溶液冷却至40℃一定有晶体析出 C.60℃时,高氯酸钾饱和溶液中溶质的质量分数小于7.3% D.20℃时,向2g高氯酸钾中加入98g水,所得溶液的溶质质量分数为2% 3.实验室配制100g溶质质量分数为8%的氯化钠溶液,下列说法中错误的是( ) A.若在量取水时俯视凹液面的最低处,则配制溶液的质量分数小于8% B.溶解过程中玻璃棒搅拌的作用是加快氯化钠的溶解速率 C.实验的步骤为计算、称量、量取、溶解、装瓶贴标签 D.量取水时,用规格为l00mL的量筒 4.某同学配制50 g 9%的氯化钠溶液,整个操作过程如图所示,回答下列问题:
(1)配制溶液的正确操作顺序为 (填序号),其中操作错误的是 (填序号)。 (2)图②中盛放氯化钠固体的仪器名称是 ,需称取氯化钠 g。 (3)量水时选用的量筒的量程最合适的是 (填字母),读数时视线要与量筒内 保持水平。 A.10mL B.25mL C.50mL D.100mL 5.2017年4月17日,张掖市畜牧局发布消息称,张掖市检出H7N9病毒,但人畜均未感染。已知:帕拉米韦氯化钠注射液是治疗H7N9亚型禽流感的有效药物之一,帕拉米韦的化学式为C15H28N4O4。试计算: (1)帕拉米韦中H、O元素质量比为 ; (2)328 g的帕拉米韦中氧元素的质量为 g; 把125 g10%的帕拉米韦氯化钠注射液稀释成5%的稀溶液需要加水 g。 5
2020中考复习 化学基础知识演练——专题五十八:溶液参考答案 考点一:溶液的形成 1.化学知识中有很多的“相等”。请你判断下列说法中不正确的是( ) A.溶液稀释前后,溶质的质量相等 B.在中性原子中,质子数等于核外电子数 C.50mL的水和50mL的酒精混合,所得溶液的体积等于100mL D.50g水和50g酒精混合,所得溶液的质量等于100g 【答案】C 2.下列物质分别加入适量水中,充分搅拌,能够得到溶液的是( ) A.蔗糖 B.花生油 C.面粉 D.冰块 【答案】A 3.下列说法错误的是( ) A.洗涤剂具有乳化功能,能洗去餐具上的油污 B.武德合金熔点低,可以作保险丝 C.二氧化锰可以作任何反应的催化剂 D.空气中体积分数最大的气体是氮气 【答案】C 4.下列物质溶于水的过程中,溶液温度会明显降低的是( ) A.氯化钠 B.硝酸铵 C.浓硫酸 D.氢氧化钠 【答案】B 5.洗洁精是家庭必备的清洁用品,可迅速分解油腻、去污、除菌, 有 味道淡雅、洁净温和、泡沫柔细、低残留的优点。洗洁精的有效成分是表面 活性剂,还含有泡沫剂、香精、水、色素等多种成分。请回答:
(1)洗洁精去除油污的有效成分是 ; (2)洗洁精去除油污的原理是 。 【答案】(1)表面活性剂 (2)洗洁精有乳化功能,能把油污分解成细小的小液滴,能随水流走,起到去油污的作用 6
考点二:饱和溶液与不饱和溶液 1.从海水中提取食盐的流程如下,下列说法错误的是( )
A.经过第①步操作,海水中的成分基本不变 B.蒸发池中,氯化钠溶液逐渐变浓 C.经过第③步的操作,进入结晶池后,继续蒸发水,有④发生 D.析出食盐晶体后的母液是氯化钠的不饱和溶液 【答案】D 2.对“20℃时,硝酸钾溶解度为31.6g”这句话解释正确的是( ) A.20℃时,100g硝酸钾溶液中含有31.6g硝酸钾 B.在100g水中溶解31.6g硝酸钾就达到饱和状态 C.20℃时,100g水中最多能溶解31.6g硝酸钾 D.20℃时,溶解31.6g硝酸钾最多需要100g水 【答案】C 3.2017年《科学报告》一篇文章称,只需在普通口罩上添加氯化钠涂层,就能将其转化为“特效口罩”。口罩使用过程中,涂层中的氯化钠会溶解于病毒自身携带的水中,形成溶液,杀死病毒;杀死病毒后,水分蒸发,一段时间后,氯化钠再次析出。 (1)钠原子转化为钠离子,其核外电子数 (填“变大”或“变小”),常温下,氯化钠的饱和溶液中,氯化钠与水的质量比为 (已知:常温下,氯化钠的溶解度为36 g)。 (2)构成氯化钠的阳离子符号为 ,口罩使用过程中,氯化钠溶液中溶质质量分数一直保持不变,此判断 。(填“正确”或“错误”)。 【答案】(1)变小 9:25 (2)Na+ 错误 4.小王同学用某固体物质进行了如图所示的实验(实验中水的损失忽略不计,操作M过程中未发生化学变化且温度没有变化),请回答下列问题:
(1)在10℃~40℃时,该物质的溶解度随温度的升高而(填“増大”或“减小”)。 7
(2)实验所得的溶液中肯定不饱和的有 (填溶液编号) (3)实验所得的溶液中溶质质量分数相同的有 和 、 和(均填溶液编号)。 (4)溶液c到溶液d的转化过程中,最多可能析出晶体(不带结晶水) g。 (5)操作M的名称是 。 【答案】(1)增大 (2)溶液b (3)溶液a和溶液b,溶液d和溶液e (4)20g (5)过滤 考点三:溶解度曲线 1.甲、乙两种物质(不含结晶水)的溶解度曲线如图所示,下列叙述正确的是( )
A.甲和乙的溶解度相等且均为30g B.甲物质的溶解度随温度的升高而减小 C.a1℃时,乙的饱和溶液中溶质与溶剂的质量比为3:7 D.将a2℃150g甲的饱和溶液降温到t1℃,有20g固体析出 【答案】D 2.如图是甲,乙、丙三种固体物质的溶解度曲线,据图回答下列问题:
(1)P点的含义是 。 (2)t2℃时,把50g甲中加入到200g水中充分搅拌,静置,形成的是 溶液(填“饱和”或“不饱和”)。 (3)稍微加热丙的饱和溶液即出现浑浊现象,其原因是 。 (4)除去甲中混有的少量乙,步骤是:加水溶解、加热浓缩、 、 过滤、洗涤、干燥。 (5)将t2℃时等质量的甲、乙两物质的饱和溶液分别降温至t1℃,对所得溶液的叙述正确的是 (填字母序号) A.溶剂质量:甲>乙