合成氨工艺设计
- 格式:doc
- 大小:4.02 MB
- 文档页数:5

合成氨生产工艺流程合成氨是一种重要的化学原料,在许多行业中被广泛应用。
本文将介绍合成氨的生产工艺流程,以及其中涉及到的化学反应和工艺设备。
生产工艺流程合成氨的生产工艺流程可以分为以下几个步骤:1.准备原料:其中主要原料是氢气和氮气,同时需要一定的催化剂。
2.压缩空气:将空气压缩到一定程度,将其中的氧和氩排除掉,以保证原料中的氮气含量高达99%以上。
3.合成反应:在特定的反应器中,将氢气和氮气进行反应,并通过催化剂加速反应过程,生成合成氨。
该反应通常采用哈伯-卡西反应。
4.分离纯化:将合成氨从反应器中分离出来,并通过分离纯化设备进行纯化。
5.尾气处理:将反应器中剩余的气体进行处理,通常采用吸收、脱附等方法,以减少尾气对环境的污染。
化学反应哈伯-卡西反应是合成氨生产的核心化学反应,其化学方程式为:N2(g) + 3H2(g) ⇌ 2NH3(g)该反应是一个可逆反应,所以产物中可能存在一定量的氮气和氢气。
催化剂通常采用铁-铝-钾等复合催化剂,以加速反应并提高反应的选择性。
工艺设备在合成氨生产过程中,涉及到以下几个主要的工艺设备:1.压缩机:用于将氧、氩等杂质气体排除,将气体压缩。
2.反应器:用于进行哈伯-卡西反应,通常采用固定床反应器,反应器内填充着催化剂。
3.分离塔:用于从反应器中分离出合成氨。
4.吸收塔:用于处理反应器中剩余的尾气。
合成氨是一种十分重要的化学原料,其生产工艺流程麻烦且多种化学反应涉及其中,因此需要一系列的工艺设备来完成整个生产过程。
哈伯-卡西反应是该生产过程的核心反应,通过复合催化剂加速反应过程并提高反应的选择性。
通过合理的工艺流程设计和设备选型,能够实现高效、稳定的合成氨生产。
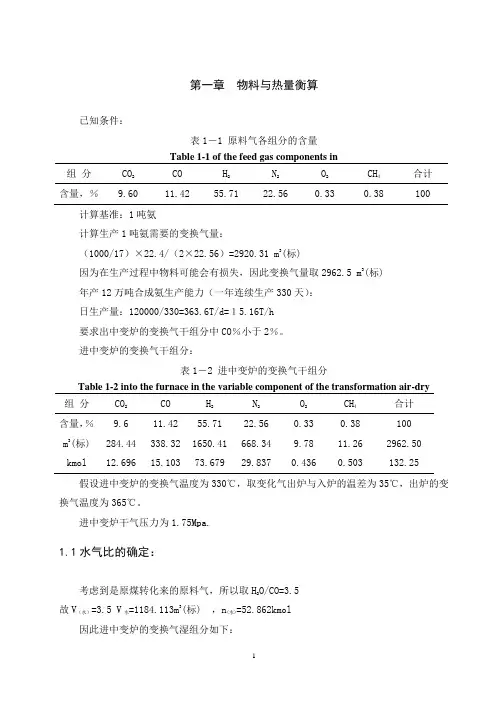
第一章 物料与热量衡算已知条件:表1-1 原料气各组分的含量 Table 1-1 of the feed gas components in组 分 CO 2 CO H 2 N 2 O 2 CH 4 合计 含量,%9.6011.4255.7122.560.330.38100计算基准:1吨氨计算生产1吨氨需要的变换气量:(1000/17)×22.4/(2×22.56)=2920.31 m 3(标)因为在生产过程中物料可能会有损失,因此变换气量取2962.5 m 3(标) 年产12万吨合成氨生产能力(一年连续生产330天): 日生产量:120000/330=363.6T/d=15.16T/h 要求出中变炉的变换气干组分中CO %小于2%。
进中变炉的变换气干组分:表1-2 进中变炉的变换气干组分Table 1-2 into the furnace in the variable component of the transformation air-dry 组 分 CO 2 CO H 2 N 2 O 2 CH 4 合计 含量,% 9.611.4255.7122.560.33 0.38 100 m 3(标) 284.44 338.32 1650.41 668.34 9.78 11.26 2962.50 kmol12.696 15.103 73.67929.8370.4360.503132.25假设进中变炉的变换气温度为330℃,取变化气出炉与入炉的温差为35℃,出炉的变换气温度为365℃。
进中变炉干气压力为1.75Mpa.1.1水气比的确定:考虑到是原煤转化来的原料气,所以取H 2O/CO=3.5 故V (水)=3.5 V 水=1184.113m 3(标) ,n (水)=52.862kmol因此进中变炉的变换气湿组分如下:表1-3 进中变炉的变换气湿组分Table 1-3 into the furnace of transformation in the variable component wet gas组分CO2CO H2N2O2CH4H2O 合计含量% 6.86 8.16 39.80 16.12 0.24 0.27 28.56 100m3(标) 284.42 338.32 1650.42 668.34 9.77 11.26 1184.12 4146.61 kmol 12.69 15.10 73.68 29.84 0.44 0.50 52.86 185.121.2中变炉CO的实际变换率的求取:假定湿转化气为100mol,其中CO湿基含量为8.16%,要求变换气中CO含量为2%,故根据变换反应:CO+H2O=H2+CO2,则CO的实际变换率公式为:X p =X2/X1×100%式中X1、X2分别为原料及变换气中CO的摩尔分率(湿基)所以:Xp= 74%则反应掉的CO的量为:8.16×74%=6.04则反应后的各组分的量分别为:H2O%=28.56%-6.04%+0.48%=23%CO%=8.16% -6.04%=2.12%H2% =39.8%+6.04%-0.48%=45.36%CO2%=6.86%+6.04%=12.9%中变炉出口的平衡常数:K p = (H2%×CO2%)/(H2O%×CO%)=12查《小合成氨厂工艺技术与设计手册》可知Kp=12时温度为397℃。

合成氨的工艺流程1. 空气分离:首先,空气中的氮气和氧气需要被分离。
这可以通过空气压缩和冷却,然后用分子筛或液化分离技术将氮气和氧气分离出来。
2. 氮气制备:通过空气分离得到的氮气需要被进一步提纯。
这可以通过低温分馏或其他技术将氮气提纯到适当的纯度。
3. 氢气制备:氢气可以通过天然气蒸汽重整反应或者电解水得到。
4. 催化剂制备:制备出合成氨反应所需的催化剂,通常是以铁为主要成分的铁钼镍催化剂。
5. 合成氨反应:将氮气和氢气在高压高温的条件下通过催化剂进行反应,生成合成氨。
6. 分离纯化:将合成氨经过冷却和减压,然后通过吸收剂、冷却和压缩等工艺步骤来分离纯化合成氨。
7. 储存和运输:将合成氨储存于合适的储罐中,并通过管道或其他运输方式将其运输到需要的地点。
以上就是合成氨的工艺流程,通过这个工艺流程可以高效地制备出高纯度的合成氨,供给各种化工生产需要。
合成氨的工艺流程是一个复杂而精细的过程,其中的每一步都需要严格控制,以确保产出的合成氨的纯度和质量能够满足工业需求。
在合成氨的工艺中,采用了一系列先进的化工技术和设备,以下将进一步细说合成氨的工艺流程过程。
8. 催化剂再生:在合成氨反应中使用的催化剂需要不断地被再生。
随着反应进行,催化剂表面会积聚一定量的杂质物质,从而影响催化剂的活性和选择性。
因此,通过热气流或蒸汽来清洁催化剂表面,以恢复催化剂的活性和选择性。
9. 热力学控制:合成氨的反应是放热反应,因此需保持适宜的温度。
以确保反应不至于过热,影响产品的选择性及催化剂的稳定性。
使用适当的冷却系统来维持反应温度,是非常关键的。
10. 蒸汽重整制氢:氢气是合成氨反应的一种重要原料。
而氢气通常是通过天然气蒸汽重整反应得到的。
在这个过程中,通过加热天然气并与水蒸气反应,生成氢气和二氧化碳。
11. 压缩系统:由于合成氨反应需要高压,所以需要使用高效的压缩系统,来将氮气和氢气压缩至合适的反应压力。
一般情况下,合成氨反应的压力约为100至200大气压。

合成氨的合成工段工艺要点
合成氨的合成工艺有以下几个要点:
1. 催化剂选择:合成氨的催化剂通常采用铁、钼和钾的化合物。
常见的催化剂有铁钼催化剂和铁钾催化剂。
催化剂的选择要考虑到催化剂的活性、稳定性和寿命等因素。
2. 反应条件:合成氨的合成反应是在高温高压下进行的。
典型的反应条件为350-450摄氏度和100-250大气压。
高温高压有利于提高反应速率和提高氨的产率。
3. 进料气体配比:合成氨的进料气体通常是氢气和氮气。
为了提高氨的产率,进料气体的氢气和氮气的摩尔比要控制在3:1到3.2:1之间。
4. 反应器设计:合成氨的反应器通常采用垂直管式反应器。
反应器内部通常有多层催化剂床。
反应器的设计要考虑到反应器的温度和压力控制,以及催化剂的补给和废物处理等因素。
5. 中间产品的处理:合成氨反应过程中会生成一些副产物和杂质,如水、氨基酸和硫化物等。
这些中间产品需要进行处理和去除,以保证合成氨的纯度和质量。
6. 能源利用:合成氨的合成过程需要大量的能源。
为了提高能源利用效率,可
以采用废热回收和氨合成废气回收等技术手段。
综上所述,合成氨的合成工艺要点包括催化剂选择、反应条件控制、进料气体配比、反应器设计、中间产品的处理和能源利用等方面。
这些要点的合理选择和控制对于提高氨的产率和质量非常重要。

年产三万吨合成氨厂变换工段工艺设计一、工艺流程概述1.原料准备:将天然气(主要是甲烷)与空气作为主要原料,通过气体净化系统去除其中的杂质、硫化物和水分。
2.原料配送:将净化后的天然气和空气分别输送至气体净化系统进行进一步的处理和分析。
3.变换反应槽:将净化后的天然气和空气通过压缩机压缩至一定压力后,经过暖气交换器加热至高温(约500-600℃),再进入变换反应槽。
4.变换催化剂:在变换反应槽中,使用催化剂(通常是高温高压下的铁-钴催化剂)促进N2和H2的反应。
反应生成的合成氨会随气流从反应槽中流出。
5.除气系统:将反应槽中的气体通过除尘器,冷却器和吸附剂等设备进行处理,去除其中的固体颗粒、水分和其他杂质。
6.合成氨回收:经过除气系统处理后的气体中仍含有未反应的氮气和氢气,通过压缩机再次压缩进入蒸馏塔。
在蒸馏塔中,根据不同的沸点,将氨气和氮气分离开来,再通过冷凝器冷凝为液态氨。
7.废水处理:在工艺过程中产生的废水会经过处理系统去除其中的有机物和杂质,以保证排放的废水符合环保要求。
二、设备布置和操作要点1.变换反应槽的设计要考虑到温度、压力和气体流动速度的控制。
同时,需要定期更换催化剂,以维持优良的反应性能。
2.除气系统中的设备要进行定期维护和清洁,确保其正常工作和去除气体中的杂质、固体颗粒和水分。
3.合成氨回收装置要根据产品质量要求设置合适的操作参数,例如蒸馏塔的温度和压力。
此外,冷凝器的冷却水流需要保持稳定,以确保气体顺利冷凝为液态氨。
4.废水处理系统应配置适当的物理和化学处理单元,如过滤器、沉淀池和生物处理等,以达到废水排放标准。
5.需要建立相应的安全措施,如设立监测系统,确保气体和液体在整个工艺中的安全运输和使用。
三、工艺控制和性能优化1.在变换反应槽中,可以通过调节供气比例、压力和温度等参数来控制合成氨的产率和选择性。
同时,也可以根据反馈控制系统监测和调整催化剂的性能。
2.除气系统中的设备可以通过监测气体的组成和温度、压力等参数,来调整操作参数,以达到满足产品质量要求的除气效果。
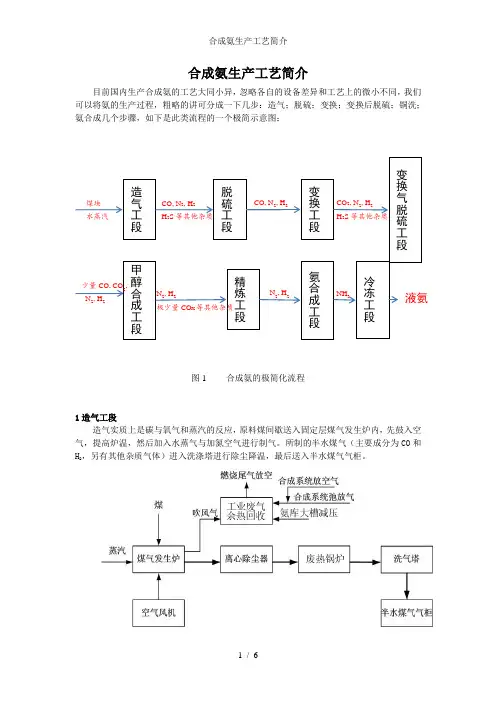
合成氨生产工艺简介目前国内生产合成氨的工艺大同小异,忽略各自的设备差异和工艺上的微小不同,我们可以将氨的生产过程,粗略的讲可分成一下几步:造气;脱硫;变换;变换后脱硫;铜洗;氨合成几个步骤,如下是此类流程的一个极简示意图:图1 合成氨的极简化流程1造气工段造气实质上是碳与氧气和蒸汽的反应,原料煤间歇送入固定层煤气发生炉内,先鼓入空气,提高炉温,然后加入水蒸气与加氮空气进行制气。
所制的半水煤气(主要成分为CO和H2,另有其他杂质气体)进入洗涤塔进行除尘降温,最后送入半水煤气气柜。
造气工段脱硫工段变换工段煤块水蒸汽CO, N2, H2H2S等其他杂质CO, N2, H2变换气脱硫工段CO2, N2, H2H2S等其他杂质甲醇合成工段少量CO, CO2,N2, H2精炼工段N2, H2极少量CO X等其他杂质氨合成工段N2, H2冷冻工段NH3液氨图2 造气工艺流程示意图2脱硫工段煤中的硫在造气过程中大多以H2S的形式进入气相,它不仅会腐蚀工艺管道和设备,而且会使变换催化剂和合成催化剂中毒,因此脱硫工段的主要目的就是利用DDS脱硫剂脱出气体中的硫。
气柜中的半水煤气经过静电除焦、罗茨风机增压冷却降温后进入半水煤气脱硫塔,脱除硫化氢后经过二次除焦、清洗降温送往压缩机一段入口。
脱硫液再生后循环使用。
图3 脱硫工艺流程图3变换工段气体从脱硫工艺中处理过后,已不含H2S等有毒气体。
变换工段的主要任务是将半水煤气中的CO在催化剂的作用下与水蒸气发生放热反应,生成CO2和H2。
经过两段压缩后的半水煤气进入饱和塔升温增湿,并补充蒸汽后,经水分离器、预腐蚀器、热交换器升温后进入中变炉回收热量并降温后,进入低变炉,反应后的工艺气体经回收热量和冷却降温后作为变换气送往压缩机三段入口。
说明:合成气的中的CO(一氧化碳)经蒸汽转换成CO2(二氧化碳)与H2,转换后气体称为“变换气”。
图4 变换工艺流程图4变换气脱硫与脱碳经变换后,气体中的有机硫转化为H2S,需要进行二次脱硫,使气体中的硫含量在25mg/m3。

合成氨的工艺流程1. 原料准备:合成氨的原料是氮气和氢气。
氮气通常是从空气中提取,而氢气则是通过蒸汽重整或其他化学反应得到。
这两种气体需要经过净化和压缩处理以确保其纯度和适当的压力。
2. 氮氢混合:氮气和氢气按照一定的比例混合到合成氨反应器中。
通常情况下,氮气和氢气的摩尔比是3:1,经过混合后形成氢气和氮气的混合气体。
3. 合成氨反应:混合气体经过压缩以提高反应速率,并在高温(通常在400-500摄氏度)和高压(通常在100-250大气压)下进入合成氨反应器。
在反应器中,混合气体经过催化剂的作用,发生一系列的化学反应,最终生成合成氨。
4. 分离和提纯:合成氨反应产物中还包含未反应的氮气和氢气,以及少量的副产物。
通过冷凝和减压操作,将未反应的气体和副产物从合成氨中分离出来。
之后,通过蒸馏或其他分离技术提纯合成氨,以得到符合工业标准的合成氨产品。
5. 储存和运输:合成氨产品可以被存储在压力容器中,并通过管道或其他方式进行运输到需要的地方,用于化肥生产或其他工业应用。
以上是合成氨的基本工艺流程,工艺中还有一些细节操作和工艺条件的优化,以确保合成氨的产率和纯度达到要求。
合成氨是一种重要的工业气体,广泛用于农业和工业领域。
它通过哈贝-玻斯过程(Haber-Bosch process)进行生产。
这个过程是由德国化学家弗里茨·哈贝和卡尔·博世于20世纪初发现的,如今,仍然是工业生产合成氨的主要方法。
在合成氨的工艺流程中,反应器是一个关键的组成部分。
工业上通常使用固定床催化剂反应器,其在高压和高温下通过催化剂的作用来促进氮气和氢气之间的反应。
这个过程对反应条件的要求极为严格,既要求高温高压,又要求催化剂的有效性和稳定性。
随着全球工业化的不断发展,对合成氨生产过程的节能减排和工艺的优化也提出了更高的要求。
在现代的合成氨生产过程中,节能减排已经成为了一个重要的发展趋势。
通过改进反应条件和提高生产效率,减少能源消耗,降低碳排放已经成为了工业化生产合成氨的重要目标。

合成氨的工艺流程合成氨是一种重要的化工原料,广泛应用于农药、化肥、塑料、纺织品和燃料电池等工业领域。
合成氨的工艺流程主要包括催化剂的选择、反应条件的控制、氨的分离和纯化等几个关键步骤。
下面将详细介绍合成氨的工艺流程。
1.催化剂的选择:2.原料准备:合成氨的原料主要包括空气和氢气。
空气中的氮气和氧气是制取氨的主要原料,而氢气则是为了提供还原剂。
为了保证原料的纯净度,通常会进行空气分离和氢气净化处理。
3.原料压缩:由于合成氨反应需要较高的压力,所以需要将原料气体进行压缩。
通常采用多级压缩机将氮气和氢气分别压缩到较高压力下。
4.原料进料与预热:将压缩后的氮气和氢气分别进入合成氨反应器前的预热器进行预热,提高其反应温度。
预热器中通常使用废热回收的方式,将反应后的热量传递给进料气体,以提高能量利用效率。
5.反应器:合成氨反应通常采用通过铁-铝催化剂催化的低温高压合成方法。
反应器中的催化剂床层通常采用多层填料堆积,以增加反应面积和接触时间,提高反应效率。
同时,反应器内部的温度和压力需要严格控制,一般为300-400℃和100-250atm。
6.反应气体的冷却与净化:经过反应后,反应气体中除了产生的氨气外,还会有未反应的氮气、氢气以及其他杂质气体。
这些气体需要经过冷却器和废热回收器进行冷却和净化处理,以去除其中的杂质。
7.氨的分离与纯化:在反应气体中,氨气的浓度相对较低,需要进行分离与纯化。
常用的方法是采用低温吸附分离技术,将氨气吸附在吸附剂上,然后通过加热解吸的方式将氨气从吸附剂中释放出来。
8.尾气处理:总的来说,合成氨的工艺流程包括催化剂的选择、原料准备、压缩、进料与预热、反应器、冷却与净化、分离与纯化以及尾气处理等主要步骤。
合理控制每个步骤的条件和参数,能够提高合成氨的产率和质量,减少能源消耗和环境污染。

合成氨工艺————————————————————————————————作者:————————————————————————————————日期:合成氨工艺流程(1)原料气制备将煤和天然气等原料制成含氢和氮的粗原料气。
对于固体原料煤和焦炭,通常采用气化的方法制取合成气;渣油可采用非催化部分氧化的方法获得合成气;对气态烃类和石脑油,工业中利用二段蒸汽转化法制取合成气。
(2)净化对粗原料气进行净化处理,除去氢气和氮气以外的杂质,主要包括变换过程、脱硫脱碳过程以及气体精制过程。
①一氧化碳变换过程在合成氨生产中,各种方法制取的原料气都含有CO,其体积分数一般为12%~40%。
合成氨需要的两种组分是H2和N2,因此需要除去合成气中的CO。
变换反应如下:CO+H2OH→2+CO2 =-41.2kJ/mol 0298HΔ由于CO变换过程是强放热过程,必须分段进行以利于回收反应热,并控制变换段出口残余CO含量。
第一步是高温变换,使大部分CO转变为CO2和H2;第二步是低温变换,将CO含量降至0.3%左右。
因此,CO变换反应既是原料气制造的继续,又是净化的过程,为后续脱碳过程创造条件。
②脱硫脱碳过程各种原料制取的粗原料气,都含有一些硫和碳的氧化物,为了防止合成氨生产过程催化剂的中毒,必须在氨合成工序前加以脱除,以天然气为原料的蒸汽转化法,第一道工序是脱硫,用以保护转化催化剂,以重油和煤为原料的部分氧化法,根据一氧化碳变换是否采用耐硫的催化剂而确定脱硫的位置。
工业脱硫方法种类很多,通常是采用物理或化学吸收的方法,常用的有低温甲醇洗法(Rectisol)、聚乙二醇二甲醚法(Selexol)等。
粗原料气经CO变换以后,变换气中除H2外,还有CO2、CO和CH4等组分,其中以CO2含量最多。
CO2既是氨合成催化剂的毒物,又是制造尿素、碳酸氢铵等氮肥的重要原料。
因此变换气中CO2的脱除必须兼顾这两方面的要求。
一般采用溶液吸收法脱除CO2。

合成氨是一种重要的化学原料,广泛用于生产农药、肥料、染料、塑料等。
年产10万吨合成氨的合成工艺设计是一个复杂而重要的任务,下面我将简要介绍该设计。
1.原料和质量要求:合成氨的原料主要包括氢气和氮气,其中氢气的纯度要求大于99.9%,氮气的纯度要求大于99.99%。
同时,还需要考虑进口原料的安全运输和储存条件。
2.选择合适的合成工艺:常用的合成氨工艺包括海勒过程、普朗特-阿谷耳过程、卡尔费-波斯特过程和道尔顿法等。
根据不同的条件和需求,选择适合的合成工艺。
3.反应装置设计:反应装置是合成氨工艺的核心部分,一般采用催化剂床反应器。
设计时需要考虑反应器的尺寸、催化剂的选择、温度和压力的控制等因素,以确保合成氨反应的高效进行。
4.适当的温度和压力控制:合成氨的反应温度通常在300-450摄氏度之间,反应压力则在100-300兆帕之间。
温度和压力的控制对于合成氨生成率、选择率和产量等方面有着重要影响。
5.废热利用和能源消耗:设计过程中应考虑废热的利用和能源的消耗。
常见的做法包括采用余热锅炉进行废热回收、通过换热器进行能量的转移和节约等。
6.安全生产和环境保护:在工艺设计中,安全生产和环境保护是至关重要的。
需要加强对装置的安全设计和监控,采取相应的防爆措施和防火措施。
同时,合成氨生产工艺会产生一定的废水和废气,需要采取相应的处理措施,保护环境。
7.过程控制和自动化:为了实现稳定、高效的生产,需要引入先进的自动化设备和系统进行过程控制。
采用先进的仪表、自控设备和自动控制系统,实现对合成氨生产过程的自动控制和调节。
以上是年产10万吨合成氨合成工艺设计的一些主要内容。
当然,实际的工艺设计还需要详细考虑其他因素,如设备选型、物料流动和传热、工艺流程优化等。
希望以上内容对您有所帮助!。

年产20万吨合成氨合成工艺设计The Process Design of 200kta of Synthetic AmmoniaSynthesis目录摘要 (I)Abstract (I)引言 (1)第一章综述 (2)1.1 氨的研究背景 (2)1.2 氨的用途 (2)1.3 氨的生产方法的选择 (3)第二章氨合成过程的步骤及工艺流程 (5)2.1 氨合成的步骤 (5)2.2 氨合成工艺流程简述 (6)第三章工艺计算 (9)3.1 原始条件 (9)3.2 物料衡算 (9)3.2.1 合成塔物料衡算 (9)3.2.2 氨分离器气液平衡计算....................... 错误!未定义书签。
3.2.3 冷凝塔气液平衡计算......................... 错误!未定义书签。
3.2.4 液氨贮槽气液平衡计算....................... 错误!未定义书签。
3.2.5 液氨贮槽物料计算 (14)3.2.6 合成系统物料计算........................... 错误!未定义书签。
3.2.7 合成塔物料计算............................. 错误!未定义书签。
3.2.8 水冷器物料计算 (17)3.2.9 氨分离器物料计算 (18)3.2.10 冷凝塔物料计算 (19)3.2.11 氨冷器物料计算............................ 错误!未定义书签。
3.2.12 冷凝塔物料计算............................ 错误!未定义书签。
3.2.13 液氨贮槽物料计算.......................... 错误!未定义书签。
3.3 热量衡算 (26)3.3.1合成塔热量计算 (26)3.3.2 废热锅炉热量计算 (28)3.3.3 热交换器热量计算 (29)第四章设备的计算与选型..................... 错误!未定义书签。
合成氨工艺条件的优化设计
合成氨工艺是一种通过催化剂将氮气与氢气反应生成氨气的过程。
优化工艺条件可以提高产氨效率和减少能耗。
以下是一些常见的合成氨工艺条件的优化设计方法:
1. 压力优化:合成氨反应需要高压条件,但过高的压力会增加设备成本和能耗。
通过优化压力条件,可以找到产氨效率和能耗之间的平衡点。
一般来说,合成氨反应的压力范围为100-300大气压。
2. 温度优化:合成氨反应需要高温条件,但过高的温度会导致催化剂活性降低和设备磨损加剧。
通过优化反应温度,可以提高催化剂的利用率和减少设备的磨损。
一般来说,合成氨反应的温度范围为300-550C。
3. 催化剂优化:选择合适的催化剂对合成氨反应至关重要。
一种常用的催化剂是铁-铝催化剂,但还有其他一些选择,如铂-钪催化剂、钌-铁催化剂等。
优化催化剂的选择和配比可以提高反应速率和选择性。
4. 气体比例和流速优化:氮气和氢气的比例和流速对合成氨反应的效果有很大影响。
优化气体比例和流速可以提高氨气的产量和选择性。
一般来说,氮气和氢气的摩尔比为1:3,气体的流速要保证与催化剂的接触时间充分。
5. 催化剂再生优化:催化剂在反应过程中会逐渐失活,需要定期进行再生。
优
化催化剂的再生过程可以延长催化剂的使用寿命和提高反应效果。
常见的再生方法包括氧化再生、还原再生和混合再生等。
通过对合成氨工艺条件的优化设计,可以实现更高的产氨效率和更低的能耗,提高工艺的经济性和环境友好性。
但需要注意的是,优化设计应综合考虑设备成本、工艺可行性、催化剂选择等因素,以达到最佳的综合效益。
合成氨典型工艺流程及特点下载温馨提示:该文档是我店铺精心编制而成,希望大家下载以后,能够帮助大家解决实际的问题。
文档下载后可定制随意修改,请根据实际需要进行相应的调整和使用,谢谢!并且,本店铺为大家提供各种各样类型的实用资料,如教育随笔、日记赏析、句子摘抄、古诗大全、经典美文、话题作文、工作总结、词语解析、文案摘录、其他资料等等,如想了解不同资料格式和写法,敬请关注!Download tips: This document is carefully compiled by theeditor. I hope that after you download them,they can help yousolve practical problems. The document can be customized andmodified after downloading,please adjust and use it according toactual needs, thank you!In addition, our shop provides you with various types ofpractical materials,such as educational essays, diaryappreciation,sentence excerpts,ancient poems,classic articles,topic composition,work summary,word parsing,copy excerpts,other materials and so on,want to know different data formats andwriting methods,please pay attention!合成氨典型工艺流程。
合成氨的典型工艺流程主要包括以下六个步骤:1. 原料气制备,原料气主要包括氢气和氮气。
合成氨生产工艺流程合成氨是一种重要的化学原料,广泛应用于农业、医药、冶金、塑料等行业。
合成氨的工艺流程主要包括两个步骤:制备氢气和制备氮气。
以下是合成氨的详细工艺流程:1.制备氢气合成氨的生产需要大量的氢气。
目前常用的制备氢气的方法有水煤气转化法和重油加热法。
水煤气转化法是将煤炭和水蒸气在高温下进行催化反应,生成一氧化碳和氢气。
反应过程中产生的一氧化碳和氢气通过一系列的分离和净化步骤,得到纯净的氢气。
重油加热法是将重油和蒸汽在高温下进行催化反应,生成氢气和炭黑。
反应过程中的氢气经过冷却和净化,得到纯净的氢气。
制备氢气的方法还包括天然气蒸气重整法、煤气重整法等。
2.制备氮气制备氮气有很多方法,包括空分法、膜法和吸附法等。
其中,空分法是最常用的制备氮气的方法。
空分法是将空气通过冷凝和膜分离等步骤,将氧气和其他杂质去除,得到纯净的氮气。
3.合成氨反应合成氨反应是指将制备好的氢气和氮气进行催化反应,生成氨气。
合成氨反应一般采用哈布斯过程。
哈布斯过程是将氢气和氮气通过铁催化剂进行反应,在高温和高压下,生成氨气。
反应过程中,氮气和氢气经过多级催化剂反应器,进行一系列的反应和净化步骤,得到高浓度的氨气。
为了提高合成氨的产量和效率,可以采用以下措施:1.优化催化剂:改进催化剂的配方和制备工艺,提高催化剂的活性和稳定性。
2.调整反应条件:通过调整反应温度、压力和气体流量等参数,优化反应条件,提高反应效率。
3.循环气体:将反应后的气体进行回收和再利用,减少气体的浪费,提高氨气的产量。
4.节能减排:采用节能的加热和冷却设备,减少能量的消耗和二氧化碳的排放。
5.安全措施:建立完善的安全管理系统,确保生产过程中的安全。
总之,合成氨的生产工艺流程包括制备氢气和制备氮气两个步骤,通过优化反应条件和提高催化剂的活性,可以提高合成氨的产量和效率,从而满足农业、医药、冶金等行业对氨气的需求。
合成氨各工序工艺详细流程
一、蒸汽炒烧式合成氨工艺
1、反应原料预处理及收集:以天然气为反应原料进行洁净预处理,将其中的硫氢离子捕集处理;
2、冷凝:利用空冷凝器将原料液冷凝后进入反应釜;
3、蒸汽炒烧:将原料液放入釜中增温,增温到某个温度时,将蒸汽灌进反应釜并炒烧反应;
4、气-液回收:将反应釜中产生的氰气和氨气经过冷凝式压缩凝结回收;
5、洗涤液回收:将氰气和氨氧化后产生的洗涤液回收处理;
7、回收固体:将反应釜中凝聚的氯化磷等固体物质回收并进行进一步处理;
二、NH3-NH3-N2反应式氨的制备
1、原料准备:准备碘化氨、碳氢气、氮气等原料进行反应;
2、液-液混合:将碳氢气、碳氢气、氮气和碘化氨通过特定设备混合液化;
3、反应:将液态原料放入反应器中,加热反应工艺,由气相催化剂催化反应,化学反应过程中产生的氨收集回收;
4、冷凝:将反应后的气体回收到冷凝器中,通过冷凝介质冷凝凝结;
5、收集:将氨从冷凝罐中收集。
合成氨工艺流程详解
《合成氨工艺流程详解》
合成氨是一种重要的化工原料,广泛用于生产化肥、燃料和塑料等。
合成氨工艺是通过Haber-Bosch过程进行的,下面将详细介绍合成氨工艺的流程。
1. 原料准备
合成氨的主要原料是氮气和氢气。
氮气来自空气分离,而氢气通常是通过天然气蒸汽重整来生产。
这两种气体经过先进的处理和净化,保证了反应过程的纯净度和稳定性。
2. 催化剂制备
合成氨的制备需要采用催化剂,通常是铁或钴等金属催化剂。
这些催化剂需要经过一系列特殊的处理和制备工艺,以保证其表面活性和稳定性,从而提高反应的效率和产率。
3. 氮氢气混合
经过处理和净化后的氮气和氢气被混合到一定的比例,通常是3:1的比例。
这样的混合气体通过加热和压缩,使得反应物具备更高的能量和活性,有利于反应的进行。
4. 催化反应
混合气体经过预热后进入反应器,反应器内填充着催化剂,以提供表面反应条件。
在高温和高压下,氮气和氢气发生催化反应,生成合成氨。
这个反应过程是一个放热反应,所以需要控制反应温度和排放反应热。
5. 分离和提纯
产生的混合气体经过冷却后进入分离装置,将产生的合成氨和未反应的氮氢气体进行分离。
分离得到的合成氨会进一步进行脱水和提纯处理,使其符合工业用途的级别。
通过以上的工艺流程,合成氨可以有效地得到,而且具有较高的产率和纯度。
这个工艺流程成为了化工工业中的一种重要生产方式,为生产化肥和其他化工产品提供了重要的原料支持。
合成氨工艺流程详解
第一步,氮气和氢气制备。
氮气可以通过空分装置从空气中分离得到,氢气可以通过蒸汽重整、加气鼓风等工艺得到。
两种气体需要经过严格的
处理,包括除尘、除湿、除CO2等。
第二步,催化剂的制备。
合成氨反应需要使用催化剂,一般使用铁、钴、钼等金属催化剂。
制备催化剂时需要先制备金属盐溶液,再与载体进
行混合、干燥、焙烧等处理步骤,最后制得活性催化剂。
第三步,反应器的设计。
合成氨反应一般通过用反应管搅拌气液相过
程来实现,在反应器中加入氮气、氢气和催化剂。
反应器的设计需要考虑
反应温度、压力、催化剂种类及其活性等因素,以确保反应的高效进行。
合成氨反应的主要反应过程为:N2+3H2->2NH3
反应发生在高温高压下,通常反应温度在300-500摄氏度之间,反应
压力在100-250atm之间。
催化剂起到了加速反应速率的作用,而反应速
率与催化剂的活性有关。
合成氨工艺的特点是需要消耗大量的能量,工艺设备的运行和维护费
用也很高。
此外,合成氨反应的平衡位置靠近氨气一侧,所以需要通过一
系列措施来提高氨的合成率,如适当降低反应温度、增加反应压力、优化
催化剂的选择等。
综上所述,合成氨工艺是一项复杂而重要的化学反应过程。
通过控制
反应条件、催化剂的选择和改进工艺设备,可以提高合成氨的产率和质量,满足不同领域的需求。
合成氨工艺设计
摘要:介绍了不同原料的合成氨和合成氨各个工段工艺流程,指出了我国合成氨工艺技术现状及其未来发展趋势,认为未来合成氨技术进展的主要趋势是大型化、低能耗、结构调整、清洁生产、长周期运行。
关键词:合成氨;发展现状;发展趋势
氨是最为重要的基础化工产品之一, 其产量居各种化工产品的首位; 同时也是能源消耗的大户, 世界上大约有10% 的能源用于生产合成氨。
氨主要用于农业, 合成氨是氮肥工业的基础, 氨本身是重要的氮素肥料, 其他氮素肥料也大多是先合成氨、再加工成尿素或各种铵盐肥料, 这部分约占70% 的比例, 称之为“化肥氨”; 同时氨也是重要的无机化学和有机化学工业基础原料, 用于生产铵、胺、染料、炸药、制药、合成纤维、合成树脂的原料, 这部分约占30%的比例, 称之为“工业氨”。
未来合成氨技术进展的主要趋势是“大型化、低能耗、结构调整、清洁生产、长周期运行”。
一、不同原料合成氨工艺流程
1、以固体燃料(煤或焦炭)为原料的合成氨的简要生产过程
煤或焦炭造气脱硫 CO变换
精制脱CO2
压缩
合成合成尿素
氨尿素
2、以天然气或轻油为原料的合成氨的简要生产过程
天然气或轻油脱硫一段转化二段转化
CO高变
CO低变
压缩甲烷化脱CO2
合成合成尿素
氨尿素
3、以重油为原料的合成氨的简要生产过程
重油油气化除炭黑脱硫 CO变化
空气空分脱CO
2
液氨洗涤合成尿素
尿素
压缩合成
氨
二、合成氨各工段工艺流程(以煤为原料)
1、造气工段(间歇式气化过程在固定床煤气发生炉中进行的)
(1)五个阶段:
①吹风阶段:吹入空气,提高燃料层温度,吹风气放空。
工艺流程:空气—煤气炉底部—燃料层—炉顶—上旋风除尘器—废热锅炉—烟囱放空或送吹风气系统回收。
②一次上吹制气阶段:自下而上送入水蒸汽进行气化反应,燃料层下部温度下降,上部升高。
工艺流程:水蒸汽和加氮空气—煤气炉底部—燃料层—炉顶—上旋风除尘器—废热锅炉—洗气箱—洗气塔—煤气总管—气柜
③下吹制气阶段:水蒸汽自上而下进行反应,使燃料层温度趋下均衡。
工艺流程:蒸汽(不加空气)—炉顶—燃料层—炉底—废热锅炉—洗气箱—洗气塔—煤气总管—气柜
④二次上吹制气阶段:使底部下吹煤气排净,为吹入空气做准备。
工艺流程与一次上吹阶段相同。
⑤空气吹净阶段:此部分吹风气加以回收,作为半水煤气中氮的主要来源。
工艺流程:空气—煤气炉底部—燃料层—炉顶—上旋风除尘器—废热锅炉—洗气箱—洗气塔—煤气总管—气柜
(2)工艺条件:
①温度:炉温应较熔点温度低50℃
②吹风速度:吹风速度直接决定放热。
③蒸汽用量:是改善煤气质量和提高煤气产量的重要手段之一。
④循环时间及其分配:等于或略少于3min
2、净化工段
(1)原料气的脱硫:合成氨原料气中,一般总含有一定数量的无机硫化物(主要是硫化氢H2S),其次是有机硫化物如二硫化碳(CS2)、硫氧化碳(COS)、硫醇(RSH)、噻吩(C4H4S)等
①湿法脱硫:在吸收塔中用液体吸收剂(脱硫剂)吸收煤气中的硫化氢,而后再将吸收剂再生,再生后的吸收剂再送回吸收塔中循环使用。
按硫的回收形态,可分为循环法和氧化法:
循环法:(以氨水脱硫为例)
NH3·H2O+H2S=NH4HS+H2O
氧化法:(改良ADA法)
脱硫塔中的反应:
Na2CO3+H2S→NaHS+NaHCO3
2NaHS+4NaVO3+H2O→Na2V4O9+4NaOH+2S
Na2V4O9+2ADA(氧化态)+2NaOH+H2O→4NaVO3+2ADA(还原态)
再生塔中反应:
2ADA(还原态)+O2→2ADA(氧化态)+H2O
②干法脱硫(氧化锌法最为常见)
脱硫反应:
ZnO+H2S=ZnS+H2O
ZnO+C2H5SH=ZnS+C2H5OH
ZnO+C2H5SH=ZnS+C2H4+H2O
氧化锌脱硫剂:以ZnO为主体,其余为Al2O3,还有的加入CuO、MoO3、TiO2、MnO2、MgO等以增进脱硫效果。
(2)一氧化碳变换:一氧化碳不仅不是合成氨所需的直接原料,而且对氨合成催化剂有毒害作用,因此原料气送往合成工序之前必须将一氧化碳彻底清除。
主反应:CO+H2O CO2+H2 △H0298=-41.19KJ/mol
副反应:CO+H2 C+H2O
CO+3H2 CH4+H2O
(3)二氧化碳的除净:原料气经CO变换后都含有相当量的CO2, CO2的存在对下步的反应不利,但其又是制造尿素、碳酸氢铵、纯碱等工业的原料。
根据所用吸收剂的性质不同,可分为物理吸收和化学吸收两类。
物理吸收法利用二氧化碳能溶解于水或有机溶剂来完成的。
常用的有水、甲醇、碳酸丙烯酯、磷酸三丁酯等。
化学吸收法是用氨水、碳酸钾、有机胺等碱性溶液为吸收剂,基于二氧化碳是酸性气体能与溶液中的碱性物质进行化学反应而将其吸收。
(4)原料气的精制:经一氧化碳变换和二氧化碳脱除后的原料气尚有少量含有少量的一氧化碳和二氧化碳会对氨合成催化剂毒害。
方法有铜氨液吸收、甲烷化法、深冷液氮洗涤法、变压吸附法。
3、合成氨工段
(1)氨的合成:
0.5N2+1.5H2 NH3+46.22kJ/mol
氨合成反应为气固非均相反应。
当气流速度较大、催化剂粒度足够小时,整个过程速度为动力学控制。
工艺条件选择:最佳温度:(400~500℃)。
压力:中小型厂20~32MPa;大型厂15MPa)。
空间速度:中压法空速(30Mpa),20000~30000h-1;低压法空速(15Mpa),10000h-1。
(2)氨的分离:氢氮混合气经过合成塔催化剂床反应后,只有很少部分氢氮气合成为氨,产物与未反应的氢氮气一起离开合成塔,因此需要进行氨的分离。
分离方法有:
冷凝法:把含氨混合气冷却,使其中大部分氨冷凝与循环气分开。
目前工业上常用此法。
水吸收法:此法利用氨易溶于水得到浓氨水,氨水经蒸馏、冷凝成为液氨。
缺点:能耗较大,工厂用之较少。
有机溶剂吸收法(三甘醇等):溶剂易挥发至混合器中分离不净对催化剂有影响,用之较少
三、我国合成氨工艺技术现状及其未来发展趋势
我国的氮肥工业自20 世纪50年代以来, 不断发展壮大, 目前合成氨产量已跃居世界第一位,现已掌握了以焦炭、无烟煤、焦炉气、天然气及油田伴生气和液态烃多种原料生产合成氨、尿素的技术, 形成了特有的煤、石油、天然气原料并存和大、中、小生产规模并存的生产格局。
1、大型合成氨生产工艺技术现状
2、中、小型合成氨生产工艺技术现状
我国目前有中型合成氨装置55套, 生产能力约为500 万t /a; 其下游产品主要是尿素和硝酸铵; 其中以煤、焦为原料的装置有34套, 以渣油为原料的装置有9套, 以气为原料的装置有12 套。
目前有小型合成氨装置700多套, 生产能力约为3 000万t /a; 其下游产品原来主要是碳酸氢铵, 现有112套经过改造生产尿素。
原料以煤、焦为主,其中以煤、焦为原料的占96% , 以气为原料的仅占4%。
3、合成氨技术未来的发展趋势
(1) 大型化、集成化、自动化, 形成经济规模的生产中心、低能耗与环境更友好将是未来合成氨装置的主流发展方向。
在合成氨装置大型化的技术开发过程中, 其焦点主要集中在关键性的工序和设备, 即合成气制备、合成气净化、氨合成技术、合成气压缩机:在低能耗合成氨装置的技术开发过程中, 其主要工艺技术将会进一步发展。
(2)以“油改气”和“油改煤”为核心的原料结构调整和以“多联产和再加工”为核心的产品结构调整, 是合成氨装置“改善经济性、增强竞争力”的有效途径。
(3) 实施和环境友好的清洁生产时未来合成氨装置的必须和唯一的选择。
(4)提高生产运转的可靠性, 延长运行周期是未来合成氨装置 善经济性、增强竞争力 必要保证。
四、参考文献
[1]韩冬冰等,化工工艺学[M],中国石油出版社.
[2]孙凤伟,栾智宇,合成氨工艺技术的现状及其发展趋势[J],辽宁化工,2010.04.
[3]蒋德军,合成氨工艺技术的现状及其发展趋势[J],现代化工,2005.08.。