(4)C=3, Φ =2, f = 3– 2 + 1 = 2 (T以及I2在任一相
中的浓度)
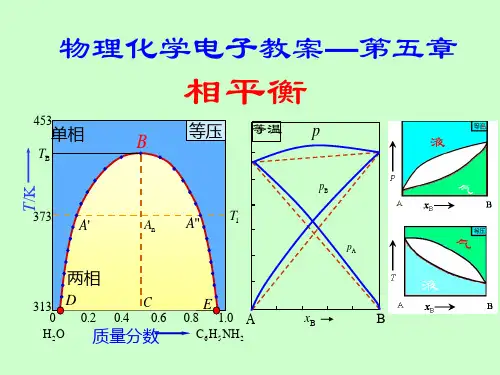
§5.4 单组分系统的相平衡
1、Clapeyron方程 2、Clausius-Clapeyron方程
液-气平衡 固-气平衡 固-液平衡 3、单组分系统相律——水的相图
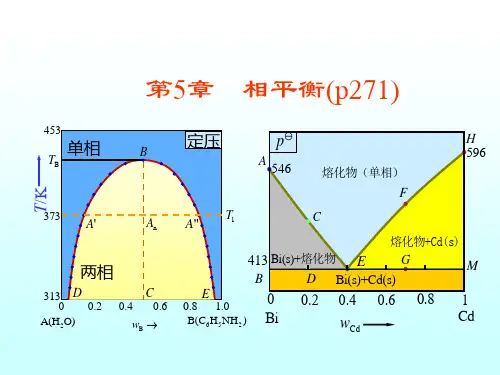
第五章 多相平衡
返回目录 退出
单组分系统的相律
若将CaCO3(s)单独放在一密闭容器中,达平衡后C=?
容器内有CaCO3(s)+CaO(s)+CO2(g)。 S=3,R=1,R’=0,C=3– 1– 0=2。 因CaO(s)和CO2(g)在两相中,没有浓度关系。
注意:系统确定后,其组分数是确定的,物种数有一定随 意性,可以随人们考虑问题的出发点不同而不同。
=RT/p (设气体为理想气体)
整理为:
vapH m RT 2
dp pdT
d ln p dT
Clausius---
Clapeyron方程
积分:
d ln p
vapH m RT 2
dT
适用于液气或固气 两相平衡
第五章 多相平衡
返回目录 退出
若温度变化不大时,vapHm为常数 d ln p
பைடு நூலகம்
第五章 多相平衡
第五章 多相平衡
返回目录 退出
例 NaCl-H2O系统
NaCl,H2O: S=2, R=0, R’=0, C=2 NaCl不饱和水溶液 S=3: Na+, Cl-, H2O, R=0, R’=1: [Na+]=[Cl-], 所以 C= 3– 1=2 NaCl饱和水溶液,有NaCl(s)存在
S=4:NaCl(s), Na+, Cl-, H2O, R=1: NaCl(s) = Na++ Cl-,