高一化学乙酸和羧酸
- 格式:pdf
- 大小:1.01 MB
- 文档页数:8

高一化学必修三羧酸知识点羧酸是有机化合物中十分重要的一类物质,它在生物学、医药学、化工等领域都扮演着重要角色。
羧酸可用于制药、生物催化、有机合成等领域,因此,对于高中化学学生来说,了解羧酸的性质、结构和反应十分重要。
一、羧酸的基本结构羧酸分子由一个羧基(-COOH)和一个碳链组成。
羧基是由一个碳原子与一个氧原子和一个氢原子连接而成的。
羧酸的碳链可以是直链、支链或环状结构,其中直链和支链结构的羧酸是最常见的。
二、羧酸的命名和表示方法羧酸的命名通常以其碳链的命名为基础,然后在末端加上“酸”字。
例如,乙酸就是由两个碳原子组成的羧酸分子。
除了常见的化学式表示外,羧酸还可以用分子式、结构式和简图表示。
三、羧酸的性质1. 酸性:羧酸具有较强的酸性。
它们可以与碱反应生成相应的盐和水。
例如,乙酸与氢氧化钠反应生成乙酸钠和水。
2. 气味:羧酸在溶液中具有特殊的气味,例如,乙酸的气味呛鼻且具有辛辣的性质。
3. 溶解性:羧酸在水中具有一定的溶解性。
溶解度与羧酸的碳链长度有关,碳链越短,溶解度越高。
4. 沸点和熔点:羧酸的沸点和熔点与其分子大小、分子间相互作用力有关。
一般来说,分子量较大的羧酸沸点和熔点较高。
四、羧酸的常见反应1. 氧化反应:羧酸可以在适当条件下发生氧化反应,生成相应的醛、酮或羧酸。
例如,乙酸可以被氧气氧化生成乙醛。
2. 脱羧反应:羧酸可以在加热条件下发生脱羧反应,生成相应的酸酐和水。
例如,乙酸可以加热生成醋酸酐和水。
3. 还原反应:羧酸可以通过还原剂还原为相应的醛、酮或烃。
还原反应的条件取决于具体的羧酸和还原剂。
例如,乙酸可以被还原为乙醛。
五、羧酸的应用领域1. 制药:许多药物都是羧酸衍生物,包括乙酸钠、阿司匹林等。
羧酸可以增加药物的水溶性和生物利用度。
2. 化学工业:羧酸可用于合成香料、润滑剂、染料和橡胶等化工产品。
3. 生物学:在生物学中,羧酸是脂肪酸和氨基酸的重要成分,参与体内能量代谢和脂质合成等生物过程。
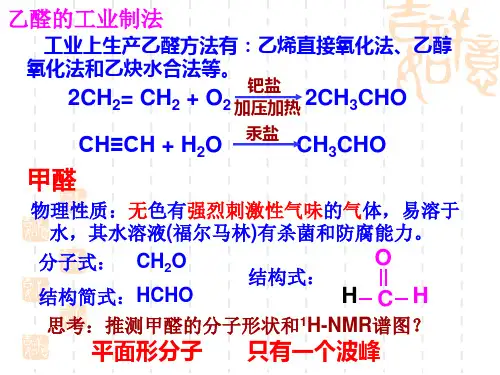



乙酸羧酸物理性质。
一、乙酸1·分子结构2·物理性质:无色有强烈刺激性气味的液体、易凝结成冰一样的晶体、易溶于水和乙醇—COOH叫羧基,乙酸是由甲基和羧基组成。
羧基是由羰基和羟基组成,这两个基团相互影响,结果不再是两个单独的官能团,而成为一个整体。
羧基是乙酸的官能团。
(1)弱酸性:(2) 酯化反应——取代反应注:①浓硫酸的作用:催化剂、吸水剂。
②反应过程:酸脱羟基、醇脱氢。
③饱和碳酸钠溶液作用:中和乙酸,溶解乙醇,便于闻乙酸乙酯的气味;降低乙酸乙酯的溶解度,便于分层析出。
④导气管不能伸入碳酸钠溶液中,防止加热不匀,液体倒吸。
二、酯1·定义:羧酸和醇反应,脱水后生成的一类物质叫酯2·通式:RCOOR/3·物理性质:低级酯有芳香气味、密度比水小、难溶于水。
4·水解反应:强调断键位置和反应条件。
RCOOR/ + NaOH→RCOONa + R/OH加碱为什么水解程度大?——中和酸,平衡右移。
像乙酸一样,分子由烃基和羧基相连构成的有机物还很多,统称为羧酸,看课本P176 二、羧酸,了解羧酸的分类、性质和用途。
三、羧酸1·定义2·按羧基数目分:一元酸(如乙酸)、二元酸(如乙二酸又叫草酸HOOC-COOH)和多元酸分 按烃基类别分:脂肪酸(如乙酸)、芳香酸(苯甲酸C 6H 5OH) 按含C 多少分: 低级脂肪酸(如丙酸)、类 高级脂肪酸(如硬脂酸C 17H 35COOH 、软脂酸C 15H 31COOH 、油酸C 17H 33COOH )3·饱和一元酸:烷基+一个羧基(1)通式:C n H 2n+1COOH 或C n H 2n O 2、R —COOH (2) 性质:弱酸性、能发生酯化反应。
3.例题精讲例1.有机物(1)CH 2OH (CHOH )4CHO (2)CH 3CH 2CH 2OH (3)CH 2=CH —CH 2OH (4)CH 2=CH —COOCH 3(5)CH 2=CH —COOH 中,既能发生加成、酯化反应,又能发生氧化反应的是 ( )A .(3)(5)B .(1)(3)(5)C .(2)(4)D .(1)(3)例2.一种含碳、氢、氧三种元素的有机化合物。





乙酸脱羧反应
乙酸脱羧反应是一种有机化学反应,其反应的底物为羧酸。
在反应中,羧酸的羧基(-COOH)被还原成一个羰基(-CO-),同时释放出一分子的二氧化碳。
这种反应一般需要使用一种还原剂,如氢气或金属碱金属,以及一种催化剂,如铜或镍。
乙酸脱羧反应在有机合成中广泛使用,可以用于制备醛、酮和醇等有机分子。
例如,将苯甲酸进行乙酸脱羧反应,可以得到苯乙酮。
此外,还可以使用乙酸脱羧反应来制备一些药物和生物活性分子。
尽管乙酸脱羧反应在实验室中很常见,但是应该注意它的危险性。
在进行反应时,由于反应产生的氢气和二氧化碳的积聚,容易引起爆炸。
因此,在实验室中进行此类反应时,必须采取安全措施,如在通风良好的地方进行、佩戴防护服和防护眼镜等。
- 1 -。

考点10 乙酸与羧酸【考点定位】本考点考查乙酸的化学性质,主要是乙酸具有酸的通性,能发生酯化反应等,特别注意乙酸是比碳酸强的一种弱酸。
【精确解读】1.羧酸的概念:在分子里烃基跟羧基直接连接的有机化合物叫做羧酸.官能团:羧基(-COOH).2.羧酸的分类①根据分子里羧基的数目分类.如:一元羧酸(R-COOH),如:HCOOH、CH3COOH、CH2=CHCOOH(丙烯酸)、C6H5COOH(苯甲酸)二元羧酸,如:HOOC-COOH(乙二酸)、HOOCCH2CH2CH2CH2COOH(己二酸)②根据分子里的烃基分类.a.脂肪酸(饱和脂肪酸、不饱和脂肪酸); b.芳香酸.c.高级脂肪酸:硬脂酸(C17H35COOH)油酸(C17H33COOH,烃基中含有1个双键)3.羧酸通式与同分异构(1)饱和一元羧酸通式:C n H2n O2(n≥1).(2)同分异构:脂肪酸:C n H2n O2(n≥2)与芳香酸:C n H2n-8O2(n≥7)①类别异构:饱和一元脂肪酸(羧基取代法)与酯(从右向左移碳法).②位置异构与碳链异构.4.羧酸的化学性质:(1)酸的通性主要是与活泼性的金属、碱性氧化物、碱及盐反应(2)酯化反应①羧酸与醇酯化:(羧酸脱羧羟基,醇脱羟基氢)②无机含氧酸与醇酯化生成无机酯:(酸脱羟基氢,醇脱羟基)CH3CH2OH+HNO3→C2H5ONO2+H2O硝酸乙酯①利用醇、酚、羧酸与Na完全反应时:-OH~Na、-OH~H2;②利用酚、羧酸与碱反应时,-OH(-COOH)~NaOH、-COOH~Cu(OH)2;③利用酚、羧酸与Na2CO3反应时,-OH~Na2CO3、-COOH~Na2CO3;④利用羧酸与NaHCO3反应时,-COOH~NaHCO3.【典例剖析】乙酸分子的结构式为,下列反应及断键部位正确的是( )(1)乙酸的电离,是①键断裂;(2)乙酸与乙醇发生酯化反应,是②键断裂;(3)在红磷存在时,Br2与CH3COOH的反应:CH3COOH+Br2CH2Br-COOH+HBr,是③键断裂;(4)乙酸变成乙酸酐的反应:2CH3COOH→+H2O,是①②键断裂A.(1)(2)(3) B.(1)(2)(3)(4) C.(2)(3)(4) D.(1)(3)(4)【剖析】(1)乙酸的电离,氢氧键断裂,即①键断裂,故正确;(2)乙酸与乙醇发生酯化反应,碳氧单键断裂,即②键断裂,故正确;(3)Br2与CH3COOH的反应:CH3COOH+Br2CH2Br-COOH+HBr,甲基上碳氢键断裂,即③键断裂,故正确;(4)乙酸变成乙酸酐的反应:2CH3COOH→+H2O,一个乙酸碳氧键断裂,另1个乙酸氢氧键断裂,即①②键断,故正确;故答案为B。
羧酸1 羧酸的基本知识温故乙酸的分子式是C2H4O2,结构简式是CH3COOH,是由甲基(—CH3)与羧基(—COOH)相连而构成的有机化合物。
(1)概念:羧酸是由烃基(或氢原子)与羧基()相连而构成的有机化合物。
(2)官能团:羧基(或—COOH)。
(3)通式:饱和一元脂肪酸的通式为C n H2n O2(n≥1)或C n H2n+1COOH(n≥0)。
注意最简单的羧酸是甲酸,其结构简式为HCOOH(4)分类(5)命名注意对于芳香羧酸和脂环羧酸,可把苯环和脂环作为取代基来命名。
如的名称为3-苯基丙烯酸。
2 羧酸的物理性质物理性质规律举例溶解性分子中碳原子数较少的羧酸能够与水互溶甲酸、乙酸、乙二酸随着分子中碳原子数的增加,一元羧酸在水中的溶解度迅速减小,甚至不溶于水高级脂肪酸是不溶于水的蜡状固体沸点随着分子中碳原子数的增加,一元羧酸的沸点逐渐升高丙酸>乙酸>甲酸注意羧酸的沸点一般高于与其相对分子质量相当的其他有机化合物,原因是羧酸分子间可以形成氢键。
3 羧酸的化学性质羧酸的化学性质主要取决于羧基官能团。
由于受氧原子电负性较大等因素的影响,当羧酸发生化学反应时,羧基中C—O和O—H容易断裂:(1)酸性①羧酸是一类弱酸,具有酸的通性,羧酸的电离方程式为RCOOH RCOO-+H+。
表现酸性的反应如下:反应现象或化学方程式与酸碱指示剂作用羧酸能使紫色石蕊溶液变红与碱反应RCOOH+NaOH—→RCOONa+H2O与碱性氧化物反应CuO+2RCOOH—→(RCOO)2Cu+H2O与活泼金属反应2RCOOH+2Na—→2RCOONa+H2↑RCOOH+NaHCO3—→RCOONa+H2O+CO2↑与某些盐反应2RCOOH+Na2CO3—→2RCOONa+H2O+CO2↑②教材P73·探究比较乙酸、碳酸和苯酚的酸性强弱实验装置CH3COOH与Na2CO3反应,有气体生成;生成的气体经过装有饱和NaHCO3实验现象溶液的洗气瓶后通入苯酚钠溶液中,溶液变浑浊实验结论酸性:化学方程式名师提醒(1)羧基(—COOH)由羰基()和羟基(—OH)构成,由于二者之间的相互影响,羧基上的氢原子比醇羟基上的氢原子易电离,因此羧酸具有酸性。
第六节乙酸羧酸一、乙酸1、分子结构分子式C2H4O2, 结构简式:CO O H3CHO HOC3CH或2、物理性质无色、强烈刺激性气味的液体,熔点为16.6℃,低于16.6℃凝结成冰状晶体,故无水乙酸又称冰醋酸。
能与水和乙醇任意比互溶。
3、化学性质由于羰基对羟基影响,使羟基活性增强。
(1)酸性:乙酸在水溶液里部分电离-++C O O3C HHC O O H3C H具有无机酸通性:①与指示剂反应,如使紫色石蕊试液变红色。
②与金属活动顺序表中排了H前金属反应生成乙酸盐和H2③与碱性氧化物反应生成盐和水④与碱反应生成盐和水⑤与某些弱酸盐或不稳定酸盐反应注意:CH3CH2OH、H、CH3COOH 酸性比较:乙醇:中性,能与活泼金属反应,不与盐和碱反应。
苯酚:弱酸性,不能使指示剂变色,能与强碱反应,不与NaHCO3反应(更不会产生CO2)。
乙酸:弱酸性,能使指示剂变色,能与NaOH反应,能与碳酸盐反应产生CO2。
故酸性:乙酸﹥碳酸﹥苯酚﹥乙醇(2)酯化反应:酸与醇作用生成酯和水的反应O2H5H2CO18OC3CH4SO2H5H2CO18HO HOC3CH+∆+浓注意:a)经同位素氧-18测定,乙酸与乙醇作用生成乙酸乙酯的反应原理是:乙酸脱去羧基上的羟基,乙醇脱去羟基上的氢原子。
b)反应中浓硫酸起催化、吸水作用。
c)吸收装置(如右图)中导管口不与液面接触是防止试管中液体倒吸入反应容器中。
d)试管中用饱和Na2CO3溶液收集乙酸乙酯,目的是中和蒸气中的乙酸,溶解乙醇,降低乙酸乙酯的溶解度。
e)酯与混合液分离:用分液漏斗分液,取上层油状液体得酯。
4、乙酸的制法(1)发酵法乙酸氧化乙醛发酵氧化乙醇酶发酵糖类淀粉−−−→−()((2)乙烯氧化法C O O H3CH 22O CHO 3CH 2CHO 3CH 22O 2CH 2CH 2−−−→−+−−−→−+=催化剂催化剂此法原料来源丰富,生产工艺流程简单 (3)烷烃直接氧化法—丁烷氧化法O 2H 2C O O H3CH 2O 53CH 2CH 2CH 3CH 2++5、乙酸的用途生产醋酸纤维 、合成维纶纤维 、作溶剂、制香料、染料、医药、农药等。
乙酸 羧酸 一、乙酸 羧酸1、 定义:分子中烃基(或氢原子)跟羧基()相连的化合物属于羧酸。
2、 物理性质:无色液体,易溶于水,随着碳原子数增多,水溶性降低。
具有弱酸性,随着碳原子数增多,酸性降低。
3、 饱和一元酸的通式_________________________ 二、乙酸(冰醋酸即无水乙酸) 1、 分子结构:分子式为___________,结构式为_______________,结构简式为_________________,俗称_______2、乙酸的化学性质 (1)酸性乙酸水溶液中存在以下电离方程式:CH 3COOH CH 3COO -+H +,故乙酸为弱酸,能体现酸的性质。
乙酸能与Na 、NaOH 、NaHCO 3、Na 2CO 3反应,酸性大于碳酸。
酸性比较:在某有机物A 的分子中,其结构简式如右图。
写出: A 跟NaOH 溶液反应的化学方程式是A 跟NaHCO 3溶液反应的化学方程式是A 在一定条件下跟Na 反应的化学方程式是:(2)酯化反应在一支试管中加入3 mL 乙醇,然后边摇动试管边慢慢加入2 mL 浓硫酸和2 mL 冰醋酸。
按图连接好装置用酒精灯小心均匀地加热试管3~5 min ,产生的蒸气经导管通到饱和的碳酸钠溶液的液面上。
可以看到碳酸钠饱和溶液的液面上有透明的油状液体产生,并可闻到香味。
生成乙酸乙酯的反应A 、这种有香味的无色透明油状液体就是乙酸乙酯,反应的化学方程式可以表示如下:+CH 3CH 2OH浓硫酸+H 2OCH 3COOH CH 3COOCH 2CH3反应类型:酯化反应(取代反应),反应规律:_______________________________酸和醇起作用,生成酯和水的反应叫做酯化反应,这里的酸是指像乙酸之类的有机酸和像硝酸之类的无机含氧酸。
如果用含氧的同位素188O 的乙醇与乙酸作用,请写出化学方程式:B 、乙酸乙酯是酯类化合物的一种,乙酸乙酯的密度约为0.9 g·cm -3,沸点77 ℃,易溶于乙醇等,微溶于水。