鲁教版化学九年级下册《碱及其性质》常见的酸和碱
- 格式:pptx
- 大小:1.17 MB
- 文档页数:14


第二节碱及其性质(一)教材分析本节内容是选自九年级在学习了常见的酸(硫酸和盐酸)的性质后对另一类物质------常见的碱的学习,酸和碱是常见的两类化学物质,也是化学实验室中最常用的试剂。
理解酸和碱的性质,有助于学生学好化学,进一步理解化学与人类生活的密切关系。
而且对于培养学生从诸事物个性中概括出共性并达到理解事物的水平,使学生在增长知识的同时,逐步学会分析和解决问题的方法,培养学生的比较、归纳水平。
(二)学情分析学生学习了常见的酸——盐酸和硫酸的性质和用途后,具备了探究酸的化学性质的基础和水平,为学习常见的碱奠定了学习物质性质的基础和方法。
学生已经通过探究学习常见的酸的性质,具有一定的学习方法基础。
(三)教学目标知识与技能(1)理解氢氧化钠的吸水性和腐蚀性,了解其用途。
(2)理解氢氧化钠和氢氧化钙的化学性质。
和NaOH的反应。
(3)探究CO2过程与方法通过一些探究活动,进一步理解与体验科学探究的过程;学会用碱的相关性质解释相关生活现象。
情感态度与价值观(1)通过实验设计及实验分析,培养学生的创新水平。
(2)通过学生亲自参与科学探究活动,激发学习化学的兴趣,培养学生尊重事实的科学态度,发展善于合作,勤于思考的科学精神。
(四)教学重点和难点重点:氢氧化钠和氢氧化钙的性质。
难点:碱的化学性质。
(五)教学设计思想总的思路是先设置情景,通过“活动与探究”和“小组实验”,让学生归纳总结常见碱的性质,通过“活动与探究”,探究CO 2和NaOH 的反应。
以学生为主体,培养学生的探究水平和动手操作水平,激发学生学习化学的兴趣。
(六)实验准备:教师准备:NaOH 固体、20%NaOH 溶液、CaO 固体、澄清的石灰水、盐酸、硫酸、蒸馏水、乙醇、石蕊试液、酚酞试液、洗净的鸡爪、去壳的熟鸡蛋、导线、灯泡、烧杯、试管、软塑料瓶、表面皿、滴管、点滴板。
学生准备:生石灰干燥剂、生鹧鸪蛋。
(七)教学设计过程:教学环节 教师活动 学生活动 教学意图引入新课 一、新课导入 【创设问题情境】 演示: 1、实验(如图)观察图中发生的现象。



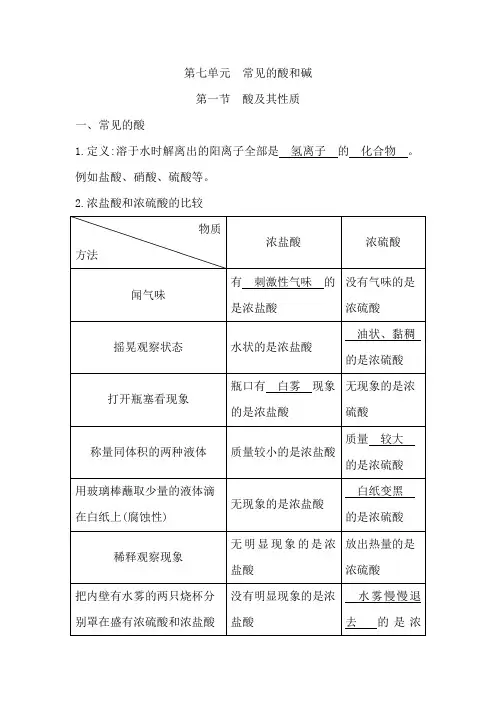
第七单元常见的酸和碱第一节酸及其性质一、常见的酸1.定义:溶于水时解离出的阳离子全部是氢离子的化合物。
例如盐酸、硝酸、硫酸等。
2.浓盐酸和浓硫酸的比较的表面皿上(吸水性的应用) 硫酸3.浓硫酸特性的应用(1)浓硫酸具有吸水性,可以做某些气体(如氢气、氧气等)的干燥剂。
如图所示,一般是长进短出。
(2)浓硫酸溶于水时会放出大量的热,稀释浓硫酸时应该把浓硫酸慢慢地倒入蒸馏水中,防止因放热液滴飞溅伤人,并且用玻璃棒慢慢地搅拌。
二、酸的化学性质1.因为酸的溶液中都有自由移动的氢离子,所以酸有相似的化学性质。
2.酸的共性(以盐酸为例)(1)酸性溶液都能使紫色石蕊试液变红。
(2)稀盐酸可以与活泼金属反应产生氢气和盐。
例如:铁和稀盐酸反应会冒出大量的气泡:Fe+2HCl FeCl2+H2↑。
(3)稀盐酸可以除去钢铁表面的锈,生成盐和水。
例如:生产生活中钢铁表面的锈往往可以用酸溶液除去,同时溶液变为黄色:Fe2O3+6HCl2FeCl3+3H2O 。
(4)稀盐酸可以与碳酸钠发生化学反应,产生二氧化碳气体和水以及盐。
例如:可以用稀盐酸来区分氯化钠和碳酸钠两种白色粉末状物质,有气泡冒出的是碳酸钠:Na2CO3+2HCl2NaCl+CO2↑+H2O 。
3.复分解反应酸的化学性质中,其中酸与金属氧化物的反应以及酸和碳酸钠的反应都是两种化合物相互交换成分生成另外两种新的化合物的反应,这类反应属于基本反应类型中的复分解反应。
从化合价的角度来分析复分解反应时,它的前后没有发生化合价的变化。
4.盐酸的化学性质中产物中几乎都存在盐。
它的组成中包括了金属阳离子和酸根阴离子两大部分。
注意:铵根离子属于金属阳离子,但不含金属元素。
5.稀盐酸和稀硫酸的个性(1)不同的酸中酸根阴离子不同,从而导致不同的酸之间化学性质也存在着差异。
(2)可以用氯化钡溶液来区分稀盐酸和稀硫酸。
化学方程式为H2SO4+BaCl22HCl+BaSO4↓。
6.酸的主要用途(1)硫酸是重要的化工原料,用于生产化肥、农药、染料、冶炼金属、精炼石油、金属除锈以及实验室中作为干燥气体的干燥剂。

九年级下册化学鲁教版知识点
九年级下册化学鲁教版的知识点主要包括以下几部分:
1. 常见的酸和碱:了解酸和碱的基本性质,如何识别酸,以及酸和碱的化学性质。
2. 酸的性质:理解酸能使指示剂变色,与金属反应生成盐和氢气,与金属氧化物反应生成盐和水等性质。
3. 碱的性质:理解碱能使指示剂变色,与非金属氧化物反应生成盐和水等性质。
4. 盐的性质:了解盐的生成和反应,以及盐的溶解性和沉淀等性质。
5. 溶液的酸碱度:了解酸碱度的概念和表示方法,掌握酸碱度对物质性质的影响。
6. 化学方程式:学习化学方程式的书写和配平,理解化学反应的基本原理。
7. 化学实验安全知识:了解化学实验的基本安全知识和注意事项,掌握常见化学品的存储和使用方法。
8. 元素周期表:了解元素周期表的结构和元素的基本性质,掌握元素周期表在化学学习和研究中的应用。
9. 有机化学基础:初步了解有机化学的基本概念和重要应用,包括有机物的分类、结构、性质、合成等方面。
10. 化学与社会发展:了解化学在人类生产和生活中的重要作用,包括能源、材料、环境等方面的应用。
以上是九年级下册化学鲁教版的一些主要知识点,通过学习和掌握这些知识,学生可以建立起较为完整的化学基础知识体系,为进一步学习高中化学和其他学科打下坚实的基础。



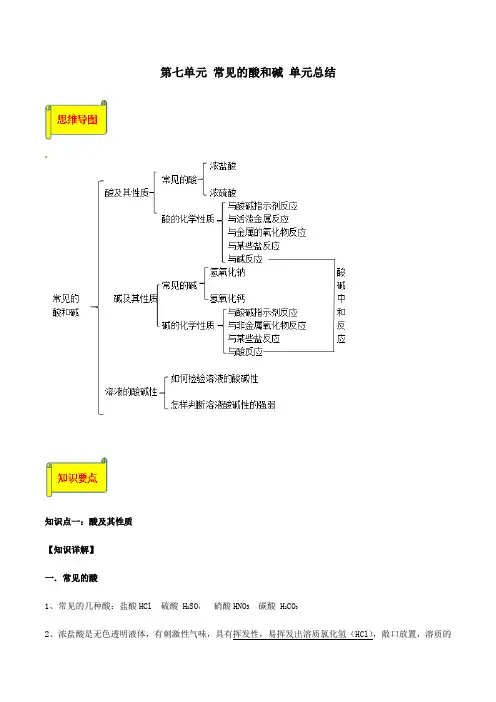
第七单元常见的酸和碱单元总结知识点一:酸及其性质【知识详解】一.常见的酸1、常见的几种酸:盐酸HCl 硫酸 H2SO4硝酸HNO3碳酸 H2CO32、浓盐酸是无色透明液体,有刺激性气味,具有挥发性,易挥发出溶质氯化氢(HCl),敞口放置,溶质的质量分数变小。
浓硫酸是无色、粘稠、油状液体,不易挥发。
浓硫酸的特性:(1)吸水性:可做气体干燥剂,用于干燥酸性或中性气体,不能干燥氨气(NH3);浓硫酸敞口放置,易吸收空气中得水,溶质的质量分数变小;(2)腐蚀性:在稀释浓硫酸时,一定要把浓硫酸沿器壁慢慢倒入水里,并不断用玻璃棒搅拌,切不可将水到人浓硫酸中。
3、打开盛浓盐酸的瓶盖,瓶口会出现白雾,原因是:盐酸易挥发,挥发氯化氢气体和空气中的水蒸气结合,形成盐酸小液滴的缘故。
二、酸的化学性质1.酸的通性:酸中含有: H+(1)酸 + 金属 ----- 盐 + 氢气铁和稀盐酸反应Fe + 2HCl === FeCl2 +H2↑铁和稀硫酸反应 Fe + H2SO4 ===FeSO4 +H2↑现象:有气泡产生,溶液由无色变为浅绿色。
(2)酸 + 金属氧化物----- 盐 + 水(复分解反应)氧化铁和稀盐酸反应(除铁锈):Fe2O3 + 6HCl === 2FeCl3 + 3H2O氧化铁和稀硫酸反应(除铁锈):Fe2O3 + 3H2SO4 === Fe2(SO4)3 + 3H2O现象:固体逐渐溶解,溶液由无色变为黄色。
(3)酸 + 碱 -----盐 + 水(复分解反应)盐酸和烧碱反应:HCl + NaOH === NaCl +H2O盐酸和氢氧化钙反应:2HCl + Ca(OH)2 === CaCl2 + 2H2O氢氧化铝药物治疗胃酸过多:3HCl + Al(OH)3 ===AlCl3 + 3H2O硫酸和烧碱反应:H2SO4 + 2NaOH ===Na2SO4 + 2H2O(4)酸 + 碳酸盐 -----盐 + 水 + 二氧化碳(复分解反应)大理石与稀盐酸反应:CaCO3 + 2HCl === CaCl2 + H2O + CO2↑碳酸钠与稀盐酸反应: Na2CO3 + 2HCl === 2NaCl + H2O + CO2↑(5)酸的特性:(酸根的性质)硫酸和氯化钡溶液反应:H2SO4 + BaCl2 ===BaSO4 ↓+ 2HCl盐酸和硝酸银溶液反应:HCl + AgNO3 ====AgCl↓ + HNO32.复分解反应(1)定义:两种化合物互相交换成分生成另外两种化合物,像这样的反应叫做复分解反应。
九年级化学下册《碱及其性质》知识点鲁教版九年级化学下册《碱及其性质》知识点鲁教版知识点1、常见的碱(1)氢氧化钠、氢氧化钙的物理性质、用途注意:①氢氧化钠的潮解属于物理变化。
②氢氧化钠密封保存的原因:氢氧化钠易吸收空气中的水蒸汽而潮解,同时又能与空气中的二氧化碳反应而变质。
③如果不慎将碱液沾到皮肤上,要用较多的水冲洗,再涂上硼酸溶液。
2、碱的化学性质(具有相似性质的原因:碱离解时所生成的阴离子全部是OH-):(1)碱溶液与酸碱指示剂的反应:使紫色石蕊试液变蓝色,使无色酚酞试液变红色。
(2)非金属氧化物+碱==盐+水2NaOH+CO2==Na2CO3+H2O(氢氧化钠敞口放置在空气中变质的原因)2NaOH+SO2==Na2SO3+H2O2NaOH+SO3==Na2SO4+H2O(3)酸+碱==盐+水NaOH+HCl==NaCl+H2OCa(OH)2+2HCl==CaCl2+2H2O2NaOH+H2SO4==Na2SO4+2H2O(4)盐+碱→另一种盐+另一种碱(反应物均可溶,产物符合复分解条件)课后习题1.下列实例不属于中和反应的是( )A.土壤酸化后加入熟石灰改良B.胃酸分泌过多的病人遵医嘱服用含有氢氧化铝的药物以中和过多胃酸C.蚊虫叮咬人的皮肤分泌出蚁酸,如果涂含碱性物质的药水就可减轻痛痒D.金属表面锈蚀后,可用稀盐酸进行清洗思路解析:金属表面腐蚀后,产生的主要是金属氧化物,而不是碱,故金属氧化物与酸的反应不属于中和反应。
其他三项均为中和反应。
答案:D2.两种溶液混合后能发生化学反应,且总质量不会发生变化的是( )A.食盐溶液和稀盐酸B.碳酸钠溶液和稀盐酸C.氢氧化钾溶液和硫酸溶液D.石灰水和氢氧化钠溶液思路解析:反应前后没有物质脱离体系的反应,反应前后的质量都不会发生变化。
A、D不发生反应,不符合要求;B中产生的CO2逸出体系;C则都发生化学反应且无物质逸出。
答案:C3.下列各组物质按酸、碱、单质、氧化物顺序排列的是( )A.H2SO4 Na2O C COB.Mg(OH)2 CuSO4 CO2C.KOH HNO3 O2 SO3D.HCl NaOH O2 P2O5思路解析:A中的Na2O属于碱性氧化物;B中的CuSO4属于盐;C中KOH是碱,HNO3是酸。