IR红外吸收光谱
- 格式:ppt
- 大小:558.50 KB
- 文档页数:27



ir(红外光谱)的原理
红外光谱法(IR)的原理是:分子能选择性吸收某些波长的红外线,而引起分子中振动能级和转动能级的跃迁,检测红外线被吸收的情况可得到物质的红外吸收光谱,又称分子振动光谱或振转光谱。
在红外线照射下,当辐射能量与分子振动、转动频率相一致时,被测物质分子会产生其特定的红外光谱,据此可鉴定出化合物中各种原子团。
IR具有测定快速、特征性强、试样用量少、操作简便等优点。
但是,红外光谱一般只提供物质分子中官能团的相关信息,而对于一些复杂化合物,特别是新化合物,单靠IR 检测技术并不能解决问题,需要与其他分析手段互相配合,才能确定分子结构。
如需了解更多关于IR的原理,建议查阅相关文献或咨询专业化学家。




红外吸收光谱基本原理及应用
红外吸收光谱(IR)是一种分析技术,利用物质的分子振动和转动产生
的特定吸收窗口,实现对物质结构、组成和化学键的定性和定量分析。
红
外光谱技术不需要对物质进行分离和纯化,具有非破坏性、灵敏度高、分
析速度快等优点,被广泛应用于化学、生物、环境、医药等领域。
红外光谱的应用非常广泛。
下面将介绍几个主要的应用领域:
1.有机化学领域:红外光谱可以用于有机化学品的鉴定和结构分析。
通过红外光谱可以确定化合物中的官能团,从而判断其化学性质和结构。
红外光谱还可以用于有机合成的反应监测和催化剂的评价。
2.无机化学领域:红外光谱在无机化学中的应用主要是对无机物质的
结构分析和表征。
通过测定无机物质的红外吸收光谱,可以确定其化学键
类型和强度,进而了解其分子结构和化学性质。
3.生物医学领域:红外光谱在生物医学领域的应用非常广泛。
红外光
谱可以用于分析生物体内的有机物和无机物,研究生物分子的结构和组成。
另外,红外光谱还可以用于红外光热治疗、红外光谱诊断等。
4.环境监测领域:红外光谱在环境监测中可以用于检测空气中的污染物、土壤和水中的污染物等。
利用红外光谱可以快速分析环境中的有机物
和无机物,为环境保护和治理提供依据。
总之,红外吸收光谱是一种重要的分析技术,具有广泛的应用。
它在
化学、生物、医药和环境等领域中发挥着重要的作用。
随着科学技术的不
断发展,红外吸收光谱将会在更多领域得到应用和发展。


红外吸收光谱定性和定量红外吸收光谱法(infrared absorption spectroscopy,IR)是利用物质分子对红外光的吸收及产生的红外吸收光谱来鉴别分子的组成和结构或定量的方法。
当以连续波长的红外光为光源照射样品,引起分子振动能级之间跃迁,所生的分子振动光谱,称红外吸收光谱。
在引起分子振动能级跃迁的同时不可避免的要引起分子转动能级之间的跃迁,故红外吸收光谱又称振-转光谱。
早在19世纪初人们通过实验证实了红外光的存在,二十世纪初人们进一步系统地了解了不同官能团具有不同红外吸收频率这一事实,1950年以后出现了自动记录式红外分光光度计。
随着量子力学和计算机科学的迅速发展,1970年以后出现了傅立叶变换型红外光谱仪。
红外测定技术如全反射红外、显微红外、光声光谱以及色谱-红外联用等也不断发展和完善,使红外光谱法得到广泛应用。
IR主要用于分子结构的基础研究以及化学组成的分析,其中应用最广泛的是中红外光区有机化合物的结构鉴定。
由于每种化合物均有红外吸收,而且任何气态、液态、固态样品均可进行红外吸收光谱测定,因此红外光谱是有机化合物结构解析的重要手段之一。
近年来,红外光谱的定量分析应用也有不少报导,主要是近红外和远红外光区的应用。
如,近红外光区用于含有与C,H,O等原子相连基团化合物的定量;远红外光区用于无机化合物的定量等。
本章主要讨论中红外吸收光谱法。
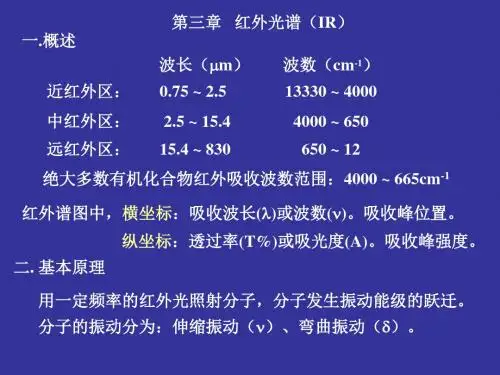
红外光区的划分及主要应用红外光谱在可见光区和微波光区之间,其波数范围约为12 800~10 cm-1(0.75~1 000 μm)。
根据仪器及应用不同,习惯上又将红外光区分为三个区:近红外光区;中红外光区;远红外光区。
每一个光区的大致范围及主要应用如表4.1所示。
4.1.1.1近红外光区它处于可见光区到中红外光区之间。
因为该光区的吸收带主要是由低能电子跃迁、含氢原子团(如O—H、N—H、C—H)伸缩振动的倍频及组合频吸收产生,摩尔吸收系数较低,检测限大约为0.1%。

红外吸收光谱(IR)的基本原理及应用1. 红外吸收光谱(IR)的概述•红外光谱是指电磁波谱中波长范围在红光与微波之间的区域,其波长范围大约为0.78~1000微米。
•红外光谱可分为近红外(NIR)波段(0.782.5微米)、中红外(MIR)波段(2.525微米)和远红外(FIR)波段(25~1000微米)。
•红外吸收光谱是利用物质分子对入射红外光的吸收来研究化学成分和分子结构的一种非常重要的分析技术。
2. 红外吸收光谱的基本原理•红外光谱采用红外光通过样品后的吸收强度与波长的关系来表征样品的化学组成和结构。
•红外光与样品中的化学键振动、分子转动等相互作用,导致了特定波长的红外光被吸收。
•红外光谱图是以波数(单位:cm^(-1))或波长(单位:微米)为横坐标,红外光吸收强度为纵坐标绘制的曲线图。
3. 红外光谱仪的工作原理•红外光谱仪由光源、样品室、光谱仪和检测器等组成。
•光源产生红外光,通过样品室后,红外光与样品相互作用并发生吸收。
•吸收的红外光经过光谱仪的分光装置分解成不同波长的光,然后通过检测器进行信号转换和放大,最后生成红外光谱图。
4. 红外吸收光谱的应用4.1 分析化学领域•红外光谱是分析化学中常用的手段之一,可用于定性分析、定量分析和结构鉴定等。
•红外光谱可用于分析无机物、有机物、大分子化合物、生物分子等不同类型的样品。
4.2 药物研究与制药工业•红外光谱可用于药物的研究与开发,包括药物的成分分析、相互作用研究和质量控制等方面。
•在制药工业中,红外光谱被广泛应用于药物的质量检验、药物的鉴别、药物的含量测定等。
4.3 环境与食品安全监测•红外光谱可用于环境监测和食品安全监测,通过检测样品中的化学成分和有害物质来评估环境和食品的安全性。
•红外光谱还可用于检测食品中的添加剂、农药残留和毒素等。
4.4 材料科学和工业控制•红外光谱在材料科学和工业控制中有着广泛的应用,可用于材料的组分分析、结构表征和物性研究等。
红外光谱(IR)(InfraredSpectroscopy)红外光谱(I R)(Infrared Spectroscopy)第一节:概述1、红外吸收光谱与紫外吸收光谱一样是一种分子吸收光谱。
红外光的能量(△E=0.05-1.0ev)较紫外光(△E=1-20ev)低,当红外光照射分子时不足以引起分子中价电子能级的跃迁,而能引起分子振动能级和转动能级的跃迁,故红外吸收光谱又称为分子振动光谱或振转光谱。
2、红外光谱的特点:特征性强、适用范围广。
红外光谱对化合物的鉴定和有机物的结构分析具有鲜明的特征性,构成化合物的原子质量不同、化学键的性质不同、原子的连接次序和空间位置不同都会造成红外光谱的差别。
红外光谱对样品的适用性相当广泛,无论固态、液态或气态都可进行测定。
3、红外光谱波长覆盖区域:0.76 mm ~ 1000mm.红外光按其波长的不同又划分为三个区段。
(1)近红外:波长在0.76-2.5mm之间(波数12820-4000cm-1)(2)中红外:波长在2.5-25mm(在4000-400 cm-1)通常所用的红外光谱是在这一段的(2.5-15mm,即4000-660 cm-1)光谱范围,本章内容仅限于中红外光谱。
(3)远红外:波长在25~1000mm(在400-10 cm-1)转动光谱出现在远红外区。
4、红外光谱图:当物质分子中某个基团的振动频率和红外光的频率一样时,分子就要吸收能量,从原来的振动能级跃迁到能量较高的振动能级,将分子吸收红外光的情况用仪器记录,就得到红外光谱图。
5、红外光谱表示方法:(1)红外光谱图红外光谱图以透光率T%为纵坐标,表示吸收强度,以波长l ( mm)或波数s (cm-1)为横坐标,表示吸收峰的位置,现主要以波数作横坐标。
波数是频率的一种表示方法(表示每厘米长的光波中波的数目)。
通过吸收峰的位置、相对强度及峰的形状提供化合物结构信息,其中以吸收峰的位置最为重要。
(2)将吸收峰以文字形式表示:如下图可表示为,3525cm-1(m),3097cm-1(m),1637cm-1(s)。
红外吸收光谱(IR)的大体原理及应用一、红外吸收光谱的历史太阳光透过三棱镜时,能够分解成红、橙、黄、绿、蓝、紫的光谱带;1800年,发此刻红光的外面,温度会升高。
如此就发觉了具有热效应的红外线。
红外线和可见光一样,具有反射、色散、衍射、干与、偏振等性质;它的传播速度和可见光一样,只是波长不同,是电磁波总谱中的一部份。
(图一)、波长范围在微米到大约1000微米左右。
红外区又能够进一步划分为近红外区<到2微米,基频红外区(也称指纹区,2至25微米)和远红外区(25微米至1000微米)三个部份。
1881年以后,人们发觉了物质对不同波长的红外线具有不同程度的吸收,二十世纪初,测量了各类无机物和有机物对红外辐射的吸收情形,并提出了物质吸收的辐射波长与化学结构的关系,慢慢积存了大量的资料;与此同时,分子的振动――转动光谱的研究慢慢深切,确立了物质分子对红外光吸收的大体理论,为红外光谱学奠定了基础。
1940年以后,红外光谱成为化学和物理研究的重要工具。
今年来,干与仪、运算机和激光光源和红外光谱相结合,诞生了运算机-红外分光光度计、傅立叶红外光谱仪和激光红外光谱仪,开辟了崭新的红外光谱领域,增进了红外理论的进展和红外光谱的应用。
二、红外吸收的本质物质处于不断的运动状态当中,分子经光照射后,就吸收了光能,运动状态从基态跃迁到高能态的激发态。
分子的运动能量是量子化的,它不能占有任意的能量,被分子吸收的光子,其能量等于分子动能的两种能量级之差,不然不能被吸收。
分子所吸收的能量可由下式表示:E=hυ=hc/λ式中,E为光子的能量,h为普朗克常数,υ为光子的频率,c为光速,λ为波长。
由此可见,光子的能量与频率成正比,与波长成反比。
分子吸收光子以后,依光子能量的大小,能够引发转动、振动和电子能阶的跃迁,红外光谱确实是由于分子的振动和转动引发的,又称振-转光谱。
把分子看成由弹簧和小球组成的结构。
小球代表原子或原子团,弹簧代表原子间的化学键。