原电池以及电解池复习讲义讲义
- 格式:ppt
- 大小:1.49 MB
- 文档页数:60


电解与原电池电解:在电解槽中,直流电通过电极和电解质,在两者接触的界面上发生电化学反应,以制备所需产品的过程。
(电化学是有关电与化学变化关系的一个化学分支)(电能转化为化学能)。
原电池:直接将化学能转化为电能的装置。
(是利用两个电极之间金属性的不同,产生电势差,从而使电子的流动,产生电流.又称非蓄电池,是电化电池的一种,其电化反应不能逆转,即是只能将化学能转换为电能,简单说就即是不能重新储存电力,与蓄电池相对。
)Eg:充电电池:充电电解反应,供电原电池电解发生的条件:电源,电极(惰性电极,氧化,还原性弱的)电解质(水溶液,融融状态)注:纯水是无法电解的,必须加入电解质(不参与电解反应)。
%%%%在水溶液中电解氯化2NaCl+2H2o==2Na(OH)+CL2+H2(电解)电解熔融状态下的氯化钠2NaCl=====2Na+ CL2(电解)电解的作用:使一些在普通的氧化还原反应中很难得到或者失去电子离子比较容易得到电子或失去电子,促进氧化还原反应进行进而得到一些在普通的化学反应中无法或者很难得到的物质。
吸氧腐蚀和析氢腐蚀的区别电解方程式的实例(用惰性电极电解):负极:Zn + 2OH - -2e -=== ZnO + H2O 正极:Ag2O + H2O + 2e - === 2Ag + 2OH - 电池的总反应式为:Ag2O + Zn ====== 2Ag + ZnO 电化腐蚀:发生原电池反应,有电流产生 (1)吸氧腐蚀负极:Fe -2e -==Fe 2+正极:O 2+4e -+2H 2O==4OH - 总式:2Fe+O 2+2H 2O==2Fe(OH)24Fe(OH)2+O 2+2H 2O==4Fe(OH)3 2Fe(OH)3==Fe 2O 3+3H 2O(2)析氢腐蚀: CO 2+H 2O H 2CO 3H ++HCO 3-负极:Fe -2e -==Fe 2+ 正极:2H + + 2e -==H 2↑总式:Fe + 2CO 2 + 2H 2O = Fe(HCO 3)2 + H 2↑ Fe(HCO 3)2水解、空气氧化、风吹日晒得Fe 2O 3。

化学原电池和电解池知识点原电池和电解池是化学中两个重要的概念,两者的区别在于其电化学反应的方向。
本文将介绍原电池和电解池的基本概念、工作原理、以及一些相关实验和应用。
一、原电池原电池是指能够产生电流的装置,由电池内部的氧化还原(redox)反应释放出电子,从而产生电势差,并推动电流在电路中流动。
在原电池中,产生电流的反应是不可逆的,电极上的材料一旦被消耗,电池就无法再产生电流。
原电池也叫做伏安电池或电化学电池。
1. 基本概念(1)电极原电池中的电极一般由金属或导电材料制成,分为阳极和阴极两种。
阳极是电池的正极,是一个能够氧化的电极,在化学变化中会释放出电子。
阴极是电池的负极,是一个容易被还原的电极,在化学变化中会吸收电子。
(2)电解质电解质是电池中起电离导电作用的化学物质,能够分解成离子,从而产生电荷泵效应。
常用的电解质包括酸、碱、盐等。
(3)电动势电动势是指电池产生电流的能力,是一个能够推动电流流动的力量。
单位为伏特(V),一般用符号E表示。
在原电池中,电动势是由电池两极之间的电势差产生的。
2. 工作原理锌铜电池是最简单的原电池之一,由一个锌(Zn)电极和一个铜(Cu)电极以及一个电解质(如盐酸)组成。
阳极为锌电极,阴极为铜电极,电解质中含有氯离子和氢离子。
当锌电极和铜电极连接起来时,锌原子向氯离子释放电子,形成锌离子和电子。
电子从锌电极流向铜电极,由于电子流向铜电极,就形成了电流。
在铜电极上,铜离子由于吸收了电子而被还原成为铜原子。
锌电极逐渐消耗,铜电极上的铜原子逐渐增多。
当锌电极完全消耗时,电池停止工作。
铅酸电池是一种常见的存储电池,由铅(Pb)的阴极、氧化铅(PbO2)的阳极和硫酸(H2SO4)的电解质组成。
在电池工作时,硫酸电解质会溶解掉氧化铅阳极上的物质,同时,铅阴极上的铅物质也会随着电池工作逐渐脱落。
铅酸电池是一种可逆反应,即可以通过外部电源来反向充电。
在充电状态下,电池的阴极和阳极会反转,电池会从外部电源吸收电能,并将电能存储在电池中。



原电池和电解池---过关讲解一、原电池;原电池的工作原理原电池反应属于放热的氧化还原反应,但区别于一般的氧化还原反应的是,电子转移不是通过氧化剂和还原剂之间的有效碰撞完成的,而是还原剂在负极上失电子发生氧化反应,电子通过外电路输送到正极上,氧化剂在正极上得电子发生还原反应,从而完成还原剂和氧化剂之间电子的转移。
两极之间溶液中离子的定向移动和外部导线中电子的定向移动构成了闭合回路,使两个电极反应不断进行,发生有序的电子转移过程,产生电流,实现化学能向电能的转化。
从能量转化角度看,原电池是将化学能转化为电能的装置;从化学反应角度看,原电池的原理是氧化还原反应中的还原剂失去的电子经导线传递给氧化剂,使氧化还原反应分别在两个电极上进行。
原电池的构成条件有三个:(1)电极材料由两种金属活动性不同的金属或由金属与其他导电的材料(非金属或某些氧化物等)组成。
(2)两电极必须浸泡在电解质溶液中。
(3)两电极之间有导线连接,形成闭合回路。
只要具备以上三个条件就可构成原电池。
而化学电源因为要求可以提供持续而稳定的电流,所以除了必须具备原电池的三个构成条件之外,还要求有自发进行的氧化还原反应。
也就是说,化学电源必须是原电池,但原电池不一定都能做化学电池。
形成前提:总反应为自发的氧化还原反应电极的构成:a.活泼性不同的金属—锌铜原电池,锌作负极,铜作正极;b.金属和非金属(非金属必须能导电)—锌锰干电池,锌作负极,石墨作正极;c.金属与化合物—铅蓄电池,铅板作负极,二氧化铅作正极;d.惰性电极—氢氧燃料电池,电极均为铂。
电解液的选择:电解液一般要能与负极材料发生自发的氧化还原反应。
原电池正负极判断:负极发生氧化反应,失去电子;正极发生还原反应,得到电子。
电子由负极流向正极,电流由正极流向负极。
溶液中,阳离子移向正极,阴离子移向负极电极反应方程式的书写负极:活泼金属失电子,看阳离子能否在电解液中大量存在。
如果金属阳离子不能与电解液中的离子共存,则进行进一步的反应。
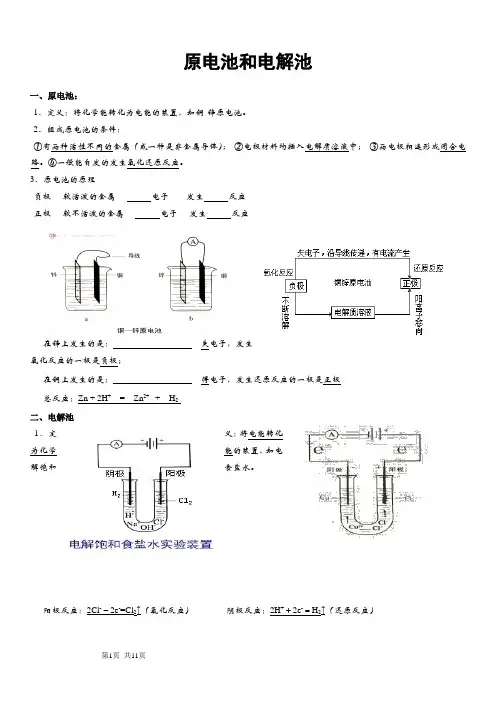
原电池和电解池一、原电池:1、定义:将化学能转化为电能的装置,如铜-锌原电池。
2、组成原电池的条件:①有两种活性不同的金属(或一种是非金属导体);②电极材料均插入电解质溶液中;③两电极相连形成闭合电路。
④一般能自发的发生氧化还原反应。
3、原电池的原理负极----较活泼的金属---- 电子------发生反应正极----较不活泼的金属---- 电子----发生反应在锌上发生的是:失电子,发生氧化反应的一极是负极;在铜上发生的是:得电子,发生还原反应的一极是正极总反应:Zn + 2H+= Zn2+ + H2二、电解池1.定义:将电能转化为化学能的装置,如电解饱和食盐水。
阳极反应:2Cl--2e-=Cl2↑(氧化反应)阴极反应:2H++2e-=H2↑(还原反应)总反应:2NaCl+2H2O2NaOH+H2↑+Cl2↑注意:①电流必须是直流②熔融态的电解质也能被电解③阴极上放电的先后顺序是:Ag+>Hg2+>Fe3+>Cu2+>(H+)>Fe2+>Zn2+;阳极上放电的先后顺序是:活泼金属电极›S2->I->Br->Cl->OH ->(F-、NO3-、SO42-等)(惰性电极)④用石墨、金、铂等还原性很弱的材料制做的电极叫做惰性电极,理由是它们在一般的通电条件下不发生化学反应。
用铁、锌、铜、银等还原性较强的材料制做的电极又叫做活性电极,它们做电解池的阳极时,先于其他物质发生氧化反应。
电解的电极反应式的书写思路与步骤:分电极(判断正负极)-----析溶液(分析电解质溶液中含有哪些离子)---判流向(判断电子流动方向、离子移动方向)-----断微粒(确定在两极上反应的是什么微粒)----写电极(书写电极反应方程式)---写方程(书写电解质电解的化学方程式或离子方程式)1)电解时溶液pH值的变化规律电解质溶液在电解过程中,有时溶液pH值会发生变化。
判断电解质溶液的pH值变化,有时可以从电解产物上去看。
①若电解时阴极上产生H2,阳极上无O2产生,电解后溶液pH值增大;②若阴极上无H2,阳极上产生O2,则电解后溶液pH值减小;③若阴极上有H2,阳极上有O2,且V(H2)=2V(O2),则有三种情况:a 如果原溶液为中性溶液,则电解后pH值不变;b 如果原溶液是酸溶液,则pH值变小;c 如果原溶液为碱溶液,则pH值变大;④若阴极上无H2,阳极上无O2产生,电解后溶液的pH可能也会发生变化。

原电池和电解池知识点一、原电池1.原理:原电池利用化学反应的放电过程产生电能。
化学反应中,发生氧化反应的电极称为阳极,发生还原反应的电极称为阴极。
阳极和阴极之间通过导电介质(如电解质溶液)连接起来,形成一个闭合的电路。
在化学反应过程中,氧化反应释放出的电子从阳极流出,经过外部电路进入阴极,参与还原反应。
同时,电解质中的阳离子在阴极处得到电子而还原,而阴离子则在阳极处失去电子而氧化,完成整个电池的放电过程。
2.构造:原电池一般由两个不同的电金属和一个电解质溶液组成。
电金属通常选择容易氧化(失去电子)而不容易被还原(得到电子)的金属。
常用的原电池有干电池(如锌-碳电池,锌-锰电池)、铅蓄电池、锂电池等。
阳极和阴极通常以导电材料(如金属箔)制成,再涂覆上催化剂,以促进氧化和还原反应的发生。
电解质的选择取决于所使用的金属和化学反应的特点。
3.应用:原电池广泛应用于我们的日常生活和工业生产中。
干电池被用于给家电产品、手动工具等提供电源。
铅蓄电池被用于汽车、UPS电源等领域。
锂电池被广泛应用于便携式设备(如手机、笔记本电脑)和电动车等。
二、电解池1.原理:电解池是一种将电能转化为化学能的装置。
它利用外部电源的电能驱动化学反应,使一种物质在阳极发生氧化反应,而在阴极发生还原反应。
与原电池类似,电解池的阳极和阴极通过电解质连接起来,形成一个闭合的电路。
2.构造:电解池一般由电解槽(容器)、两个电极和电解质组成。
电解槽通常由耐腐蚀的材料(如玻璃或塑料)制成,以容纳电解质溶液。
两个电极一般由导电性能良好的材料制成,如铂或金属箔。
电解质的选择取决于所需的化学反应。
3.应用:电解池在生产和实验室中有广泛的应用。
它可以用来电镀、电解制取金属、电解水制氢氧化钠等。
工业上最常见的应用是电解铜、电解钯、电解腐蚀金属表面等。
总结:原电池和电解池是两种常见的电化学装置。
原电池将化学能转化为电能,而电解池将电能转化为化学能。
原电池利用化学反应的放电过程产生电能,结构上由两个不同的电金属和一个电解质溶液组成。
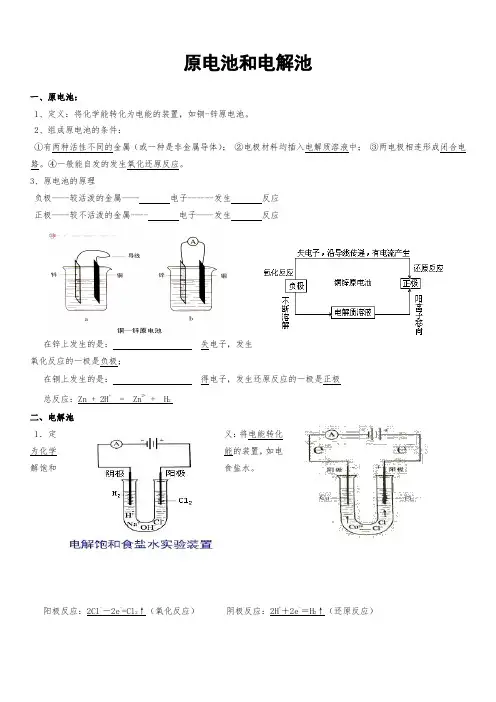
原电池和电解池一、原电池:1、定义:将化学能转化为电能的装置,如铜-锌原电池。
2、组成原电池的条件:①有两种活性不同的金属(或一种是非金属导体);②电极材料均插入电解质溶液中;③两电极相连形成闭合电路。
④一般能自发的发生氧化还原反应。
3、原电池的原理负极----较活泼的金属---- 电子------发生反应正极----较不活泼的金属---- 电子----发生反应在锌上发生的是:失电子,发生氧化反应的一极是负极;在铜上发生的是:得电子,发生还原反应的一极是正极总反应:Zn + 2H+ = Zn2+ + H2二、电解池1.定义:将电能转化为化学能的装置,如电解饱和食盐水。
阳极反应:2Cl--2e-=Cl2↑(氧化反应)阴极反应:2H++2e-=H2↑(还原反应)总反应:2NaCl+2H2O2NaOH+H2↑+Cl2↑注意:①电流必须是直流②熔融态的电解质也能被电解③阴极上放电的先后顺序是:Ag+>Hg2+>Fe3+>Cu2+>(H+)>Fe2+>Zn2+;阳极上放电的先后顺序是:活泼金属电极›S2->I->Br->Cl->OH ->(F-、NO3-、SO42-等)(惰性电极)④用石墨、金、铂等还原性很弱的材料制做的电极叫做惰性电极,理由是它们在一般的通电条件下不发生化学反应。
用铁、锌、铜、银等还原性较强的材料制做的电极又叫做活性电极,它们做电解池的阳极时,先于其他物质发生氧化反应。
电解的电极反应式的书写思路与步骤:分电极(判断正负极)-----析溶液(分析电解质溶液中含有哪些离子)---判流向(判断电子流动方向、离子移动方向)-----断微粒(确定在两极上反应的是什么微粒)----写电极(书写电极反应方程式)---写方程(书写电解质电解的化学方程式或离子方程式)1)电解时溶液pH值的变化规律电解质溶液在电解过程中,有时溶液pH值会发生变化。
判断电解质溶液的pH值变化,有时可以从电解产物上去看。

原电池和电解池知识点一.原电池和电解池的比较:二.原电池正负极的判断:⑴根据电极材料判断:活泼性较强的金属为负极,活泼性较弱的或者非金属为正极。
⑵根据电子或者电流的流动方向:电子流向:负极→正极。
电流方向:正极→负极。
⑶根据电极变化判断:氧化反应→负极;还原反应→正极。
⑷根据现象判断:电极溶解→负极;电极重量增加或者有气泡生成→正极。
⑸根据电解液内离子移动的方向判断:阴离子→移向负极;氧离子→移向正极。
三.电极反应式的书写:*注意点:1.弱电解质、气体、难溶物不拆分,其余以离子符号表示;2.注意电解质溶液对正负极的影响;3.遵守电荷守恒、原子守恒,通过添加H+ 、OH- 、H2O 来配平1.负极:⑴负极材料本身被氧化:①如果负极金属生成的阳离子与电解液成分不反应,则为最简单的:M-n e-=M n+如:Zn-2 e-=Zn2+②如果阳离子与电解液成分反应,则参与反应的部分要写入电极反应式中:如铅蓄电池,Pb+SO42--2e-=PbSO4⑵负极材料本身不反应:要将失电子的部分和电解液都写入电极反应式,如燃料电池CH4-O2(C作电极)电解液为KOH:负极:CH4+10OH-8 e-=C032-+7H2O2.正极:⑴当负极材料能自发的与电解液反应时,正极则是电解质溶液中的微粒的反应,H2SO4电解质,如2H++2e=H2 CuSO4电解质: Cu2++2e= Cu⑵当负极材料不与电解质溶液自发反应时,正极则是电解质中的O2反正还原反应①当电解液为中性或者碱性时,H2O参加反应,且产物必为OH-,如氢氧燃料电池(KOH电解质)O2+2H2O+4e=4OH-②当电解液为酸性时,H+参加反应,产物为H2O如氢氧燃料电池(KOH电解质) O2+4O2+4e=2H2O四.常见的原电池1.银锌电池:(负极—Zn、正极--Ag2O、电解液NaOH )负极:Zn+2OH––2e-== Zn(OH)2 (氧化反应)正极:Ag2O + H2O + 2e-== 2Ag + 2 OH-(还原反应)化学方程式Zn + Ag2O + H2O== Zn(OH)2 + 2Ag2.铝–空气–海水(负极--铝、正极--石墨、铂网等能导电的惰性材料、电解液--海水)负极:4Al-12e-==4Al3+ (氧化反应)正极:3O2+6H2O+12e-==12OH-(还原反应)总反应式为:4Al+3O2+6H2O===4Al(OH)3(铂网增大与氧气的接触面)——海洋灯标电池装置原电池电解池实例原理使氧化还原反应中电子作定向移动,从而形成电流。

高考电化学知识点总结1.原电池和电解池的比较:2原电池正负极的判断:⑴根据电极材料判断:活泼性较强的金属为负极,活泼性较弱的或者非金属为正极。
⑵根据电子或者电流的流动方向:电子流向:负极→正极。
电流方向:正极→负极。
⑶根据电极变化判断:氧化反应→负极;还原反应→正极。
⑷根据现象判断:电极溶解→负极;电极重量增加或者有气泡生成→正极。
⑸根据电解液内离子移动的方向判断:阴离子→移向负极;氧离子→移向正极。
3电极反应式的书写:负极:⑴负极材料本身被氧化:①如果负极金属生成的阳离子与电解液成分不反应,则为最简单的:M-n e-=M n+如:Zn-2 e-=Zn2+②如果阳离子与电解液成分反应,则参与反应的部分要写入电极反应式中:如铅蓄电池,Pb+SO42--2e-=PbSO4⑵负极材料本身不反应:要将失电子的部分和电解液都写入电极反应式,如燃料电池CH4-O2(C作电极)电解液为KOH:负极:CH4+10OH-8 e-=C032-+7H2O 正极:⑴当负极材料能自发的与电解液反应时,正极则是电解质溶液中的微粒的反应,H2SO4电解质,如2H++2e=H2CuSO4电解质:Cu2++2e= Cu⑵当负极材料不与电解质溶液自发反应时,正极则是电解质中的O2反正还原反应①当电解液为中性或者碱性时,H2O比参加反应,且产物必为OH-,如氢氧燃料电池(KOH电解质)O2+2H2O+4e=4OH-②当电解液为酸性时,H +比参加反应,产物为H 2O O 2+4O 2+4e=2H 2O4.化学腐蚀和电化腐蚀的区别5.吸氧腐蚀和析氢腐蚀的区别6.金属的防护⑴改变金属的内部组织结构。
合金钢中含有合金元素,使组织结构发生变化,耐腐蚀。
如:不锈钢。
⑵在金属表面覆盖保护层。
常见方式有:涂油脂、油漆或覆盖搪瓷、塑料等;使表面生成致密氧化膜;在表面镀一层有自我保护作用的另一种金属。
⑶电化学保护法①外加电源的阴极保护法:接上外加直流电源构成电解池,被保护的金属作阴极。