2020-2021年化学计算题中考试题分类汇编
- 格式:doc
- 大小:372.00 KB
- 文档页数:8



一、中考初中化学计算题1.取某碳酸钠样品(含有一定量的氯化钠)15g,加入80g水,固体完全溶解,再向其中加入76g氯化钙溶液,两者恰好完全反应,过滤后得到161g滤液。
请计算:(1)产生沉淀的质量是________g;(2)反应后所得溶液中溶质的质量分数_______。
【答案】10g 10%【解析】【分析】(1)根据氯化钠、碳酸钠的性质,氯化钠不能与加入的氯化钙发生反应,碳酸钠与氯化钙生成碳酸钙沉淀和氯化钠,根据质量守恒计算碳酸钙沉淀的质量;(2)恰好完全反应后所得溶液为氯化钠溶液,此时溶液中的溶质氯化钠由原固体中的氯化钠和反应后生成的氯化钠两部分构成。
【详解】(1)产生沉淀的质量为15g+80g+76g-161g=10g;(2)设Na2CO3的质量为x,生成NaCl的质量为y,2323Na CO+CaCl=CaCO+2NaCl106100117x10g y106100117==x10g yx=10.6g,y=11.7g反应后所得溶液中溶质的质量=15g-10.6g+11.7g=16.1g;反应后所得溶液中溶质质量分数为16.1g161g×100%=10%答:(1)产生沉淀的质量为10g;(2)反应后所得溶液中溶质质量分数为10%.【点睛】本道题比较难,难点有两个:一是滤液中的溶质氯化钠包括原混合物中的氯化钠和反应生成的氯化钠;二是所得滤液的质量比较难算,不是用溶质的质量+溶剂的质量,而是将所加入的物质的质量全部加起来,再减去生成沉淀的质量。
2.在一烧杯中盛有24.3g Na2SO4和NaCl组成的固体混合物,加入100g水使Na2SO4和NaCl全部溶解。
向其中逐渐滴加溶质质分数为20%的氯化钡溶液,生成沉淀的总质量与所滴入氯化钡溶液的质量关系曲线如图所示。
(1)请分析当BaCl2溶液滴加到B点时,溶液中的溶质是。
(2)请计算当滴加BaCl2溶液至图中A点时,所得溶液的溶质质量分数(计算结果保留一位小数)。
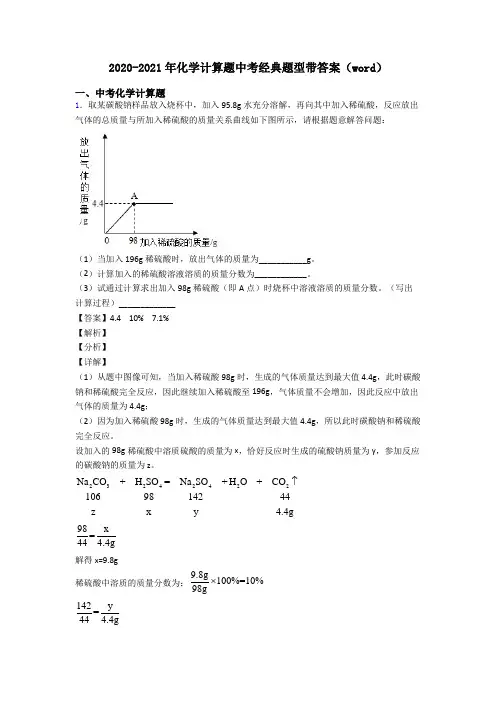
2020-2021年化学计算题中考经典题型带答案(word )一、中考化学计算题1.取某碳酸钠样品放入烧杯中,加入95.8g 水充分溶解,再向其中加入稀硫酸,反应放出气体的总质量与所加入稀硫酸的质量关系曲线如下图所示,请根据题意解答问题:(1)当加入196g 稀硫酸时,放出气体的质量为___________g 。
(2)计算加入的稀硫酸溶液溶质的质量分数为____________。
(3)试通过计算求出加入98g 稀硫酸(即A 点)时烧杯中溶液溶质的质量分数。
(写出计算过程)_____________ 【答案】4.4 10% 7.1% 【解析】 【分析】 【详解】(1)从题中图像可知,当加入稀硫酸98g 时,生成的气体质量达到最大值4.4g ,此时碳酸钠和稀硫酸完全反应,因此继续加入稀硫酸至196g ,气体质量不会增加,因此反应中放出气体的质量为4.4g ;(2)因为加入稀硫酸98g 时,生成的气体质量达到最大值4.4g ,所以此时碳酸钠和稀硫酸完全反应。
设加入的98g 稀硫酸中溶质硫酸的质量为x ,恰好反应时生成的硫酸钠质量为y ,参加反应的碳酸钠的质量为z 。
23242422Na CO Na SO +H SO =++1069814244zxyH C gO O 4.4↑98x =44 4.4g解得x=9.8g稀硫酸中溶质的质量分数为:9.8g100%=10%98g⨯ 142y=44 4.4g解得y=14.2g106z=44 4.4g解得z=10.6g(3)加入98g稀硫酸溶液时的溶液为碳酸钠和稀硫酸恰好完全反应时的溶液,溶液中溶质的质量分数为:14.2g100%=7.1% 10.6g+95.8g+98g-4.4g⨯答:稀硫酸的溶质质量分数为10%;A点时烧杯中溶液的溶质质量分数为7.1%。
2.徐州地区石灰石资源丰富。
某化学兴趣小组称取4.0g石灰石样品,把40g稀盐酸分4次加入样品中(假设杂质不反应也不溶解),得实验数据如下:请计算:(1)4.0g石灰石样品中碳酸钙的质量是____g。

一、中考初中化学计算题1.小新用20g含碳酸钠53%的天然碱制取氢氧化钠用于制作“叶脉书签”(杂质不参加反应)。
操作过程如下:请计算:(1)20g样品中碳酸钠的质量为__________g;(2)反应后所得滤液中氢氧化钠的质量分数为多少?__________(写出计算过程)(3)将200g滤液浓缩制成“叶脉书签”所需质量分数为10%的氢氧化钠溶液,需蒸发水__________g.【答案】10.6 4% 120【解析】【分析】【详解】(1)20g样品中碳酸钠的质量为20g×53%=10.6 g(2)解:设反应生成氢氧化钠的质量为x;Na CO+Ca(OH)=CaCO+2NaOH23231068010.6g x106/10.6g=80/x 解得x=8 g氢氧化钠的质量分数=8g/200g×100%=4%答:反应后所得滤液中氢氧化钠的质量分数为4% 。
(3)将200g滤液浓缩制成“叶脉书签”所需质量分数为10%的氢氧化钠溶液,需蒸发水的质量为X根据溶液稀释前后溶质的质量不变有:200g ×4%=(200g-X) ×10%X=120g2.为测定一瓶久置的烧碱中氢氧化钠的含量,某同学取25.0g样品,溶于水得到100g溶液,再加入100g足量稀硫酸,充分反应至不再产生气体,测得溶液质量为197.8g。
请计算:(1)反应产生CO2的质量。
(2)样品中NaOH的质量分数(结果保留至0.1%)。
(3)最后所得溶液中的钠元素的质量(结果保留至0.1)。
【答案】(1)2.2g;(2)78.8%;(3)13.6g【解析】(1)根据质量守恒定律,反应过程中所生成的气体的质量等于反应前后溶液质量的减少;(2)样品中NaOH的质量分数等于样品中NaOH的质量除以样品的总质量,所以我们可以根据上一步所求得二氧化碳的质量,根据质量守恒定律,求得样品中NaOH的质量,而后再求样品中NaOH的质量分数;(3)根据NaOH的质量、碳酸钠的质量分别乘以它们的质量分数可求得钠元素的质量;解:(1)根据质量守恒定律,反应前后溶液质量的减少就等于反应过程中所生成的气体的质量,所以反应产生的CO2的质量为100 g+100 g-197.8 g=2.2g。

2020-2021年化学计算题压轴试题分类汇编及答案(word )一、中考化学计算题1.氧化亚铜(Cu 2O )可用于生产船底防污漆,防止海生物对船舶设备的污损。
现将Cu 2O 和Cu 的固体混合物20g 放入烧杯中,加入质量分数为24.5%的稀硫酸50g ,恰好完全反应。
已知:Cu 2O+H 2SO 4═CuSO 4+Cu+H 2O .计算:(1)所加稀硫酸中溶质的质量为_____g 。
(2)原混合物中Cu 2O 与Cu 的质量比_____(写出计算过程,结果用最简整数比表示) (3)在图中画出向20g Cu 2O 和Cu 的固体混合物中逐滴加入24.5%的稀硫酸至过量,铜的质量变化曲线_____。
【答案】12.25 9: 1 。
【解析】 【分析】根据加入的硫酸中溶质的质量和对应的化学方程式求算氧化亚铜的质量,进而求算对应的比值以及画图。
【详解】(1)所加稀硫酸中溶质的质量为24.5%×50g =12.25g ;故填:12.25 (2)设原混合物中Cu 2O 的质量为x ,生成的铜的质量为y 。
224421449864x 12.Cu O+H SO CuSO +C 2u +H 5Og y═ 1449864==x 12.25g y解得:x =18 g ;y =8g ; 原混合物中Cu 2O 与Cu 的质量比为18 g :(20 g ﹣18 g )=9:1;故填:9:1(3)没加入硫酸时,铜的质量为2g ,加入到50g 稀硫酸时铜的质量为2g+8g =10g 。
如下图所示;故填:【点睛】根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整。
2.取一定量的木炭在氧气中燃烧,生成23.2 g气体(氧气已完全反应)。
将气体通入过量的澄清石灰水中,生成40 g沉淀。
计算:(1)生成气体的成分及质量___________。
(2)生成气体中碳元素的质量分数_________。

2020-2021 年化学计算题中考试题分类汇编一、中考化学计算题1.某石化厂有一种石油产品含有质量分数为 4.9%的剩余硫酸,过去他们都是用NaOH 溶液来冲洗这些硫酸。
请你计算:(1)若要冲洗 1000kg 的这类石油产品,需要 _____kg 的 NaOH。
(2)该石化厂进行了技术改造,采纳Ca(OH)2中和这些剩余硫酸。
每办理1000kg 这类产品,他们能够节俭多少经费_____?请你写出详细的计算过程。
工业级的NaOH 和 Ca(OH)2的最新市场批发价以下表:试剂Ca(OH)2NaOH价钱(元 /kg) 1.00 6.00(3)请你在图中画出氢氧化钠和氢氧化钙办理1000kg 该石油产品时,剩余硫酸溶质的质量变化曲线;氢氧化钠用虚线表示,氢氧化钙用实线表示。
_____(请你注明详细的坐标)【答案】 40203 元【分析】【详解】1000kg 的这类石油产品所含硫酸的质量为1000kg × 4.9%=49kg设耗费的氢氧化钠的质量为x,耗费的氢氧化钙的质量为y依据 2NaOH+H2SO4=Na2SO4 +2H2O 和 Ca( OH)2+H2SO4=CaSO4+2H2O 2NaOH : H 2SO4 : Ca(OH)2可得关系式80x9849kg74y80 =98 x 49kg = 74yx=40kgy=37kg每理 1000kg 种品,他能够 6.00 元 /kg ×40kg-1.00元/kg ×37kg=203元中画出用氧化和氧化理1000kg 石油品,剩余硫酸溶的量化曲;氧化用虚“⋯”表示,氧化用“一”表示,答:( 1)若要冲洗1000kg 的种石油品,需要40kg 的 NaOH。
(2)石化厂行了技改造,采纳Ca( OH)2中和些剩余硫酸。
每理1000kg 种品,他能够203 元。
(3)剩余硫酸溶的量化曲;氧化用虚“⋯”表示,氧化用“一”表示,2.某化学趣小同学含有Na2SO4的Na2CO3固体品行了以下研究。

2020-2021年中考化学计算题汇编一、中考化学计算题1.化学兴趣小组取26g石灰石样品(杂质不参加反应,也不溶于水)放在烧杯中,向其中加入90g稀盐酸,恰好完全反应,反应后烧杯中物质的总质量为105g,计算:(1)生成二氧化碳的质量是____。
(2)反应后所得溶液的溶质质量分数是____。
【答案】(1)11克(2) 26.7%【解析】试题解析:由质量守恒定律可以知道反应前的各物质的总质量等于反应后各物质的总质量的,所以二氧化碳的质量=26+90-105=11克,反应后的溶质是CaCl2,而溶液的质量等于105克减去石灰石中的不反应的杂质的质量,设:石灰石中CaCO3质量为X,生成的CaCl2质量为Y,CaCO3+ 2HCl==CaCl2 + CO2↑ + H2O100 111 44X Y 11克列比例式:100:X=44::11克解得:X=25克111:Y=44:11克解得:Y="27.75" 克反应后所得溶液的溶质质量分数=27.75/105-(26-25)×100%≈26.7%考点:质量守恒定律及其根据化学方程式的计算溶液的相关计算2.某化学兴趣小组用化学方法测定一种钢样品中铁的含量。
同学们称取了5.7g钢样品,投入装有10.0g稀盐酸(足量)的烧杯(烧杯质量也为10.0g)中。
在化学反应过程中对烧杯(包括溶液和残余固体)进行了四次称量,记录如下表:(1)反应中产生氢气_________克,这种钢样品中铁的含量是多少?(精确到0.1%) ______(2)钢的类型分为:含碳质量(C%)0.03%~0.3%为低碳钢;0.3%~0.6%为中碳钢;0.6%~2%为高碳钢。
假设残留在烧杯中的黑色固体全部是炭,则这种钢属于________。
(3)有同学提出:灼烧可使钢中的炭变为CO2挥发掉,灼烧后钢样品质量会减轻。
可是他们将一定量的钢样品灼烧后,发现质量反而增加了很多。

2020-2021年化学计算题中考试题分类汇编(word )一、中考化学计算题1.某校兴趣小组在实验室中完成制取氧气的实验。
他们取氯酸钾和二氧化锰的混合物共6g 放入大试管中加热,并在同时测定试管中剩余固体物质的质量(如下表),请分析表中数据,完成下列问题:(1)完全反应时,生成氧气的质量为_____g ;(2)原混合物中氯酸钾的质量分数是____________?(计算结果精确到0.1%) 【答案】1.92g 81.7% 【解析】(1)氯酸钾发生分解反应生成氯化钾和氧气,二氧化锰作催化剂,反应前后二氧化锰的质量不变,根据质量守恒定律,生成氧气的质量为:6g-4.08g=1.92g 。
(2)设原混合物中氯酸钾的质量为x 。
2KClO 32MnO Δ2KCl+3O 2↑ 245 96 x 1.92g24596=1.92x g,解得x=4.9g 原混合物中氯酸钾的质量分数是:4.96gg×100%=81.7%点睛:首先根据质量守恒定律求出氧气的质量,然后根据化学方程式找出氧气与氯酸钾的质量关系,利用反应中物质的质量比不变进行列比例式计算,易错点是,由质量比算数错误,所以这一步一定要仔细检查。
2.某纯碱样品中含有少量氯化钠。
现称量该样品15.4g 放入烧杯中,再向其中加入一定溶质质量分数的稀盐酸至100g 时恰好完全反应。
此时烧杯内的物质质量为111g 。
试计算: (1)碳酸钠中钠元素、碳元素、氧元素的质量比为__________;(化为最简比) (2)反应后生成的气体质量为_________g ;(3)恰好完全反应时所得溶液中溶质的质量分数________。
(计算结果精确到0.1%) 【答案】23:6:24。
4.4; 14.9% 【解析】 【分析】 【详解】(1)碳酸钠化学式为Na 2CO 3,其中钠元素、碳元素、氧元素的质量比=23×2:12×1:16×3=23:6:24;(2)碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,根据质量守恒定律,生成二氧化碳气体的质量=15.4g+100g-111g=4.4 g;(3)假设样品中碳酸钠质量为x,生成的氯化钠质量为y,则有:==解得x=10.6g,y=11.7g故样品中氯化钠质量=15.4g-10.6g=4.8g,反应后溶液中溶质为氯化钠,其总质量=4.8g+11.7g=16.5g,故恰好完全反应时所得溶液中溶质的质量分数=×100%≈14.9%。

2020-2021年化学计算题中考压轴题分类汇编一、中考化学计算题1.20g含杂质(杂质不溶于水,也不溶于酸)的锌样品,与一定质量的稀硫酸恰好完全反应,所得溶液质量为80.5g,同时生成氢气0.4g。
试计算:(1)样品中锌的质量分数是_____;(2)完全反应后生成溶液中溶质的质量分数是_____;(3)所用稀硫酸的质量分数是_____(计算结果保留到0.01%)。
【答案】65% 40% 28.87%【解析】【分析】样品中的锌能与稀硫酸反应生成硫酸锌和氢气。
【详解】设样品中锌的质量为x;生成的硫酸锌的质量为y;硫酸中溶质的质量为z;2442Zn+H SO=ZnSO+H65981612x z y0.4g↑65981612===x z y0.4gx=13gy=32.2gz=19.6g(1)样品中锌的质量分数为13g×100%=65% 20g(2)完全反应后生成溶液中溶质的质量分数为32.2g×100%=40% 80.5g(3)所用稀硫酸的质量分数为19.6g×100%28.87% 80.5g+0.4g-13g≈答:样品中锌的质量分数为65%,完全反应后生成溶液中溶质的质量分数为40%,所用稀硫酸的质量分数为28.87%。
【点睛】利用化学方程式根据锌与生成的氢气的质量比求出锌的质量;反应后的溶液是硫酸锌溶液,利用化学方程式可计算出溶质硫酸锌的质量。
2.实验室有化学实验考试后留下混有少量食盐的小苏打样品。
现称取样品10克,加入某溶质质量分数的稀盐酸90克,至充分反应不再有气泡产生为止,称得剩余溶液质量为95.6克。
求:(1)生成气体的质量____。
(2)反应后所得溶液的溶质质量分数____。
(结果保留至0.1%)【答案】4.4g 7.8%【解析】【详解】(1)生成气体的质量为10g+90g-95.6g=4.4g。
(2)反应后所得溶液的溶质质量为x,样品中碳酸钠的质量为y,322NaHCO+HCl=NaCl+H O+CO8458.544y x 4.4g58.54484==x 4.4g y x=5.85g y=8.4g ↑,反应后所得溶液的溶质质量分数为5.85g10g8.4g100%7.8% 90g10g 4.4g+-⨯≈+-。

2020-2021年化学计算题中考试题分类汇编经典一、中考化学计算题1.现有铜与金属X 组成的混合物粉末,金属X 是镁、铁、锌中的一种.利用该混合物进行如下实验:实验步骤及数据:取该混合物粉末8.0g 放入烧杯中,将140.0g 溶质质量分数为14.0%的稀硫酸平均分四次加入该烧杯中,充分反应后,测得烧杯内剩余固体的质量数据如下表:实验分析:通过计算,求:(1)该混合物粉末中铜的质量分数为_____; (2)该混合物是由铜粉和_____组成的;(3)第三次加入硫酸充分反应后,所得溶液中溶质的质量分数是多少?_____(写出计算过程)(4)若用溶质的质量分数为98%、密度为1.84g/cm ﹣3的浓硫酸来配制本实验中所用的稀硫酸,则需要取浓硫酸多少毫升?_____同时加入水多少毫升?_____(写出计算过程) 【答案】52.5% 镁粉 16.6% 10.87m 120mL 【解析】 【分析】 【详解】(1)铜在金属活动顺序中排在氢之后,铜与酸不能反应,反应后剩余固体质量4.2g 即为其质量。
该混合物粉末中铜的质量分数=4.2g100%52.5%8g⨯= ; (2)第一次所加稀硫酸140g ÷4=35g 完全反应时,消耗金属的质量=8.0g ﹣6.8g =1.2g ; 由于镁、铁、锌三种金属在反应中均呈+2价,设金属的相对原子质量为m ,则2442=m 981.2g 35M +H SO MSO g 14%+H ↑⨯ m 1.2g=9835g 14%⨯ m =24,所以金属为镁; (3)第三次加入硫酸后,一共加入了35g ×3=105g 硫酸设:加入105g 稀硫酸充分反应生成氢气的质量为x ,生成硫酸镁的质量为y 。
2442Mg +H SO MgSO =241202(8.0g-4.4g +H )yx↑248.0g-4.4g =2xx =0.3g , 248.0g-4.4g =120yy =18g 所得溶液的质量=(8.0g ﹣4.4g )+105g ﹣0.3g =108.3g ;溶质的质量分数=18g100%16.6%108.3g⨯≈。
一、中考初中化学计算题1.某纯碱样品中含有少量氯化钠。
为测定样品中碳酸钠的质量分数,现称取该样品11g ,加入到盛有50g 稀盐酸的烧杯中,恰好完全反应,最后称得烧杯中溶液的质量为56.6g 。
计算:(1)完全反应后生成CO 2的质量_______;(2)纯碱样品中碳酸钠的质量分数_________(结果精确到0.1%) 【答案】4.4g 96.4% 【解析】 【分析】 【详解】(1)根据质量守恒定律,完全反应后生成二氧化碳的质量=11g+50g-56.6g=4.4g (2)设参加反应的碳酸钠的质量为x2322Na CO 2HCl 2Na +=++106444.4C CO Ogl H x↑ 106x =444.4gx=10.6g纯碱样品中碳酸钠的质量分数=10.6g11g×100%≈96.4% 答:(1)完全反应后生成CO 2的质量为4.4g ;(2)纯碱样品中碳酸钠的质量分数约为96.4%.2.某碳酸钠样品中含有少量氯化钠。
现称量11 g 该样品放入烧杯中,然后加入一定量溶质的质量分数为14.6%的稀盐酸,至恰好完全反应,去除溶液中的水分,最终得到12.1g 氯化钠固体。
计算:(1)碳酸钠样品中碳酸钠的质量______________(2)反应后所得溶液中溶质的质量分数。
(结果精确到0.1%)_____________ 【答案】10.6g 21.4% 【解析】 【分析】 【详解】设样品中氯化钠的质量为x ,则生成的氯化钠质量为12.1g-x ,样品中碳酸钠的质量为11g-x ,生成的二氧化碳质量为y ,反应中消耗的盐酸质量为z 。
2322Na CO +2HCl =2NaCl +H O +CO 106731174411g-xz 14.6%12.1g-xy↑⨯1067311744 === 11g-x z14.6%12.1g-x y⨯解得x=0.4g;y=4.4g;z=50g则样品中碳酸钠的质量为10.6g反应后所得溶液中溶质质量分数为:12.1g100%11g+50g-4.4g⨯≈ 21.4%答:碳酸钠样品中碳酸钠的质量为10.6g,反应后所得溶液中溶质的质量分数为21.4%。
2020-2021年化学计算题试题分类汇编(word)一、中考化学计算题1.下图所示为实验室中常见的气体制备、干燥、收集和性质实验的部分仪器。
试根据题目要求,回答下列问题:⑴请写出能用装置A制备的一种气体的化学反应方程式_____,该气体可选用装置_____来收集(填装置序号),其选择依据是_____。
⑵小颖同学欲用干燥..、纯净..的一氧化碳气体还原某氧化铜样品(杂质只有铜),并测定其纯度。
(查阅资料)将草酸(H2C2O4)晶体与浓硫酸混合加热,会产生一氧化碳等气体,其反应原理为:H2C2O4浓硫酸CO↑+CO2↑+H2O。
①若小颖同学选用草酸来制取CO,其发生装置她应选择_____(填装置序号)。
(定量实验)②小颖同学先用电子秤称取了1.00g氧化铜样品,放入装置C中的玻璃管内并组装好所有相关仪器,再将草酸分解得到的气体产物按照以下仪器的连接顺序进行实验:混合气体→D→C→E→H,最后,通过测量反应前后装置E的质量变化进行计算。
(已知:CO+CuO ΔCu+CO2)实验过程中,在装置C的大玻璃管内可观察到的现象是_____。
③请你分析上述实验方案存在的不足之处及.对应的改进方法_____。
④实验改进后,小颖同学对实验所得的正确数据进行分析处理(设所发生的反应均完全进行):通过测定,当装置C中的氧化铜全部被还原后,装置E的质量增加了0.33g,则该样品中氧化铜的质量分数为_____(结果精确至0.1%)。
⑤小黄同学提出了异议,他认为若②中实验方案不加以改进,也能正确测算出该样品中氧化铜的纯度,他的计算依据或方法为:_____。
【答案】CaCO3 + 2HCl == CaCl2 + H2O + CO2↑ F 二氧化碳密度比空气大 B 黑色固体变成红色应该装置D前连接装置一个装置E,吸收混合气体中的二氧化碳 60.0% 根据H2C2O4浓硫酸CO↑+CO2↑+H2O,生成的一氧化碳和二氧化碳的分子个数比为1:1的关系,装置E增加的质量的一半就是氧化铜和一氧化碳反应生成的二氧化碳的质量,再根据步骤④的计算方法计算出氧化铜的质量即可【解析】【分析】【详解】⑴装置A 为固液不加热型,可用于实验室制取二氧化碳,化学反应方程式为:CaCO 3 + 2HCl = CaCl 2 + H 2O + CO 2↑;该气体可选用装置F 来收集,选择依据是二氧化碳密度比空气大。
2020-2021年化学计算题中考题集锦(word )一、中考化学计算题1.某化学兴趣小组在实验室用碳酸钠溶液和熟石灰制取少量氢氧化钠溶液,他们的实验过程和相关数据如图所示。
请计算:(1)实验中生成沉淀的质量为___________。
(2)所得氢氧化钠溶液中溶质的质量分数为___________。
【答案】10 10%【解析】【分析】【详解】(1)实验中生成沉淀的质量=195.6g-185.6g=10g(2)设氢氧化钠的质量为x 。
()2332Ca OH + Na CO CaCO + =1002N 8xaOH10g ↓ 10080=10g xx=8g所的溶液的质量=185.6g-105.6g=80g氢氧化钠溶液的溶质质量分数=8g 80g×100%=10% 答:(1)实验中生成沉淀的质量为10g ;(2)所得氢氧化钠溶液中溶质的质量分数为10%。
2.某化学兴趣小组同学对含有Na 2SO 4杂质的Na 2CO 3固体样品进行了以下实验探究。
请根据下图所示的实验过程和提供的数据,回答以下问题。
(1)过程②中产生气体的原因是______。
(2)计算溶液A 的质量(写出计算过程,结果保留一位小数)。
______【答案】①中加入过量的稀硫酸,稀硫酸与碳酸钠反应产生CO 2 106.2g【解析】【分析】【详解】(1)在过程②中加入一定量的Na 2CO 3固体恰好完全反应,说明过程①加入的稀硫酸是过量,所以过程②中产生气体的原因是:①中加入过量的稀硫酸,稀硫酸与碳酸钠反应产生CO 2(2)根据化学反应方程式:Na 2CO 3+ H 2SO 4= Na 2SO 4+ H 2O + CO 2↑中Na 2CO 3与CO 2的质量关系,可求出所加的Na 2CO 3固体质量,进而算出溶液A 的质量设②中加入的碳酸钠的质量为x23242422Na CO +H SO =Na SO +H O +CO 10644x4.4g↑10644=x 4.4gx =10.6 gm(溶液A) =100g + 10.6 g – 4.4 g =106.2 g答:溶液A 的质量为106.2 g 。
2020-2021年化学计算题中考题集锦经典一、中考化学计算题1.为测定某样品中锌的质量分数,取10g此样品,分五次向其中加入稀硫酸使之充分反应(假设锌的样品中杂质不与稀硫酸反应,且不溶于水),每次加入的稀硫酸质量及测定剩余固体的质量,记录数据如下表:第一次第二次第三次第四次第五次加入稀硫酸的质量/g1010101010剩余固体质量/g8.4 6.8 5.2 3.6 3.6请认真分析表中的数据,回答下列问题:(1)表示样品与稀硫酸恰好完全反应的是上表中第________次操作;(2)计算样品中锌的质量分数;(3)计算实验中所用稀硫酸的溶质质量分数。
【答案】(1)4(2)锌的质量分数(3)设恰好完全反应时消耗硫酸的质量为x【解析】本题考查的是实验数据处理的探究和根据化学反应方程式的计算。
(1)根据金属活动性,锌在活动性顺序中处于H之前,能与稀硫酸反应,而锌的样品中杂质不与稀硫酸反应,且不溶于水。
由记录数据表可知:第五次加入10g稀硫酸时,剩余固体质量不变仍为3.6g,说明混合物中的锌在第四次加酸后就已完全反应,剩余固体为不与硫酸反应的杂质。
另据上表可见,前三次中每加入10g的稀硫酸,都消耗1.6g的锌,二者结合分析故知第四次恰好完全反应。
(2)则样品中锌的质量分数m=(3)设恰好完全反应时消耗硫酸的质量为x65 98(10﹣3.6) X65/98=(10﹣3.6)/xX=9.6g∴所用稀硫酸的溶质质量分数==24℅2.某校化学兴趣小组为了测定某一碳酸钠样品中碳酸钠的质量分数,进行如下实验,取13.25g碳酸钠样品(杂质既不溶于酸也不溶于水)放入烧杯中,加入95.8g水使其完全溶解,再向其中加入稀盐酸,测得反应放出气体的总质量与所加入稀盐酸的质量关系曲线如图所示,请回答:(1)当加入212g稀盐酸时,放出气体的质量为_____g。
(2)碳酸钠样品中碳酸钠的质量分数为多少?_____(写出计算过程)(3)加入106g稀盐酸(即A点)时烧杯中溶液的溶质质量分数为多少?_____(写出计算过程)【答案】4.4g 80% 5.6%【解析】【分析】【详解】(1)根据图像,可以看出当加入106g稀盐酸的时候,反应就结束,产生气体质量为4.4g,所以当加入212g稀盐酸时,放出气体的质量仍然为4.4g(2)发生反应:Na2CO3+2HCl=2NaCl+H2O+CO2↑,根据方程式中碳酸钠与二氧化碳的质量关系可算出碳酸钠的质量,进而可以计算碳酸钠样品中碳酸钠的质量分数,反应后得到的是NaCl溶液,所以也可根据方程式中NaCl与二氧化碳的质量关系,求出溶液中溶质的质量解:设碳酸钠的质量为x,生成的NaCl质量为y。
2020-2021年化学计算题测试题及答案一、中考化学计算题1.某氢氧化钠样品中混有氯化钠,为测定样品中氢氧化钠的质量分数,在 20℃时,称取5g 样品,加入27g 水完全溶解后,缓慢加入稀盐酸,至恰好完全反应时,用去 10%的稀盐酸 36.5g。
(该反应的化学方程式为:NaOH+HCl=NaCl+H2O)试计算:(1)样品中氢氧化钠的质量分数。
(2)反应后所得溶液中溶质的质量分数。
(3)已知 20℃时,氯化钠的溶解度为 36 g,试通过简单计算确定反应后所得溶液是否为20℃时该溶质的饱和溶液。
【答案】80% 10% 不是【解析】恰好完全反应时,消耗氯化氢的质量为:10%×36.5 g3.65g。
设样品中氢氧化钠的质量为x,反应后所得溶液中溶质的质量为yNaOH + HCl = NaCl+ H2O40 36.5 58.5x 3.65g y40/x=36.5/3.65g x=4g58.5/y=36.5/3.65g y=5.85g反应后所得溶液中溶质的质量分数=4g÷5g×100%=80%。
反应后所得溶液中溶质的质量分数5.8554100%10% 52736.5g g gg g g+-⨯=++饱和溶液溶质的质量分数=溶解度÷(溶解度+100g)×100% , 20℃时,20℃时,氯化钠的溶解度为36g,其饱和溶液溶质的质量分数=36g÷(36g +100g)×100%≈26.5%>10%;点睛:方程式的计算,关键根据化学反应方程式找出相关物质的质量关系,利用反应中物质的质量比不变进行列比例计算,易错点是,由方程式求质量比算数错误,所以这一步要仔细检查。
2.工业上“侯氏”制碱法制得的纯碱产品中常含有少量的氯化钠。
为测定纯碱品中碳酸钠的含量,取23克样品置于大烧杯中,然后在滴加稀盐酸,至两者恰好完全反应共滴加稀盐酸255.8g,生成的气体全部逸出,测得反应后烧杯中的溶液质量为270g,计算:(1)生成二氧化碳的质量为_____。
2020-2021年化学计算题中考试题分类汇编一、中考化学计算题1.某石化厂有一种石油产品含有质量分数为4.9%的残余硫酸,过去他们都是用NaOH溶液来清洗这些硫酸。
请你计算:(1)若要清洗1000kg的这种石油产品,需要_____kg的NaOH。
(2)该石化厂进行了技术改造,采用Ca(OH)2中和这些残余硫酸。
每处理1000kg这种产品,他们可以节约多少经费_____?请你写出具体的计算过程。
工业级的NaOH和Ca(OH)2的最新市场批发价如下表:试剂Ca(OH)2NaOH价格(元/kg) 1.00 6.00(3)请你在图中画出氢氧化钠和氢氧化钙处理1000kg该石油产品时,残余硫酸溶质的质量变化曲线;氢氧化钠用虚线表示,氢氧化钙用实线表示。
_____(请你注明具体的坐标)【答案】40 203元【解析】【详解】1000kg的这种石油产品所含硫酸的质量为1000kg×4.9%=49kg设消耗的氢氧化钠的质量为x,消耗的氢氧化钙的质量为y根据2NaOH+H2SO4=Na2SO4+2H2O和Ca(OH)2+H2SO4=CaSO4+2H2O可得关系式为242 2NaOH H SO Ca(OH)809874x49kg y::809874==x49kg yx=40kgy=37kg每处理1000kg这种产品,他们可以节约经费为6.00元/kg×40kg-1.00元/kg×37kg=203元图中画出用氢氧化钠和氢氧化钙处理1000kg该石油产品时,残余硫酸溶质的质量变化曲线;氢氧化钠用虚线“…”表示,氢氧化钙用实线“一”表示,答:(1)若要清洗1000kg的这种石油产品,需要 40kg的NaOH。
(2)该石化厂进行了技术改造,采用Ca(OH)2中和这些残余硫酸。
每处理1000kg这种产品,他们可以节约203元经费。
(3)残余硫酸溶质的质量变化曲线;氢氧化钠用虚线“…”表示,氢氧化钙用实线“一”表示,2.某化学兴趣小组同学对含有Na2SO4杂质的Na2CO3固体样品进行了以下实验探究。
请根据下图所示的实验过程和提供的数据,回答以下问题。
(1)过程②中产生气体的原因是______。
(2)计算溶液A的质量(写出计算过程,结果保留一位小数)。
______【答案】①中加入过量的稀硫酸,稀硫酸与碳酸钠反应产生CO2 106.2g【解析】【分析】【详解】(1)在过程②中加入一定量的Na2CO3固体恰好完全反应,说明过程①加入的稀硫酸是过量,所以过程②中产生气体的原因是:①中加入过量的稀硫酸,稀硫酸与碳酸钠反应产生CO2(2)根据化学反应方程式:Na2CO3+ H2SO4= Na2SO4+ H2O + CO2↑中Na2CO3与CO2的质量关系,可求出所加的Na2CO3固体质量,进而算出溶液A的质量设②中加入的碳酸钠的质量为xNa CO+H SO=Na SO+H O+CO2324242210644x 4.4g10644=x 4.4gx =10.6 gm(溶液A) =100g + 10.6 g – 4.4 g =106.2 g答:溶液A的质量为106.2 g。
3.取一定量的木炭在氧气中燃烧,生成23.2 g气体(氧气已完全反应)。
将气体通入过量的澄清石灰水中,生成40 g沉淀。
计算:(1)生成气体的成分及质量___________。
(2)生成气体中碳元素的质量分数_________。
【答案】CO、CO2的混合气体,其中CO为5.6g,CO2为17.6g 31%【解析】【详解】(1)设生成二氧化碳的质量为x2232 Ca(OH)+CO=CaCO+H O44100x40g↓44100=x40g, x=17.6gCO 的质量=23.2g-17.6g=5.6g;(2)生成气体中碳元素的质量分数= (17.6g× 12100%44⨯+5.6g×1228×100%)÷23.2 g ≈31%;答:此气体为CO、CO2混合气体,其中CO为5.6g,CO217.6g;气体中碳元素的质量分数为31%。
4.某小组同学将530 g碳酸钠溶液加入到280 g石灰乳(水和氢氧化钙的混合物)中,使之恰好完全反应,所得溶液中溶质的质量分数为1%,计算加入的碳酸钠溶液中溶质的质量分数。
【答案】2%【解析】【详解】设原碳酸钠溶液中溶质的质量为xNa2CO3+ Ca(OH)2=CaCO3↓+ 2NaOH106 100 80X则解得x =10.6g所以加入的碳酸钠溶液中溶质的质量分数为答:加入的碳酸钠溶液中溶质的质量分数为2%。
5.将14.06g粗还原铁粉(假设粗还原铁粉中杂质仅含少量Fe x C)与足量稀硫酸反应,得到0.48gH2(Fe x C与稀硫酸反应不产生H2)。
若将相同质量的粗还原铁粉在氧气流中完全反应,得到0.22gCO2.试通过计算确定:(1)此粗还原铁粉中单质铁的质量_____(2)此粗还原铁粉中杂质Fe x C的化学式。
_____【答案】13.44g Fe2C【解析】【分析】【详解】若将14.06g还原铁粉(含少量Fe x C)在氧气流中加热,得到0.22gCO2,碳元素的质量=0.22g×1244=0.06g(1)将相同质量的还原铁粉与足量硫酸反应,得到0.48gH2,设消耗铁的质量为x。
2442Fe+H SO=FeSO+562x0H.48g↑562=x0.48gx=13.44gFe x C的质量=14.06g﹣13.44g=0.62g;Fe x C的中铁元素的质量=0.62g﹣0.06g=0.56g则:56x0.56g=120.06gx=2所以化学式为Fe2C6.向盛有28g氯化钡和氯化钠固体混合物的烧杯中加入273.3g水,待固体完全溶解后,再逐滴加入一定质量分数的硫酸钠溶液,反应过程中生成沉淀的质量与所加硫酸钠溶液的质量关系如图所示。
试计算(1)恰好完全反应时,生成沉淀的质量是___g;(2)恰好完全反应时,所得溶液中溶质的质量分数____。
【答案】23.3 5%【解析】【详解】(1)由图可知生成的硫酸钡的质量为23.3g(2)设氯化钡的质量为x,生成的氯化钠的质量为y2424Na SO BaCl BaSO+=+208233117x23.2NaCl3g y↓208233117==x23.3g y解得:x=20.8g y=11.7g恰好完全反应时,所得溶液中溶质的质量分数为28g-20.8g+11.7g100%=5% 28g+273.3g+100g-23.3g⨯答:(1)恰好完全反应时,生成沉淀的质量是23.3g;(2)恰好完全反应时,所得溶液中溶质的质量分数为5%。
7.BaCl2是一种重金属盐,其水溶液具有很强的毒性,若误服了BaCl2溶液可立即服用MgSO4溶液解毒。
为测定某BaCl2溶液的溶质质量分数,现向BaCl2溶液不断加入MgSO4溶液,并将反应过程中溶液总质量与加入MgSO4溶液的质量关系绘制成曲线如图所示,请回答:(1)P点时溶液中的离子有_____。
(2)求原BaCl2溶液的溶质质量分数。
________【答案】Mg2+和Cl- 20.8%【解析】【详解】加入100g硫酸镁出现明显的拐点,说明此时恰好完全反应。
此时溶液为氯化镁,对应的离子有 Mg2+和Cl-。
根据质量守恒定律可得,生成硫酸钡的质量为100g+100g-176.7g=23.3g解:设原BaCl2溶液的溶质质量分数为xMgSO4+BaCl2=BaSO4↓+MgC l2208 233100gx 23.3g208100x23323.3g=x=20.8%答:(1)P点时溶液中的离子有 Mg2+和Cl-。
(2)原BaCl2溶液的溶质质量分数为20.8%。
【点睛】此题为图形计算题,解题关键是对图形的理解,图中转折点表示氯化钡和硫酸镁恰好完全反应,此时消耗硫酸镁溶液的质量为100g,而生成沉淀的质量等于反应前两种溶液质量总和与反应后溶液的质量差,此点也是解答该题的一个重点。
8.向一定质量的5%的氢氧化钠溶液中加入66.9g硫酸铜溶液,恰好完全反应,得到4.9g 蓝色沉淀。
请计算:(1)所用氢氧化钠溶液的质量________。
(2)反应后所得溶液的溶质质量分数__________。
【答案】80g5%【解析】设参加反应的氢氧化钠的质量为x,反应生成硫酸钠的质量为y;2NaOH + CuSO4 = Cu(OH)2↓+ Na2SO480 98 142x 4.9g y80/98=x/4.9g x= 4g142/98=y/4.9g y=7.1g氢氧化钠溶液的质量为:4g÷5%=80g反应后所得溶液中溶质的质量分数是:答:所用氢氧化钠溶液的质量80g;反应后所得溶液的溶质质量分数为5%。
9.在一烧杯中盛有24.3g Na2SO4和NaCl组成的固体混合物,加入100g水使Na2SO4和NaCl全部溶解。
向其中逐渐滴加溶质质分数为20%的氯化钡溶液,生成沉淀的总质量与所滴入氯化钡溶液的质量关系曲线如图所示。
(1)请分析当BaCl2溶液滴加到B点时,溶液中的溶质是。
(2)请计算当滴加BaCl2溶液至图中A点时,所得溶液的溶质质量分数(计算结果保留一位小数)。
【答案】(1)BaCl2NaCl (2)10.6%【解析】试题分析:(1)当沉淀的质量不再增加时,说明反应已经进行完毕,所以当BaCl2溶液滴加到B点时说明氯化钡溶液滴加过量,当BaCl2溶液滴加到B点时,溶液中的溶质有刚生成的氯化钠和原来的氯化钠以及过量的氯化钡。
(2)根据当滴加BaCl2溶液至图中A点时沉淀的质量不再增加说明氯化钡溶液和硫酸钠溶液恰好完全反应,利用氯化钡的质量求出生成氯化钠的质量以及沉淀的质量即可求出所得溶液的溶质质量分数。
解:设参加反应的硫酸钠的质量为x,生成的硫酸钡的质量为y,生成的氯化钠的质量为z BaCl2 + Na2SO4=2NaCl+BaSO4↓208 142 117 233104g×20% x z y=解得x=14.2g=解得y=23.3g=解得z=11.7g当滴加BaCl2溶液至图中A点时,所得溶液的溶质质量分数×100%=10.6%答:当滴加BaCl2溶液至图中A点时,所得溶液的溶质质量分数为10.6%考点:考查根据化学反应方程式的计算;有关溶质质量分数的简单计算10.某同学将一定质量的锌粒放入200g稀硫酸溶液中,恰好完全反应,并产生了0.4g氢气。
计算:(1)参加反应的锌的质量。
(2)所用稀硫酸溶液中溶质的质量分数。
【答案】(1)13g(2)9.8%【解析】(1)设参与反应的锌的质量为x,200g稀硫酸溶液中硫酸的质量为y,Zn+H2SO4=ZnSO4+H2↑65 98 2x y 0.4g∴x=13gy=19.6g(2)所用稀硫酸溶液中溶质的质量分数为:×100%=9.8%答:(1)参加反应的锌的质量为13g.(2)所用稀硫酸溶液中溶质的质量分数为9.8%。