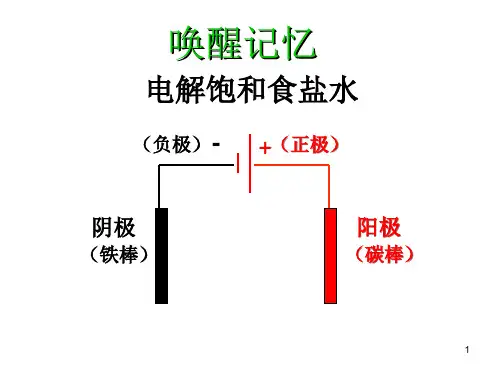
电解原理电解食盐水(课件PPT)
- 格式:ppt
- 大小:1.35 MB
- 文档页数:53
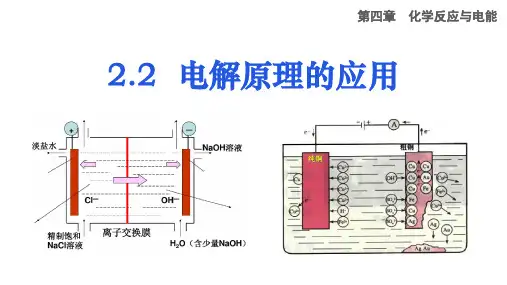



第九章电化学反应过程和氯化过程9.2电解食盐水溶液制烧碱一、基本概念1.法拉第电解定律法拉第在1834年提出的电解定律可表示为:在电解中,96500C(即1法拉第)的电量产生1克当量物质的化学变化。
G= (M/nF)*It=K*QM:物质的相对原子量,n:物质的原子价(电极反应中的电子数)Q=It F=96500C=26.8Ah电化当量:为1Ah电量析出的物质克数。
K= M/nF例如:电解食盐水的反应整个阴极反应总反应:在阳极极上析出C12的电化当量为:在阴极生成的烧碱的电化当量:K=40/26.8=1.4925(g/Ah)2.分解电压、过电压和电压效率a分解电压:对于化学反应:此反应的逆反应需要的电压即为理论分解电压。
化学反应达到平衡时,理论分解电压为:还可以通过阴极、阳极半反应的能斯特方程计算。
Er =φ(阳极)-φ(阴极),φ表示半反应的平衡电位,E 表示实际电位,Er 表示理论分解电位。
如,298.15K ,阳极液中NaCl 265kg/m 3,阴极液中NaOH 100 kg/m 3时, φ(Cl )=1.332V φ(H )=-0.840VEr =φ(阳极)-φ(阴极)=1.332+0.840=2.172Vb 过电压实际反应的电极电位与理论分解电压的差称为该电极的过电压。
影响过电压的因素:电极材料、电极表面状态、电流密度、温度、电解时间、电解质的性质和浓度以及电解质中的杂质等。
气体电极过程,产生的过电压相当大,而析出金属则除Fe 、Co 和Ni 外,产生的过电压一般均很小。
电极表面粗糙,电解的电流密度降低以及电解液的温度升高,可以降低电解时的过电压。
其中,电极材料对过电压的影响最大。
如:石墨阳极上析出氯气、析出氧气的实际电位(1000A/cm 2, NaCl 265kg/m 3) E (Cl )=φ(Cl )+E o (Cl )=1.332+0.25=1.582V E (O )=φ(O )+ E o (O )=0.814+1.09=1.904Vc 槽电压和电压效率电解槽两极上所加的电压称为槽电压,即实际分解电压, E (实)=Er +Eo +△E (降) △E (降):电流通过电解液、电极、导线、接点等的电压降 电压效率(ηE )3. 电流效率、电流密度和电能效率电流效率I η:在实际生产过程中,由于有一部分电流耗于电极上产生的副反应和漏电现象,电流不能100%被利用,所以不能按前述的法拉第电解定律来精确计算所需的电量。



电解饱和食盐水实验演示操作方法向U形管里倒入饱和食盐水,插入一根碳棒作阳极,一根铁钉作阴极。
同时在U形管的两端各滴入几滴酚酞试液,并用湿润的碘化钾淀粉试纸检验阳极放出的气体。
接通直流电源后,注意U形管内发生的现象。
实验现象两极都有气体放出,阳极放出的气体有刺激性气味,且能使湿润的碘化钾淀粉试纸变蓝。
同时发现阴极附近溶液变红。
实验结论从实验现象看阳极产生气体为Cl2,阴极附近有碱性物质产生。
并有氢气放出。
因在食盐水里存在着Na+、H+和Clˉ、OHˉ,当接通直流电源后,Clˉ、OHˉ移向阳极,Na+、H+移向阴极。
Cl-较易失电子,失去电子生成Cl2,H+较易得电子,得到电子生成H2,所以在阴极附近水的电离平衡被破坏,溶液里的OHˉ数目相对增多,溶液显碱性。
反应方程式为:2NaCl+2H2O 2NaOH+H2↑+Cl2↑实验考点1、电解原理;2、氧化还原反应原理以及放电顺序;3、电极反应式的书写与判断;4、电子守恒、电荷守恒的应用。
经典考题1、电解下列溶液,两极均产生气体的是[ ]A. CuCl2溶液B. HCl溶液C. CuSO4溶液D. NaCl溶液试题难度:易2、用Pt电极长时间电解下列溶液,整个溶液的pH不发生变化的是A. KNO3B. Ba(OH)2C. NaClD. H2SO4试题难度:中3、将含0.4molCuSO4和0.4molNaCl的水溶液1L,用惰性电极电解一段时间后,在一个电极上得到0.3mol铜,在另一个电极上析出气体在标准状况下的体积是______(不考虑生成的气体在水中的溶解)A. 5.6LB. 6.72LC. 13.44LD. 11.2L试题难度:难1 答案:BD解析:AC中铜离子会放电,生成Cu,不会在阴极得到气体。
2 答案:A解析:电解ABD的溶液都是电解水,溶质的浓度变大。
若原来是中性溶液,电解后仍为中性;若原来是酸性溶液,则因浓度增大,酸性增强;同理,若原来是碱性溶液,碱性增强。

电解饱和食盐水⒈电解饱和食盐水的实验“奇观”以铁钉作阴极、石墨棒为阳极,在U 型管中做电解饱和食盐水演示实验。
观察两极产生气泡,并用酚酞试液滴入阴极区变红,用湿润的KI —淀粉试纸放在阳极管口变蓝,实验结束后,将直流电源反接(在U 型管中插入的两极保持不变)于是出现以下四道奇观:第一道奇观:铁钉变成了点“雪”魔棒。
阳极铁钉身上包满白色絮状物,铁钉下端产生白色絮状沉淀缓缓下落,犹如下起鹅毛般大雪。
第二道奇观:当白色絮状物沉到管底部时,便形成翠绿色环状物,随着时间的推移,阳极区形成上端呈白色絮状,中部为白色和翠绿色交融状,底部呈翠绿色,犹如翡翠玉镯,令大自然羞涩。
第三道奇观:关闭电源后,阳极区沉淀继续下移,最终在U型管底部形成3~5 厘米长的翠绿色环状物。
(以上全过程约需20 分钟) 第四道奇观:将上述翠绿色环状物放置于安全处,第二天观看,呈灰绿和翠绿相伴状。
原理分析:在原电解池中,铁钉作阴极,该区产生H2 和NaOH,使该区呈现碱性和还原性。
反接电源后,铁钉作阳极电极反应:Fe - 2e - = Fe2 +亚铁离子与原来产生的NaOH结合生成白色絮状的Fe (OH)2 ,由于该区上中部呈还原环境,Fe (OH) 2 絮状物可保持较长时间不变色。
而该区下半部食盐水中,仍含有极少量O2 ,Fe (OH)2和O2 反应、生成翠绿色物质,经过一夜,由于空气中O2的溶解,使翠绿色的外表呈灰绿色。
⒉用铜作电极电解饱和食盐水如图,试管里盛有约1P2 体积的饱和食盐水,剥开电话用的导线两端,露出一红一蓝塑料包裹的铜丝。
导线的一端伸入饱和食盐水中,另一端跟2 个1 号(或5 号) 干电池的两极相连接,电解饱和食盐水立即开始,可观察到的趣味现象如下:(1) 液面下跟电池负极相连的铜丝(阴极) 变黑,同时伴有大量气泡(H2 ) 产生;跟电池正极相连的铜丝(阳极) 的色光泽(紫红色) 不变,只是铜丝由粗变细。
(2) 溶液导电开始的30 秒内,略显白色浑浊,然后开始呈现橙黄色浑浊,进而生成较多的橙黄色沉淀。

二、离子膜选择透过性基本原理
在离子交换膜发电解槽中,由一种具有选择性透过性能的阳离子交换膜将电解槽分成阳极室和阴极室
以Nafion膜为例,离子膜的选择性透过
离子膜是多孔结构物质,由孔和骨架组成,孔内是水相,
骨架是含氟聚合物
2、离子膜性能降低的主要因素
1)、钙和镁正离子在电场作用下,易进入离子膜内,形成沉积物堵塞孔通道
2)、为稳定操作,膜内的负离子团的数目要求相对稳定,电解液温度不宜过高,碱液浓度不宜过浓,避免出现脱水现象,在膜内产生结晶,造成膜的永久性损坏
3)、溶液碱浓度过低而温度较高时,在膜的界面处也可能出现积水。

电解食盐水的反应原理
电解食盐水的反应原理是基于离子化的化学反应。
当食盐(氯化钠)溶解在水中时,会形成离子化的离子。
在水中,食盐(NaCl)的分子会被水分子(H2O)的极性所
吸引,导致食盐分子分解为两种离子:钠离子(Na+)和氯离
子(Cl-)。
这个过程称为离解。
离解后的离子在水中自由移动,并且可以传导电流。
当两个电极(一个是正极,一个是负极)插入盛有食盐水的容器中,食盐溶液中的离子将会从正极移动到负极。
正极吸引阴离子(Cl-),负极吸引阳离子(Na+)。
这个过程称为电解。
在正极的位置,阴离子会接收电子并发生还原反应,生成氯气(Cl2)。
在负极的位置,阳离子会失去电子并发生氧化反应,生成氢气(H2)。
这个电解食盐水的过程不仅仅是一种化学反应,同时也是电能转化为化学能和热能的过程。
通过电解食盐水,我们可以观察到氯气和氢气的释放,这是由于电流通过食盐水溶液中的离子产生的。