内部审核计划表
- 格式:doc
- 大小:190.00 KB
- 文档页数:10
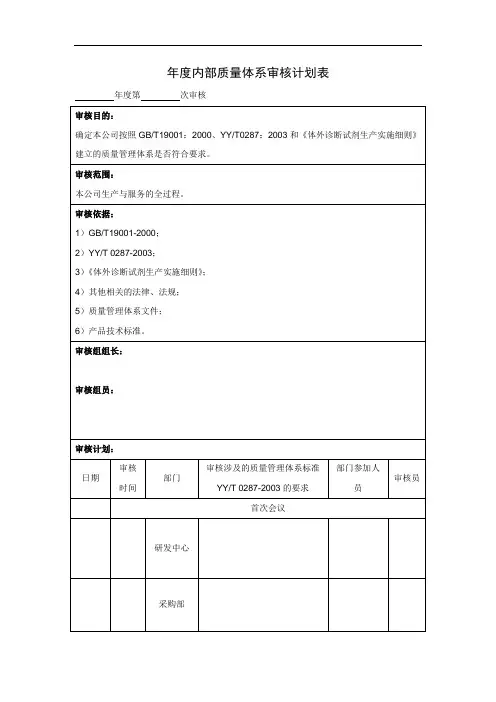
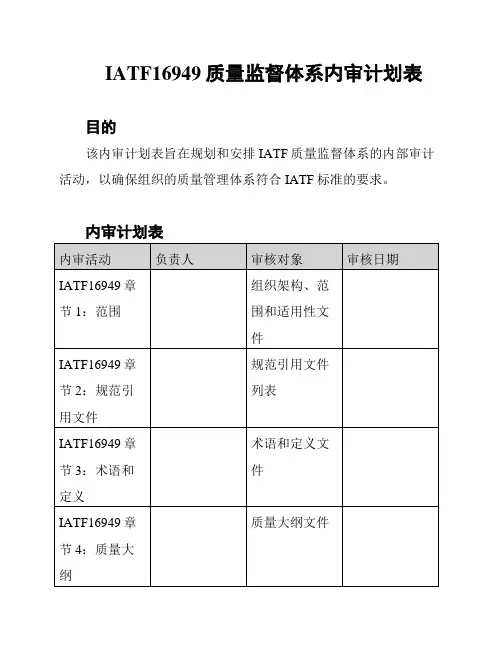
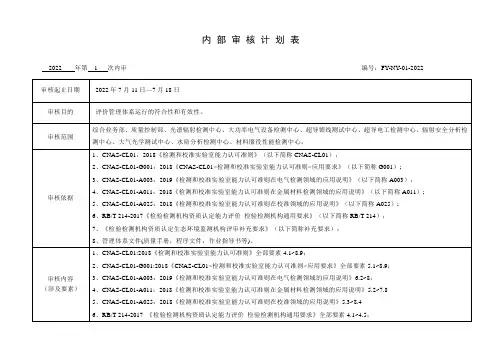
IATF16949质量监督体系内审计划表
目的
该内审计划表旨在规划和安排IATF质量监督体系的内部审计活动,以确保组织的质量管理体系符合IATF标准的要求。
内审计划表
内审计划流程
1. 确定内审计划的目标和范围;
2. 选择内审团队成员和负责人;
3. 根据内审计划表中的内容,制定详细的审核指导文件;
4. 安排内审的日期和时间,并通知相关部门和人员;
5. 进行内审活动,包括对文件的审查、现场观察和面谈;
6. 记录和整理内审的结果和发现;
7. 提出内审报告和改进建议;
8. 协助组织制定并执行改进措施;
9. 跟踪和验证改进措施的有效性。
注意事项
- 内审活动应该按照计划表的顺序进行,确保覆盖所有的章节
和要求;
- 内审团队成员应具备相应的知识和技能,并严格遵守内审程序;
- 内审报告应详细记录内审结果和改进建议,并及时提交给管
理层;
- 内审活动应保持客观、公正和独立,不受个人或部门的影响。
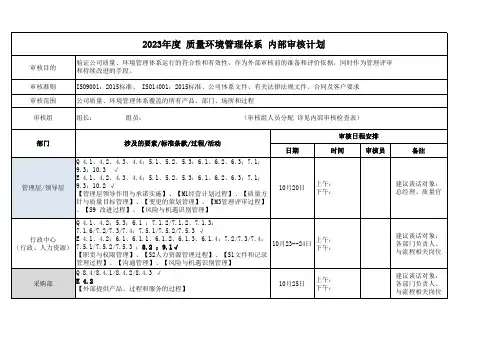
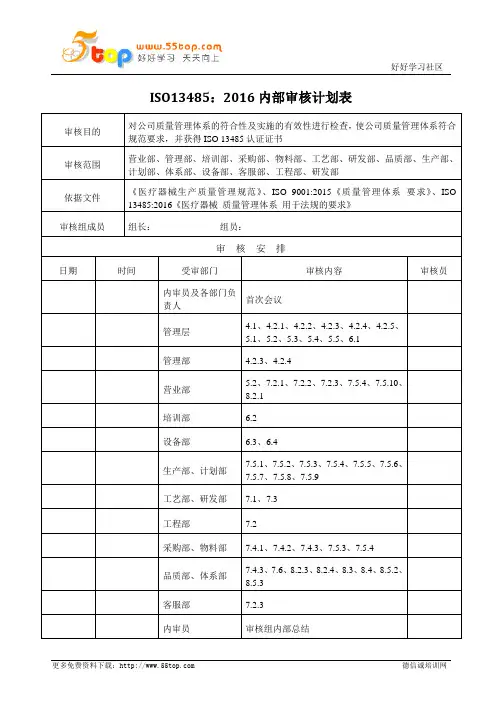
ISO13485:2016内部审核计划表
审核目的对公司质量管理体系的符合性及实施的有效性进行检查,使公司质量管理体系符合规范要求,并获得ISO 13485认证证书
审核范围营业部、管理部、培训部、采购部、物料部、工艺部、研发部、品质部、生产部、计划部、体系部、设备部、客服部、工程部、研发部
依据文件《医疗器械生产质量管理规范》、ISO 9001:2015《质量管理体系要求》、ISO 13485:2016《医疗器械质量管理体系用于法规的要求》
审核组成员组长:组员:
审核安排
日期时间受审部门审核内容审核员
内审员及各部门负
责人
首次会议
管理层4.1、4.2.1、4.2.2、4.2.3、4.2.4、4.2.5、
5.1、5.2、5.3、5.4、5.5、
6.1
管理部 4.2.3、4.2.4
营业部5.2、7.2.1、7.2.2、7.2.3、7.5.4、7.5.10、8.2.1
培训部 6.2
设备部 6.3、6.4
生产部、计划部7.5.1、7.5.2、7.5.3、7.5.4、7.5.5、7.5.6、7.5.7、7.5.8、7.5.9
工艺部、研发部7.1、7.3
工程部7.2
采购部、物料部7.4.1、7.4.2、7.4.3、7.5.3、7.5.4
品质部、体系部7.4.3、7.6、8.2.3、8.2.4、8.3、8.4、8.5.2、
8.5.3
客服部7.2.3
内审员审核组内部总结
内审员及各部门负
末次会议
责人
编制人∕日期:批准人∕日期:。

QR-025
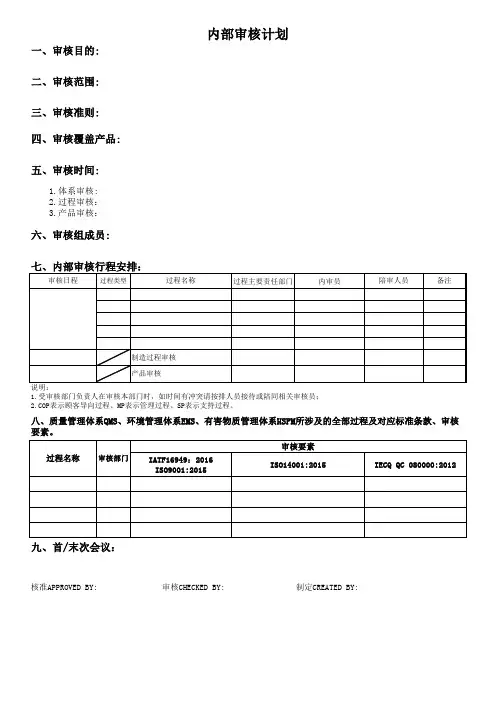
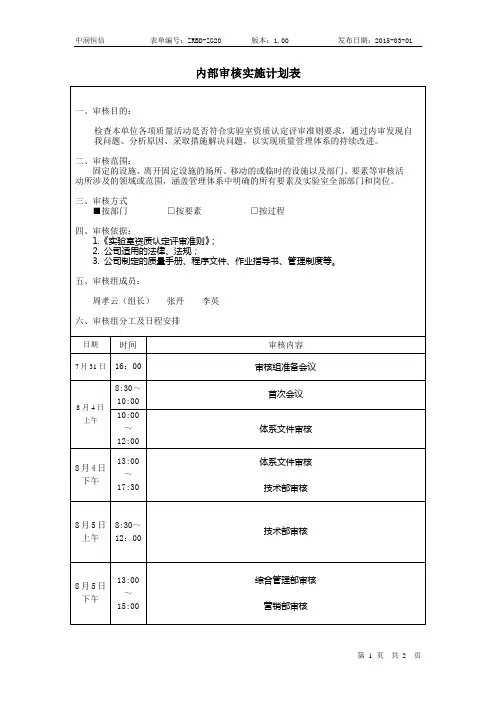
内部审核实施计划
审核目的:检查QMS各过程的实施情况,评估ISO9001:2015标准实施的适宜性、有效性,体系是否正常有效的运行。
审核范围:关于我公司质量管理体系所涉及的相关部门、办公区域、作业场所的质量管理审核依据:1. ISO 9001:2015标准。
2.公司的品质管理体系文件。
3.相关的法律法规。
4.合同的要求。
审核组长:
第一组:
(集成项目部/研发部/行政人事部)
第二组:
(采购部/营销部/财务部/管理者代表/总经理)
审核日期:XXXX年3月1日
审核日程安排表
备注:审核员不能审核本部门的内容.
总经理批准:管理者代表:
日期:日期:。
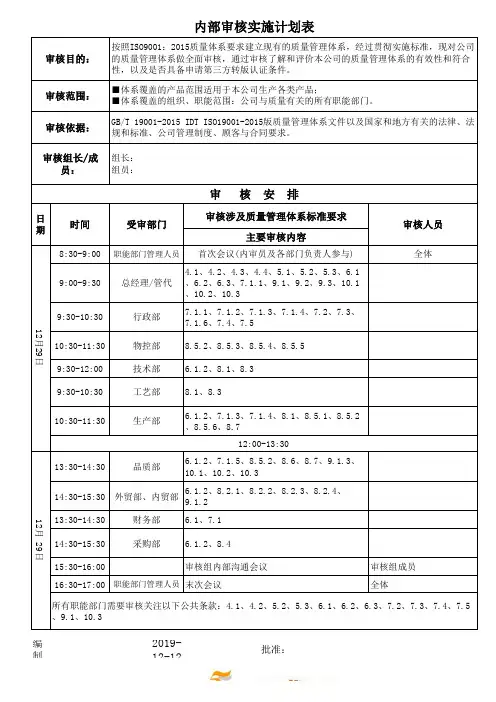
审核涉及质量管理体系标准要求主要审核内容8:30-9:00职能部门管理人员首次会议(内审员及各部门负责人参与)全体9:00-9:30总经理/管代 4.1、4.2、4.3、4.4、5.1、5.2、5.3、6.1、6.2、6.3、7.1.1、9.1、9.2、9.3、10.1、10.2、10.39:30-10:30行政部7.1.1、7.1.2、7.1.3、7.1.4、7.2、7.3、7.1.6、7.4、7.510:30-11:30物控部8.5.2、8.5.3、8.5.4、8.5.59:30-12:00技术部 6.1.2、8.1、8.39:30-10:30工艺部8.1、8.310:30-11:30生产部 6.1.2、7.1.3、7.1.4、8.1、8.5.1、8.5.2、8.5.6、8.713:30-14:30品质部 6.1.2、7.1.5、8.5.2、8.6、8.7、9.1.3、10.1、10.2、10.314:30-15:30外贸部、内贸部 6.1.2、8.2.1、8.2.2、8.2.3、8.2.4、9.1.213:30-14:30财务部 6.1、7.114:30-15:30采购部 6.1.2、8.415:30-16:00审核组内部沟通会议审核组成员16:30-17:00职能部门管理人员末次会议全体编制: 2019-12-12批准:受审部门内部审核实施计划表审核目的:按照ISO9001:2015质量体系要求建立现有的质量管理体系,经过贯彻实施标准,现对公司的质量管理体系做全面审核,通过审核了解和评价本公司的质量管理体系的有效性和符合性,以及是否具备申请第三方转版认证条件。
审核范围:■体系覆盖的产品范围适用于本公司生产各类产品;■体系覆盖的组织、职能范围:公司与质量有关的所有职能部门。
审核依据:GB/T 19001-2015 IDT ISO19001-2015版质量管理体系文件以及国家和地方有关的法律、法规和标准、公司管理制度、顾客与合同要求。

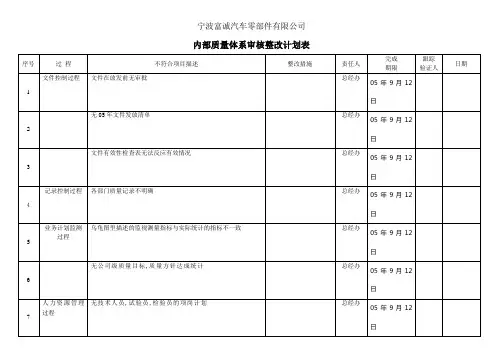
2015年度内部审核计划
编制:毕晓腾审核:连志钢批准:尹民贤日期:2015/4/1 日期:2015/4/1 日期:2015/4/1
2015年度内部审核计划
编制:毕晓腾审核: 连志钢批准:尹民贤
日期:2015/4/10
审核报告
不合格报告
不合格项分布表
日期:2015-4-11 日期:2015-4-11
内审首(末)次会议签到表
关于质量管理体系内部审核的
通知
各部门:
为了检查公司质量管理体系运行以来的效果,确保公司质量方针和目标的实现,按照标准的要求以及公司贯标工作计划,经公司研究决定,成立审核组并进行公司质量管理体系内部审核,请做好准备工作。
一、审核组成员:
组长:唐翠华
组员:夏辛生邓斌熊波
二、审核时间:
2007年5月10日—11日
特此通知
江西贝思特科技有限公司 2007年5月1日
附:2007年度内部审核计划
欢迎您的下载,
资料仅供参考!
致力为企业和个人提供合同协议,策划案计划书,学习资料等等
打造全网一站式需求。