高中化学会考复习-有机反应类型
- 格式:ppt
- 大小:303.50 KB
- 文档页数:33

高中化学十二种有机反应类型本文将介绍高中化学中的十二种有机反应类型。
这些反应类型涵盖了烃、醇、醛、酸、酯等常见有机化合物之间的基本转化。
了解这些反应对于学习有机化学至关重要。
一、烷烃的取代反应烷烃在光照或高温条件下,可以与氯气、溴蒸气等发生取代反应。
例如,甲烷与氯气在光照条件下反应,生成一氯甲烷和氯化氢。
二、烯烃的加成反应烯烃在催化作用下,可以与氢气、卤素等发生加成反应。
例如,乙烯与氢气在催化作用下反应,生成乙烷。
三、炔烃的加成反应炔烃在催化作用下,可以与氢气、卤素等发生加成反应。
例如,乙炔与氢气在催化作用下反应,生成乙烯和氢气。
四、醇的氧化反应醇可以在催化作用下,被氧化成醛或酮。
例如,乙醇在催化作用下被氧化成乙醛。
五、醛的氧化反应醛可以在催化作用下,被氧化成酸。
例如,乙醛在催化作用下被氧化成乙酸。
六、醛的还原反应醛可以在催化作用下,被还原成醇。
例如,乙醛在催化作用下被还原成乙醇。
七、酯的合成反应酯可以通过酸和醇的酯化反应生成。
例如,乙酸和乙醇在浓硫酸和加热条件下反应,生成乙酸乙酯和水。
八、酯的水解反应酯可以在水溶液中,发生水解反应生成酸和醇。
例如,乙酸乙酯在酸性条件下水解生成乙酸和乙醇。
九、酰胺的合成反应酰胺可以通过氨和羧酸或酸酐反应生成。
例如,氨和乙酸在浓硫酸和加热条件下反应,生成乙酸铵(酰胺)。
十、酮的双分子亲核取代反应酮可以在强碱条件下,发生双分子亲核取代反应生成烯烃和卤代烃。
例如,环己酮在强碱条件下反应,生成乙烯酮和卤代烃。
十一、羧酸的氧化反应羧酸可以在氧化剂作用下,被氧化生成过氧化物。
例如,乙酸在氧化剂作用下被氧化成过氧乙酸。
十二、环氧化合物的开环反应环氧化合物可以在酸或碱的作用下,发生开环反应生成醇或醚。
例如,环氧乙烷在酸性条件下开环生成乙醇。
以上是高中化学中常见的十二种有机反应类型。
这些反应为有机化合物之间的转化提供了基础理论依据。
在学习有机化学的过程中,掌握这些基本反应类型对于理解有机化合物的性质和合成具有重要意义。


高中有机化学反应类型的总结1、取代反应(1)能发生取代反应的官能团有:醇羟基(-OH)、卤原子(-X)、羧基(-COOH)、酯基(-COO-)、肽键(-CONH-)等。
(2)能发生取代反应的有机物种类如下图所示:2、加成反应1.能发生加成反应的官能团:双键、三键、苯环、羰基(醛、酮)等。
2.加成反应有两个特点:①反应发生在不饱和的键上,不饱和键中不稳定的共价键断裂,然后不饱和原子与其它原子或原子团以共价键结合。
②加成反应后生成物只有一种(不同于取代反应)。
说明:1.羧基和酯基中的碳氧双键不能发生加成反应。
2.醛、酮的羰基只能与H2发生加成反应。
3.共轭二烯有两种不同的加成形式。
3、消去反应(1)能发生消去反应的物质:醇、卤代烃;能发生消去反应的官能团有:醇羟基、卤素原子。
(2)反应机理:相邻消去发生消去反应,必须是与羟基或卤素原子直接相连的碳原子的邻位碳上必须有氢原子,否则不能发生消去反应。
如CH3OH,没有邻位碳原子,不能发生消去反应。
4、聚合反应(1)加聚反应:烯烃加聚的基本规律:(2)缩聚反应:(1)二元羧酸和二元醇的缩聚,如合成聚酯纤维:(2)醇酸的酯化缩聚:此类反应若单体为一种,则通式为:若有两种或两种以上的单体,则通式为:(3)氨基与羧基的缩聚(1)氨基酸的缩聚,如合成聚酰胺6:(2)二元羧酸和二元胺的缩聚:5、氧化反应与还原反应1.氧化反应就是有机物分子里“加氧”或“去氢”的反应。
能发生氧化反应的物质和官能团:烯(碳碳双键)、醇、酚、苯的同系物、含醛基的物质等。
烯(碳碳双键)、炔(碳碳叁键)、苯的同系物的氧化反应都主要指的是它们能够使酸性高锰酸钾溶液褪色,被酸性高锰酸钾溶液所氧化。
含醛基的物质(包括醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖等)的氧化反应,指银镜反应及这些物质与新制氢氧化铜悬浊液的反应。
要注意把握这类反应中官能团的变化及化学方程式的基本形式2.还原反应是有机物分子里“加氢”或“去氧”的反应,其中加氢反应又属加成反应。
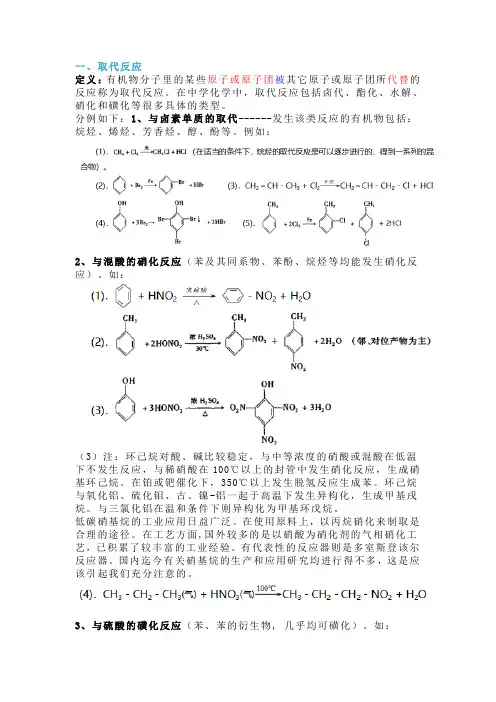
一、取代反应定义:有机物分子里的某些原子或原子团被其它原子或原子团所代替的反应称为取代反应。
在中学化学中,取代反应包括卤代、酯化、水解、硝化和磺化等很多具体的类型。
分例如下:1、与卤素单质的取代------发生该类反应的有机物包括:烷烃、烯烃、芳香烃、醇、酚等。
例如:2、与混酸的硝化反应(苯及其同系物、苯酚、烷烃等均能发生硝化反应)。
如:(3)注:环己烷对酸、碱比较稳定,与中等浓度的硝酸或混酸在低温下不发生反应,与稀硝酸在100℃以上的封管中发生硝化反应,生成硝基环己烷。
在铂或钯催化下,350℃以上发生脱氢反应生成苯。
环己烷与氧化铝、硫化钼、古、镍-铝一起于高温下发生异构化,生成甲基戌烷。
与三氯化铝在温和条件下则异构化为甲基环戊烷。
低碳硝基烷的工业应用日益广泛。
在使用原料上,以丙烷硝化来制取是合理的途径。
在工艺方面,国外较多的是以硝酸为硝化剂的气相硝化工艺,已积累了较丰富的工业经验。
有代表性的反应器则是多室斯登该尔反应器。
国内迄今有关硝基烷的生产和应用研究均进行得不多,这是应该引起我们充分注意的。
3、与硫酸的磺化反应(苯、苯的衍生物, 几乎均可磺化)。
如:4、羧酸和醇的酯化反应5、水解反应(卤代烃、酯、多糖、二糖、蛋白质都能在一定条件下发生水解反应)。
如:6、与活泼金属的反应:(醇、酚、羧酸等均能与活泼金属如钠反应生成氢气)。
如:7、醇与卤化氢(HX)的反应。
如:8、羧酸或醇的分子间脱水。
如:二、加成反应定义:有机物分子里不饱和碳原子跟其它原子或原子团直接结合生成化合物的反应叫加成反应。
在中学化学中,分子结构中含有“双键”或“叁键”的化合物均能发生加成反应。
如烯烃、二烯烃、炔烃、苯及其同系物、醛、酮、不饱和高级脂肪酸及其甘油脂、单糖等。
通常参与加成反应的无机试剂包括H2、X2(X为Cl、Br、I)、HX、H2O、HCN等小分子(对称或不对称试剂)起加成反应。
说明:i.羧基和酯基中的碳氧双键不能发生加成反应。

高中化学重要知识点有机化合物的反应类型与机理高中化学重要知识点:有机化合物的反应类型与机理有机化合物是由碳与氢以及其他元素组成的化合物。
在有机化学中,研究有机化合物的反应类型和机理是非常重要的。
本文将介绍一些常见的有机化合物反应类型及其机理。
一、取代反应(Substitution Reaction)取代反应是指有机化合物中的一个原子或基团被另一个原子或基团取代的反应。
常见的取代反应有卤代烃的取代反应、芳香族化合物的取代反应等。
1. 卤代烃的取代反应卤代烃的取代反应是指卤代烃中的卤素被另一原子或基团取代的反应。
典型的例子是卤代烃与氢氧化钠(NaOH)的反应,生成相应的醇。
该反应的机理是亲核取代反应(Nucleophilic Substitution),其中亲核试剂(如氢氧根离子)攻击卤素离子的碳原子,形成中间物,最终生成醇。
2. 芳香族化合物的取代反应芳香族化合物的取代反应是指芳香环中的一个或多个氢原子被其他基团取代的反应。
其中,最常见的芳香族取代反应是芳香族氢原子取代反应。
该反应的机理涉及亲电取代反应(Electrophilic Substitution)。
在该反应中,芳香环上的亲电试剂(如卤素)攻击芳香环上不饱和键的位置,形成最终产物。
二、加成反应(Addition Reaction)加成反应是指有机化合物中的两个分子通过共有键结合而形成一个分子的反应。
常见的加成反应有烯烃的加成反应、炔烃的加成反应等。
1. 烯烃的加成反应烯烃的加成反应是指烯烃分子与另一分子发生共有键结合形成新的化合物的反应。
一个典型的例子是烯烃与溴水的反应,在反应中,烯烃分子的双键被溴分子的溴原子攻击,形成溴代烃。
该反应的机理是亲电加成反应(Electrophilic Addition),其中亲电试剂(如溴分子)与双键上的云区发生相互作用。
2. 炔烃的加成反应炔烃的加成反应是指炔烃分子与其他分子通过共有键结合形成新的化合物的反应。

高中化学知识点总结:有机化学反应类型归纳1.取代反应(1)定义:有机物分子里的某些原子或原子团被其他原子或原子团所代替的反应。
(2)能发生取代反应的物质:烷烃、芳香烃、醇、酚、酯、羧酸、卤代烃。
(3)典型反应:CH4 + Cl2 CH3Cl + HCl2.加成反应(1)定义:有机物分子里不饱和碳原子跟其他原子或原子团直接结合生成别的物质的反应。
(2)能发生加成反应的物质:烯烃、炔烃、苯及其同系物。
醛、酮、单糖等等。
(3)典型反应:CH2=CH2 + Br2 → CH2Br-CH2Br3.加聚反应(1)定义:通过加成聚合反应形成高分子化合物。
(2)特征:生成物只有高分子化合物,其组成与单体相同。
(3)典型反应:4.缩聚反应(1)定义:通过缩合反应生成高分子化合物,同时还生成小分子。
(如H2O、NH3等)的反应。
(2)特征:除生成高分子化合物还有小分子生成。
(3)典型反应:5.消去反应:(1)定义:从一个有机物分子中脱去小分子(如H2O、HX等)而生成不饱和化合物(含双键或叁键)的反应。
(2)能发生消去反应的物质:醇、卤代烃。
(3)典型反应:6.氧化反应(1)定义:有机物加O或去H的反应。
(2)类型:①在空气中或氧气中燃烧②催化氧化如:2C2H5OH + O2 2 CH3CHO + 2H2O③某些有机物被非O2氧化剂氧化如:烯、炔、苯的同系物被酸性,KMnO4氧化;醛类,甲酸及甲酸酯葡萄糖被银氢溶液,新制Cu(OH)2氧化:CH3CHO+2Cu(OH)2 → CH3COOH+Cu2O↓+2H2O7.还原反应(1)定义:有机物加H或去O的反应(2)典型反应:CH3CHO+H2→ CH3CH2OH(也是加成反应)8.酯化反应:(也属于取代反应)(1)定义:酸与醇起作用、生成酯和水的反应(2)典型反应:C2H5OH + CH3COOH CH3COOC2H5 + H2O9.水解反应(属于取代反应)(1)反应特征:有水参加,有机物分解成较小分子。

有机反应方式
1、取代反应:也叫置换反应,是有机化合物分子中的原子或原子团被其它原子或原子团所代替的反应.
2、消去反应:指从一个大的有机分子中失去一个小分子,形成不饱和键的反应.
3、加成反应:是消去反应的逆反应,是有机化合物中不饱和键断裂,加入其他原子或原子团的反应.
4、重排反应:是指有机化合物分子中原子顺序重新进行改组,形成新一类有机化合物的反应.绝大多数有机反应都可包括在这四种类型之中(少数例外,如水解反应),很多有机反应还可能由两种或两种以上类型的反应所组成.。
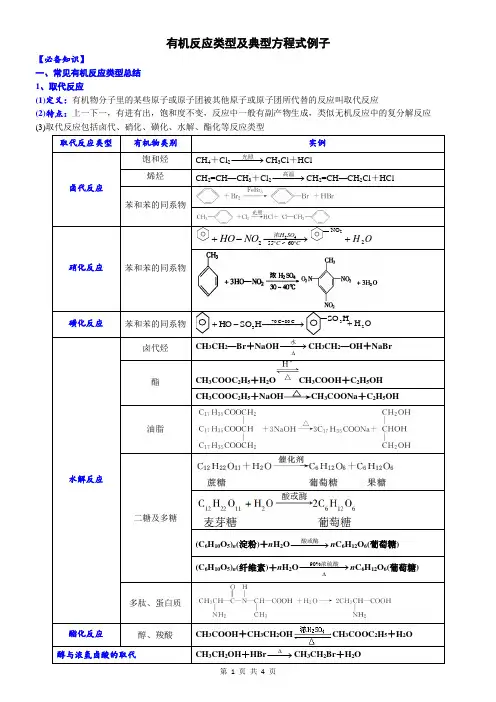
有机反应类型及典型方程式例子【必备知识】一、常见有机反应类型总结1、取代反应(1)定义:有机物分子里的某些原子或原子团被其他原子或原子团所代替的反应叫取代反应(2)特点:上一下一,有进有出,饱和度不变,反应中一般有副产物生成,类似无机反应中的复分解反应(3)取代反应类型有机物类别实例卤代反应饱和烃CH4+Cl2−−→−光照CH3Cl+HCl烯烃CH2=CH—CH3+Cl2−−→−高温CH2=CH—CH2Cl+HCl 苯和苯的同系物硝化反应苯和苯的同系物CCSOHNOHO︒︒−−−→−-+60~55242浓NO2OH2+磺化反应苯和苯的同系物HSO3−−−→−-+C80~C703..HSOHO OH2+水解反应卤代烃CH3CH2—Br+NaOH∆−→−水CH3CH2—OH+NaBr酯CH3COOC2H5+H2O CH3COOH+C2H5OHCH3COOC2H5+NaOH CH3COONa+C2H5OH油脂二糖及多糖(C6H10O5)n(淀粉)+n H2O−−→−酸或酶n C6H12O6(葡萄糖)(C6H10O5)n(纤维素)+n H2O∆−−−→−浓硫酸%90n C6H12O6(葡萄糖) 多肽、蛋白质(1)定义:有机物分子里不饱和的碳原子跟其他原子或原子团直接结合生成新物质的反应(2)特点:“断一,加二,都进来,不饱和度降低”;“断一”是指双键中的一个不稳定键断裂;“加二”是指加上两个其他原子或原子团,一定分别加在两个不饱和碳原子上,此反应类似无机反应中的化合反应,理论上原子利用率为100%(3)能发生加成反应的物质有:烯烃(碳碳双键)、炔烃(碳碳三键)、苯环、醛、酮等有机物类别实例烯烃(与X 2、H 2、HX 、H 2O)的加成CH 2==CH 2+Br 2−−→−4CCl CH 2Br —CH 2BrCH 2==CH 2+H 2O 加热、加压催化剂−−→−CH 3CH 2OH CH 2==CH 2+HCl ∆−−→−催化剂CH 3CH 2Cl CH 2==CH 2+H 2∆−→−NiCH 3—CH 3炔烃(与X 2、H 2、HX 、H 2O)的加成HC≡CH +H 2∆−→−Ni CH 2==CH 2,CH 2==CH 2+H 2∆−→−NiCH 3—CH 3 HC≡CH +Br 2―→CHBr ==CHBr ,CHBr==CHBr +Br 2―→CHBr 2—CHBr 2HC≡CH +HCl ∆−−→−催化剂CH 2==CHC l (氯乙烯) HC≡CH +H 2O −−→−催化剂CH 3CHO苯环只能与氢气加成醛(醛基)只能与氢气加成CH 3CHO +H 2∆−→−NiCH 3CH 2—OH 酮(羰基)只能与氢气加成+H 2∆−→−Ni不饱和油脂与H 2加成Diels-Alder 反应3(1)定义:有机化合物在一定条件下,从一个分子中脱去一个或几个小分子(如水、卤化氢等),而生成含不饱和键化合物的反应。

有机化学的反应类型
1. 加成反应:在反应中,两种或两种以上的分子结合成一个分子。
2. 消除反应:在反应中,一个大分子分解成两个小分子。
3. 取代反应:在反应中,一个原子或官能团被另一个原子或官能团取代。
4. 氧化还原反应:在反应中,一个物质失去电子而被氧化,而另一个物质获得电子而被还原。
5. 酸碱反应:在反应中,酸和碱互相中和形成盐和水的反应。
6. 缩合反应:在反应中,两个分子结合形成一个分子的过程。
7. 开环反应:在反应中,环形化合物断裂成直线化合物的过程。
8. 重排反应:在反应中,原始分子中原子或官能团排列位置的变化。
9. 氢解反应:在反应中,有机化合物和水反应,水分子加入到化合物中使其分解成两个分子。
10. 还原反应:在反应中,有机化合物和还原剂(如氢气、亚
硫酸盐等)反应,使化合物中的官能团发生还原反应。
11. 消除加成反应:在反应中,两个分子结合成一个分子,同
时又失去一些原子或官能团。
12. 氧杂化反应:在反应中,有机化合物中的氮、硫等杂原子
和氧反应,形成新的化合物。
13. 氧杂化加成反应:在反应中,两个分子结合成一个分子,
并且有机化合物中的氮、硫等杂原子和氧反应。
14. 核替换反应:在反应中,有机化合物中的核被另一个原子
或核替换。
15. 氧化反应:在反应中,有机化合物和氧反应,官能团中的双键或多键与氧反应,形成新的化合物。

高中化学:解读十二种有机反应类型连续几年的高考中都涉及到描述有机反应类型,在描述有机反应类型时,必须注意语言的准确性。
•例如醇分子之间脱水成醚的反应不能叫做脱水反应,只能叫做取代反应;同时注意不能用无机反应类型套用到有机反应中,•例如,裂化反应和裂解反应不能叫做分解反应。
本文通过全面归纳有机反应类型,理清学习有机的思绪,给学生形成一个整体影响,避免在学习考试中出现误区。
1、取代反应取代反应是指有机物分子里的某些原子或原子团被其他原子或原子团所代替的反应。
包括:卤代反应、硝化反应、磺化反应、卤代烃的水解反应、酯化反应、酯的水解反应等。
由于取代反应广泛存在,几乎所有的有机物都能发生取代反应。
2、加成反应加成反应是指有机物分子中不饱和的碳原子跟其他原子或原子团直接结合生成新的化合物的反应。
包括:与氢气的加成反应 (烯、炔和苯环的催化加氢;醛、酮催化加氢;油脂的加氢硬化)、与卤素单质的加成反应、与卤化氢的加成反应、与水的加成反应等。
只有不饱和有机物才能发生加成反应。
3、消去反应消去反应是指有机物在适当条件下,从一个分子脱去一个小分子(如水、HX等),而生成不饱和(双键或三键)化合物的反应。
包括醇的消去反应和卤代烃的消去反应。
在中学阶段,酚不能发生消去反应,并不是所有的醇或卤代烃都能发生消去反应。
4、脱水反应脱水反应是指有机物在适当条件下,脱去相当于水的组成的氢氧元素的反应。
包括分子内脱水(消去反应)和分子间脱水(取代反应)。
脱水反应不一定是消去反应,比如乙醇脱水生成乙醚就不属于消去反应。
5、水解反应广义的水解反应,指的凡是与水发生的反应。
中学有机化学里能够与水发生水解反应的物质,一般指的卤代烃水解、酯的水解、油脂的水解(含皂化)、糖类的水解、多肽或蛋白质的水解等。
6、氧化反应氧化反应是指有机物加氧或去氢的反应。
包括:•①醇的催化氧化:羟基的O—H键断裂,与羟基相连的碳原子的C—H键断裂,去掉氢原子形成C=O键;•②醛类及含醛基的化合物与新制碱性Cu(OH)2或银氨溶液的反应;•③乙烯在催化剂存在下氧化成CH3CHO;•④有机物的燃烧、不饱和烃和苯的同系物使酸性KMnO4溶液褪色等。

化学有机反应类型总结有机化学是研究有机物质的结构、性质和反应的科学。
有机反应是有机化学的重要组成部分,是指有机物质之间或有机物质与其他物质之间发生的化学变化。
有机反应类型繁多,下面我们将对常见的有机反应类型进行总结。
1. 取代反应取代反应是指有机物中的一个官能团被另一个官能团所取代的反应。
常见的取代反应有卤代烃的取代反应、醇的取代反应、酸的取代反应等。
取代反应的机理一般是通过亲核试剂或电子受体试剂的作用,使原有官能团离去,再由新的试剂与空位上的碳原子形成新的官能团。
2. 加成反应加成反应是指两个或多个分子中的双键或三键被破裂,形成新的单键或双键的反应。
常见的加成反应有烯烃的加成反应、芳香族化合物的加成反应等。
加成反应的机理是通过亲电试剂或自由基试剂的作用,使原有的双键或三键断裂,再由新的试剂与空位上的碳原子形成新的单键或双键。
3. 消除反应消除反应是指有机物中的两个官能团之间的原子或原子团被消除,形成双键或三键的反应。
常见的消除反应有醇的消除反应、卤代烃的消除反应等。
消除反应的机理是通过碱性试剂或热作用,使原有官能团中的原子或原子团离去,再由空位上的碳原子形成新的双键或三键。
4. 氧化还原反应氧化还原反应是指有机物中的氧化剂和还原剂之间的电子转移反应。
常见的氧化还原反应有醇的氧化反应、醛的还原反应等。
氧化还原反应的机理是通过氧化剂或还原剂的作用,使电子从一个分子转移到另一个分子,形成氧化物或还原物。
5. 缩合反应缩合反应是指两个或多个分子中的官能团之间形成新的化学键的反应。
常见的缩合反应有醛的缩合反应、胺的缩合反应等。
缩合反应的机理是通过亲核试剂或电子受体试剂的作用,使原有官能团之间形成新的化学键。
有机反应类型繁多,每种反应都有其独特的机理和应用场景。
在实际应用中,我们需要根据不同的反应类型和反应条件,选择合适的试剂和反应条件,以达到预期的反应目的。
干货--高中有机反应类型都在这儿了!一、取代反应有机物分子里的某些原子或原子团被其他原子或原子团所代替的反应叫做取代反应。
根据取代反应中反应物的不同及产物的特点,中学课本中常有这样一些形式。
(1)卤代反应,有机物分子里的某些原子或原子团被和卤素原子所代替的反应。
例如:CH4+Cl2 CH3Cl+HCl注意:甲苯和溴发生卤代反应时,反应条件的不同决定了到底是烃基发生取代(光照)还是和苯环发生取代(铁作催化剂)。
(2)硝化反应,有机物分子里的某些原子或原子团被和-NO2所代替的反应,一般是苯环上的原子被-NO2取代。
例如:(3)磺化反应,有机物分子里的某些原子或原子团被和-SO3H 所代替的反应,一般是苯环上的原子被-SO3H取代(注意磺酸基的书写,硫原子和碳原子相连接)。
例如:(4)成醚反应,醇分子之间脱水生成醚。
例如:(5)酯化反应,醇和羧酸及无机含氧酸可以根据“酸失羟基醇失氢”的原则发生酯化反应。
例如:此外,有机物的水解反应按照上述概念也应当属于取代反应,但由于发生水解的有机物种类较多,且特点各有不同,因此在描述这些反应时,常把它们剔出来,单列一个水解反应。
二、加成反应有机物分子中双键或三键或醛基等两端的碳原子或氧原子与其他原子或原子团直接结合生成新的化合物的反应,叫做加成反应。
(1)与H2加成,例如:(2)与H2O加成,例如:(3)与卤素单质加成,例如:(4)与卤化氢加成,例如:三、聚合反应(1)加聚反应,例如:(2)缩聚反应,醇与醇通过羟基之间脱水、醇与羧酸通过酯化反应、酚羟基和醛、氨基酸的羧基和氨基之间都可以在一定条件下通过缩聚反应形成高分子化合物。
例如:四、消去反应有机物在一定的条件下,从一个分子中脱去一个小分子(如H2O、HBr等),而生成不饱和(含双键或者三键)化合物的反应,叫做消去反应。
(1)卤代烃的消去反应,例如:(2)醇的消去反应,例如:注意:与-X、-OH相连的碳原子的邻位碳原子上如果没有氢原子,则卤代烃、醇一般不会发生消去反应。
高中化学:有机化学反应类型总结1. 能与Na反应的有机物①醇类:醇类物质的羟基能与Na反应产生氢气。
例如:②酚类:酚类物质的羟基能与Na反应产生氢气。
例如:③苦味酸:④糖类:糖类物质的羟基能与Na反应产生氢气。
例如:。
⑤羧酸:羧酸类物质的羧羟基能与Na反应产生氢气。
例如:。
⑥蛋白质、氨基酸:蛋白质和氨基酸等物质含有的羧羟基能与Na 反应产生氢气。
例如:。
⑦磺酸:磺酸类物质的磺酸基能与Na反应产生氢气。
例如:2. 能与反应的有机物①酚类:酚类物质的羟基能与NaOH发生反应生产酚钠。
例如:②苦味酸:③羧酸:羧酸类物质的羧基能与发生中和反应产生羧酸钠。
例如:。
④蛋白质、氨基酸:蛋白质和氨基酸等物质含有的羧基能与NaOH发生中和反应。
例如:。
⑤磺酸:磺酸类物质的磺酸基能与发生中和反应。
例如:⑥卤代烃的水解:卤代烃与NaOH溶液能发生水解反应。
例如:。
⑦卤代烃的消去:卤代烃与的醇溶液在加热条件下能发生消去反应。
例如:。
⑧酯和油脂的水解:酯和油脂的酯基在碱性条件下能够发生水解反应。
例如:⑨无水羧酸钠与NaOH固体在加热条件下能够反应产生烷烃。
例如:。
3. 能与反应的有机物①羧酸:羧酸类物质的羧基能与发生反应。
例如:。
②蛋白质、氨基酸:蛋白质和氨基酸等物质含有的羧基能与发生反应。
例如:。
③磺酸:磺酸类物质的磺酸基能与发生反应。
例如:4. 能与反应的有机物①酚类:酚类物质的羟基能与发生反应。
例如:②苦味酸:③羧酸:羧酸类物质的羧基能与发生反应。
例如:。
④蛋白质、氨基酸:蛋白质和氨基酸等物质含有的羧基能与发生反应。
例如:。
⑤磺酸:磺酸类物质的磺酸基能与发生反应。
例如:综上所述,含羧基的物质与(与反应,可以1:1生成,也可以2:1生成和)都反应;含酚羟基的物质只能与Na、NaOH、(与反应,只能以1:1生成)反应。
含醇羟基的物质只能与Na反应。
一、有机反应归类有机反应官能团及类别反应条件重点反应方程式举例取代反应卤代反应烷烃(通式)光照苯(通式)及同系物光照催化剂苯酚(-OH)醇(-OH)加热硝化反应苯及同系物浓硫酸、加热酯化反应酸(-COOH)醇(-OH):浓硫酸、加热水解卤代烃(-X)NaOH、水加热|+ HClCH3COOH+ CH3CH2OH CH3COOCH2CH3+H2O浓硫酸△CH4+Cl2CH3Cl+HCl光CH2Cl2+Cl2CHCl3+HCl(CHCl3又叫氯仿)光C2H5—Br + H2OC2H5—OH + HBr△CH3|+Cl2光照CH2Cl反应酯稀硫酸,加热碱、加热糖类稀酸C12H22O11+H2O 2 C6H12O6分子间脱水醇浓硫酸,140℃加成反应与H2(还原反应)烯烃、炔烃:苯及同系物:醛:加热、Ni作催化剂与X2、HX与H2O烯烃:炔烃:加热消去反应卤代烃NaOH、醇加热CH3COOC2H5+H2O CH3COOH + C2H5OH无机酸△CH3COOC2H5+H2O CH3COOH + C2H5OH无机酸△CH3COOC2H5+H2O CH3COOH + C2H5OH无机酸△CH3—C—H +H2 CH3C H2OHO催化剂△CH2=CH2+Br2 CH2Br—CH2BrCH2=CH2+ H2CH3CH3催化剂△CH2=CH2+Br2 CH2Br—CH2BrCH2=CH2+ H2O CH3CH2OH高温高压催化剂催化剂△CH3COOC2H5+NaOH CH3COONa + C2H5OH△醇 浓硫酸,加热170℃氧化反应有机物大多都能燃烧,碳碳双键、碳碳三键、苯的同系物、醛基都能被酸性高锰酸钾溶液氧化,乙醇能使重铬酸钾溶液变色。
醇催化氧化醛催化氧化被其他氧化剂氧化聚合 反应加聚反应缩聚反应n HOOC-COOH +n HOCH 2-CH 2OH HO[ OC-COOCH 2CH 2O]n H +(2n-1)H 2O中和 反应苯酚羧酸CH 3COOHCH 3COO -+H +具有酸的通性CH 3CHO +2Ag(NH 3)2OHCH 3COONH 4+2Ag+3NH 3+H 2O△CH 3CH 2OHH 2C=CH 2↑+H 2O浓硫酸 170℃一定条件CH 2-CH 2n CH 2=CH 2n2CH 3—C —H+O 2 2CH 3COOH O催化剂 △CH 3CHO+2Cu(OH)2CH 3COOH+C△CH 3CHO+2Cu(OH)2+NaOHCH 3COONa+Cu 2O+3H 2O△中和反应CH3COOH +NaOH = CH3COONa+H2O氨基酸NH2-CH2-COOH + NaOH NH2-CH2-COONa + H2O置换反应醇有机实验(反应)制取乙烯1、石蜡油分解制取乙烯2、制取乙炔淀粉水解(C6H10O5)n + nH2O nC6H12O6苯酚弱酸性蛋白质盐析(可逆)、变性(不可逆)、颜色反应(遇浓硝酸变黄)、水解反应(最终氨基酸)二、烃基及其衍生物的相互转化CaC2 + 2H2O HC CH↑+Ca(OH)2CH3CH2OH H2C=CH2↑+H2O浓硫酸170℃烃的衍生物的重要类别和主要化学性质:类别通式代表物分子结构特点主要化学性质卤代烃R—X溴乙烷C2H5BrC—X键有极性,易断裂1.取代反应:与NaOH溶液发生取代反应,生成醇;2.消去反应:与强碱的醇溶液共热,生成烯烃。
高三专题复习:有机化学的反应类型重要有机反应类型取代反应、加成反应、消去反应、聚合反应(含加聚反尖和缩聚反应)、氧化反应、还原反应 一、取代反应1.概念:有机物分子里某些原子或原子团被其它原子或原子团所代替的反应。
2.常见能发生取代反应的官能团有:醇羟基(-OH )、卤原子(-X )、羧基(-COOH )、酯基(-COO -)、肽键(-CONH -)等。
3.常见能发生取代反应的有机物如下图所示:(1)卤代反应:烃分子的氢原子被—X 所取代的反应。
(2)硝化反应:苯分子里的氢原子被—NO 2所取代的反应。
(3)磺化反应:苯分子里的氢原子被硫酸分子里的磺酸基(—SO 3H )所取代的反应。
(4)酯化反应:酸和醇起作用生成酯和水的反应。
羧酸和醇的酯化反应的脱水方式是“酸脱羟基醇脱氢”。
这种反应的机理可通过同位素原子示踪法进行测定。
(5)水解反应:一般指有机化合物在一定条件下跟水作用生成两种或多种物质的化学反应。
水解反应包括卤代烃水解、酯水解、糖水解、蛋白质水解。
其中皂化反应也属于水解反应。
皂化反应是指油脂在有碱存在的条件下水解,生成高级脂肪酸钠和甘油的反应。
取代反应 烃的卤代苯的磺化醇与氢卤酸的反应 酯化反应水解反应 醇、氨基酸等分子间的脱水苯的硝化塑料注意水解反应发生时有机物的断键部位,如乙酸乙酯水解时是与羰基相连的C -O 键断裂。
(蛋白质水解,则是肽键断裂) 二、加成反应1.能发生加成反应的官能团:碳碳双键、碳碳三键、苯环、羰基(醛、酮)等(包括:加水、加卤素、加氢、加卤化氢等) 2.加成反应有两个特点:(1)反应发生在不饱和的键上,不饱和键中不稳定的共价键断裂,然后不饱和原子与其它原子或原子团以共价键结合。
(2)加成反应后生成物只有一种(不同于取代反应)。
说明:(1)羧基和酯基中的碳氧双键不能发生加成反应。
(2)醛、酮的羰基与H 2发生加成反应,与其它物质一般难于加成。
三、加聚反应1.本质:通过自身加成反应形成高分子化合物。
高中化学反应类型归纳一、取代反应:1、卤代反应:有烃与卤素单质反应如423CH Cl CH Cl HCl +−−→+光(烷烃:光照) 2Fe Br +−−→Br -HBr+(芳香烃:催化剂)醇与氢卤酸反应例:25252C H OH HBr C H Br H O +→+2、硝化反应:如3|CH 2433H SO HNO +−−−−→浓2O N -2NO -2|NO 3|CH 23H O+ 3、碘化反应:如:()24H SO ∆+−−→浓3SO H -2H O+4、有机物的水解(卤代烃水解和酯的水解)例:25225C H Br H O C H OH HBr ∆+−−→+ 3252325H CH COOC H H O CH COOH C H OH +++5、分子间脱水(酯化反应,醇分子间脱水)例如:243253252H SO CH COOH C H OH CH COOC H H O ∆+−−−−→+浓 24025252521402H SO CC H OH C H OC H H O −−−−→+浓二、加成反应:1、不饱和烃与H2、X 2、HX 、H 2O 等加成如2332Ni CH CH H CH CH ∆≡+−−→ 22222||CH CH Br CH CH Br Br=+→-2、芳香烃与X 2、H 2加成例:23Ni H ∆+−−→ 3、||O C --与H 2加成(包括醛、酮单糖与H 2加成)如3232Ni CH CHO H CH CH OH ∆+−−→ 三、消去反应:1、卤代烃消去:X 所连碳原子上连有H 原子的卤代烃才能消去(NaOH 醇溶液)。
如:322322CH CH CH X NaOH CH CH CH NaX H O ∆-+−−→=++醇2、醇消去:羟基所连碳原子上的相邻碳原子上必须连有H 原子的醇才能消去(浓H 2SO 4,加热)。
如:2403232217033|||H SO C CH CH CH CH C CH H O CH CH OH --−−−−→-=+浓 四、聚合反应:1、加聚反应:不饱和有机物彼此加成而生成高分子化合物的反应。