化学反应工程二,三章答案
- 格式:doc
- 大小:450.50 KB
- 文档页数:33

化学反应工程第二章习题答案化工103班2-1银催化剂上进行甲醇氧化为甲醛的反应2CH3OHO22HCHO2H2O2CH3OH3O22CO24H2O进入反应器的原料中,甲醇:空气:水蒸气=2:4:1.3(摩尔比),反应后甲醇转化率达72%,甲醛的收率为69.2%,试计算:(1)反应的总选择性;(2)反应器出口组成。
解:根据甲醇:空气:水蒸气=2:4:1.3(摩尔比),以100mol进料为基准设χy分别为HCOH和co2生成量2CH3OHO22HCHO2H2O2CH3OH3O22CO24H2O对上式积分(n1)kct1cn1kcAcn1AOn111cn1n1AcA①0①式为无量纲对数形式可判别出kc的单位molm3n1kt111同理pn1pn1n1kn11ApAp的单位pa02-4在间歇反应器中进行等温二级、一级、零级均相反应,求出转化率由0变为0.9所需的时间,与转化率由0.9变为0.99所需时间之比。
解:等温二级反应111kt1ckt21AcA0cA2cA某A0.9某A0.999t190A0kcA0t1:t21:10等温一级反应ktlncA0cAln10同上解得t1t2kt1:t21:1等温零级反应ktcA0cA同上解得t10.9cA0A0kt20.09ck10:12-5某一反应在间歇反应器中进行,经8min后反应物转化了80%,经过18min后转化了90%,求表达此反应的动力学方程。
解dnrAAVdt积分后:tcA0dcArACcA0dcAcAcAn111n1n1AkcAkn1cA0cAt8min某A180%t18min某A290%28111kn1cn1cn1n1A0A01某A11811kn1cn11n1n1A0cA01某A2n2r2AkcA2-6某一气相一级反应A2RS,在恒温、恒压的实验反应器中进行,原料含75%A及25%惰性气体(摩尔比),经8min后其体积增加一倍。
求此时的转化率及该反应在此温度下的速率常数。


3 釜式反应器3.1在等温间歇反应器中进行乙酸乙酯皂化反应:325325+→+CH COOC H NaOH CH COONa C H OH该反应对乙酸乙酯及氢氧化钠均为一级。
反应开始时乙酸乙酯及氢氧化钠的浓度均为0.02mol/l ,反应速率常数等于5.6l/mol.min 。
要求最终转化率达到95%。
试问:(1) (1) 当反应器的反应体积为1m 3时,需要多长的反应时间?(2) (2) 若反应器的反应体积为2m 3,,所需的反应时间又是多少?解:(1)00222000001()(1)110.95169.6min(2.83)5.60.0210.95===⨯---=⨯=⨯-⎰⎰Af Af X X A A A A A A A A AA A dX dX X t C C R k C X kC X h(2) 因为间歇反应器的反应时间与反应器的大小无关,所以反应时间仍为2.83h 。
3.2拟在等温间歇反应器中进行氯乙醇的皂化反应:223222+→++CH ClCH OH NaHCO CH OHCH OH NaCl CO以生产乙二醇,产量为20㎏/h ,使用15%(重量)的NaHCO 3水溶液及30%(重量)的氯乙醇水溶液作原料,反应器装料中氯乙醇和碳酸氢钠的摩尔比为1:1,混合液的比重为 1.02。
该反应对氯乙醇和碳酸氢钠均为一级,在反应温度下反应速率常数等于5.2l/mol.h ,要求转化率达到95%。
(1) (1) 若辅助时间为0.5h ,试计算反应器的有效体积;(2) (2) 若装填系数取0.75,试计算反应器的实际体积。
解:氯乙醇,碳酸氢钠,和乙二醇的分子量分别为80.5,84 和 62kg/kmol,每小时产乙二醇:20/62=0.3226 kmol/h 每小时需氯乙醇:0.326680.591.11/0.9530%⨯=⨯kg h每小时需碳酸氢钠:0.326684190.2/0.9515%⨯=⨯kg h 原料体积流量:091.11190.2275.8/1.02+==Q l h 氯乙醇初始浓度:00.32661000 1.231/0.95275.8⨯==⨯A C mol l反应时间:02000110.95 2.968(1) 5.2 1.23110.95===⨯=-⨯-⎰⎰AfAf X X A A A A B A A dX dX t C h kC C kC X反应体积:0(')275.8(2.9680.5)956.5=+=⨯+=r V Q t t l (2) (2) 反应器的实际体积:956.512750.75===r V V l f3.3丙酸钠与盐酸的反应: 2525+⇔+C H COONa HCl C H COOH NaCl为二级可逆反应(对丙酸钠和盐酸均为一级),在实验室中用间歇反应器于50℃等温下进行该反应的实验。

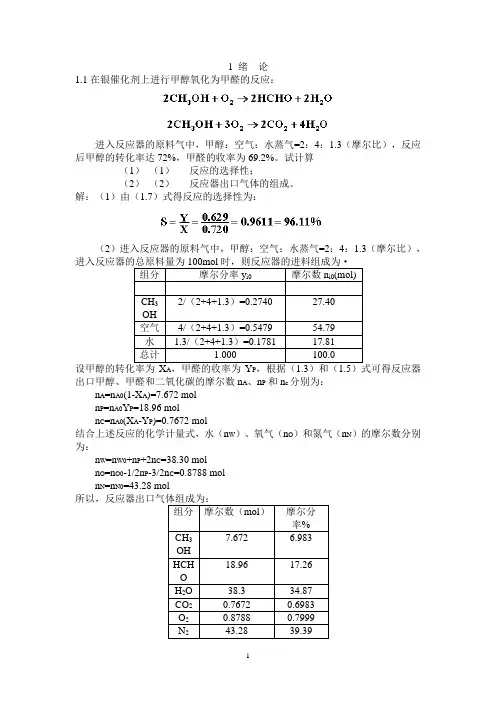
1 绪论1.1在银催化剂上进行甲醇氧化为甲醛的反应:进入反应器的原料气中,甲醇:空气:水蒸气=2:4:1.3(摩尔比),反应后甲醇的转化率达72%,甲醛的收率为69.2%。
试计算(1)(1)反应的选择性;(2)(2)反应器出口气体的组成。
解:(1)由(1.7)式得反应的选择性为:(2)进入反应器的原料气中,甲醇:空气:水蒸气=2:4:1.3(摩尔比),组分摩尔分率y i0 摩尔数n i0(mol)CH32/(2+4+1.3)=0.2740 27.40OH空气4/(2+4+1.3)=0.5479 54.79水 1.3/(2+4+1.3)=0.1781 17.81总计 1.000 100.0A P出口甲醇、甲醛和二氧化碳的摩尔数n A、n P和n c分别为:n A=n A0(1-X A)=7.672 moln P=n A0Y P=18.96 moln C=n A0(X A-Y P)=0.7672 mol结合上述反应的化学计量式,水(n W)、氧气(n O)和氮气(n N)的摩尔数分别为:n W=n W0+n P+2n C=38.30 moln O=n O0-1/2n P-3/2n C=0.8788 moln N=n N0=43.28 mol组分摩尔数(mol)摩尔分率%7.672 6.983CH3OH18.96 17.26HCHOH2O 38.3 34.87CO2 0.7672 0.6983O2 0.8788 0.7999N2 43.28 39.392 反应动力学基础2.4在等温下进行液相反应A+B→C+D,在该条件下的反应速率方程为:若将A和B的初始浓度均为3mol/l的原料混合进行反应,求反应4min时A的转化率。
解:由题中条件知是个等容反应过程,且A和B的初始浓度均相等,即为1.5mol/l,故可把反应速率式简化,得由(2.6)式可知代入速率方程式化简整理得积分得解得X A=82.76%。
2.6下面是两个反应的T-X图,图中AB是平衡曲线,NP是最佳温度曲线,AM是等温线,HB是等转化率线。

《化学反应工程》第三版(陈甘堂著)课后习题答案第二章均相反应动力学基础2-4三级气相反应2NO+O22NO2,在30℃及1kgf/cm2下反应,已知反应速率常数2kC=2.65×104L2/(mol2 s),若以rA=kppApB表示,反应速率常数kp应为何值?解:原速率方程rA=dcA2cB=2.65×104cAdt由气体状态方程有cA=代入式(1)2-5考虑反应A课所以kp=2.65×104×(0.08477×303) 3=1.564后当压力单位为kgf/cm2时,R=0.08477,T=303K。
答p p 2rA=2.65×10 A B =2.65×104(RT) 3pApBRT RTp表示的动力学方程。
解:.因,wwnAp=A,微分得RTVdaw案24网pAp,cB=BRTRT3P,其动力学方程为( rA)=dnAn=kA。
试推导:在恒容下以总压VdtVδA=3 1=21dnA1dpA=VdtRTdt代入原动力学方程整理得wdpA=kpAdt设初始原料为纯A,yA0=1,总量为n0=nA0。
反应过程中总摩尔数根据膨胀因子定义δA=n n0nA0 nA若侵犯了您的版权利益,敬请来信通知我们!Y http://.cn.co(1)mol/[L s (kgf/cm2) 3]m(1)则nA=nA01(n n0)δA1(P P0)δA(2)恒容下上式可转换为pA=P0所以将式(2)和式(3)代入式(1)整理得2-6在700℃及3kgf/cm2恒压下发生下列反应:C4H10发生变化,试求下列各项的变化速率。
(1)乙烯分压;(2)H2的物质的量,mol;(3)丁烷的摩尔分数。
解:P=3kgf/cm2,(1)课MC4H10=58,(2)w.krC2H4=2( rC4H10)=2×2.4=4.8kgf/(cm2 s)PC4H10=PyC4H101 dpC4H10= P dt2.4-1==0.8 s 3w(3)nC4H10=nyC4H10=n0(1+δC4H10yC4H10,0xC4H10)yC4H10dnH2dtdnH2dt=hdaw后n0=nC4H10,0=δC4H10rC4H10=反应开始时,系统中含C4H*****kg,当反应完成50%时,丁烷分压以2.4kgf/(cm2 s)的速率dyC4H10dt答1rCH=2.4224wdnC4H10dt案116×1000=2000mol582+1 1==21网dyC4H10=n0(1+δC4H10yC4H10,0xC4H10) dt=2000×(1+2×1×0.5)×0.8=3200 mol/s若侵犯了您的版权利益,敬请来信通知我们!Y http://.cno2C2H4+H2,dP=k[(δA+1)P0 P]=k(3P0 P)dtm(3)dpA1dP= dtδAdt2-9反应APS,( r1)=k1cA , ( r2)=k2cp,已知t=0时,cA=cA0 ,cp0=cS0=0, k1/k2=0.2。



3釜式反应器在等温间歇反应器中进行乙酸乙酯皂化反应:该反应对乙酸乙酯及氢氧化钠均为一级。
反应开始时乙酸乙酯及氢氧化钠的浓度均为 l ,反应速率常数等于。
要求最终转化率达到 95%。
试问:3( 1)( 1)当反应器的反应体积为1m 时,需要多长的反应时间?3,( 2)( 2)若反应器的反应体积为2m ,所需的反应时间又是多少?解:( 1)(2)因为间歇反应器的反应时间与反应器的大小无关,所以反应时间仍为。
拟在等温间歇反应器中进行氯乙醇的皂化反应:以生产乙二醇,产量为20 ㎏/h ,使用 15%(重量)的 NaHCO3水溶液及 30%(重量)的氯乙醇水溶液作原料,反应器装料中氯乙醇和碳酸氢钠的摩尔比为 1:1,混合液的比重为。
该反应对氯乙醇和碳酸氢钠均为一级,在反应温度下反应速率常数等于,要求转化率达到 95%。
(1)( 1)若辅助时间为,试计算反应器的有效体积;(2)( 2)若装填系数取,试计算反应器的实际体积。
62kg/kmol,每小时产解:氯乙醇,碳酸氢钠,和乙二醇的分子量分别为,84和乙二醇: 20/62= kmol/h每小时需氯乙醇:每小时需碳酸氢钠:原料体积流量:氯乙醇初始浓度:反应时间:反应体积:(2)( 2)反应器的实际体积:丙酸钠与盐酸的反应:为二级可逆反应(对丙酸钠和盐酸均为一级),在实验室中用间歇反应器于 50℃等温下进行该反应的实验。
反应开始时两反应物的摩尔比为 1,为了确定反应进行的程度,在不同的反应时间下取出10ml 反应液用的NaOH溶液滴定,以确定未反应盐酸浓度。
不同反应时间下,NaOH溶液用量如下表所示:时间, min0 10 20 30 50∝NaOH用量, ml现拟用与实验室反应条件相同的间歇反应器生产丙酸,产量为500kg/h ,且丙酸钠的转化率要达到平衡转化率的 90%。
试计算反应器的反应体积。
假定( 1)原料装入以及加热至反应温度( 50℃)所需的时间为 20min,且在加热过程中不进行反应;(2)卸料及清洗时间为 10min;(3)反应过程中反应物密度恒定。

3 釜式反应器在等温间歇反应器中进行乙酸乙酯皂化反应:该反应对乙酸乙酯及氢氧化钠均为一级。
反应开始时乙酸乙酯及氢氧化钠的浓度均为l,反应速率常数等于。
要求最终转化率达到95%。
试问:(1)(1)当反应器的反应体积为1m3时,需要多长的反应时间?(2)(2)若反应器的反应体积为2m3,,所需的反应时间又是多少?解:(1)(2) 因为间歇反应器的反应时间与反应器的大小无关,所以反应时间仍为。
拟在等温间歇反应器中进行氯乙醇的皂化反应:以生产乙二醇,产量为20㎏/h,使用15%(重量)的NaHCO水溶液及30%(重3量)的氯乙醇水溶液作原料,反应器装料中氯乙醇和碳酸氢钠的摩尔比为1:1,混合液的比重为。
该反应对氯乙醇和碳酸氢钠均为一级,在反应温度下反应速率常数等于,要求转化率达到95%。
(1)(1)若辅助时间为,试计算反应器的有效体积;(2)(2)若装填系数取,试计算反应器的实际体积。
解:氯乙醇,碳酸氢钠,和乙二醇的分子量分别为,84 和 62kg/kmol,每小时产乙二醇:20/62= kmol/h每小时需氯乙醇:每小时需碳酸氢钠:原料体积流量:氯乙醇初始浓度:反应时间:反应体积:(2)(2)反应器的实际体积:丙酸钠与盐酸的反应:为二级可逆反应(对丙酸钠和盐酸均为一级),在实验室中用间歇反应器于50℃等温下进行该反应的实验。
反应开始时两反应物的摩尔比为1,为了确定反应进行的程度,在不同的反应时间下取出10ml反应液用的NaOH溶液滴定,以确定500kg/h,且丙酸钠的转化率要达到平衡转化率的90%。
试计算反应器的反应体积。
假定(1)原料装入以及加热至反应温度(50℃)所需的时间为20min,且在加热过程中不进行反应;(2)卸料及清洗时间为10min;(3)反应过程中反应物密度恒定。
解:用A,B,R,S分别表示反应方程式中的四种物质,利用当量关系可求出任一时刻盐酸的浓度(也就是丙酸钠的浓度,因为其计量比和投量比均为1:1)为:于是可求出A的平衡转化率:现以丙酸浓度对时间作图:由上图,当CA=×l时,所对应的反应时间为48min。

第二章 均向反应动力学1.在473K 等温及常压下进行气相反应:(1)3→A R 1.5R A r C = (2)2→A S0.5S Ar C =(3)→A T 2.1TA r C= 式中C A 为反应物A 的浓度(kmol/l ),原料中A 和惰性气体各为一半(体积比),试求当A 的转化率达85%时,其转化速率是多少?解:先求出总摩尔变化数δA ,首先将产物的生成速率变为对应的反应物的转化速率:10.53AR R A r r C ==10.252AS S A r r C == 2.1AT T A r r C== 总反应速率为: 2.85A AR AS AT AR r r r C =++= 以一摩尔反应物A 为基准,总摩尔变化数为:0.50.25 2.13210.4392.85 2.85 2.85A δ=⨯+⨯+-=初始浓度为:200030.10130.5 1.28810/8.31410473A A P y C kmol l RT --⨯===⨯⨯⨯则有:2300(1) 1.288100.151.62810/110.50.4390.85A A A A A A C X C kmol ly X δ---⨯⨯===⨯++⨯⨯332.85 2.85 1.62810 4.64010/(.min)A A R C kmol l --==⨯⨯=⨯2.可逆一级液相反应PA −−←−→−,已知0,m kmol 5.0P030=⋅=-c c A ;当此反应在间歇反应器中进行,经过8min 后,A 的转化率为33.3%,而平衡转化率是66.7%,求此反应的动力学方程式。
解:()()x c k x c k txc t c x c c x c c c c k c k c k c k tc r A02A01A0A A0P A0A A A02A 1P 2A 1AA 1d d d d )1(d d --==-=-=--=-=-=-⎩⎨⎧=====+-+-=xx t t x t txk k k xx k k k tx,0,0d )(d )(d d 2112118333.022667.01667.01)1()(ln 121e e e 0A e 0A Ae Pe 21121121=====-=-=-====+-+-t x k k K x x x c x c c c k k K t k xk k k k k ()PA A A 1211212121212102888.005776.0d d min02888.0min 05776.02/08664.086931.05.0ln 18333.02111ln 1c c tcr k k k k k k k k k k k k -=-=-⎩⎨⎧==⎩⎨⎧==+=+=+-=⎪⎪⎭⎫ ⎝⎛⨯⎪⎭⎫ ⎝⎛+-+--- 3.液相自催化反应的动力学方程A+P-P+P 速率表达式00()/(.) c 0.95/ c 0.05/AA A P A P dc r kc c mol l h mol L mol L dt -=-===,1h 后测得速率最大值,求反应速率常数。
化学反应工程知到章节测试答案智慧树2023年最新天津大学第一章测试1.碳球在空气中燃烧生成二氧化碳,初始的碳和氧气的摩尔比为1:2,初始的碳球直径为5mm,随着反应的进行,碳球直径变为1mm。
请问此时气相的总摩尔数是:参考答案:不变的2.碳球在空气中燃烧生成一氧化碳,初始的碳和氧气的摩尔比为1:1,初始的碳球直径为5mm,随着反应的进行,碳球直径变为1mm。
请问此时气相的总摩尔数是:参考答案:增加的3.碳球在空气中燃烧生成二氧化碳,初始的碳和氧气的摩尔比为1:1,初始的碳球直径为5mm,随着反应的进行,碳球直径变为1mm。
请问此时碳的转化率与氧气的转化率:参考答案:相等4.碳球在空气中燃烧生成一氧化碳,初始的碳和氧气的摩尔比为1:0.5,初始的碳球直径为5mm,随着反应的进行,碳球直径变为1mm。
请问此时碳的转化率与氧气的转化率:参考答案:相等5.碳球在空气中燃烧首先生成一氧化碳,随后深度氧化成二氧化碳,初始的碳和氧气的摩尔比为1:1,初始的碳球直径为5mm,随着反应的进行,碳球直径变为1mm。
两步反应的反应进度:参考答案:只有当两种碳氧化物的生成量相同时才相等;两步反应有各自的反应进度第二章测试1.反应速率定量描述了反应器中某一点的反应快慢。
参考答案:对2.当多个反应同时发生时,只有一个相对反应速率,即。
参考答案:错误;各步反应有各自的相对反应速率3.非基元反应的化学计量系数可以同时乘或除以非零的数,基元反应也同样。
参考答案:仅对非基元反应的描述正确;错误;仅对基元反应的描述错误4.对气相反应因其总摩尔数发生变化,所以CO2的浓度由下式计算:参考答案:错误5.反应速率方程中的摩尔浓度可以替换成摩尔数或反应体积。
参考答案:错第三章测试1.参考答案:2.参考答案:越小3.判断正误:在间歇釜式反应器中进行的反应,达到一定转化率所需反应时间与反应原料的初始浓度无关。
()参考答案:错4.在绝热的理想连续釜式反应器中进行某放热反应,关于反应器中温度分布描述正确的是()参考答案:反应温度高于进料温度;反应釜内的温度均一5.C点;A点第四章测试1.参考答案:1台PFR2.判断正误:相同的原料及温度条件下,在由两台反应体积均为1m3的串联活塞反应器(工况1)和一台反应体积为2 m3的活塞流反应器(工况2)中,分别进行反应A→P。
2 反应动力学基础2.1在一体积为4L 的恒容反应器中进行A 的水解反应,反应前 A 的含量为12.23%(重量),混合物的密度为1g/mL ,反应物A 的分子量为88。
在等温常压解:利用反应时间与组分A 的浓度变化数据,作出C A ~t 的关系曲线,用镜面法求得t=3.5h 时该点的切线,即为水解速率。
切线的斜率为0.760.125/.6.1α-==-mol l h由(2.6)式可知反应物的水解速率为 0.125/.-==dC A r mol l h A dt2.2在一管式反应器中常压300℃等温下进行甲烷化反应:2423+→+CO H CH H O催化剂体积为10ml ,原料气中CO 的含量为3%,其余为N 2,H 2气体,改变进口原料气流量Q 0解:是一个流动反应器,其反应速率式可用(2.7)式来表示00000(1)(1)-==-=-=-A A RA A A A A A A AdF r dV F F X Q C X dF Q C dX 故反应速率可表示为:0000(/)==A A A A A R R dX dX rQ C C dV d V Q用X A ~V R /Q 0作图,过V R /Q 0=0.20min 的点作切线,即得该条件下的dX A /d(V R /Q 0)值α。
0.650.04 1.790.34α-==故CO 的转化速率为 40030.10130.03 6.3810/8.31410573--⨯===⨯⨯⨯A A P C mol l RT4300 6.3810 1.79 1.1410/.min (/)--==⨯⨯=⨯A A A R dX r C mol l d V Q2.3已知在Fe-Mg 催化剂上水煤气变换反应的正反应动力学方程为:20.850.4/-=⋅w CO CO r k y y kmol kg h式中y CO 和y C O2为一氧化碳及二氧化碳的瞬间摩尔分率,0.1MPa 压力及700K 时反应速率常数k W 等于0.0535kmol/kg.h 。
2 反应动力学基础2.1在一体积为4L 的恒容反应器中进行A 的水解反应,反应前 A 的含量为12.23%(重量),混合物的密度为1g/mL ,反应物A 的分子量为88。
在等温常压解:利用反应时间与组分A 的浓度变化数据,作出C A ~t 的关系曲线,用镜面法求得t=3.5h 时该点的切线,即为水解速率。
切线的斜率为0.760.125/.6.1α-==-mol l h由(2.6)式可知反应物的水解速率为0.125/.-==dC A r mol l hAdt2.2在一管式反应器中常压300℃等温下进行甲烷化反应:2423+→+CO H CH H O催化剂体积为10ml ,原料气中CO 的含量为3%,其余为N 2,H 2气体,改变进口原料气流量Q 0解:是一个流动反应器,其反应速率式可用(2.7)式来表示00000(1)(1)-==-=-=-A A RA A A A A A A AdF r dV F F X Q C X dF Q C dX故反应速率可表示为:000(/)==A AA A A R R dX dX r QC C dV d V Q用X A ~V R /Q 0作图,过V R /Q 0=0.20min 的点作切线,即得该条件下的dX A /d(V R /Q 0)值α。
0.650.04 1.790.34α-==故CO 的转化速率为40030.10130.03 6.3810/8.31410573--⨯===⨯⨯⨯A A P C mol l RT4300 6.3810 1.79 1.1410/.min(/)--==⨯⨯=⨯AA A R dX r C mol l d V Q2.3已知在Fe-Mg 催化剂上水煤气变换反应的正反应动力学方程为: 20.850.4/-=⋅w CO CO r k y y kmol kg h式中y CO 和y CO2为一氧化碳及二氧化碳的瞬间摩尔分率,0.1MPa 压力及700K 时反应速率常数k W 等于0.0535kmol/kg.h 。
(完整版)化学反应⼯程作业答案3-2 在等温间歇反应器中进⾏皂化反应325325CH COOC H NaOH CH CHCOONa C H OH +→+ 该反应对⼄酸⼄酯和氢氧化钠均为⼀致,反应开始时⼄酸⼄酯和氢氧化钠的浓度均为0.02mol/L ,反应速率常数为5.6L/(min ·mol ),要求最终转化率为0.95,试求当反应器体积为31m 、32m 时,所需的反应时间是多少?解: A B C D +=+A AB r kC C =?? 设A 的转化率为A x ,B 的转化率为B xB B BB B B n n n x n n --?== ∵ 00A B n n = , A B n n ?=? ,∴ A BC C =t=0Afx AA adx C r ?=020Afx AA A dx C k C ??=01(1)A Af kC x --01A k C =169.6 min t 与反应体积⽆关。
∴31m 、所需反应时间均为169.6min3-3 在平推流反应器中进⾏等温⼀级反应,出⼝转化率为0.9,现将该反应移到⼀个等体积的全混流反应器中进⾏,且操作条件不变,问出⼝转化率是多少?解:对于平推流反应器: 1ln1Af k x τ=- 0Bv v τ= 对于全混流反应器: ''1Af Afx k x τ=- 0Rv v τ=∴ 1ln1Af x -='1Af Afx x -=2.3 ∴ 'Af x =0.6973-6 已知某均相反应,反应速率2,17.4A A r kC k ml ==/(mol ﹒min ),物料密度恒定为0.75g/ml ,加料流量为7.14L/min ,0A C =7.14mol/L ,反应在等温下进⾏,试计算下列⽅案的转化率各为多少?(1) 串联两个体积0.253m 的全混流反应器。
(1) 0R v v τ==30.251027.14=35mm ,设转化率为12,f f x x 12011(1)f A f x k C x τ=-?121(1)f f x x -=4.35 ?1f x =0.622∴ 101(1)A A f C C x =-=7.14×(1-0.622)=2.7mol/L 22221221(1)(1)f f A f f x x k C x x τ=--=1.64∴ 20.467f x = 12(1)Af A f C C x =-=1.44 ∴ 0(1)0.80Af A Af Af C C x x =-?= (2) 00.2510007.14R V V τ?===35min 12011(1)f A f x k C x τ=-?121(1)f f x x -=4.35 ?1f x =0.622 ∴ 101(1)A A f C C x =-=7.14×(1-0.622)=2.7mol/L 2212211.64(1)(1)f f A f f x x k C x x τ=?=--∴20.62f x =12(1)Af A f C C x =-=2.7×(1-0.62)=1.026∵0(1)Af A Af C C x =-∴ 0.856Af x = (3) 00.2510007.14R v v τ?===35min 1011(1)f A f x k C x τ=?-1f x =0.813∴ 101(1)A A f C C x =-=7.14×(1-0.813)=1.3422121(1)f A f x k C x τ=-?222(1)f f x x -=0.816∴ 2f x =0.347∴ 12(1)Af A f C C x =-=1.34×(1-0.347)=0.875 ∵0(1)∴ 0.877Af x = (4) 35min τ=1011(1)f A f x k C x τ=?-1f x =0.813101(1)A A f C C x =-=1.342121(1)f A f x k C x τ=?-2f x 0.449∴ 12(1)Af A f c C x =-=1.34×(1-0.449)=0.738 ∵0(1)Af A Af C C x =-0.897Af x =3-7 液相⾃催化反应A →P,反应速率23,10/()A A p r kc c k m kmol s -==?,进料体积流量300.002/,V m s =进料浓度3002/,0.01A p c kmol m c ==。
第一章1. Fogler 《化学反应工程》(英文版)Page 31,P1-11B.解:摩尔衡算:0Vj j j j dN F F r dV dt-+=⎰C :the corn steep liquor ;R :RNA ;P :penicillin.假设细胞为全混釜反应器,C 完全反应,R 不排出反应器,P 全部排出反应器 在非稳态操作条件的摩尔平衡:(质量平衡类似,将各量表示成以质量为基准就行)0C F =,0CdN dt=,00C C F r V += 00R F =,0R F =,R R dN r V dt=0P F =,0CdN dt=,0P P F r V -+=2. Fogler 《化学反应工程》(英文版)Page 33,P1-15B.解:由题目给出的条件可知,对于A B →的反应F A0=5 mol/h ,v 0=10 L/h ,C A0=0.5 mol/L对于CSTR : 摩尔衡算:0A AAF F V r -=- 动力学:(1)A r k -=(2)A A r kC -=(3)2A A r kC -=摩尔流率与浓度关系:000A A F C v =0A A A F C v C v ==浓度为变量的摩尔衡算方程:00000A A A AA AC v C v C C V v r r --==--当消耗99%的组分A 时,00.01A A C C =,代入上式可得:000000.010.99A A A A AC C C V v v r r -==--代入动力学: (1)00000.990.99A A A C C V v v r k==- 代入数据得到:V=99 L (2)000000000.990.990.9999(0.01)A A A A A A C C C v V v v v r kC k C k====- 代入数据得到:V=2750 L (3)000000022000.990.990.999900(0.01)A A A A A A A C C C v V v v v r kC k C kC ====- 代入数据得到:V=66000 L对于PFR : 摩尔衡算:AA dF r dV= 动力学:(1)A r k -=(2)A A r kC -=(3)2A A r kC -=摩尔流率与浓度关系:000A A F C v =0A A A F C v C v ==浓度为变量的摩尔衡算方程:0()A A d C v r dV= 0AAdC dV v r = 00AA C AC AdC V v r =⎰代入动力学: (1)000000000000.99()(0.01)AA A A C C A AA A A A A C C A v v v dC dC V v v C C C C C r k k k k ===-=-=-⎰⎰ 代入数据得到:V=99 L (2)00000000ln ln ln1000.01AA C A A AC A A A v C v C v dC V v kC k C k C k ====-⎰代入数据得到:V=127.9 L (3)000020001111()()0.01AA C A C AA A A A v v dC V v kC k C C k C C ==-=--⎰ 代入数据得到:V=660 L 对于BR : 摩尔衡算:AA dN r V dt= 动力学:(1)A r k -=(2)A A r kC -=(3)2A A r kC -=浓度为变量的摩尔衡算方程:AA C A A C dC dt r =⎰代入动力学: (1)000.001A A C C t k-=代入数据得到:t=9.99h (2)001ln0.001A A C t k C =代入数据得到:t=19.2h (3)00111()0.001A A t k C C =- 代入数据得到:t=666h3. Fogler 《化学反应工程》(中文版)Page 23,P1-12C.解:由题目条件可知,反应A B C →+,在恒体积、等温、完全混合的间歇釜中进行,且V=20 L ,N A0=20 mol ,C A0=N A0/V=1 mol/L (1) 摩尔衡算:AA dN r V dt= 动力学:A A r kC -=物质量与浓度的关系:A A N C V =浓度为变量的摩尔衡算方程:()A A d C V r V dt= A A dC V r V dt=AA dC dt r =0AA C AC AdC t r =⎰代入动力学:001ln AA C A A C A A C dC t kC k C ==-⎰代入数据得:t=7.99 min(2) 摩尔衡算:AA dN r V dt= 动力学:2A A r kC -=物质量与浓度的关系:A A N C V = 浓度为变量的摩尔衡算方程:()A A d C V r V dt= A A dC V r V dt=AA dC dt r =0AA C AC AdC t r =⎰代入动力学:020111()AA C A C AA A dC t kC k C C ==--⎰ 代入数据得:t=9.5 min(3)假设反应气体为理想气体: 状态方程:PV NRT =00208.31440033256000.02N RT P Pa Pa V ⨯⨯=== 408.31440066512000.02t t N RT P Pa Pa V ⨯⨯===第二章1. 在一个恒体积的间歇反应器中进行液相等温不可逆反应:A B →若反应为二级、一级、零级均相反应,分别求出转化率由0至0.9所需时间与转化率由0.9至0.99所需时间之比。
第二章习题1.动力学方程的实验测定时,有采用循环反应器的,为什么?答:循环反应器行为与全混流反应器相同,可以得到反应速率的点数据,而且反应器进出口浓度差比较大,对分析精度要求不很高。
2.为什么可逆吸热反应宜选平推流反应器且在高温下操作,而可逆放热反应却不是?根据可逆放热反应的特点,试问选用何种类型反应器适宜?为什么?答:可逆吸热反应的反应速率与化学平衡都随温度的升高而升高,高温下操作对二者都有利。
可逆放热反应的化学平衡随温度的升高向反应物方向移动,对达到高转化率不利。
对此类反应,可选用多段绝热反应器或换热条件较好的管式反应器。
3.一级反应A→P,在一体积为V P的平推流反应器中进行,已知进料温度为150℃,活化能为84kJ·mol-1,如改用全混流反应器,其所需体积设为V m,则V m/V p应有何关系?当转化率为0.6时,如果使V m=V p,反应温度应如何变化?如反应级数分别为n=2,1/2,−1时,全混流反应器的体积将怎样改变? 解:)1ln()1()exp()1ln()1()1(CSTR )1ln(11d 1)(d PFR )exp()(A A Ap mA A A pm A 0A AA0m A A00AA A00A A A0P A 0A A AAx x x RT ERT E x x k kx V V x k c x F V x kc x x kc r x F V c RTE k kc r x x ----=---=-=--=-=-=-==-⎰⎰)1ln()1()1ln()1( IF A A A A A P m m p x x x x x k k x V V T T A---=---==()()K07.43215.42302064.015.423876.234929.015.423876.23exp 6109.0637.115.42315.423314.884000exp 1)6.01ln(6.016.0exp 10.6and 1IF m m mmmmm m m P m P A Pm =-=--=-⎪⎪⎭⎫ ⎝⎛⎪⎪⎭⎫ ⎝⎛-=⨯⎪⎪⎭⎫⎝⎛⎪⎪⎭⎫⎝⎛-=--⨯⎪⎪⎭⎫ ⎝⎛--===T T T T T T T TT T T T T R E x V V mnn n n kc x F V c V V cV V kc x F V n c V V kc x F V n c V V kc x F V n AfAf A0m 1Am1m 2A1m 1m 1AAA0m 2/1A 1m 2/1m 2/1A A A0m A1m 2m 2A A 0A m 1,1,2/11,2==⎪⎪⎪⎩⎪⎪⎪⎨⎧==-=======---或4. 在体积V R =0.12m 3的全混流反应器中,进行反应S R B A 21+−−←−→−+kk,式中k 1=7m 3kmol -1min -1,k 2=3m 3kmol -1min -1,两种物料以等体积加入反应器中,一种含2.8kmolA ·m -3,另一种含1.6kmolA ·m -3。
设系统密度不变,当B 的转化率为75%时,求每种物料的流量。
解()13B A 13A B0B 13A 3A 3S R 3B 3B030A hrm 24.0248.0hrm 48.0156012.0min1504.02.08.0minmkmol 04.06.06.032.08.07mkmol 8.06.04.1m kmol 6.075.08.0mkmol 2.075.018.0mkmol 8.026.1m kmol 4.128.2---------====⨯==-=--=⋅=⨯⨯-⨯⨯=-⋅=-=⋅=⨯==⋅=-=⋅==⋅==v v v r c c r c c c c c c 半:每一股是总物料量的一τ5. 可逆一级液相反应PA −−←−→−,已知0,m kmol 5.0P030=⋅=-c c A ;当此反应在间歇反应器中进行,经过8min 后,A 的转化率为33.3%,而平衡转化率是66.7%,求此反应的动力学方程式。
解()()xc k x c k tx c tc x c c x c c c c k c k c k c k tc r A02A01A0A A0P A0A A A02A 1P 2A 1A A 1d d d d )1(d d --==-=-=--=-=-=-⎩⎨⎧=====+-+-=xx t t x t txk k k xx k k k tx ,0,0d )(d )(d d 2112118333.022667.01667.01)1()(ln 121e e e 0A e0A AePe 21121121=====-=-=-====+-+-t x k k K x x x c x c c c k k K t k xk k k k k()PA A A 1211212121212102888.005776.0d d min 02888.0min 05776.02/08664.086931.05.0ln 18333.02111ln 1c c tc r k k k k k k k k k k k k -=-=-⎩⎨⎧==⎩⎨⎧==+=+=+-=⎪⎪⎭⎫⎝⎛⨯⎪⎭⎫ ⎝⎛+-+---6. 平行液相反应A →P r P =1 A →R r R =2c A A →S r S =c A 2已知c A0=2kmol ·m -3,c Af =0.2kmol ·m -3,求下列反应器中,c P 最大为多少? (1) 平推流反应器;(2)全混流反应器;(3)两相同体积的全混流反应器串联,c A1=1 kmol ·m -3。
解3-A0Af A2A Af 0A p P AP AfA0p 2A 2AA SR P PP mkmol 5.02112.011)1(1)1(1d )1(1)(d 1PFR For )1(1211A0AfA Af⋅=+-+=+-+=+=-=-=+=++=++=⎰⎰c c c c c c S c c S c c S c c c r r r r S c c c c3-22Af Af A0Af A0p P mkmol 25.1)2.01(1)2.02()1(1)()(CSTRFor ⋅=+-=+-=-=c c c c c S c3-22P2Af A1P1A1A0P mkmol 81.056.025.0)2.01(1)2.01()11(1)12()()(Seriesin CSTR For two ⋅=+=+-++-=-+-=S c c S c c c7. 自催化反应A+P →2P 的速率方程为:−r A =kc A c P ,k =l m 3kmol -1min -1,原料组成为含A 13%,含P 1%(摩尔百分数),且c A0+c P0= l kmol ·m -3,出口流中c P = 0.9 kmol ·m -3,计算采用下列各种反应器时的空间时间(τ=V R /V 0)。
(1)平推流反应器;(2)全混流反应器;(3)平推流与全混流反应器的最佳组合;(4)全混流反应器与一分离器的最佳组合。
解AA 2A0A A0A A0P A A Af Ain 3A0)1()1(9.00714.0141m1kmol x x kc x c x kc c kc r x x c -=-==-===⋅=()()min 76.40714.010714.09.019.0ln 11111ln1d 11111d 1d PFRFor Ain Ain Af AfA0A A 0A AAAA0A AA0Af AinAfAinAf Ain=⎪⎭⎫ ⎝⎛-⎪⎭⎫ ⎝⎛-⨯=⎪⎪⎭⎫⎝⎛-⎪⎪⎭⎫⎝⎛-=⎪⎪⎭⎫⎝⎛+-=-=-=⎰⎰⎰xx xx kc x x x kc xx x kc r x c x x x x x x τ()()min2.99.09.010714.09.01111CSTRFor AfAf 20A Ain Af 0A =⨯--⨯⨯=--=x x kc x x c τ()min91.320.271.120.25.015.09.019.0ln m kmol 5.0)1(min71.15.0)5.01(0714.05.0111)1(15.00210d d ,1PFR CSTR For 2123A1A0A1A11A Ain Af 0A 1A1A AA A A =+=+==⎪⎭⎫ ⎝⎛-⎪⎭⎫ ⎝⎛-=⋅=-==⨯--⨯⨯=--⨯===-=---+-τττττx c c x x x x kc x x x r r r ,,有令的极值点相同与由于()min71.15.0)5.01(0714.05.0111)1(15.0,0d d CSTR For A1A1AinAf A01A AA =⨯--⋅⨯=--===-+x x x x kc x x r τ分离器8. 在两个串联的全混流反应器中进行一级反应,进出口条件一定时,试证明当反应器大小相同时,两个反应器的总容积最小。
证AfA0A1Af0A 2A1Af2A11A 21Af1A AfAf1A 21A 0A 1A 1A 0A 1fA Af A0010d )(d 11)(c c c c c c kc kcc c kkc c kc c c kkc c kc c c r c c A ===+-=+-=-=-=-=--=τττττR2R121AfA0AfAf A02AfA0Af0A 0A 1111111V V c c k kkc c c c c k kc c k c ==⎪⎪⎭⎫⎝⎛-=-=⎪⎪⎭⎫⎝⎛-=-=ττττ9. 半衰期为20小时的放射性流体以0.1m 3hr -1的流量通过两个串联的40m 3全混流反应器后,其放射性衰减了多少? 解()()()()()()9955.09327.0119327.09327.0103466.0400111.040hr03466.05.02A A AA A0A A0A0A AA01200A A =--=-=---=--====---总转化率。
为第二釜,单釜转化率仍:第一釜代入数据对全混流反应器,首先求反应速率常数:期的概念。
只有一级反应存在半衰x x x x kc x c c r c c k eec c kktτ10. A 进行平行分解反应,其速率式为↗R r R =1 kmol ·m -3min -1 A →S r S =2c A kmol ·m -3min -1↘T r T =c A kmol ·m -3min -1其中R 是所要求的目的产物,c A0=1kmol ·m -3。