
1.A rndt-Eister 反应
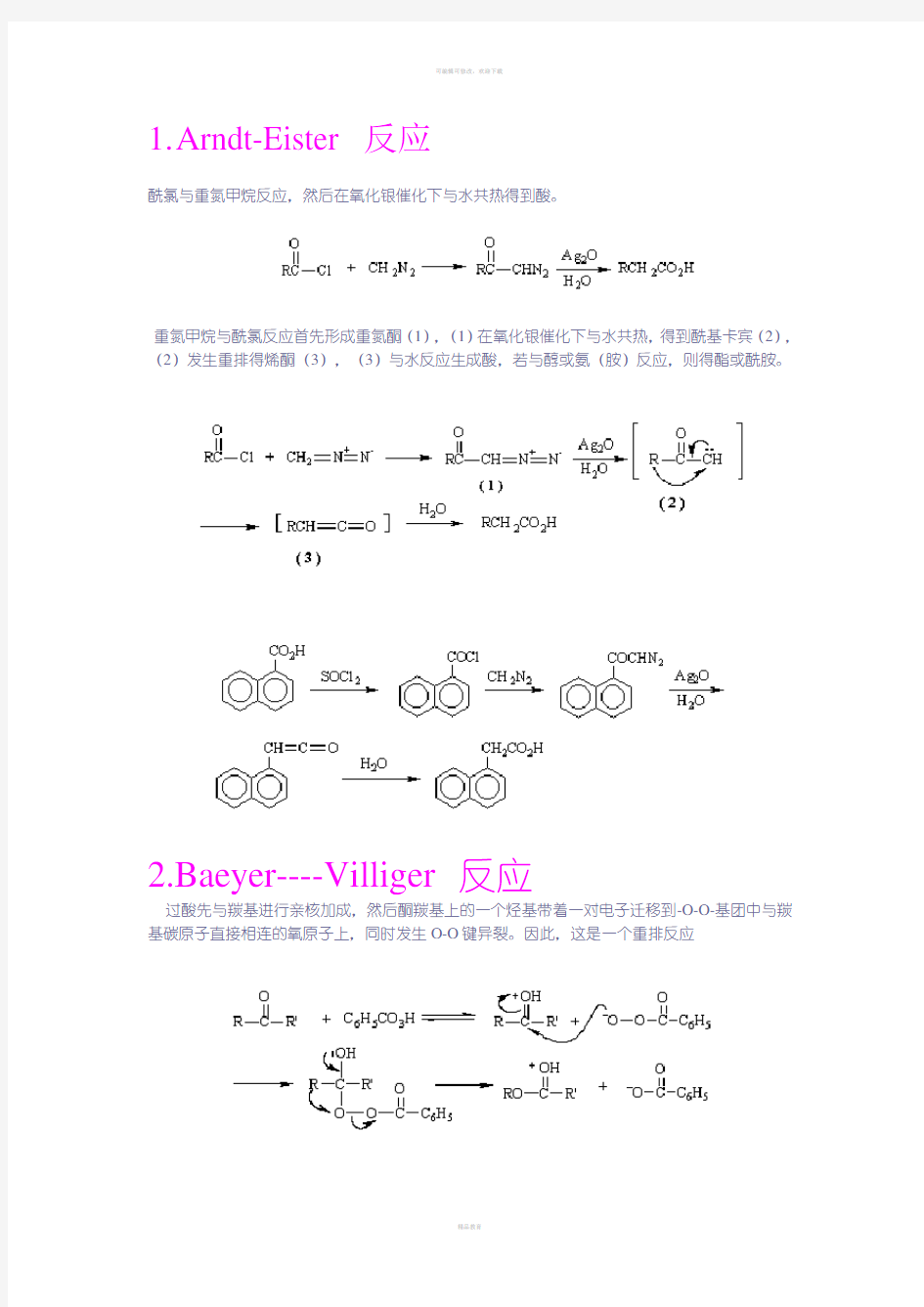
酰氯与重氮甲烷反应,然后在氧化银催化下与水共热得到酸。
重氮甲烷与酰氯反应首先形成重氮酮(1),(1)在氧化银催化下与水共热,得到酰基卡宾(2),(2)发生重排得烯酮(3),(3)与水反应生成酸,若与醇或氨(胺)反应,则得酯或酰胺。
2.Baeyer----Villiger 反应
过酸先与羰基进行亲核加成,然后酮羰基上的一个烃基带着一对电子迁移到-O-O-基团中与羰基碳原子直接相连的氧原子上,同时发生O-O键异裂。因此,这是一个重排反应
具有光学活性的3---苯基丁酮和过酸反应,重排产物手性碳原子的枸型保持不变,说明反应
属于分子内重排:
不对称的酮氧化时,在重排步骤中,两个基团均可迁移,但是还是有一定的选择性,按迁移能力其顺序为:
醛氧化的机理与此相似,但迁移的是氢负离子,得到羧酸。
酮类化合物用过酸如过氧乙酸、过氧苯甲酸、间氯过氧苯甲酸或三氟过氧乙酸等氧化,可在
羰基旁边插入一个氧原子生成相应的酯,其中三氟过氧乙酸是最好的氧化剂。这类氧化剂的特点
是反应速率快,反应温度一般在10~40℃之间,产率高。
3.Beckmann 重排
肟在酸如硫酸、多聚磷酸以及能产生强酸的五氯化磷、三氯化磷、苯磺酰氯、亚硫酰氯等作用下发生重排,生成相应的取代酰胺,如环己酮肟在硫酸作用下重排生成己内酰胺:
在酸作用下,肟首先发生质子化,然后脱去一分子水,同时与羟基处于反位的基团迁移到缺电子的氮原子上,所形成的碳正离子与水反应得到酰胺。
迁移基团如果是手性碳原子,则在迁移前后其构型不变,例如:
例
4.Birch还原
芳香化合物用碱金属(钠、钾或锂)在液氨与醇(乙醇、异丙醇或仲丁醇)的混合液中还原,苯环可被还原成非共轭的1,4-环己二烯化合物。
首先是钠和液氨作用生成溶剂化点子,然后苯得到一个电子生成自由基负离子(Ⅰ),这是苯环的л电子体系中有7个电子,加到苯环上那个电子处在苯环分子轨道的反键轨道上,自由基负离子仍是个环状共轭体系,(Ⅰ)表示的是部分共振式。(Ⅰ)不稳定而被质子化,随即从乙醇中夺取一个质子生成环己二烯自由基(Ⅱ)。(Ⅱ)在取得一个溶剂化电子转变成环己二烯负离子(Ⅲ),(Ⅲ)是一个强碱,迅速再从乙醇中夺取一个电子生成1,4-环己二烯。
环己二烯负离子(Ⅲ)在共轭链的中间碳原子上质子化比末端碳原子上质子快,原因尚不清楚。
取代的苯也能发生还原,并且通过得到单一的还原产物。例如
5.Bouveault---Blanc 还原
脂肪族羧酸酯可用金属钠和醇还原得一级醇。α,β-不饱和羧酸酯还原得相应的饱和醇。芳香酸酯也可进行本反应,但收率较低。本法在氢化锂铝还原酯的方法发现以前,广泛地被使用,非共轭的双键可不受影响。
首先酯从金属钠获得一个电子还原为自由基负离子,然后从醇中夺取一个质子转变为自由基,再从钠得一个电子生成负离子,消除烷氧基成为醛,醛再经过相同的步骤还原成钠,再酸化得到相应的醇。
醛酮也可以用本法还原,得到相应的醇:
6.Cannizzaro 反应
凡α位碳原子上无活泼氢的醛类和浓NaOH或KOH水或醇溶液作用时,不发生醇醛缩合或树脂化作用而起歧化反应生成与醛相当的酸(成盐)及醇的混合物。此反应的特征是醛自身同时发生氧化及还原作用,一分子被氧化成酸的盐,另一分子被还原成醇:
脂肪醛中,只有甲醛和与羰基相连的是一个叔碳原子的醛类,才会发生此反应,其他醛类与强碱液,作用发生醇醛缩合或进一步变成树脂状物质。
具有α-活泼氢原子的醛和甲醛首先发生羟醛缩合反应,得到无α-活泼氢原子的β-羟基醛,然后再与甲醛进行交叉Cannizzaro反应,如乙醛和甲醛反应得到季戊四醇:
醛首先和氢氧根负离子进行亲核加成得到负离子,然后碳上的氢带着一对电子以氢负离子的形式转移到另一分子的羰基不能碳原子上。
7.Claisen 酯缩合反应
含有α-氢的酯在醇钠等碱性缩合剂作用下发生缩合作用,失去一分子醇得到β-酮酸酯。如2分子乙酸乙酯在金属钠和少量乙醇作用下发生缩合得到乙酰乙酸乙酯。
二元羧酸酯的分子内酯缩合见Dieckmann缩合反应。
乙酸乙酯的α-氢酸性很弱(pK a-24.5),而乙醇钠又是一个相对较弱的碱(乙醇的pK a~15.9),因此,乙酸乙酯与乙醇钠作用所形成的负离子在平衡体系是很少的。但由于最后产物乙酰乙酸乙酯是一个比较强的酸,能与乙醇钠作用形成稳定的负离子,从而使平衡朝产物方向移动。所以,尽管反应体系中的乙酸乙酯负离子浓度很低,但一形成后,就不断地反应,结果反应还是可以顺利完成。
常用的碱性缩合剂除乙醇钠外,还有叔丁醇钾、叔丁醇钠、氢化钾、氢化钠、三苯甲基钠、二异丙氨基锂(LDA)和Grignard试剂等。
如果酯的α-碳上只有一个氢原子,由于酸性太弱,用乙醇钠难于形成负离子,需要用较强的碱才能把酯变为负离子。如异丁酸乙酯在三苯甲基钠作用下,可以进行缩合,而在乙醇钠作用下则不能发生反应:
两种不同的酯也能发生酯缩合,理论上可得到四种不同的产物,称为混合酯缩合,在制备上没有太大意义。如果其中一个酯分子中既无α-氢原子,而且烷氧羰基又比较活泼时,则仅生成
一种缩合产物。如苯甲酸酯、甲酸酯、草酸酯、碳酸酯等。与其它含α-氢原子的酯反应时,都只生成一种缩合产物。
实际上这个反应不限于酯类自身的缩合,酯与含活泼亚甲基的化合物都可以发生这样的缩合反应,这个反应可以用下列通式表示:
8.Claisen—Schmidt 反应
一个无氢原子的醛与一个带有氢原子的脂肪族醛或酮在稀氢氧化钠水溶液或醇溶液存在下发生缩合反应,并失水得到不饱和醛或酮:
9.Claisen 重排
烯丙基芳基醚在高温(200°C)下可以重排,生成烯丙基酚。
当烯丙基芳基醚的两个邻位未被取代基占满时,重排主要得到邻位产物,两个邻位均被取代基占据时,重排得到对位产物。对位、邻位均被占满时不发生此类重排反应。
有机化学试卷 班级姓名分数 一、机理题 ( 共44题 288分 ) 1. 8 分 (2701) 2701 为下述实验事实提出合理的、分步的反应机理(用弯箭头表示电子对的转移,用鱼钩箭头表示单电子的转移,并写出各步可能的中间体)。 邻苯二甲酰亚胺用Br2-NaOH处理获得邻氨基苯甲酸。 2. 8 分 (2702) 2702 为下述实验事实提出合理的、分步的反应机理(用弯箭头表示电子对的转移,用鱼钩箭头表示单电子的转移,并写出各步可能的中间体。 2,4-二硝基氟苯(A)及2,4-二硝基溴苯(B)分别用C2H5NH2处理,都获得N-乙基-2,4-二硝基苯胺,但A比B速率快。 3. 8 分 (2703) 2703 为下述实验事实提出合理的、分步的反应机理(用弯箭头表示电子对的转移,用鱼钩箭头表示单电子的转移,并写出各步可能的中间体)。 异丙苯过氧化氢用酸处理,获得苯酚和丙酮(石油化工生产)。 4. 8 分 (2704) 2704 为下述实验事实提出合理的、分步的反应机理(用弯箭头表示电子对的转移,用鱼钩箭头表示单电子的转移,并写出各步可能的中间体)。 用14C标记的2-甲基-6-烯丙基苯酚的烯丙醚(A)加热发生Claisen重排反应,生成的2-甲基-4,6-二烯丙基苯酚中有一半以上含14C的烯丙基在对位。
5. 6 分 (2705) 2705 为下述实验事实提出合理的、分步的反应机理(用弯箭头表示电子对的转移,用鱼钩箭头表示单电子的转移,并写出各步可能的中间体)。 邻位和对位的羟基苯甲酸容易失羧,而间位异构体无此特征。 6. 6 分 (2706) 2706 为下述实验事实提出合理的、分步的反应机理(用弯箭头表示电子对的转移,用鱼钩箭头表示单电子的转移,并写出各步可能的中间体)。 旋光的苯基二级丁基酮在碱性溶液中发生外消旋化;这个酮失去旋光性的速率正好和它在碱性条件下溴化的速率相等。 7. 6 分 (2707) 2707 为下述实验事实提出合理的、分步的反应机理。 旋光的扁桃酸乙酯[C6H5CH(OH)CO2C2H5]在碱性条件下易外消旋化。 8. 6 分 (2708) 2708 为下述实验事实提出合理的、分步的反应机理。 旋光的扁桃酸[C6H5CH(OH)CO2H]在碱中的外消旋化比其酯慢得多。 9. 6 分 (2709) 2709 为下述实验事实提出合理的、分步的反应机理(用弯箭头表示电子对的转移,用鱼钩箭头表示单电子的转移,并写出各步可能的中间体)。 苯基二级丁基酮进行酸催化的外消旋化与其碘代反应的速率常数相等。 *. 6 分 (2710) 2710 为下述实验事实提出合理的、分步的反应机理(用弯箭头表示电子对的转移,用鱼钩箭头表示单电子的转移,并写出各步可能的中间体)。 醇醛缩合(aldol)反应亦可酸催化,如乙醛在酸催化下可生成-羟基丁醛。
基础有机化学反应总结 一、烯烃 1、卤化氢加成 (1) CH CH 2 R HX CH CH 3R X 【马氏规则】在不对称烯烃加成中,氢总是加在含碳较多的碳上。 【机理】 CH 2 C H 3+ CH 3 C H 3X + CH 3 C H 3 +H + CH 2 +C 3X + C H 3X 主 次 【本质】不对称烯烃的亲电加成总是生成较稳定的碳正离子中间体。 【注】碳正离子的重排 (2) CH CH 2 R CH 2CH 2 R Br HBr ROOR 【特点】反马氏规则 【机理】 自由基机理(略) 【注】过氧化物效应仅限于HBr 、对HCl 、HI 无效。 【本质】不对称烯烃加成时生成稳定的自由基中间体。 【例】 CH 2 C H 3Br CH CH 2Br C H 3CH + CH 3 C H 3HBr Br CH 3CH 2CH 2Br CH CH 3 C H 3 2、硼氢化—氧化 CH CH 2 R CH 2CH 2R OH 1)B 2H 62)H 2O 2/OH -
【特点】不对称烯烃经硼氢化—氧化得一反马氏加成的醇,加成是顺式的,并且不重排。 【机理】 2 C H 33H 32 3H 32 CH CH 2C H 3 2 CH CH=CH (CH 3CH 2CH 2)3 - H 3CH 2CH 2C 22CH 3 CH 2O CH 2CH 2CH 3 3CH 2CH 2C 2CH 2CH 3 + O H - O H B - OCH 2CH 2CH 3CH 2CH 2CH 3 H 3CH 2CH 2B OCH 2CH 2CH 3 CH 2CH 2CH 32CH 2CH 3 HOO -B(OCH 2CH 2CH 3)3 B(OCH 2CH 2CH 3)3 + 3NaOH3NaOH 3HOCH 2CH 2CH 33 + Na 3BO 3 2 【例】 CH 3 1)BH 32)H 2O 2/OH -CH 3 H H OH 3、X 2加成 C C Br /CCl C C Br Br 【机理】
有机化学规律总结 一.有机物组成和结构的规律 1.在烃类中,烷烃CnH2n+2随分子中碳原子的增多,其含碳量增大;炔烃、二烯烃、苯的同系物随着碳原子增加,其含碳量减少;烯烃、环烷烃的含碳量为常数(85.71%)2.一个特定的烃分子中有多少种结构的氢原子,一般来说其一卤代物就有多少种同分异构体. 3.最简式相同的有机物,不论以何种比例混合,其元素的质量分数为常数.例:m克葡萄糖,n克甲醛,x克乙酸,y克甲酸甲酯,混合后,求混合物碳的质量分数. 4.烃及烃的含氧衍生物中,氢原子个数一定为偶数. 6.常见有机物中最简式同为"CH"的有乙炔、苯、苯乙烯;同为“CH2”的为单烯烃和环烷烃; 7、烃类的熔、沸点变化规律 (1)有机物一般为分子晶体,在有机物同系物中,随碳原子数增加,相对分子质量增大,分子间作用力增大,熔、沸点逐渐升高。如:气态烃:CxHy x≤4 (2)分子式相同的烃,支链越多,熔、沸点越低。如沸点: 正戊烷(36.07℃)>异戊烷(27.9℃)>新戊烷(9.5℃) (3)苯的同系物,熔沸点。邻位>间位>对位, 如沸点: 邻二甲苯(144.4℃)>间二甲苯(139.1℃)>对二甲苯(138.4℃) 二.有机物燃烧规律 1.有机物燃烧通式:CxHy+(x+y/4)O2 xCO2+y/2H2O 2、烃(CXHY)完全燃烧前后物质的量的变化 (1)当Y=4时,反应前后物质的量相等。若同温同压下,100℃以上时,反应前后体积不变。 (2)当Y〈4时,燃烧后生成物分子数小于反应物分子总数。 (3)当Y〉4时,燃烧后生成物分子数大于反应物分子总数。 3、若分子为CnH2n、CnH2nO 或CnH2nO2时,其完全燃烧时生成CO2和H2O的物质的量之比为1:1。 4、若有机物在足量的氧气里完全燃烧,其所耗氧气物质的量与燃烧后生成CO2的物质的量相当,则有机物分子组成中氢与氧原子数比为2:1. 5、等质量的烃完全燃烧时,耗氧量决定于氢元素的含量,它越高,耗氧量越高,如甲烷耗氧量最高。 6、最简式相同的有机物,不论以何种比例混合,只要混合物的质量一定,它们完全燃烧后生成CO2总量为常数。 7.不同的有机物完全燃烧时,若生成CO2和H2O的质量比相同,则它们分子中碳与氢的原子个数也相同。 8、烃CXHY燃烧后体积变化规律 (1)当100℃以上,水为气态,若烃中H数或混合烃中平均H数小于4时,体积减小,1体积烃减少(1-Y/4)体积,若有a体积烃,则减少(1-Y/4)a 即△V=(1-Y/4)a 若烃中H数或混合烃中平均H数等于4时,△V=0。 若烃中H数或混合烃中平均H数大于4时,气体体积增大。1体积烃增大(Y/4-1)体积,若有a体积烃增大(Y/4-1)a体积,即 △V=(Y/4-1)a (2)当生成的水被浓H2SO4吸收或水蒸汽冷却为液体时。气体的体积会减少,每体积烃减少(1+Y/4)体积,若有a体积烃,则减少(1+Y/4)a体积即:△V=(1+Y/4)a 三、有机物的水溶性和密度大小规律
有机化学复习总结 一.有机化合物的命名 1. 能够用系统命名法命名各种类型化合物: 包括烷烃,烯烃,炔烃,烯炔,脂环烃(单环脂环烃和多环置换脂环烃中的螺环烃和桥环烃),芳烃,醇,酚,醚,醛,酮,羧酸,羧酸衍生物(酰卤,酸酐,酯,酰胺),多官能团化合物(官能团优先顺序:-COOH >-SO3H >-COOR >-COX >-CN >-CHO >>C =O >-OH(醇)>-OH(酚)>-SH >-NH2>-OR >C =C >-C ≡C ->(-R >-X >-NO2),并能够判断出Z/E 构型和R/S 构型。 2. 根据化合物的系统命名,写出相应的结构式或立体结构式(伞形式,锯架式,纽曼投影式,Fischer 投影式)。 立体结构的表示方法: 1 )伞形式: COOH OH H 3 2)锯架式:CH 3 OH H H OH C 2H 5 3) 纽曼投影式: H H 4)菲舍尔投影式:COOH CH 3 OH H 5)构象(conformation) (1) 乙烷构象:最稳定构象是交叉式,最不稳定构象是重叠式。 (2) 正丁烷构象:最稳定构象是对位交叉式,最不稳定构象是全重叠式。 (3) 环己烷构象:最稳定构象是椅式构象。一取代环己烷最稳定构象是e 取代的椅 式构象。多取代环己烷最稳定构象是e 取代最多或大基团处于e 键上的椅式构象。 立体结构的标记方法 1. Z/E 标记法:在表示烯烃的构型时,如果在次序规则中两个优先的基团在同一侧,为Z 构型, 在相反侧,为E 构型。 CH 3 C H C 2H 5CH 3C C H 2H 5Cl (Z)-3-氯-2-戊烯 (E)-3-氯-2-戊烯 2、 顺/反标记法:在标记烯烃和脂环烃的构型时,如果两个相同的基团在同一侧,则为顺式; 在相反侧,则为反式。
1.A rndt-Eister 反应 酰氯与重氮甲烷反应,然后在氧化银催化下与水共热得到酸。 反应机理 重氮甲烷与酰氯反应首先形成重氮酮(1),(1)在氧化银催化下与水共热,得到酰基卡宾(2),(2)发生重排得烯酮(3),(3)与水反应生成酸,若与醇或氨(胺)反应,则得酯或酰胺。 反应实例
2.Baeyer----Villiger 反应 反应机理 过酸先与羰基进行亲核加成,然后酮羰基上的一个烃基带着一对电子迁移到-O-O-基团中与羰基碳原子直接相连的氧原子上,同时发生O-O键异裂。因此,这是一个重排反应 具有光学活性的3---苯基丁酮和过酸反应,重排产物手性碳原子的枸型保持不变,说明反应属于分子内重排: 不对称的酮氧化时,在重排步骤中,两个基团均可迁移,但是还是有一定的选择性,按迁移能力其顺序为: 醛氧化的机理与此相似,但迁移的是氢负离子,得到羧酸。 反应实例
酮类化合物用过酸如过氧乙酸、过氧苯甲酸、间氯过氧苯甲酸或三氟过氧乙酸等氧化,可在羰基旁边插入一个氧原子生成相应的酯,其中三氟过氧乙酸是最好的氧化剂。这类氧化剂的特点是反应速率快,反应温度一般在10~40℃之间,产率高。 3.Beckmann 重排 肟在酸如硫酸、多聚磷酸以及能产生强酸的五氯化磷、三氯化磷、苯磺酰氯、亚硫酰氯等作用下发生重排,生成相应的取代酰胺,如环己酮肟在硫酸作用下重排生成己内酰胺:
反应机理 在酸作用下,肟首先发生质子化,然后脱去一分子水,同时与羟基处于反位的基团迁移到缺电子的氮原子上,所形成的碳正离子与水反应得到酰胺。 迁移基团如果是手性碳原子,则在迁移前后其构型不变,例如: 反应实例
3.Baeyer----Villiger 反应拜耳-维立格氧化重排反应 过酸先与羰基进行亲核加成,然后酮羰基上的一个烃基带着一对电子迁移到-O-O-基团中与羰基碳原子直接相连的氧原子上,同时发生O-O键异裂。因此,这是一个重排反应 具有光学活性的3---苯基丁酮和过酸反应,重排产物手性碳原子的枸型保持不变,说明反应属于分子内重排: 不对称的酮氧化时,在重排步骤中,两个基团均可迁移,但是还是有一定的选择性,按迁移能力其顺序为: 4.Beckmann 重排 肟在酸如硫酸、多聚磷酸以及能产生强酸的五氯化磷、三氯化磷、苯磺酰氯、亚硫酰氯等作用下发生重排,生成相应的取代酰胺,如环己酮肟在硫酸作用下重排生成己内酰胺: 在酸作用下,肟首先发生质子化,然后脱去一分子水,同时与羟基处于反位的基团迁移到缺电子的氮原子上,所形成的碳正离子与水反应得到酰胺。
迁移基团如果是手性碳原子,则在迁移前后其构型不变。 7.Cannizzaro 反应 凡α位碳原子上无活泼氢的醛类和浓NaOH或KOH水或醇溶液作用时,不发生醇醛缩合或树脂化作用而起歧化反应生成与醛相当的酸(成盐)及醇的混合物。此反应的特征是醛自身同时发生氧化及还原作用,一分子被氧化成酸的盐,另一分子被还原成醇: 脂肪醛中,只有甲醛和与羰基相连的是一个叔碳原子的醛类,才会发生此反应,其他醛类与强碱液,作用发生醇醛缩合或进一步变成树脂状物质。 醛首先和氢氧根负离子进行亲核加成得到负离子,然后碳上的氢带着一对电子以氢负离子的形式转移到另一分子的羰基不能碳原子上。 9.Claisen 酯缩合反应
含有α-氢的酯在醇钠等碱性缩合剂作用下发生缩合作用,失去一分子醇得到β-酮酸酯。如2分子乙酸乙酯在金属钠和少量乙醇作用下发生缩合得到乙酰乙酸乙酯。 乙酸乙酯的α-氢酸性很弱(pK a-24.5),而乙醇钠又是一个相对较弱的碱(乙醇的 pK a~15.9),因此,乙酸乙酯与乙醇钠作用所形成的负离子在平衡体系是很少的。但由于最后产物乙酰乙酸乙酯是一个比较强的酸,能与乙醇钠作用形成稳定的负离子,从而使平衡朝产物方向移动。所以,尽管反应体系中的乙酸乙酯负离子浓度很低,但一形成后,就不断地反应,结果反应还是可以顺利完成。 10.Claisen 重排 烯丙基芳基醚在高温(200°C)下可以重排,生成烯丙基酚。 当烯丙基芳基醚的两个邻位未被取代基占满时,重排主要得到邻位产物,两个邻位均被取代基占据时,重排得到对位产物。对位、邻位均被占满时不发生此类重排反应。
有机反应和反应机理总结(二) 来源:王悦的日志 有机反应和反应机理总结(二) (5)还原反应 1乌尔夫-凯惜纳-黄鸣龙还原:将醛或酮、肼和氢氧化钾在一高沸点的溶剂如一缩二乙二醇(HOCH2CH2OCH2CH2OH,沸点245˚C)中进行反应,使醛或酮的羰基被还原成亚甲基,这个方法称为乌尔夫-凯惜纳(Wolff L−Kishner N M)-黄鸣龙方法还原。对酸不稳定而对碱稳定的羰基化合物可以用此法还原。 2去氨基还原:重氮盐在某些还原剂的作用下,能发生重氮基被氢原子取代的反应,由于重氮基来自氨基,因此常称该反应为去氨基还原反应。 3异相催化氢化:适用于烯烃氢化的催化剂有铂、钯、铑、钌、镍等,这些分散的金属态的催化剂均不溶于有机溶剂,一般称之为异相催化剂。在异相催化剂作用下发生的加氢反应称为异相催化氢化。 4麦尔外因—彭杜尔夫还原:醛酮用异丙醇铝还原成醇的一种方法。这个反应一般是在苯或甲苯溶液中进行。异丙醇铝把氢负离子转移给醛或酮,而自身氧化成丙酮,随着反应进行,把丙酮蒸出来,使反应朝产物方面进行。这是欧芬脑尔氧化法的逆反应,叫做麦尔外因—彭杜尔夫(Meerwein H-Ponndorf W)反应。5卤代烃的还原:卤代烃被还原剂还原成烃的反应称为卤代烃的还原。还原试剂很多,目前使用较为普遍的是氢化锂铝,它是个很强的还原剂,所有类型的卤代烃包括乙烯型卤代烃均可被还原,还原反应一般在乙醚或四氢呋喃(THF)等溶剂中进行。 6伯奇还原:碱金属在液氨和醇的混合液中,与芳香化合物反应,苯环被还原为1,4-环己二烯类化合物,这种反应被称为伯奇还原。 7均相催化氢化:一些可溶于有机溶剂中的催化剂称为均相催化剂。在均相催化剂作用下发生的加氢反应称为均相催化氢化。 8克莱门森还原:醛或酮与锌汞齐和浓盐酸一起回流反应。醛或酮的羰基被还原成亚甲基,这个方法称为克莱门森还原。 9罗森孟还原法:用部分失活的钯催化剂使酰氯进行催化还原生成醛。此还原法称为罗森孟(Posenmund, K. W.)还原法。 10斯蒂芬还原:将氯化亚锡悬浮在乙醚溶液中,并用氯化氢气体饱和,将芳腈加入反应,水解后得到芳醛。此还原法称为斯蒂芬(Stephen, H.)还原。 11催化氢化:在催化剂的作用下,不饱和化合物与氢发生的加氢反应称之为催化氢化。 12催化氢解:用催化氢化法使碳与杂原子(O,N,X等)之间的键断裂,称为催化氢解。苯甲位的碳与杂原子之间的键很易催化氢解。 13酮的双分子还原:在钠、铝、镁、铝汞齐或低价钛试剂的催化下,酮在非质子溶剂中发生双分子还原偶联生成频哪醇,该反应称为酮的双分子还原。 14硼氢化-还原反应:烯烃与甲硼烷作用生成烷基硼的反应称为烯烃的硼氢化反
有机化学规律方法总结 第一:有机化学中的方法规律 1.有机物同分异构体的书写方法 〖碳链异构的书写方法〗以己烷( )为例,共五种同分异构体(氢原子省略) (1)先直链、一条线 (2)摘一碳、挂中间、往边移、不到端 (3)摘两碳、二甲基、同邻间、不重复、要写全 如果碳链更长,还可以摘两碳、三碳,先甲基,后乙基…… 〖取代基位置异构的书写方法〗 1、对称法(等效氢法) a、同一碳原子上的氢原子是等效的; b、同一碳原子所连甲基上的氢原子是等效的; c、处于镜面对称位置上的氢原子是等效的 2、换元法 详解:同分异构体书写规律:遵循对称性、有序性原则,一般按照下列顺序书写:官能团类型异构;碳链异构;官能团或取代基位置异构;立体异构(较少涉及)口诀:主链长到短,支链整到散,位置心到边,排布对邻间 2.有机物类型异构大全
3.常见有机物的分离提纯方法
4.常见有机物的检验与鉴别
第二:有机化学知识点总结 1.需水浴加热的反应有:(1)、银镜反应(2)、乙酸乙酯的水解(3)苯的硝化(4)糖的水解(5)、酚醛树脂的制取(6)固体溶解度的测定凡是在不高于100℃的条件下反应,均可用水浴加热,其优点:温度变化平稳,不会大起大落,有利于反应的进行。 2.需用温度计的实验有:(1)、实验室制乙烯(170℃)(2)、蒸馏(3)、固体溶解度的测定(4)、乙酸乙酯的水解(70-80℃)(5)、中和热的测定(6)制硝基苯(50-60℃) 〔说明〕:(1)凡需要准确控制温度者均需用温度计。(2)注意温度计水银球的位置。 3.能与Na反应的有机物有:醇、酚、羧酸等——凡含羟基的化合物。
大学有机化学反应方程 式总结较全 Document serial number【NL89WT-NY98YT-NC8CB-NNUUT-NUT108】
有 机化学 一、烯烃 1、卤化氢加成 (1) CH CH 2 R HX CH CH 3R X 【马氏规则】在不对称烯烃加成中,氢总是加在含碳较多的碳上。 【机理】 CH 2 C H 3CH + CH 3 C H 3X + CH 3 C H 3 +H + CH 2 +C 3X + C H 3X 主 次 【本质】不对称烯烃的亲电加成总是生成较稳定的碳正离子中间体。 【注】碳正离子的重排 (2) CH CH 2 R CH 2CH 2 R Br HBr ROOR 【特点】反马氏规则 【机理】 自由基机理(略) 【注】过氧化物效应仅限于HBr 、对HCl 、HI 无效。 【本质】不对称烯烃加成时生成稳定的自由基中间体。 【例】 CH 2 C H 3Br CH CH 2Br C H 3CH + CH 3 C H 3HBr Br CH 3CH 2CH 2Br CH CH 3 C H 3 2、硼氢化—氧化 CH CH 2 R CH 2CH 2R OH 1)B 2H 62)H 2O 2/OH - 【特点】不对称烯烃经硼氢化—氧化得一反马氏加成的醇,加成是顺式的,并且不重排。
【机理】 2 C H3 3 H3 2 3 H3 2 CH CH2 C H3 2 CH CH=CH (CH3CH2CH2)3 - H3CH2CH2C 22 CH3 CH2 O CH 2 CH2CH3 H3CH2CH2C 2 CH2CH3 +O H- O H B-OCH2CH2CH3 CH2CH2CH3 H3CH2CH2C B OCH2CH2CH3 CH2CH2CH3 2 CH2CH3 HOO- B(OCH2CH2CH3)3 B(OCH2CH2CH3)3+3NaOH3NaOH3HOCH2CH2CH33+Na3BO3 2 【例】 CH3 1)BH 3 2)H 2 O 2 /OH- CH3 H H OH 3、X 2 加成 C C Br/CCl C C Br Br 【机理】 C C C C Br Br C Br +C C Br O H2+ -H+ C C Br O H
欢迎阅读 有机化学复习总结 一.有机化合物的命名 1.能够用系统命名法命名各种类型化合物: 包括烷烃,烯烃,炔烃,烯炔,脂环烃(单环脂环烃和多环置换脂环烃中的螺环烃和桥环烃),芳烃,醇,酚,醚,醛,酮,羧酸,羧酸衍生物(酰卤,酸酐,酯,酰胺),多官能团化合物(官能团优先顺序:-COOH >-SO3H >-COOR >-COX >-CN >-CHO >>C =O >-OH(醇)>-OH(酚)>-SH >-NH2>-OR >C =C >-C ≡C ->(-R >-X >-NO2),并能够判断出Z/E 构型和R/S 构型。 2.根据化合物的系统命名,写出相应的结构式或立体结构式(伞形式,锯架式,纽曼投影式,Fischer 投影式)。 立体结构的表示方法: 1)伞形式:C COOH OH H 3C H 2)锯架式:CH 3 OH H H OH C 2H 5 3)纽曼投影式: H H H H H H H H H H H H 4)菲舍尔投影式:COOH CH 3 OH H 5)构象(conformation) (1) 乙烷构象:最稳定构象是交叉式,最不稳定构象是重叠式。 (2) 正丁烷构象:最稳定构象是对位交叉式,最不稳定构象是全重叠式。 (3) 环己烷构象:最稳定构象是椅式构象。一取代环己烷最稳定构象是e 取代的椅式构象。多取代环己烷最稳定构象是e 取代最多或大基团处于e 键上的椅式构象。 立体结构的标记方法 1. Z/E 标记法:在表示烯烃的构型时,如果在次序规则中两个优先的基团在同一侧,为Z 构型,在相反侧,为E 构型。 2、 顺/反标记法:在标记烯烃和脂环烃的构型时,如果两个相同的基团在同一侧,则为顺式;在相反侧,则为反式。 3、 R/S 标记法:在标记手性分子时,先把与手性碳相连的四个基团按次序规则排序。然后将最不优先的基团放在远离观察者,再以次观察其它三个基团,如果优先顺序是顺时针,则为R 构型,如果是逆时针,则为S 构型。 注:将伞状透视式与菲舍尔投影式互换的方法是:先按要求书写其透视式或投影式,然后分别标出其R/S 构型,如果两者构型相同,则为同一化合物,否则为其对映体。 二.有机化学反应及特点 1.反应类型 还原反应(包括催化加氢):烯烃、炔烃、环烷烃、芳烃、卤代烃
大学有机化学反应方程式总 结(较全) -标准化文件发布号:(9556-EUATWK-MWUB-WUNN-INNUL-DDQTY-KII
有机化学 一、烯烃 1、卤化氢加成 (1) CH CH 2 R HX CH 3R X 【马氏规则】在不对称烯烃加成中,氢总是加在含碳较多的碳上。 【机理】 CH 2 C H 3+ CH 3 C H 3X + CH 3 C H 3 +H + CH 2 +C 3X + C H 3X 主 次 【本质】不对称烯烃的亲电加成总是生成较稳定的碳正离子中间体。 【注】碳正离子的重排 (2) CH CH 2 R CH 2CH 2 R Br HBr ROOR 【特点】反马氏规则 【机理】 自由基机理(略) 【注】过氧化物效应仅限于HBr 、对HCl 、HI 无效。 【本质】不对称烯烃加成时生成稳定的自由基中间体。 【例】 CH 2 C H 3Br CH CH 2Br C H 3CH + CH 3 C H 3HBr Br CH 3CH 2CH 2Br CH CH 3 C H 3 2、硼氢化—氧化 CH CH 2 R CH 2CH 2R OH 1)B 2H 62)H 2O 2/OH -
【特点】不对称烯烃经硼氢化—氧化得一反马氏加成的醇,加成是顺式的,并且不重排。 【机理】 2 C H 33H 32 3H 32 CH CH 2C H 3H BH 2 CH CH=CH (CH 3CH 2CH 2)3 - H 3CH 2CH 2C 22CH 3 CH 2O CH 2CH 2CH 3 H 3CH 2CH 2C 2CH 2CH 3 + O H - O H B - OC H 2CH 2CH 3CH 2CH 2CH 3 H 3CH 2CH 2B OC H 2CH 2CH 3 CH 2CH 2CH 3H 2CH 2CH 3 HOO -B(OCH 2CH 2CH 3)3 B(OCH 2CH 2CH 3)3 + 3NaOH 3NaOH 3HOC H 2CH 2CH 33 + Na 3BO 3 2 【例】 CH 3 1)BH 32)H 2O 2/OH -CH 3H H OH 3、X 2加成 C C Br /CCl C C Br Br 【机理】
有机化学 一、烯烃 1、卤化氢加成 (1) CH CH 2 R HX CH CH 3R X 【马氏规则】在不对称烯烃加成中,氢总是加在含碳较多的碳上。 【机理】 CH 2 C H 3+ CH 3 C H 3X + CH 3 C H 3 +H + CH 2 +C 3X + C H 3X 主 次 【本质】不对称烯烃的亲电加成总是生成较稳定的碳正离子中间体。 【注】碳正离子的重排 (2) CH CH 2 R CH 2CH 2 R Br HBr ROOR 【特点】反马氏规则 【机理】 自由基机理(略) 【注】过氧化物效应仅限于HBr 、对HCl 、HI 无效。 【本质】不对称烯烃加成时生成稳定的自由基中间体。 【例】 CH 2 C H 3Br CH CH 2Br C H 3CH + CH 3 C H 3HBr Br CH 3CH 2CH 2Br CH CH 3 C H 3 2、硼氢化—氧化 CH CH 2 R CH 2CH 2R OH 1)B 2H 62)H 2O 2/OH - 【特点】不对称烯烃经硼氢化—氧化得一反马氏加成的醇,加成是顺式的,并且不重排。 【机理】
2 C H3 3 H3 2 3 H3 2 CH CH2 C H3 2 CH CH=CH (CH3CH2CH2)3 - H3CH2CH2C 22 CH3 CH2 B O CH2CH2CH3 3 CH2CH2C 2 CH2CH3 +O H- O H B-OCH2CH2CH3 CH2CH2CH3 H3CH2CH2 B OCH2CH2CH3 CH2CH2CH3 2 CH2CH3 HOO- B(OCH2CH2CH3)3 B(OCH2CH2CH3)3+3NaOH3NaOH3HOCH2CH2CH33+Na3BO3 2 【例】 CH3 1)BH 3 2)H 2 O 2 /OH- CH3 H H OH 3、X2加成 C C Br 2 /CCl 4 C C Br Br 【机理】 C C C C Br Br C Br +C C Br O H2+ -H+ C C Br O H
有机反应机制的研究方法 有机化学中用来解释反应机理的传统方法主要集中在Kinetics 和Dynamics两方面,即理解势能面、深入研究分子运动和碰撞、测定活化参数、测定速率常数、确定某个反应机理中一系列化学步骤的顺序、确定反应限速步骤和决速步骤。 研究机理的关键目的是反应机理知识可以对如何在原子或分子水平上操纵物质给出最快速的洞察,而不是依靠运气来获得偶然性的变化从而获得想要的结果。由于动力学在辨别机理方面起着关键作用,所以动力学是整个有机反应机理研究领域中最重要的分支之一。 传统的反应机理研究方法除了动力学分析之外,还有同位素效应、结构-功能分析等。这些都是研究有机反应机理的标准实验工具,然后实验化学家可以根据其想象力和化学创造性,设计出一些完全不同于之前出现过的研究方法。因此,本文总结了一些最为常见的方法。首先分析最简单的实验,例如产物和中间体的鉴定。但也会分析一些更为微妙、精细的实验,如交叉和同位素置乱(cross-over and isotope scrambling)实验。 1.改变反应物结构以转变或捕获预想的中间体 有时可以通过合成一种类似于所研究的反应物的新反应物来破译中间体的性质,但是这需要所预测的中间体能以一种可预想的方式进行反应。没有标准的方式来处理这一类实验,所以实验者必须根据具体实验情况来设计实验。下面以酶反应作为此方法的应用实例。 Lin[1]等人设计了一种转变中间体的方法。扁桃酸消旋化酶可使扁
桃酸根离子的对映体(2-羟基苯甲酸)互换。位于羧酸跟α位的碳负离子被认为是中间体。为了测试此中间体是否存在,作者合成设计了扁桃酸跟离子的类似物i,并用酶对其进行了外消旋化。其过程是首先形成碳负离子,然后经过溴化物的1,6-消除,最后经过互变异构化,分离得到产物ii。此结果支持了在扁桃酸根离子路径中碳负离子中间体iii的存在。 2.捕获实验和竞争实验 鉴定中间体的一种常见方法是通过加入额外的试剂来捕获中间体。目前存在着几种自由基不伙计,许多好的亲核试剂是半衰期很短的亲电试剂(如碳正离子)的可行的捕获剂。必须以自己的化学知识来设计捕获中间体(如碳正离子、卡宾等)的捕获剂。但是活泼中间体的半衰期很短,所以捕获剂必须是具有很高的活性,并能与活泼中间体的标准反应路径进行竞争。同样,因为捕获反应是典型的双分子反应,所以要求捕获剂具有高的浓度。另外,还可以将捕获剂与反应物共价结合,以便更容易地捕获活泼中间体。 与捕获反应所不同的另一种反应是竞争反应。在一般的动力学实
有机化学反应机理总结 引言 反应机理是对一个反应过程的详细描述,在表述反应机理时,必须指出电子的流向,并规定用箭头表示一对电子的转移。 摘要:反应机理是根据很多实验事实总结后提出的,它有一定的适用范围,能解释很多实验事实,并能预测反应的发生。如果发现新的实验事实无法用原有的反应机理来解释,就要提出新的反应机理。反应机理已成为有机结构理论的一部分。 关键词:反应反应机理自由基反应 有机化合物分子中的某个原子或基团被其它原子或基团所置换的反应称为取代反应。若取代反应是按共价键均裂的方式进行的,即是由于分子经过均裂产生自由基而引发的,则称其为自由基型取代反应。 自由基反应包括链引发、链转移、链终止三个阶段。链引发阶段是产生自由基的阶段。由于键的均裂需要能量,所以链引发阶段需要加热或光照。链转移阶段是由一个自由基转变成另一个自由基的阶段,犹如接力赛一样,自由基不断地传递下去,像一环接一环的链,所以称之为链反应。链终止阶段是消失自由基的阶段。自由基两两结合成键。所有的自由基都消失了,自由基反应也就终止了。 分子中的原子或基团被卤原子取代的反应称为卤化反应。若卤原子为氯原子,则该卤化反应称为氯化反应。 酯化反应是一个可逆的反应,为了使正反应有利,通常采用的手段是: ①使原料之一过量; ②不断移走产物(例如除水;乙酸乙酯、乙酸、水可形成三元恒沸物 bp 70.4℃)。
有机化学中的氧化和还原是指有机化合物分子中碳原子和其它原子的氧化和还原,可根据氧化数的变化来确定。氧化数升高为氧化,氧化数降低为还原。氧化和还原总是同时发生的,由于有机反应的属性是根据底物的变化来确定的,因此常常将有机分子中碳原子氧化数升高的反应称为氧化反应,碳原子氧化数降低的反应称为还原反应。有机反应中,多数氧化反应表现为分子中氧的增加或氢的减少,多数还原反应表现为分子中氧的减少或氢的增加。化学物质和空气中的氧在常温下温和地进行氧化,而不发生燃烧和爆炸,这种反应称为自动氧化。多数自动氧化是通过自由基机理进行的。 将分子间或分子内不相连的两个碳原子连接起来的反应统称为缩合反应。在缩合反应中,有新的碳碳键形成,同时也往往有水或其它比较简单的有机或无机分子形成。缩合反应通常需要在缩合剂的作用下进行,无机酸、碱、盐或醇钠、醇钾等是常用的缩合剂。以羟醛缩合为例:
有机化学复习总结 一.有机化合物的命名 1. 能够用系统命名法命名各种类型化合物: 包括烷烃,烯烃,炔烃,烯炔,脂环烃(单环脂环烃和多环置换脂环烃中的螺环烃和桥环烃),芳烃,醇,酚,醚,醛,酮,羧酸,羧酸衍生物(酰卤,酸酐,酯,酰胺),多官能团化合物(官能团优先顺序:-COOH >-SO3H >-COOR >-COX >-CN >-CHO >>C =O >-OH(醇)>-OH(酚)>-SH >-NH2>-OR >C =C >-C ≡C ->(-R >-X >-NO2),并能够判断出Z/E 构型和R/S 构型。 2. 根据化合物的系统命名,写出相应的结构式或立体结构式(伞形式,锯架式,纽曼投影式,Fischer 投影式)。 立体结构的表示方法: 1)伞形式:C COOH OH H 3C H 2)锯架式:CH 3 OH H H OH C 2H 5 3) 纽曼投影式: H H H H H H H H H H H H 4)菲舍尔投影式:COOH CH 3 OH H 5)构象(conformation) (1) 乙烷构象:最稳定构象是交叉式,最不稳定构象是重叠式。 (2) 正丁烷构象:最稳定构象是对位交叉式,最不稳定构象是全重叠式。 (3) 环己烷构象:最稳定构象是椅式构象。一取代环己烷最稳定构象是e 取代的椅 式构象。多取代环己烷最稳定构象是e 取代最多或大基团处于e 键上的椅式构象。 立体结构的标记方法 1. Z/E 标记法:在表示烯烃的构型时,如果在次序规则中两个优先的基团在同一 侧,为Z 构型,在相反侧,为E 构型。 CH 3 C C H Cl C 2H 5CH 3C C H C 2H 5Cl (Z)-3-氯-2-戊烯 (E)-3-氯-2-戊烯 2、 顺/反标记法:在标记烯烃和脂环烃的构型时,如果两个相同的基团在同一侧, 则为顺式;在相反侧,则为反式。 CH 3C C H CH 3H CH 3C C H H CH 3顺-2-丁烯 反-2-丁烯CH 3 H CH 3 H CH 3 H H CH 3顺-1,4-二甲基环己烷反-1,4-二甲基环己烷 3、 R/S 标记法:在标记手性分子时,先把与手性碳相连的四个基团按次序规则排序。然后将最不优先的基团放在远离观察者,再以次观察其它三个基团,如果优先顺序
Chap 1绪论 一、构造、构型、构象 二、共价键 轨道杂化:C:sp、sp2、sp3杂化方式、空间构型(键角)、未参与杂化p轨道与杂化轨道位置、电负性比较 基本属性:键长:越短键越牢固键能:越大键越牢固σ键能大于п键能 键角:取代基越大键角越大极性和极化性:偶极矩(会判断偶极矩大小:矢 量和) 键断裂方式和反应类型:自由基反应、离子型(亲电、亲核)、周环反应 Lewis酸、碱 氢键、电负性 三、官能团、优先次序(ppt) Chap 2饱和烃——烷烃 一、烃分类 烃:开链烃和环状烃 开链烃:饱和烃和不饱和烃环状烃:脂环烃和芳香烃 二、烷烃通式和构造异构、构象异构(乙烷和丁烷构象) 烷烃通式:C n H2n+2 构造异构体:分子内原子链接顺序不同 σ键形成及特性:电子云重叠程度大,键能大,不易断;可绕轴自由旋转;两核间不能有两个或以上σ键。 乙烷构象:Newman投影式、重叠式(不稳定,因为非键张力大)、交叉式(稳定,各个氢距离远,非键张力小) 丁烷构象:Newman投影式;稳定性(大到小):对位交叉式、邻位交叉式、部分重叠式、全部重叠式 甲烷结构和sp3杂化构型:正四面体型 三、命名 普通命名法(简单化合物):正、异、新 衍生物命名法:以甲烷为母体,选取取代基最多的C为母体C。 系统命名法:①选取最长碳链为主链,主链C标号从距离取代基最近的一端开始标。 ②多取代基时,合并相同取代基,尽量使取代基位次和最小。书写时按照 官能团大小(小在前)命名 ③含多个相同长度碳链时,选取取代基最多的为主链 四、物理性质 沸点(b.p.):直链烷烃随分子量增大而增大(分子间色散力与分子中原子大小和数目成正比,分子量增大,色散力增大,沸点增大) 支链越多,沸点越低(支链多,烷烃体积松散,分子间距离大,色散力小)熔点(m.p.):总趋势:分子量增大,m.p.增大 m.p.曲线(书P48) 相对密度:分子量增大,相对密度增大,接近于0.8 溶解度:不溶于水,易溶于有机溶剂(相似相溶,烷烃极性小)
目录 第一部分有机化学重要反应和机理 (1) Arbuzov 反应 (1) Arndt-Eister 反应 (2) Baeyer-Villiger 反应 (2) Beckmann 重排 (4) Birch 还原 (4) Bouveault---Blanc 还原 (5) Bamberger,E.重排 (6) Berthsen,A.Y 吖啶合成法 (7) Bucherer反应 (8) Cannizzaro 反应 (9) Chichibabin 反应 (10) Claisen 酯缩合反应 (11) Claisen—Schmidt 反应 (12) Claisen 重排 (13) Clemmensen 还原 (15) Combes 喹啉合成法 (15) Cope 消除反应 (16) Cope 重排 (17) Curtius 反应 (18) Crigee,R 反应 (19) Dakin 反应 (20) Elbs 反应 (21) Edvhweiler-Clarke 反应 (21) Elbs,K.过硫酸钾氧化法 (22) Favorskii 反应 (23) Favorskii 重排 (24) Friedel-Crafts 烷基化反应 (24) Friedel-Crafts 酰基化反应 (25) Fries 重排 (26) Fischer,O-Hepp,E 重排 (27) Gabriel 合成法 (27) Gattermann 反应 (28)
Gattermann-Koch 反应 (29) Gomberg-Bachmann 反应 (29) Hantzsch 合成法 (30) Haworth 反应 (31) Hell-Volhard-Zelinski 反应 (31) Hinsberg 反应 (32) Hofmann 烷基化 (32) Hofmann重排 (33) Hofmann 消除反应 (34) Houben-Hoesch 反应 (35) Hunsdieecker 反应 (35) Kiliani 氯化增碳法 (36) Knoevenagel 反应 (36) Koble 反应 (37) Koble-Schmitt 反应 (37) Kolbe,H.Syntbexis of Nitroparsffini 合成 (38) Leuckart 反应 (39) Lossen 反应 (39) Mannich 反应 (40) Meerwein-Ponndorf 反应 (41) Michael 加成反应 (42) Martius,C.A. 重排 (42) Norrish Ⅰ和Ⅱ型裂 (43) Oppenauer 氧化 (44) Orton,K.J.P 重排 (45) Paal-Knorr 反应 (45) Pschorr 反应 (46) Prileschajew,N.反应 (47) Prins,H.J 反应 (48) Pinacol-Pinacolone Rearrangement 重排 (49) Perkin,W.H 反应 (49) Pictet-Spengler 合成法-异喹啉 (50) Reformatsky 反应 (51) Reimer-Tiemann 反应 (52) Reppe 合成法 (53) Robinson 缩环反应 (53) Rosenmund 还原 (54)
有机化学反应机理
有机化学反应机理 对于均裂反应来说:反应物既提供电子又接受电子注意:提供和接受的电子均为单电子 对于异裂反应来说: 提供和接受的电子为电子对 反应物的分类:亲核试剂:电子云密度高的中性分子或带负电荷的原子、原子团或 分子(又为Lewis 碱)。 亲电试剂:电子云密度低的中性原子、原子团或分子或带正电荷的 任何分子、原子、原子团(Lewis酸)。 ?取代反应:SN1 和SN2 ?伯卤代烃= SN2 ?仲卤代烃= SN1 和SN2 ! ?叔卤代烃= SN1 ?离去基团:大多数是卤素 ?亲核试剂:许多亲核试剂!! 邻基取代:在离去基团的邻位上能够进行邻基参与的基团 酯基、羧基、羟基、苯基、稀基、卤素。 .波谱特征 红外光谱 红外特征吸收峰是C-X键的振动吸收,都在指纹区,其中C-F 键的吸收频率在1400~1000 cm-1,C-Cl键为800~600 cm-1,C-Br 键为600~500 cm-1,而C-I 键的吸收频率在500 cm-1附近。 核磁共振谱 1H-NMR谱中,卤素电负性较大,因此与卤素直接相连的碳上的氢的化学位移移向低场 卤代烃及亲核取代反应 反应活性次序: 叔卤烷>仲卤烷>伯卤。用于卤烷的定性分析.
卤素相同、烃基结构不同的卤代烷,其活性顺序为:1°>2°>3°。 此反应也可用于鉴别卤代烃,反应最快的是伯卤代烷,其次是仲卤代烷,反应最慢的是叔卤代烷。 Saytzeff 规则 如果分子内含有几种β-H 时,主要消除含氢较少的碳上的氢,生成双键碳上连有较多取代基的烯烃,这一经验规则称Saytzeff 规则。 RX AgNO 3 C 2H 5OH RONO 2AgX ++RBr + NaI RI + NaBr RCl + NaI RI + NaCl 丙酮丙酮R-X ROH ROR'R-CN R-NH 2O H 2NaOH ,,NH R-R R'COOR R'C CR CNa R-O-NO 2AgX AgNO 3+ △
大学有机化学知识点整理考试必备
————————————————————————————————作者:————————————————————————————————日期:
大学有机化学知识点提纲(一)绪论 共价键 价键理论(杂化轨道理论);分子轨道理论;共振论. 共价键的属性:键能;键长;键角;键的极性. 键的极性和分子极性的关系;分子的偶极矩. 有机化合物的特征 (二)烷烃和环烷烃 基本概念 烃及其分类;同分异构现象;同系物;分子间作用力;a键,e键;构型,构象,构象分析,构象异构体;烷基;碳原子和氢原子的分类(即1,2,3碳,氢;4碳);反应机理,活化能. 对于基本概念,不是要求记住其定义,而是要求理解它们,应用它们说明问题. 命名 开链烷烃和环烷烃的IUPAC命名,简单的桥环和螺环的命名. 烷烃和环烷烃的结构 碳原子sp3杂化和四面体构型;环烷烃的结构(小环的张力). 烷烃的构象 开链烷烃的构象,能量变化;环烷烃的构象:重点理解环己烷和取代环己烷的构象及能 量变化,稳定构象,十氢萘及其它桥环的稳定构象. 烷烃的化学性质 自由基取代反应—卤代反应及机理;碳游离基中间体—结构,稳定性;不同的卤素在反应中的活性和选择性;反应过程中的能量变化. 环烷烃的化学性质 自由基取代反应(与烷烃一致);小环(3,4元环)性质的特殊性—加成. (三)烯烃 烯烃的结构特点 碳的sp2杂化和烯烃的平面结构;键和键. 烯烃的同分异构,命名 碳架异构,双键位置异构,顺反异构(Z,E). 烯烃的物理和化学性质 烯烃的亲电加成及其机理,马氏规则;碳正离子中间体—结构,稳定性,重排. 其它加成反应:催化加氢(立体化学,氢化热);硼氢化—氧化(加成取向,立体化学);羟汞化—脱汞(加成取向);与HBr/过氧化物加成(加成取向);其它游离基加成. 氧化反应:羟基化反应—邻二醇的形成;KMnO4/H+的氧化,臭氧化反应,烯烃结构的测定. α-位取代反应:烯丙基型取代反应(高温卤代和NBS卤代)及机理—烯丙基自由基. (四)炔烃和二烯烃 炔烃 ①结构:碳的sp杂化和碳-碳三键;sp杂化,sp2杂化和sp3杂化的碳的电负性的差异及相应化合物的偶极矩. ②同分异构体 ③化学性质:末端炔烃的酸性及相关的反应;三键的加成:催化加氢,亲电加成,亲核加成;碳—碳三键与H2/Lindlar催化剂反应(顺式烯烃);碳—碳三键与Na/液氨的反应(反式烯烃);加卤素;加HX(马氏规则);加H2O(羰基化合物的形成);加HBr/过氧化物;硼氢化—氧化;加HCN及乙炔的二聚;氧化反应:KMnO4氧化和臭氧化. 二烯烃 ①共轭二烯烃的稳定性:键能和键长平均化,共轭效应.