
primer 6.0 引物设计教程
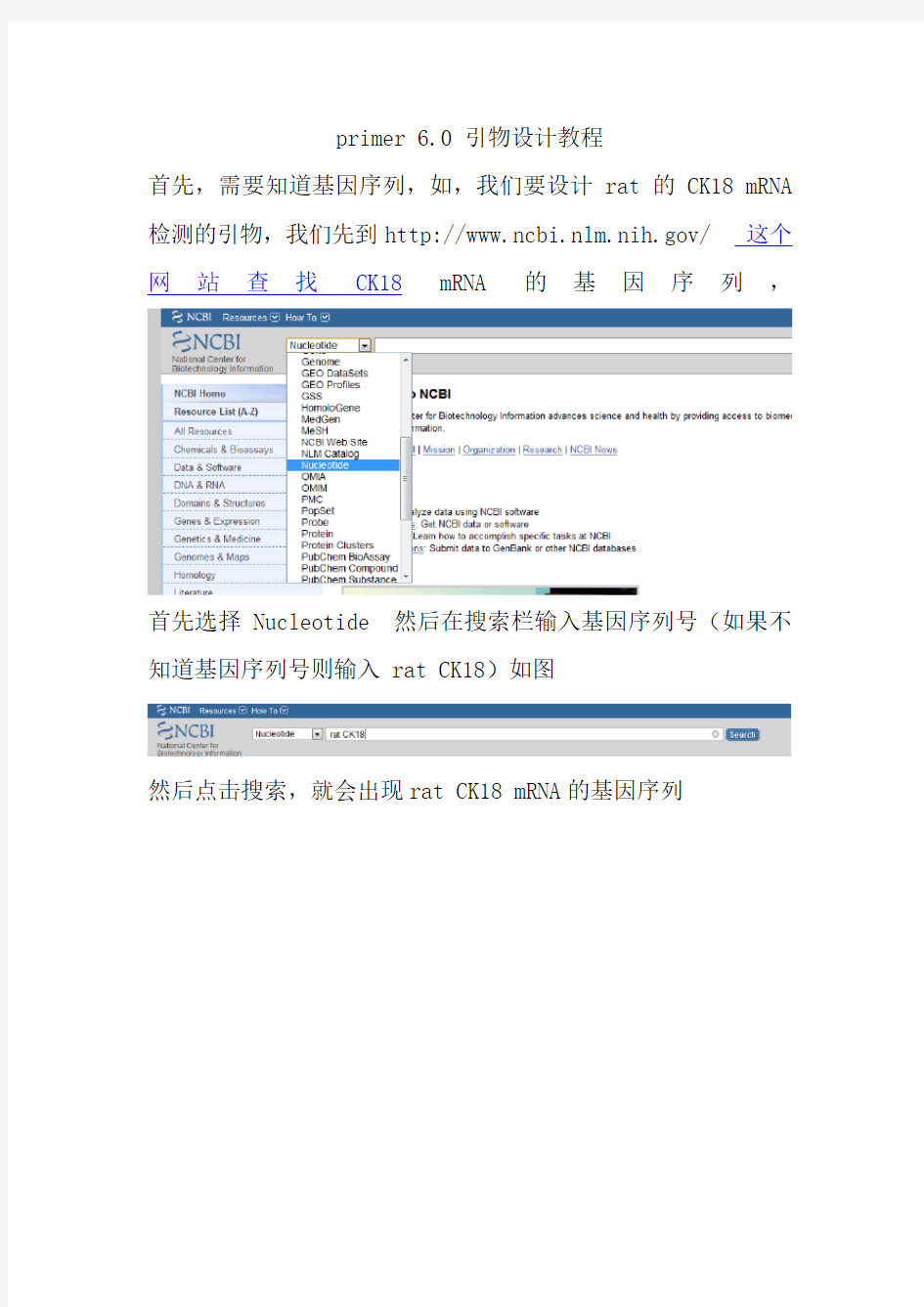
首先,需要知道基因序列,如,我们要设计rat的 CK18 mRNA 检测的引物,我们先到https://www.doczj.com/doc/fc11429442.html,/ 这个网站查找CK18mRNA的基因序列,
首先选择Nucleotide 然后在搜索栏输入基因序列号(如果不知道基因序列号则输入 rat CK18)如图
然后点击搜索,就会出现rat CK18 mRNA的基因序列
基因序列号现在,往下拉就会看到基因序列
将这个序列复制到primer 6.0中就可以进行引物设计,
我们先打开peimer 6.0
破解版打开会出现这个对话框,关闭即可
将序列复制至这个对话框
点击
Add
出现下面对话框,这里可以选择引物在序列哪些地方设计引物,我一般不更改,也就是引物可以设计在整个序列,你也可查一下序列有几个区,一般引物应该跨两个区。
之后点击 primer Parameters
这里可以设置退火温度、引物长度、产物长度等,我一般只是更改产物长度,我一般设为100到300bp,因为如果产物太大,在染料法中会影响扩增效率,
之后点击 Search 之后出现下面对话框
点击OK 出现下面引物序列
这个时候引物设计完成,我们需要对引物进行验证,我一般到NCBI (https://www.doczj.com/doc/fc11429442.html,/)上验证,进去后点击最下面菜单中的
BLAST
之后点击Primer-BLAST
将前引物复制到图中位置
后引物放到下图位置
之后将图中位置的homo sapiens 删除后输入
rat
出现上图对话框时选择Rattus (taxid :10114) 之后点击
Get Primers
这时会出现下图情况,因为服务器在国外,请耐心等待
之后出现
他能扩增很多大鼠基因,如CK18 产物为126bp ,Ahsg 产物795bp ,但是除了CK18
其他基因扩增是产物较大,而且有点突
变,所以在PCR反应时这些东西是扩增不出来的,也就是说这个引物的特异性不错,在扩增时只会扩增出我们需要的CK18这个基因,所以这个引物我们就可以订出去,找公司合成。有的时候这样的引物也不一定就可以用,所以当我们收到合成好的引物后,可以做一下预实验,看这个引物是否真的可以用,在需要引物时我们也可以到文献中查找,一般发表在全球著名杂志中的外文文献里的引物都是可以用的,查找是要注意文献中用的是染料法还是探针法,探针法的引物在染料法种效果不佳,应该舍弃,选择染料法的引物。
mi引物设计原则 1. 引物的长度一般为15-30 bp,常用的是18-27 bp,但不应大于38,因为过长会导致其延伸温度大于74℃,不适于Taq DNA聚合酶进行反应。 2. 引物序列在模板内应当没有相似性较高,尤其是3’端相似性较高的序列,否则容易导致错配。引物3’端出现3个以上的连续碱基,如GGG或CCC,也会使错误引发机率增加。 3. 引物3’端的末位碱基对Taq酶的DNA合成效率有较大的影响。不同的末位碱基在错配位置导致不同的扩增效率,末位碱基为A的错配效率明显高于其他3个碱基,因此应当避免在引物的3’端使用碱基A。另外,引物二聚体或发夹结构也可能导致PCR反应失败。5’端序列对PCR影响不太大,因此常用来引进修饰位点或标记物。 4. 引物序列的GC含量一般为40-60%,过高或过低都不利于引发反应。上下游引物的GC含量不能相差太大。 5. 引物所对应模板位置序列的Tm值在72℃左右可使复性条件最佳。Tm值的计算有多种方法,如按公式Tm=4(G+C)+2(A+T),在Oligo软件中使用的是最邻近法(the nearest neighbor method)。 6. ΔG值是指DNA双链形成所需的自由能,该值反映了双链结构内部碱基对的相对稳定性。应当选用3’端ΔG值较低(绝对值不超过9),而5’端和中间ΔG 值相对较高的引物。引物的3’端的ΔG值过高,容易在错配位点形成双链结构并引发DNA聚合反应。 7. 引物二聚体及发夹结构的能值过高(超过4.5kcal/mol)易导致产生引物二聚体带,并且降低引物有效浓度而使PCR反应不能正常进行。 8. 对引物的修饰一般是在5’端增加酶切位点,应根据下一步实验中要插入PCR 产物的载体的相应序列而确定。 引物序列应该都是写成5-3方向的, Tm之间的差异最好控制在1度之内, 另外我觉得扩增长度大一些比较好,500bp左右。 要设计引物首先要找到DNA序列的保守区。同时应预测将要扩增的片段单链是否形成二级结构。如这个区域单链能形成二级结构,就要避开它。如这一段不能
Primer 5.0搜索引物: 1.Primer Length我常设置在18-30bp,短了特异性不好,长了没有必要。当然有特殊要求的除外,如加个酶切位点什么的。 2.PCR Product size最好是100-500bp之间,小于100bp的PCR产物琼脂糖凝胶电泳出来,条带很模糊,不好看。至于上限倒也不必要求苛刻。 3.Search parameters还是选Manual吧,Search stringency应选High,GC含量一般是40-60%。其它参数默认就可以了。 4.搜索出来的引物,按Rating排序,逐个送Oligo软件里评估。当然,搜索出的引物,其扩增产物很短,你可以不选择它,或是引物3端≥2个A或T,或引物内部连续的G或C太多,或引物3端≥2个G或C,这样的引物应作为次选,没得选了就选它。对于这样的引物,如果其它各项指标还可以,我喜欢在引物末端去掉一个不满意的或加上一个碱基,看看引物的评估参数有没有变好点。 Oligo 6.0评估引物: 1.在analyze里,Duplex Formation不管是上游引物、下游引物还是上下游引物之间,The most stable 3’-Dimer绝对值应小于4.5kcal/mol, The most stable Dimer overall绝对值一般应小于多少kcal/mol跟PCR退火温度有关,我几次实验感觉在PCR退火温度在65°的时候,The most stable Dimer ove rall 6.7kcal/mol没有问题。 2.Hairpin Formation根据黄金法则 3.False priming sites: Primer的priming efficiency应该是错配地方的4倍左右,更多当然更好。 4.在PCR栏,个人感觉其所显示的optimal annealing temperature数值值得参考。在PCR摸索条件的时候,退火温度为其数值加减2的范围就可以了。 5.Internal stability很重要:我们希望引物的内部稳定性是中间高、两边低的弧形,最起码保证3端不要过于稳定。下图1引物3端过于稳定,很容易导致不适当扩增。△G参照黄金法则,这其实很好理解:把一滴水放到大海里,这滴水就会不停的扩散分布,扩散的越厉害越稳定,所以△G绝对值越大结构越稳定。 最后说一句,敢于尝试就会成功。 第二贴 --科室工作很多,小医生了,没有办法,所以肯怕不能满足很多战友的要求(qq聊或帮助设计),在此表示抱歉。就楼上的问题我试着回答一下,不一定正确,供参考吧。 --1、两个评价系统不一样,个人感觉oligo评价引物好点,primer出来的引物,我一般按效率排序,再结合退火温度和引物长度,选择引物到oligo测试。这是初步的选择,其实引物到了oligo里,退火温度也不一样。 --2、3端的二聚体应该避免,这个要看你的退火温度决定,一个50°的退火温度肯定和65°对二聚体的影响不一样了,一般来讲尽量控制在-4.5kcal/mol以下(个人观点,很多东西真得还是需要自己摸索)。 --3、个人感觉3端有A无A影响不大,3端有T的没有经验。有T是不是一定不行,个人感觉不见得。软件是评估,法则也不是没有例外,不是1+1=2那么确定。 --4、错配和二聚体谁轻谁重,个人觉得“到致命的程度”谁都重要,我也说不好。我设计的时候,尽量两个都不得罪。 --5、GC含量并非不重要,它直接影响引物各端稳定性,3端来两个G或C,稳定性就上去了,粘在模板上很牢。所以我设计的时候,尽量避免这样的情况出现。 谈一下我学这个引物设计的过程吧:
图解blast验证引物教程 1、进入网页:https://www.doczj.com/doc/fc11429442.html,/BLAST/ 2、点击Search for short, nearly exact matches 3、在search栏中输入引物系列: 注:文献报道ABCG2的引物为5’-CTGAGATCCTGAGCCTTTGG-3’; 5’-TGCCCATCACAACATCATCT-3’ (1)输入方法可先输入上游引物,进行blast程序,同样方法在进行下游引物的blast程序。这种方法叫繁琐,而且在结果分析特异性时要看能与上游引物的匹配的系列,还要看与下游引物匹配的系列——之后看两者的交叉。 (2)简便的做法是同时输入上下游引物:有以下两种方法。输入上下游引物系列都从5’——3’。 A、输入上游引物空格输入下游引物
B、输入上游引物回车输入下游引物 4、在options for advanced blasting中: select from 栏通过菜单选择Homo sapiens【ORGN】Expect后面的数字改为10 5、在format中: select from 栏通过菜单选择Homo sapiens【ORGN】Expect后面的数字填上0 10
6、点击网页中最下面的“BLAST!” 7、出现新的网页,点击Format! 果。
(1)图形格式: 图中①代表这些序列与上游引物匹配、并与下游引物互补的得分值都位于40~50分 图中②代表这些序列与上游引物匹配的得分值位于40~50分,而与下游引物不互补 图中③代表这些序列与下游引物互补的得分值小于40分,而与上游引物不匹配 通过点击相应的bar可以得到匹配情况的详细信息。 (2)结果信息概要: 从左到右分别为: A、数据库系列的身份证:点击之后可以获得该序列的信息 B、系列的简单描述 C、高比值片段对(high-scoring segment pairs, HSP)的字符得分。按照得分的高低由大到小排列。得分的计算公式=匹配的碱基×2+0.1。举例:如果有20个碱基匹配,则其得分为40.1。 D、E值:代表被比对的两个序列不相关的可能性。【The E value decreases exponentially as the Score (S) that is assigned to a match between two sequences increases】。E值最低的最有意义,也就是说序列的相似性最大。设定的E值是我们限定的上限,E值太高的就不显示了 E、最后一栏有的有UEG的字样,其中: U代表:Unigene数据库 E代表:GEO profiles数据库 G代表:Gene数据库
1.引物最好在模板cDNA的保守区内设计。 DNA序列的保守区是通过物种间相似序列的比较确定的。在NCBI上搜索不同物种的同一基因,通过序列分析软件(比如DNAman)比对(Alignment),各基因相同的序列就是该基因的保守区。 2.引物长度一般在15~30碱基之间。 引物长度(primer length)常用的是18-27 bp,但不应大于38,因为过长会导致其延伸温度大于74℃,不适于Taq DNA 聚合酶进行反应。 3.引物GC含量在40%~60%之间,Tm值最好接近72℃。 GC含量(composition)过高或过低都不利于引发反应。上下游引物的GC含量不能相差太大。另外,上下游引物的Tm值(melting temperature)是寡核苷酸的解链温度,即在一定盐浓度条件下,50%寡核苷酸双链解链的温度。有效启动温度,一般高于Tm值5~10℃。若按公式Tm= 4(G+C)+2(A+T)估计引物的Tm值,则有效引物的Tm为55~80℃,其Tm 值最好接近72℃以使复性条件最佳。 4.引物3′端要避开密码子的第3位。 如扩增编码区域,引物3′端不要终止于密码子的第3位,因密码子的第3位易发生简并,会影响扩增的特异性与效率。 5.引物3′端不能选择A,最好选择T。 引物3′端错配时,不同碱基引发效率存在着很大的差异,当末位的碱基为A时,即使在错配的情况下,也能有引发链的合成,而当末位链为T时,错配的引发效率大大降低,G、C 错配的引发效率介于A、T之间,所以3′端最好选择T。 6. 碱基要随机分布。 引物序列在模板内应当没有相似性较高,尤其是3’端相似性较高的序列,否则容易导致错误引发(False priming)。降低引物与模板相似性的一种方法是,引物中四种碱基的分布最好是随机的,不要有聚嘌呤或聚嘧啶的存在。尤其3′端不应超过3个连续的G或C,因这样会使引物在GC富集序列区错误引发。 7. 引物自身及引物之间不应存在互补序列。 引物自身不应存在互补序列,否则引物自身会折叠成发夹结构(Hairpin)使引物本身复性。这种二级结构会因空间位阻而影响引物与模板的复性结合。引物自身不能有连续4个碱基的互补。 两引物之间也不应具有互补性,尤其应避免3′ 端的互补重叠以防止引物二聚体(Dimer与Cross dimer)的形成。引物之间不能有连续4个碱基的互补。 引物二聚体及发夹结构如果不可避免的话,应尽量使其△G值不要过高(应小于4.5kcal/mol)。否则易导致产生引物二聚体带,并且降低引物有效浓度而使PCR 反应不能正常进行。 8. 引物5′ 端和中间△G值应该相对较高,而3′ 端△G值较低。 △G值是指DNA 双链形成所需的自由能,它反映了双链结构内部碱基对的相对稳定性,△G 值越大,则双链越稳定。应当选用5′ 端和中间△G值相对较高,而3′ 端△G值较低(绝对值不超过9)的引物。引物3′ 端的△G 值过高,容易在错配位点形成双链结构并引发DNA 聚合反应。(不同位置的△G值可以用Oligo 6软件进行分析) 9.引物的5′端可以修饰,而3′端不可修饰。 引物的5′ 端决定着PCR产物的长度,它对扩增特异性影响不大。因此,可以被修饰而不影响扩增的特异性。引物5′ 端修饰包括:加酶切位点;标记生物素、荧光、地高辛、Eu3+等;引入蛋白质结合DNA序列;引入点突变、插入突变、缺失突变序列;引入启动子序列等。引物的延伸是从3′ 端开始的,不能进行任何修饰。3′ 端也不能有形成任何二级结构可能。 10. 扩增产物的单链不能形成二级结构。
1. 引物的长度一般为15-30 bp,常用的是18-27 bp,但不应大于38,因为过长会导致其延伸温度大于74℃,不适于Taq DNA聚合酶进行反应。 2. 引物序列在模板内应当没有相似性较高,尤其是3’端相似性较高的序列,否则容易导致错配。引物3’端出现3个以上的连续碱基,如GGG或CCC,也会使错误引发机率增加。 3. 引物3’端的末位碱基对Taq酶的DNA合成效率有较大的影响。不同的末位碱基在错配位置导致不同的扩增效率,末位碱基为A的错配效率明显高于其他3个碱基,因此应当避免在引物的3’端使用碱基A。另外,引物二聚体或发夹结构也可能导致PCR反应失败。5’端序列对PCR影响不太大,因此常用来引进修饰位点或标记物。 4. 引物序列的GC含量一般为40-60%,过高或过低都不利于引发反应。上下游引物的GC含量不能相差太大。 5. 引物所对应模板位置序列的Tm值在72℃左右可使复性条件最佳。Tm值的计算有多种方法,如按公式Tm=4(G+C)+2(A+T),在Oligo软件中使用的是最邻近法(the nearest neighbor method)。 6. ΔG值是指DNA双链形成所需的自由能,该值反映了双链结构内部碱基对的相对稳定性。应当选用3’端ΔG值较低(绝对值不超过9),而5’端和中间ΔG值相对较高的引物。引物的3’端的ΔG值过高,容易在错配位点形成双链结构并引发DNA聚合反应。 7. 引物二聚体及发夹结构的能值过高(超过mol)易导致产生引物二聚体带,并且降低引物有效浓度而使PCR反应不能正常进行。 8. 对引物的修饰一般是在5’端增加酶切位点,应根据下一步实验中要插入PCR 产物的载体的相应序列而确定。 引物序列应该都是写成5-3方向的, Tm之间的差异最好控制在1度之内, 另外我觉得扩增长度大一些比较好,500bp左右。 要设计引物首先要找到DNA序列的保守区。同时应预测将要扩增的片段单链是否形成二级结构。如这个区域单链能形成二级结构,就要避开它。如这一段不能形成二级结构,那就可以在这一区域设计引物。
引物设计的11条黄金法则
PCR引物设计的11条黄金法则 1.引物最好在模板cDNA的保守区内设计。DNA序列的保守区是通过物种间相似序列的比较确定的。在NCBI上搜索不同物种的同一基因,通过序列分析软件(比如DNAman)比对(Alignment),各基因相同的序列就是该基因的保守区。 2.引物长度一般在15~30碱基之间。 引物长度(primerlength)常用的是18-27bp,但不应大于38,因为过长会导致其延伸温度大于74℃,不适于TaqDNA聚合酶进行反应。 3.引物GC含量在40%~60%之间,Tm值最好接近72℃。 GC含量(composition)过高或过低都不利于引发反应。上下游引物的GC含量不能相差太大。另外,上下游引物的Tm值(meltingtemperature)是寡核苷酸的解链温度,即在一定盐浓度条件下,50%寡核苷酸双链解链的温度。有效启动温度,一般高于Tm值
5~10℃。若按公式Tm=4(G+C)+2(A+T)估计引物的Tm值,则有效引物的Tm为55~80℃,其Tm值最好接近72℃以使复性条件最佳。 4.引物3′端要避开密码子的第3位。 如扩增编码区域,引物3′端不要终止于密码子的第3位,因密码子的第3位易发生简并,会影响扩增的特异性与效率。 5.引物3′端不能选择A,最好选择T。 引物3′端错配时,不同碱基引发效率存在着很大的差异,当末位的碱基为A时,即使在错配的情况下,也能有引发链的合成,而当末位链为T 时,错配的引发效率大大降低,G、C错配的引发效率介于A、T之间,所以3′端最好选择T。 6.碱基要随机分布。 引物序列在模板内应当没有相似性较高,尤其是3’端相似性较高的序列,否则容易导致错误引发(Falsepriming)。降低引物与模板相似性的一种方法是,引物中四种碱基的分布最好是随机的,不要有聚嘌呤或聚嘧啶的存在。尤其3′端
1.引物应用核酸系列保守区内设计并具有特异性。最好位于编码区5’端的300-400bp区域 内,可以用DNAman,Alignment 软件看看结果。 2. 产物不能形成二级结构(自由能小于58.61KJ/mol)。 3.引物长度一般在17-25碱基之间,上下游引物不能相差太大。 4.G+C含量在40%~60%之间,45-55%最佳。 5.碱基要随机分布,尽量均匀。 6.引物自身不能有连续4个碱基的互补。 7.引物之间不能有连续4个碱基的互补。 8.引物5′端可以修饰。 9.3′端不可修饰,而且要避开AT,GC rich的区域,避开T/C,A/G连续结构(2-3个)。 10. 引物3′端要避开密码子的第3位。 11.引物整体设计自由能分布5‘端大于3’端,且3‘端自由能最好小于9KJ/mol。 可用oligo 6 软件进行比对看结果的情况。 12.做荧光定量产物长度80-150bp最好,最长是300bp. 13.引物设计避免DNA污染,最好跨外显子接头区。 14.引物与非特异性扩增序列的同源性最好小于70%或者有8个互补碱基同源。 15.查看有无假基因的存在。假基因就是无功能的DNA序列,与需要扩增的目的片段长 度相似。 16.TM值在58-62度之间。 17.引物设计的软件Primer 5.0 有专门针对荧光的。 设计的目的是在两个目标间取得平衡:扩增特异性和扩增效率。引物分析软件将试图通过使用每一引物设计变化的预定值在这两个目标间取得平衡。设计引用有一些需要注意的基本原理: ①引物长度 一般引物长度为18~30碱基。总的说来,决定引物退火温度(Tm值)最重要的因素就是引物的长度。有以下公式可以用于粗略计算引物的退火温度。 在引物长度小于20bp时:[4(G+C)+2(A+T)]-5℃ 在引物长度大于20bp时:62.3℃+0.41℃(%G-C)-500/length-5℃ 另外有许多软件也可以对退火温度进行计算,其计算原理会各有不同,因此有时计算出的数值可能会有少量差距。为了优化PCR反应,使用确保退火温度不低于54℃的最短的引物可获得最好的效率和特异性。
引物设计step by step 1、在NCBI上搜索到目的基因,找到该基因的mRNA,在CDS选项中,找到编码区所在位置,在下面的origin中,Copy该编码序列作为软件查询序列的候选对象。 2、用Primer Premier5搜索引物 ①打开Primer Premier5,点击File-New-DNA sequence, 出现输入序列窗口,Copy目的序列在输入框内(选择As),此窗口内,序列也可以直接翻译成蛋白。点击Primer,进入引物窗口。 ②此窗口可以链接到“引物搜索”、“引物编辑”以及“搜索结果”选项,点击Search按钮,进入引物搜索框,选择“PCR primers”,“Pairs”,设定搜索区域和引物长度和产物长度。在Search Parameters里面,可以设定相应参数。一般若无特殊需要,参数选择默认即可,但产物长度可以适当变化,因为100~200bp的产物电泳跑得较散,所以可以选择300~500bp. ③点击OK,软件即开始自动搜索引物,搜索完成后,会自动跳出结果窗口,搜索结果默认按照评分(Rating)排序,点击其中任一个搜索结果,可以在“引物窗口”中,显示出该引物的综合情况,包括上游引物和下游引物的序列和位置,引物的各种信息等。 ④对于引物的序列,可以简单查看一下,避免出现下列情况:3’不要出现连续的3个碱基相连的情况,比如GGG或CCC,否则容易引起错配。此窗口中需要着重查看的包括:Tm 应该在55~70度之间,GC%应该在45%~55%间,上游引物和下游引物的Tm值最好不要相差太多,大概在2度以下较好。该窗口的最下面列出了两条引物的二级结构信息,包括,发卡,二聚体,引物间交叉二聚体和错误引发位置。若按钮显示为红色,表示存在该二级结构,点击该红色按钮,即可看到相应二级结构位置图示。最理想的引物,应该都不存在这些二级结构,即这几个按钮都显示为“None”为好。但有时很难找到各个条件都满足的引物,所以要求可以适当放宽,比如引物存在错配的话,可以就具体情况考察该错配的效率如何,是否会明显影响产物。对于引物具体详细的评价需要借助于Oligo来完成,Oligo自身虽然带有引物搜索功能,但其搜索出的引物质量感觉不如Primer5. ⑤在Primer5窗口中,若觉得某一对引物合适,可以在搜索结果窗口中,点击该引物,然后在菜单栏,选择File-Print-Current pair,使用PDF虚拟打印机,即可转换为Pdf文档,里面有该引物的详细信息。 3、用Oligo验证评估引物 ①在Oligo软件界面,File菜单下,选择Open,定位到目的cDNA序列(在primer中,该序列已经被保存为Seq文件),会跳出来两个窗口,分别为Internal Stability(Delta G)窗口和Tm窗口。在Tm窗口中,点击最左下角的按钮,会出来引物定位对话框,输入候选的上游引物序列位置(Primer5已经给出)即可,而引物长度可以通过点击Change-Current oligo length来改变。定位后,点击Tm窗口的Upper按钮,确定上游引物,同样方法定位下游引物位置,点击Lower按钮,确定下游引物。引物确定后,即可以充分利用Analyze 菜单中各种强大的引物分析功能了。
PCR引物设计原则 引物(Primer)是人工合成的两段寡核苷酸序列。 1、引物的长度一般为15-30bp,常用的是18-27bp,但不应大于38,因为过长会导致其延伸温度大于74℃,不适于Taq DNA聚合酶进行反应。 2、G十C含量:应在40%-60%之间,PCR扩增中的复性温度一般是较低Tm 值引物的Tm值减去5-10度。引物长度小于20时,其Tm恒等于4(G十C)十2(A十T)。 3、碱基分布的随机性:应避免连续出现4个以上的单一碱基。尤其是不应在其3’端出现超过3个的连续G或C,否则会使引物在G十C富集序列区错误引发. 4、引物自身:不能含有自身互补序列,否则会形成发夹样二级结构. 5、引物之间:两个引物之间不应有多于4个的互补或同源碱基,不然会形成引物二聚体,尤应避免3’端的互补重叠。引物3’端最好选T,错配的几率与A 相比大大的降低了。G、C之间错配的概率小于A、T. 6、引物的5’端可以修饰,而3’端不能进行修饰。5’端的修饰包括:加酶切位点,标记生物素,荧光,地高辛、Eu3+等,引入蛋白质结合的DNA序列,引入点突变,插入突变、缺失突变序列、引入启动子序列。因为引物的延伸是从3’端开始的,因而3’端不能进行任何修饰,另外3’端也不能有形成任何二
级结构的可能。 如何设计引物 不同的核苷酸序列表达的氨基酸氨基酸序列是相同的,所以氨基酸序列才是真正保守的。 引物最好在模板cDNA的保守区域内设计(DNA的保守区是通过物种间相似序列的比较确定的,在NCBI上搜索不同物种的同一基因,通过序列分析软件比对(Alignment),各基因相同的序列就是该基因的保守区)。 PCR引物设计 PCR反应中有两条引物,即5′端引物和3′引物。设计引物时以一条DNA单链为基准(常以信息链为基准),5′端引物与位于待扩增片段5′端上的一小段DNA序列相同;3′端引物与位于待扩增片段3′端的一小段DNA序列互补。 引物设计软件 Primer Premier5.0 (自动搜索)* vOligo6 (引物评价) vVector NTI Suit vDNAsis vOmiga vDNAstar vPrimer3 (在线服务)
引物设计的原理与方法 This model paper was revised by the Standardization Office on December 10, 2020
PCR引物设计的原理及方法 阎振鑫S111666(四川大学生命科学学院细胞生物学成都 610014) 摘要:自20世纪后期发展了PCR技术以来,PCR已经改变了整个生物学研究的进程。而PCR反应的第一步就是设计引物,引物设计的好坏直接关系到PCR的成败。PCR引物设计有许多的原则必须要遵循:引物与引物之间避免形成稳定的二聚体或发夹结构,引物与模板的序列要紧密互补。引物不能在模板的非目的位点引发DNA聚合反应等。另外,引物的设计方法也越来越多,出现了许多专门的设计软件和网站,如:PrimerPremier5.0等。 关键词:PCR 引物原理方法 NCBI PrimerPremier5.0 PCR primer design principle and method YanZhenxin (sichuan Univercity, Life science college cell biology chengdu 610014 ) Abstract: When PCR technology was find, PCR has changed all of the program in research of biology. The design of primer is the frist step of PCR. It is relation to the fate of PCR. There are some principals must be obey: dipolymer and hairpin structure must be avoid between different primers. The DNA polymerization reaction should not be triggered at the wrong site. Therefore, there are more and more methods of design primer, include the professional softwares and professional web site. Key word: PCR primer principle NCBI PrimerPremier5.0 聚合酶链式反应(Polymerase chain reaction。PCR)是20世纪后期发展起来的 一种体外扩增特异DNA片断的技术。具有快速、简便及高度敏感等优点,能极大地缩短目的基因扩增时间[1]。因此,其一直是生物学者们致力于构建cDNA文库、基因克隆以及表达调控研究的必要前提和基础[2]。PCR的第一步就是引物设计。引物设计的好坏,直接影响了PCR的结果,因此这一步很关键。成功的PCR反应既要高效,又要特异性扩增产物,因此对引物设计提出了较高的要求。引物设计需要注意的地方很多,在大多数情况下,我们都是在知道已知模板序列时进行PCR扩增的。在某些情况比如构建文库的时候也会在不知道模板序列的情况下进行设计。这个时候随机核苷酸序列
本文叙述了一种用于甲基化分析的探针法定量PCR的引物和探针设计方法,目前用于甲基化检测的引物探针设计工具非常多,都有使用成功的案例,经过初步多方尝试,本文中叙述的为本人认为较为靠谱的方法。Oligo7的优势在于专业,参数详尽且可自由设置,模块化设计,学会后使用便利。专业的活就是要专业的用专业的工具干。
首先是进行序列转换,有较多的在线工具和联机软件都可实现,这里使用https://www.doczj.com/doc/fc11429442.html,/methprimer/,较为简单直观。
直接将目标序列放入如上图的编辑框中,此也可直接用于相关引物的设计,不过本人没使用过,因为不能设计探针。submit后就有转化后的序列信息,如下图: 以上详细标记了CpG位置和非CpG位置的C,可直接复制到Word标注使用,下面就可以使用Oligo7利用上边的序列设计引物和探针了,如果是设计非甲基化引物探针,则使用原始序列。
关于引物和探针的一些主要参数,主要参考invtrogen的建议: Primer设计的基本原则: a)引物长度一般在18-35mer。 b)G-C含量控制在40-60%左右。 c)避免近3’端有酶切位点或发夹结构。 d)如果可能避免在3’端最后5个碱基有2个以上的G或C。 e)如果可能避免在3’端最后1个碱基为A。 f)避免连续相同碱基的出现,特别是要避免GGGG或更多G出现。 g)退火温度Tm控制在58-60C左右。 h)如果是设计点突变引物,突变点应尽可能在引物的中间。 T aqMan 探针设计的基本原则: a)T aqMan 探针位置尽可能靠近扩增引物(扩增产物50-150bp),但不能与引物重叠。 b)长度一般为18-40mer 。 c)G-C含量控制在40-80%左右。 d)避免连续相同碱基的出现,特别是要避免GGGG或更多G出现。 e)在引物的5’端避免使用G。 f)选用比较多的碱基C。 g)退火温度Tm控制在68-70℃左右。 另:目标变异碱基最好在3’末端或3’末端-1位置,保证扩增特异性,对于甲基化,则最好是C。
mi引物设计原则 1、引物的长度一般为15-30 bp,常用的就是18-27 bp,但不应大于38,因为过长会导致其延伸温度大于74℃,不适于Taq DNA聚合酶进行反应。 2、引物序列在模板内应当没有相似性较高,尤其就是3’端相似性较高的序列,否则容易导致错配。引物3’端出现3个以上的连续碱基,如GGG或CCC,也会使错误引发机率增加。 3、引物3’端的末位碱基对Taq酶的DNA合成效率有较大的影响。不同的末位碱基在错配位置导致不同的扩增效率,末位碱基为A的错配效率明显高于其她3个碱基,因此应当避免在引物的3’端使用碱基A。另外,引物二聚体或发夹结构也可能导致PCR反应失败。5’端序列对PCR影响不太大,因此常用来引进修饰位点或标记物。 4、引物序列的GC含量一般为40-60%,过高或过低都不利于引发反应。上下游引物的GC含量不能相差太大。 5、引物所对应模板位置序列的Tm值在72℃左右可使复性条件最佳。Tm值的计算有多种方法,如按公式Tm=4(G+C)+2(A+T),在Oligo软件中使用的就是最邻近法(the nearest neighbor method)。 6、ΔG值就是指DNA双链形成所需的自由能,该值反映了双链结构内部碱基对的相对稳定性。应当选用3’端ΔG值较低(绝对值不超过9),而5’端与中间ΔG值相对较高的引物。引物的3’端的ΔG值过高,容易在错配位点形成双链结构并引发DNA聚合反应。 7、引物二聚体及发夹结构的能值过高(超过4、5kcal/mol)易导致产生引物二聚体带,并且降低引物有效浓度而使PCR反应不能正常进行。 8、对引物的修饰一般就是在5’端增加酶切位点,应根据下一步实验中要插入PCR产物的载体的相应序列而确定。 引物序列应该都就是写成5-3方向的, Tm之间的差异最好控制在1度之内, 另外我觉得扩增长度大一些比较好,500bp左右。 要设计引物首先要找到DNA序列的保守区。同时应预测将要扩增的片段单链就是否形成二级结构。如这个区域单链能形成二级结构,就要避开它。如这一段不
Oligo 设计教程 在正式进行引物设计前,我们首先面临的一个任务就是向Oligo 程序导入模板序列,根据不同的实验情况,导入模板有三种方法:1,直接用键盘输入: a,点击file菜单中的New Sequence 浮动命令,或直接点击工具栏中的New Sequence命令,进入序列展示窗口; b,此时即可键入DNA序列; c,如果需要的话,Oligo提供碱基回放功能,在边键入时边读出碱基,防止输入错误。点击Edit菜单中的“Readback on”即可。 2,利用复制和粘贴:当我们序列已经作为TXT文件存在或其它oligo不能直接open的文件格式,如word文件.html格式,这个功能就显得很有用了。在相应文件中复制序列后在序列展示窗口粘贴,oligo会自动去除非碱基字符。当序列输入或粘贴完成后,点击Accept/Discard菜单中的Accept浮动命令,即可进入引物设计模式。 3,如果序列已经保存为Seq格式或者FASTA,GenBank格式时,oligo就可以直接打开序列文件。 点击File菜单中的“Open”浮动命令,找到所需文件,打开即可。
进入引物设计模式后,oligo一般会弹出三个窗口,分别是6-碱基频率窗口,碱基退火温度窗口以及序列内部碱基稳定性窗口,其中的退火温度窗口是我们引物设计的主窗口,其它的两个窗口则在设计过程中起辅助作用,比如6-碱基频率窗口可以使我们很直观地看到所设计引物在相应物种基因组中的出现频率,如果我们的模板是基因组DNA或混合DNA时,该信息就显得有用了,而内部稳定性窗口则可以显示引物的5’端稳定性是否稍高于3’端等。 一,普通引物对的搜索: 以Mouse 4E(cDNA序列)为例。我们的目的是以Mouse 4E (2361 bp)为模板,设计一对引物来扩增出600-800bp长的PCR产物。 1,点击“Search“菜单中的”For Primers and Probes“命令,进入引物搜索对话框; 2,由于我们要设计的是一对PCR引物,因此正、负链的复选框都要选上,同时选上Compatible pairs。 在Oligo默认的状态下,对此引物对的要求有:a,无二聚体;b,3’端高度特异,GC含量有限定,d,去除错误引发引物等。3,剩下的工作是确定上、下游引物的位置及PCR产物的长度以及引物设计参数。 ①单击:“search Ranges”按钮,弹出“Search Ranges”对
PCR引物设计原理及原则 PCR引物设计原理 PCR引物设计的目的是为了找到一对合适的核苷酸片段,使其能有效地扩增模板DNA序列。因此,引物的优劣直接关系到PCR的特异性与成功与否。 要设计引物首先要找到DNA序列的保守区。同时应预测将要扩增的片段单链是否形成二级结构。如这个区域单链能形成二级结构,就要避开它。如这一段不能形成二级结构,那就可以在这一区域设计引物。 现在可以在这一保守区域里设计一对引物。一般引物长度为15~30碱基,扩增片段长度为100~600碱基对。 让我们先看看P1引物。一般引物序列中G+C含量一般为40%~60%。而且四种碱基的分布最好随机。不要有聚嘌呤或聚嘧啶存在。否则P1引物设计的就不合理。应重新寻找区域设计引物。 同时引物之间也不能有互补性,一般一对引物间不应多于4个连续碱基的互补。 引物确定以后,可以对引物进行必要的修饰,例如可以在引物的5′端加酶切位点序列;标记生物素、荧光素、地高辛等,这对扩增的特异性影响不大。但3′端绝对不能进行任何修饰,因为引物的延伸是从3′端开始的。这里还需提醒的是3′端不要终止于密码子的第3位,因为密码子第3位易发生简并,会影响扩增的特异性与效率。 PCR引物的设计原则: ①引物应用核酸系列保守区内设计并具有特异性。 ②产物不能形成二级结构。 ③引物长度一般在15~30碱基之间。 ④G+C含量在40%~60%之间。 ⑤碱基要随机分布。 ⑥引物自身不能有连续4个碱基的互补。 ⑦引物之间不能有连续4个碱基的互补。 ⑧引物5′端可以修饰。 ⑨引物3′端不可修饰。 ⑩引物3′端要避开密码子的第3位。 PCR引物设计的目的是找到一对合适的核苷酸片段,使其能有效地扩增模板DNA序列。如前述,引物的优劣直接关系到PCR的特异性与成功与否。对引物的设计不可能有一种包罗万象的规则确保PCR的成功,但遵循某些原则,则有助于引物的设计。 1.引物的特异性 引物与非特异扩增序列的同源性不要超过70%或有连续8个互补碱基同源。 2.避开产物的二级结构区 某些引物无效的主要原因是引物重复区DNA二级结构的影响,选择扩增片段时最好避开二级结构区域。用有关计算机软件可以预测估计mRNA的稳定二级结构,有助于选择模板。实验表明,待扩区域自由能(△G°)小于58.6lkJ/mol时,扩增往往不能成功。若不能避开这一区域时,用7-deaza-2′-脱氧GTP取代dGTP对扩增的成功是有帮助的。 3.长度 寡核苷酸引物长度为15~30bp,一般为20~27mer。引物的有效长度:Ln=2(G+C)+(A+T+,Ln值不能大于38,因为>38时,最适延伸温度会超过Taq DNA聚合酶的最适温度(74℃),不能保证产物的特异性。 4.G+C含量
PCR引物设计的原理及方法 阎振鑫S111666(四川大学生命科学学院细胞生物学成都610014) 摘要:自20世纪后期发展了PCR技术以来,PCR已经改变了整个生物学研究的进程。而PCR反应的第一步就是设计引物,引物设计的好坏直接关系到PCR的成败。PCR引物设计有许多的原则必须要遵循:引物与引物之间避免形成稳定的二聚体或发夹结构,引物与模板的序列要紧密互补。引物不能在模板的非目的位点引发DNA聚合反应等。另外,引物的设计方法也越来越多,出现了许多专门的设计软件和网站,如:PrimerPremier5.0等。 关键词:PCR 引物原理方法NCBI PrimerPremier5.0 PCR primer design principle and method YanZhenxin (sichuan Univercity, Life science college cell biology chengdu 610014 ) Abstract: When PCR technology was find, PCR has changed all of the program in research of biology. The design of primer is the frist step of PCR. It is relation to the fate of PCR. There are some principals must be obey: dipolymer and hairpin structure must be avoid between different primers. The DNA polymerization reaction should not be triggered at the wrong site. Therefore, there are more and more methods of design primer, include the professional softwares and professional web site. Key word: PCR primer principle NCBI PrimerPremier5.0 聚合酶链式反应(Polymerase chain reaction。PCR)是20世纪后期发展起来的一种体外扩增特异DNA片断的技术。具有快速、简便及高度敏感等优点,能极大地缩短目的基因扩增时间[1]。因此,其一直是生物学者们致力于构建cDNA文库、基因克隆以及表达调控研究的必要前提和基础[2]。PCR的第一步就是引物设计。引物设计的好坏,直接影响了PCR的结果,因此这一步很关键。成功的PCR反应既要高效,又要特异性扩增产物,因此对引物设计提出了较高的要求。引物设计需要注意的地方很多,在大多数情况下,我们都是在知道已知模板序列时进行PCR扩增的。在某些情况比如构建文库的时候也会在不知道模板序列的情况下进行设计。这个时候随机核苷酸序列就与模板不是完全匹配。我们通常指的设计引物都是在已知模板序列的情况下进行。设计的目的是在两个目标间取得平衡:扩增特异性和扩增效率。
图解blast 验证引物教程 ——以文献报道的人类的ABCG2的引物为例 1、 进入网页:https://www.doczj.com/doc/fc11429442.html,/BLAST/ 2、 点击Basic BLAST 中的nucleotide blast 选项 3、 完成2操作后就进入了Basic Local Alignment Search Tool 界面 (1)在Enter Query Sequence 栏中输入引物序列: 注:文献报道ABCG2的引物为5’-CTGAGATCCTGAGCCTTTGG-3’; 5’-TGCCCATCACAACATCATCT-3’ 简便的做法是同时输入上下游引物。输入上下游引物系列都从5’— 3’。 输入上游引物后,加上≥20个字母n ,再输入下游引物,如下图: 生 物 秀
(2)在Choose Search Set 栏中: Database 根据预操作基因的种属定了,本引物可选Human genomic + transcript 或Others (nr etc.)。本人倾向于选后者,觉得此库信息更多。如下图: (3)在Program Selection 中:选择Somewhat similar sequences (blastn)项,如下图: (4)在此界面最下面:如下图 生物秀-专心做生物 w w w .b b i o o .c o m
Show results in a new window 项是显示界面的形式,可选可不选,在此我们选上了。关键要点击Algorithm parameters 参数设置,进入参数设置界面。 4. 参数设置: (1)在General Parameters 中:Expect thresshold 期望阈值须改为1000,大于1000也可以;在Word size 的下拉框将数字改为7。如下图: (2)Scoring Parameters 无须修改 (3)Filters and Masking 中,一般来说也没有必要改 5.点击最下面一栏的BLAST 按钮,如图: 6.点击BLAST 按钮后,跳转出现如下界面: 7. 等待若干秒之后,自动跳转出现显示BLAST 结果的网页。该网页用三种形式来显示blast 的结果。 生物秀-专心做生物 w w w .b b i o o .c o m
引物设计的原理与方法 The latest revision on November 22, 2020
PCR引物设计的原理及方法 阎振鑫S111666(四川大学生命科学学院细胞生物学成都 610014) 摘要:自20世纪后期发展了PCR技术以来,PCR已经改变了整个生物学研究的进程。而PCR反应的第一步就是设计引物,引物设计的好坏直接关系到PCR的成败。PCR引物设计有许多的原则必须要遵循:引物与引物之间避免形成稳定的二聚体或发夹结构,引物与模板的序列要紧密互补。引物不能在模板的非目的位点引发DNA聚合反应等。另外,引物的设计方法也越来越多,出现了许多专门的设计软件和网站,如:PrimerPremier5.0等。 关键词:PCR 引物原理方法 NCBI PrimerPremier5.0 PCR primer design principle and method YanZhenxin (sichuan Univercity, Life science college cell biology chengdu 610014 ) Abstract: When PCR technology was find, PCR has changed all of the program in research of biology. The design of primer is the frist step of PCR. It is relation to the fate of PCR. There are some principals must be obey: dipolymer and hairpin structure must be avoid between different primers. The DNA polymerization reaction should not be triggered at the wrong site. Therefore, there are more and more methods of design primer, include the professional softwares and professional web site. Key word: PCR primer principle NCBI PrimerPremier5.0 聚合酶链式反应(Polymerase chain reaction。PCR)是20世纪后期发展起来的 一种体外扩增特异DNA片断的技术。具有快速、简便及高度敏感等优点,能极大地缩短目的基因扩增时间[1]。因此,其一直是生物学者们致力于构建cDNA文库、基因克隆以及表达调控研究的必要前提和基础[2]。PCR的第一步就是引物设计。引物设计的好坏,直接影响了PCR的结果,因此这一步很关键。成功的PCR反应既要高效,又要特异性扩增产物,因此对引物设计提出了较高的要求。引物设计需要注意的地方很多,在大多数情况下,我们都是在知道已知模板序列时进行PCR扩增的。在某些情况比如构建文库的时候也会在不知道模板序列的情况下进行设计。这个时候随机核苷酸序列