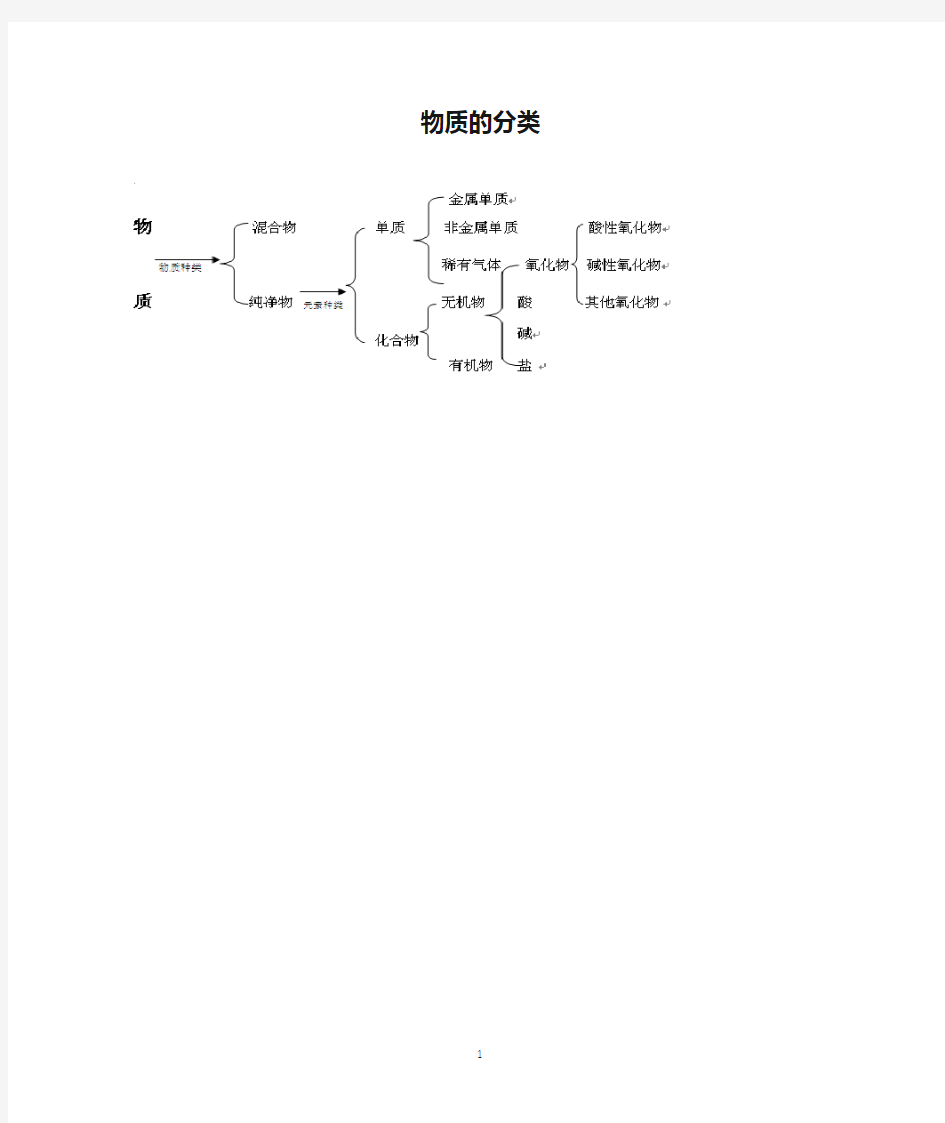

物质的分类
1.混合物:是由两种或两种以上的物质混合而成(或由不同种物质组成) 例如,空气,溶液(盐酸、澄清的石灰水、碘酒、矿泉水), 矿物(煤、石 油、天然气、铁矿石、石灰石),合金(生铁、钢)
注意:氧气和臭氧混合而成的物质是混合物,红磷和白磷混合也是混合物。纯净物、混合物与组成元素的种类无关。即一种元素组成的物质可能是纯净物也可能是混合物,多种元素组成的物质可能是纯净物或混合物。
2.纯净物:由一种物质组成的。 例如:水、 水银、 蓝矾(CuSO 4 ·5H 2 O)都是纯净物 冰与水混合是纯净物。 名称中有“某化某”“某酸某”的都是纯净物,是化合物。
注意:由同一种元素构成的物质不一定是纯净物(如O 2 、O 3 );具有相同组成(如最简式、分子式相同)的物质也不一定是纯净物。比如金刚石和石墨。
3.单质:由同种(或一种)元素组成的纯净物。例如:铁 氧气(液氧)、氢气、水银。
4.化合物:由不同种(两种或两种以上)元素组成的纯净物。名称中有“某化某”“某酸某”的是化合物。
5.有机物(有机化合物):含碳元素的化合物(除CO 、CO 2 和含碳酸根化合物外) 无机物:不含碳元素的化合物以及CO 、CO 2 和含碳酸根的化合物
6. 氧化物:由两种元素组成,其中一种是氧元素的化合物。
a.酸性氧化物:跟碱反应生成盐和水的氧化物。CO 2 ,SO 2 ,SO 3 大部分非金属氧化物都是酸性氧化物,跟水反应生成同价的含氧酸。
CO 2 + H 2O= H 2CO 3 SO 2 + H 2O= H 2SO 3 SO 3 + H 2O= H 2SO 4
b.碱性氧化物:跟酸反应生成盐和水的氧化物。CaO Na
2O MgO Fe
2
O
3
CuO
大部分金属氧化物都是碱性氧化物,BaO K
2O CaO Na
2
O溶于水立即跟水反
应生成相应的碱,其他碱性氧化物不溶于水,跟水不反应。
CaO+H2O=Ca(OH)2 BaO+H2O=Ca(OH)2 Na2O+H2O=2NaOH K2O+H2O=2KOH
c.注意:CO和H2 O既不是酸性氧化物也不是碱性氧化物,是不成盐氧化物。
7.酸:电离时生成的阳离子全部是氢离子的化合物。酸溶液的pH值小于7
酸的名称中最后一个字是“酸”,通常化学式的第一种元素是“H ”,酸由氢和酸根离子组成紫色石蕊试液遇酸变红色,无色酚酞试液遇酸不变色
根据酸的组成,通常有以下两种分类方法:
酸的电离方程式:酸=nH++酸根离子n-
a.根据酸分子电离所能生成的氢离子的个数分为:一元酸(HCl、HNO
3
)、二元
酸(H
2 SO
4
、H
2
S、H
2
CO
3
)和三元酸(H
3
PO
4
)
b.根据酸分子里有无氧原子分为:
含氧酸(H
2 SO
4
,HNO
3
, H
3
PO
4
名称为:某酸)
无氧酸(HCl, H
2
S名称为:氢某酸)
鉴定酸(鉴定H+)的方法有:①加紫色石蕊试液变红色的是酸溶液;②加活泼金属Mg、Fe、Zn等有氢气放出
8.碱:电离时生成的阴离子全部是氢氧根离子的化合物。碱通常由金属离子和氢氧根离子构成
溶碱有五种:钾钙钠钡氨(KOH,Ca(OH)
2,NaOH, Ba(OH)
2
,氨水)它们的溶液
无色。
有颜色的碱(不溶于水):红褐色的氢氧化铁(Fe(OH)
3
↓ )、蓝色的氢氧化铜
(Cu(OH)
2
↓)
其他固体碱是白色。碱的名称通常有“氢氧化某”,化学式的最后面是“OH”
可溶性碱的溶液pH值大于7,紫色石蕊试液遇溶碱变蓝色,无色酚酞试液遇溶碱变红色
鉴定可溶性碱溶液(鉴定OH-)
方法一:加紫色石蕊试液变蓝色,加无色酚酞试液变红色是碱.
方法二:加铁盐溶液有红褐色沉淀生成;加铜盐溶液有蓝色沉淀的是碱。
9.盐:电离时生成金属离子和酸根离子的化合物。第一种分类方法:
a.正盐(酸碱完全中和的产物,没有可电离的氢离子或氢氧根离子),例如NaCl、
Na
2 S KNO
3
无氧酸正盐叫“某化某”Na
2
S_______ MgCl2__________FeS__________
含氧酸盐叫“某酸某”KNO3_________ BaSO4______________Na2CO3______
b.酸式盐(多元酸里的氢部分被金属取代,H夹在中间)
NaHCO
3
____________ 、Ca(HCO3)2_____________、NaH2PO4 _____________ 常见的酸式盐的酸根有:HCO3-、HSO4-、H2PO4-、HPO42-
c.碱式盐(化学式的中间有“OH”):Cu2(OH)2CO3
第二种分类方法
按盐中相同部分的离子称为某类盐:含碳酸根离子的盐称为碳酸盐、含硫酸根离子的盐称为硫酸盐、含硝酸根离子的盐称为硝酸盐、含铁离子的盐称为铁盐,等等。
10.酸碱指示剂(石蕊试液、无色酚酞)和pH值:
酸溶液的pH值小于7(如盐酸、稀硫酸、硝酸),酸性越强pH值越小,酸性越弱pH值越大。水、中性的硫酸盐、硝酸盐和盐酸盐溶液不能使指示剂变色,pH 值等于7。不能使指示剂变色;可溶的碱溶液pH值大于7。碱性越强pH值越大,碱性越弱pH越小
11.酸碱盐溶解性口诀:
钾钠硝铵溶溶碱有五种钡钾钙钠氨
不溶氯化物AgCl 不溶硫酸盐BaSO4碳酸盐只溶钾钠铵
口诀的含义:含有钾、钠、硝酸根、铵根的物质都溶于水
溶于水的碱有:氢氧化钡、氢氧化钾、氢氧化钙、氢氧化钠和氨水,其他碱不
溶于水
含Cl的化合物只有AgCl不溶于水,其他都溶于水;
含SO42-的化合物只有BaSO4不溶于水,其他都溶于水
含CO32-的物质只有含K+ Na+ NH4+溶于水,其他都不溶于水
12.沉淀物中AgCl和BaSO4 不溶于稀硝酸,Fe(OH)3是红褐色沉淀,Cu(OH)2是蓝色沉淀
其他沉淀是白色(包括Fe(OH)2)有以下常见的沉淀:Mg(OH)
2 Al(OH)
3
CaCO
3 BaCO
3
Ag
2
CO
3
推断题中,往沉淀物加稀硝酸:若讲沉淀不溶解,则沉淀中一定有AgCl或BaSO
4
;
若讲沉淀全部溶解,则沉淀中一定没有AgCl或BaSO
4
;若讲沉淀部分溶解,则
沉淀中一定有AgCl或BaSO
4
中的一种,且还有另一种可溶于稀硝酸的沉淀。
13物质的颜色:
固体:(请在括号内填上化学式)
黑色:氧化铜(CuO),四氧化三铁(Fe3O 4),二氧化锰(MnO 2),碳粉(C);
蓝色:胆矾(CuSO4.5H2O)(即硫酸铜晶体),氢氧化铜Cu(OH)2;
绿色:铜绿Cu2(OH)2CO 3黄色:硫磺(S)紫红色:铜(Cu);
红棕色:氧化铁(即铁锈)(Fe2O 3);红褐色:氢氧化铁Fe(OH)3
紫黑色:高锰酸钾(KMnO4)
溶液:
含Cu2+的溶液呈蓝色如:CuCl2,CuSO4,Cu(NO3)2
含Fe3+的溶液呈黄色如:FeCl3Fe2(SO4)3Fe(NO3)3
其它常见的碱和盐的固体大多为白色(NaCl,KNO3等晶体为无色),溶液
大多为无色
知识产权知识点归纳总结1. 知识产权知识点总结 课本重点: 1.知识产权的性质和特征 性质:性质知识产权是一种无形财产权,客体的非物质性是知识产权的本质属性,其具体表现为 1不发生有形控制的占有 2不发生有形损耗的使用 3不发生消灭智力成果的事实处分与有形交付的法律处分 特征:知识产品之无形是相对于动产、不动产之有形而言的,他具有不同的存在、利用、处分形态 1不发生有型控制的占有 2不发生有形损耗的使用 3不发生消灭只是产品的事实处分与有形交付的法律处分 2.知识产权的独占性 1知识产权为权利人所独占,权利人垄断这种专利并受到严格保护,没有法律规定或 未经权利人许可,任何人不得使用权利人的只是产品 2对于同一项知识产品,不允许有两个或领个以上同一属性的知识产权并存
3.知识产权的地域性 知识产权作为一种专有权在空间上的效力并不是无限的,而要受到地域的限制,即具有严格的领土性,其效力只限于本国境内 4.知识产权的实践性 知识产权不是没有时间限制的永恒权利,其时间性表明:知识产权仅在法律规定的期限 内受到保护,一旦超过法律规定的有效期限,这一权利就自行消灭著作权 5.著作权的主体,公民、自然人、法人、其他组织、国家 6.某些作品著作权主体的确定 1演绎作品著作权主体 演绎作品是对现有作品进行改编、翻译、注释、整理而产生的作品。演绎作品的著 作权归演绎作者享有。演绎作品著作权人只能对其演绎作品享有著作权,对被演绎 作品不享有任何和权利。 2合作作品著作权主体 合作作品是两个以上的人合作创作的作品。判断要素 i.合作作品的创作者须为两个或者两个以上的人,一个认单独创作的作品不是合
Unit1 My day 知识整理 △话题:谈论每天的活动及时间安排 △词汇:do morning exercises(做早操) eat breakfast/lunch/dinner(吃早餐/午餐/晚餐) have...class(上…课),play sports(做运动) cleanmyroom(打扫我的房间),go forawalk (散步) go shopping(购物),takeadancingclass(上舞蹈课) △拓展词汇:get up(起床),go to bed(上床睡觉) washmy clothes(洗我的衣服), watch TV(看电视) do homework(做作业), play music(演奏音乐) cook dinner(煮晚餐), at home(在家) inthemorning(在上午),intheafternoon(在下午) intheevening(在晚上),atnight(在半夜) △句型: ①询问做某事在几点 When doyou+动词原形(短语)+其他? —— At +时间 —— I(+频度副词)+动词原形(短语)+at+时间。 例句:When do you get up in the morning? —— At 7:30. —— I often get up at 7:30. ②询问周末的活动安排
What do you often do on the weekend ? I often (always/sometime/usually) +…(周末的活动)+with … (某人)+ontheweekend (onSaturdays/on Sundays ). 例句:What do you do on the weekend ? I often take a dancing class with my friendon Sundays. △知识点: 1:注意介词的搭配 at +具体时间(几点)/night/home at 9 o ’clock in +国家/季节 in Spain on +星期 on the weekend/on Sundays with +人 with my father/mother/friend 2:表示时间频率词的区别 always 表示总是,一直; usually 表示经常,通常; often 表示经常,常常; sometimes 表示有时,间或。 按它们的频率大小排列如下: always (100%)→usually (80%)→often (60%)→sometimes (40%) 3:其他知识点 also 用于句中 1) 也 too too 用于肯定句中 用于句末
知识产权培训学习心得体1 知识产权培训学习心得体会在这学期中,我们集中学习了《知识产权法》。通过老师的讲解和自学,我对这门学科的有闭知识有了必定的认识。以下是我参加网大学习一年多来的一些心得。 一、注意学习方法,理论联系现实,注重理解二、公道摆设时间,捉住学习重点由于是在职学习,用于学习的时间有限,所以我以为公道摆设好学习时间是极度重要的。根据网大的摆设,每门课程从拿到教材到考试,至少有三个月左右的学习时间,哄骗平常空余时间将教材和课件浏览一遍,有一个大概的了解。接下来当真地将练习题做一遍,不清楚的地方再回过甚去看看书,根据考试大纲将重要的知识点记一遍,并对著作权、专利权、商标权三者之间进行比较,加深影响。比如: 1、著作权的司法保重期限: 著作权中的人身权保重不受期限限定,无限期保重;财产权的保重期限: 公民作品: 作者终生加死后50 年;合作作品:
止于最后殒命的作者殒命后 50 年;法人作品或非法人单位作品: 自尾次收表之日起 50 年。 2、专利权的保重期限: 收现: 自申请之日起 20 年,实用新型和外不雅观设计: 自申请之日起 10 年。 3、商标权的保重期限: 注册商标的保重期为 10 年,期满需要继续使用的,应当申请续展注册,每次续展的有效期为 10 年。 《知识产权法》中的一些概念是比较抽象的,若是死记硬背很难记住,所以学习方法便显然特别重要,现实生活中、电视和报刊中闭于知识产权法的内容还是比较多的,在看得时候注意和自己的学习联系起来,寓教于乐,在理解的基础上再记忆便容易的多。比如我在报上看到的一个小故事:“可口可乐”公司的老板曾说,一旦可口可乐在全球的厂房、货物局部失于火灾,自己第二天便能用“可口可乐”商标作质押,贷出资金恢复生产。因为“可口可乐”的商标被评估值数百亿美元。这从侧面反应了知识产权给企业带来的巨大价值,体现了商标权在知识产权中的重要地位,同时也让我理解了知识产权的概念、特点、分类。知识产权法是调整因知识产
1.have 1)have sb/sth do sth “让某人/物做某事”,宾语sb/sth和宾补do之间为主动. 如:Mum often has me help do some housework. 2)have sb/sth doing sth “让某人/物一直/总是做某事”,宾语sb/sth和宾补do之间为主动,且强调动作一直进行. 如:Don't have the machine working all the time. 3)have sb/sth done “让某人/物被...”,宾语sb/sth和宾补do之间为被动关系. 如:I had my hair cut yesterday. 2.get 1)get sb/sth to do sth“使得某人/物去做某事”,宾语sb/sth和宾补do之间为主动关系,且动作尚未发生. 如:Can you get us to do the experiment? 你能让我们做这个试验吗? 2)get sb/sth doing sth “使得某人/物正在做某事”,宾语sb/sth和宾补do之间是主动关系,且动作正在发生. 如:He has got the car starting. 3)get sb/sth done “使得某人/物被...”,宾语sb/sth和宾补do之间是被动关系. 如:I must get my bike repaired. 3.make make sb/sth do sth “使得某人/物做某事”,宾语sb/sth和宾补do之间是主动关系. 如:His joke made us all laugh. Unit 1 Great scientists ? 1. (v.)检查( inspect, check) 2. (vt.& vi.) 推断出,结束 3. (vt.) 分析( n. analysis) 4. (vt.& n.) 打败;战胜,使受挫;失败(beat) 5. (vt.) 出席,护理,照顾,参加 6. (vt.) 暴露,揭露,使曝光(uncover,unmask, undress,reveal ) 7. (vt.& n.) 治愈,治疗;痊愈 8. (v.) 控制 9. (vt.) 吸收,吸引;使专心 10. (vt.& n) 责备,谴责;过失,责备(criticize, scold,accuse 反praise) 11. (adv.) 立即 12. (n.& v.) 把手;处理,操纵(deal with) 13. (vt.& vi.) 贡献,捐献,捐助 14. (v.) 完成(finish) 15. (vt.) 拒绝,抛弃,不接受(refuse/ abandon) 16 . (n.) 特征,特性 17. (adj.) 严重的(serious),严厉的,剧烈的
物质的分类 九年级化学教案 (二)物质的分类金属单质 物混合物单质非金属单质 酸性氧化物 物质种类稀有气体氧化物碱性氧化物 质纯净物元素种类无机物酸 其他氧化物 化合物碱 有机物盐 3.混合物:是由两种或两种以上的物质混合而成(或由不同种物质组成) 例如,空气,溶液(盐酸、 澄清的石灰水、碘酒、矿泉水),矿物(煤、石油、天然气、铁矿石、石灰石),合金(生铁、钢) 注意:氧气和臭氧混合而成的物质是混合物,红磷和白磷混合也是混合物。
纯净物、混合物与组成元素的种类无关。即一种元素组成的物质可能是纯净物也可能是混合物,多种元素组成的物质可能是纯净或混合物。 4.纯净物:由一种物质组成的。例如:水、水银、蓝矾(cuso4 •5h2 o)都是纯净物 冰与水混合是纯净物。名称中有“某化某”“某酸某”的都是纯净物,是化合物。 5.单质:由同种(或一种)元素组成的纯净物。例如:铁氧气(液氧)、氢气、水银。 6.化合物:由不同种(两种或两种以上)元素组成的纯净物。 名称中有“某化某”“某酸某”的是化合物。 7.有机物(有机化合物):含碳元素的化合物(除co、co2 和含碳酸根化合物外) 九年级化学教案 8. 氧化物:由两种元素组成,其中一种是氧元素的化合物。 a.酸性氧化物:跟碱反应生成盐和水的氧化物。co2 ,so2 ,so3 大部分非金属氧化物都是酸性氧化物,跟水反应生成同价的含氧酸。 co2 + h2o= h2co3 so2 + h2o= h2so3 so3 + h2o= h2so4
b.碱性氧化物:跟酸反应生成盐和水的氧化物。cao na2 o mgo fe2 o3 cuo 大部分金属氧化物都是碱性氧化物,bao k2 o cao na2 o溶于水立即跟水反应 生成相应的碱,其他碱性氧化物不溶于水,跟水不反应。 cao+h2o=ca(oh)2 bao+h2o=ca(oh)2 na2o+h2o=2naoh k2o+h2o=2koh c.注意:co和h2 o既不是酸性氧化物也不是碱性氧化物,是不成盐氧化物。 9.酸:电离时生成的阳离子全部是氢离子的化合物。酸溶液的ph值小于7 酸的名称中最后一个字是“酸”,通常化学式的第一种元素是“h”,酸由氢和酸根离子组成 紫色石蕊试液遇酸变红色,无色酚酞试液遇酸不变色 根据酸的组成,通常有以下两种分类方法:酸的电离方程式:酸=nh+ +酸根离子n- a.根据酸分子电离所能生成的氢离子的个数分为:一元酸(hcl、hno3 )、 二元酸(h2 so4 、h2 s、h2 co3 )和三元酸(h3 po4 ) b.根据酸分子里有无氧原子分为:
知识产权管理工作总结 导语:公司知识产权培训的责任部门是行政部,负责组织公司知识产权宣传、培训工作。下面是小编整理的范文,欢迎查阅! 篇一:知识产权管理工作总结20XX年4月1日起,公司全面贯标《企业知识产权管理规范》GB/T29490-20XX。企业在知识产权管理方面做了以下几点工作: 一、确定知识产权管理方针、目标 企业知识产权方针是知识产权工作的宗旨和方向。企业知识产权的重要任务就是要着力提高自主创新和运用知识产权的能力,将知识产权的创造与管理真正融入到企业的生产经营各个环节,以此提高企业的市场竞争地位和核心竞争力,促进企业持续发展。以此为基,我们确定的知识产权方针是:坚持自主创新,保护知识产权,提高市场竞争力,实现持续发展。 制订了知识产权管理的中长期(3~5年)目标和年度目标,作为知识产权绩效可量化考核的指标,在各个职能部门确定了分解目标,每年进行一次考核总结。通过目标的达成和不断提升,实现公司核心竞争力的提升。 二、知识产权组织管理 1、设立了知识产权管理领导小组,由总经理为组长,结合公司各职能部门负责人为知识产权管理联络人。企业的
组织机构,在原七个部门的基础上,增设了知识产权管理部,由副总卢敏龙兼任知管部部长,牵头协调企业内外知识产权管理全过程,各职能部门负责本部门并配合知管部做好知识产权相关管理工作。 2、编制并颁布了《知识产权管理手册》、知识产权管理工作《程序文件》、《管理制度》和知识产权管理工作实施记录表单。知识产权管理手册作为公司知识产权的纲领性文件,严格按GB/T29490-20XX《企业知识产权管理规范》编制,涉及标准的全部条款内容,没有删减和变更。按照10处标准条款要形成程序的要求,我们共编制了19篇程序文件和17篇管理制度,并设置了78个记录表单。 3、资金上给予保障。我公司20XX年知识产权经费投入为万元;20XX年知识产权经费投入为万元;20XX年知识产权经费预计将达破30万元。这些经费主要用于知识产权的申报、维护;知识产权管理体系建立与维护;人员培训;专利奖励;风险备用金等。 4、设立了技术保密制度及竞业协议制度。规定对我公司的商业秘密的划分密级等级及使用权限,并与接触重要机密的员工签订了《保密合同》。 5、设立知识产权奖罚制度。公司设立“创新成果奖”、“技术发明奖”、“成果转化奖”、“技术改进奖”等八个奖项,每年评定并颁奖一次。同时,对违反《知识产权管理制度》
物质的分类知识点及题型(含答案) 一、常见的分类方法:(1)交叉分类法:对物质以不同的标准进行分类。 举例 : Na 2CO 3 钠盐 Na 2SO 4 硫酸盐 NaCl 含氧酸盐 K 2SO 4 无氧酸盐 KHCO 3 氧化物 Na 2O 酸式盐 (2)树状分类法:对同类事物进行再分类的一种方法 举例 : (3)化学反应的分类: ?? ? ?? ????? ???? ??? ?????? ?还原反应氧化反应失氧根据反应中物质得氧或分解反应化合反应的多少根据反应前后物质种类 复分解反应置换反应类别根据反应物和生成物的化学反应 二、分散系及其分类: 1、几个概念 分散系:把一种(或多种)物质分散在另一种(或多种)物质中所得到的体系,叫做分散系。 分散质:分散系由分散质和分散剂组成,前者属于被分散的物质,称作分散质; 分散剂:后者起容纳分散质的作用,称作分散剂。 2、分散系按照分散质或分散剂聚集状态不同分类,有9种类型。对比如下: 物质 混合物:NaCl 溶液 纯净物 金属单质:Cu Hg 非金属单质:S H 2 单质 化合物 碱:Ca(OH)2 NH 3·H 2O 盐:CaCO 3 酸:H 2SO 4 CH 3COOH 氧化物:CaO H 2O
3、当分散剂是水或其他液体时,如果按照分散质粒子的大小来分类,可以把分散系分为溶液、胶体和浊液。三种分散系的比较: 4、胶体及其性质 (1)定义:分散质粒子直径在1nm~100nm之间的分散系,叫胶体。 ②将烧杯中蒸馏水加热至沸腾; ③向沸水中滴加1~2mL FeCl3饱和溶液; ④继续煮沸至溶液呈红褐色,停止加热。 化学方程式:FeCl3+3H2O=Fe(OH)3(胶体)+3HCl (3)性质:当光束通过胶体时,由于胶体粒子对光线散射,而形成了一条光亮的“通路”,这种现象叫做丁达尔效应。
知识要点总结 Unit 1 一.语音 字母组合bl ,pl ,cl, gl, fl , sl 在单词中的发音二,词组总结 1.talk about 谈论 2.look at 看 3.take sb to sp 带某人到某地 4.so many 如此多 5.make model planes 制做飞机模型 6.like to do 喜欢做某事 7.like doing 8.forget to do 忘记将要做的事 9.forget doing 忘记已做过的事 10.want to do 想要做某事 11.introduce …to 介绍 12.let`s help…让我们来帮助….. 13.stay with 和….呆在一起 14.in English class 在英语课上 15.play football 踢足球 16.every day 每天 17.Thank you to every one in the family 她经常对家里的每个人说谢谢你。 18.in the family 在家里 19.clean the car 清洁汽车 20.walk the dog 溜狗 21.play with 和…..玩 22.become good friends 成为好朋友 23.go to school 上学 24.new friends 新朋友25.birthday party 生日聚会 26.big hands 大手 27.long arms 长胳膊 28.answer the questions 回答问题 29.be good at 擅长 30.be famous for 以….而著名 31.play tricks on 和…开玩笑 https://www.doczj.com/doc/f24804575.html,e to 来到 33.Beijing duck 北京烤鸭 34.at first 起初 35.a lot 许多 36.at camp 露营 37.in a boat 在小船上 38.catch fish 捕鱼 39.put…on 把…放在…上 40.pick up 拾起 41.go to bed 上床睡觉 42.Good night 晚安 43.at school 在学校 44.how to 如何去 45.cook the fish 做鱼 46.play a trick 开玩笑 47.a toy snake 玩具蛇 48.it`s time for 是该做….的时候了 49.it`s time to do 三,重点句型 What s+某人(第三人称单数)+like? …..是什么样的人? 答语: He/She is+表示人体貌特征或性格特点的形容词。 =What does+某人(Tom, your mother…)+look like ….长得什么样? What does your little sister look like.你妹妹长什么样 四,掌握句型 1.Who are Bill`s new friends? 2.Who`s this ? 3.That`s Helen. 4.Let`s talk about our classmates. 5.She`s friendly, too. 6.What is Tom like? 7.Bill takes Yaoyao to Tom`s birthday party. 8.There are so many model planes.
高中化学常见物质的分类 一、单质 按元素组成分为 1. 金属单质 K 钾、Ca 钙、Na 纳、Mg 镁、Al 铝、Zn 锌、Fe 铁、Sn 锡、Pb 铅、Cu 铜、Hg 汞、Ag 银、Pt 铂、Au 金 2. 非金属单质 氢气H 2、碳C 、氮气N 2、氧气O 2、臭氧O 3、氟气F 2、硅Si 、磷P 、硫S 、氯气Cl 2、液溴Br 2、碘I 2、氦气He 、氖气Ne 、氩气Ar 、 二、化合物 1. 有机化合物: 乙醇、甲烷、乙烷、乙烯、葡萄糖等 2. 无机化合物 三、氧化物 (1)按元素组成分为金属氧化物和非金属氧化物 1. 金属氧化物 氧化钠Na 2O 、过氧化钠Na 2O 2、氧化钙CaO 、氧化镁MgO 、氧化铝Al 2O 3、氧化锌ZnO 、氧化铁Fe 2O 3、氧化亚铁FeO 、四氧化三铁Fe 3O 4、氧化铜CuO 、氧化汞HgO 、七氧化二锰Mn 2O 7 2. 非金属氧化物 水H 2O ,过氧化氢H 2O 2、一氧化碳CO 、二氧化碳CO 2、一氧化氮NO 、五氧化二氮N 2O 5、二氧化硅SiO 2、五氧化二磷P 2O 5、二氧化硫SO 2、三氧化硫SO 3 (2)按照性质分为 碱性氧化物、酸性氧化物、不成盐氧化物、两性氧化物、过氧化物 1. 碱性氧化物 大部分的金属氧化物为碱性氧化物,但有特例:过氧化钠Na 2O 2为过氧化物、 氧化铝Al 2O 3为两性氧化物、七氧化二锰Mn 2O 7为酸性氧化物、四氧化三铁Fe 3O 4、 碱性氧化物有:氧化钠Na 2O 、氧化钙CaO 、氧化镁MgO 、氧化锌ZnO 、氧化铁Fe 2O 3、氧化亚铁FeO 、氧化铜CuO 、氧化汞HgO 、 碱性氧化物一定为金属氧化物,金属氧化物不一定为碱性氧化物 2. 酸性氧化物 大部分的非金属氧化物为,但有特例:水H 2O ,一氧化碳CO 、一氧化氮NO 不是酸性氧化物,七氧化二锰Mn 2O 7虽然为金属氧化物但属于酸性氧化物、 非金属氧化物不一定为酸性氧化物 3. 不成盐氧化物:——既不与酸反应也不与碱反应!如:一氧化碳CO 、一氧化氮NO ! 4. 两性氧化物:氧化铝Al 2O 3 5. 过氧化物:过氧化氢H 2O 2、过氧化钠Na 2O 2 四、酸 中学常见的酸:
高中化学物质的分类汇总 高中化学物质的分类知识点总结 1、物质的组成、性质和分类: (一)掌握基本概念 1. 分子 分子是能够独立存在并保持物质化学性质的一种微粒。 (1)分子同原子、离子一样是构成物质的基本微粒。 (2)按组成分子的原子个数可分为: 单原子分子:Ne 、C、 He 、Kr…… 双原子分子:H2 、O2、HCl、No…… 多原子分子:H2O、P4 、C6H12O6…… 2. 原子 原子是化学变化中的最小微粒,确切的说,化学反应中原子核不变,只有核外电子发生变化。 (1)原子是组成某些物质(如金刚石、晶体硅、二氧化硅等原子晶体)和分子的基本微粒。 (2)原子是由原子核(中子、质子)和核外电子组成的。 3. 离子 离子是指带电荷的原子或原子团。 (1)离子可分为阳离子和阴离子 阳离子:Li+、Na+、H+、NH4+…… 阴离子:Cl-、O2-、OH-、SO4-…… (2)存在离子的物质: ①离子化合物中:NaCl、CaCl2、CaSo4…… ②电解质溶液中:盐酸、氯化钠溶液中…… ③金属晶体中:钠、铁、钾、铜…… 4. 元素 元素是具有相同核电荷数的(即质子数)的同一类原子的总称。 (1)元素与物质、分子、原子的区别与联系;物质是由元素组成的(宏观看);物质是由原子、分子、或离子构成的(微观看)。 (2)某些元素可以形成不同的单质(性质、结构不同)同素异形体。(3)各元素在地壳中质量分数各不相同,占前五位的是:O、Si、Al、
Fe、Ga。 5. 同位素 同位素指同一元素不同核素之间互称同位素,即具有相同质子数不同中子数的同一类原子互称为同位素。如氢(H)有三种同位素:11H、 21H、31H(氕、氘、氚)。 6. 核素 核素是具有特定质量数、原子序数和核能态,而且其寿命足以被观察的一类原子。 (1)同种元素,可以有若干种不同的核素—同位素。 (2)同一种元素的各种核素尽管中子数不同,但他们质子数与电子数相同。核外电子排布相同,因而他们的化学性质几乎相同。 7. 原子团 原子团是指多个原子结合成的集体,在许多反应中,原子团作为一个集体参加反应。原子团有以下几种类型:根(如SO42-、OH-、CH3COO-等)、官能团(有机物分子中能反应物质特殊性质的原子团,如-OH、 -NO2、-COOH等)、游离基(又称自由基、具有不成价电子的原子团,如甲基游离基·CH3)。 8. 基 化合物中具有特殊性质的一部分原子或原子团,或化合物分子中去掉某些原子或原子团后剩下的原子团。 (1)有机物的官能团是决定物质主要性质的基,如醇的羟基(-OH)和羧酸的羧基(-COOH)。 (2)甲烷(CH4)分子中去掉一个氢原子后剩余部分(·CH3)含有未成对的价电子,称为甲基或甲基游离基,也包括单原子的游离基(·Cl)。 基(羟基):电中性,不能独立存在,只能和其他基或原子团相结合。根(氢氧根):带负电,能独立存在于溶液或离子化合物中。 9. 物理性质和化学性质 物理性质 (1)概念:(宏观)物质不需要发生化学变化就能表现出的性质。(2)实质:(微观)物质的分子组成和结构没有发生变化时所呈现的性质。 (3)物理性质一般包括:颜色、状态、气味、味道、密度、熔点、沸点、溶解性、导电性、导热性、延展性等。 化学性质
职务发明制度,就是规定关于职务发明及其专利权归属等相关方面问题地制度. 主要涉及到了两个方面,一个是职务发明地概念及其认定,另一个是职务发明创造专利权地归属.下面主要从这两个方面来论述我国地职务发明制度.文档收集自网络,仅用于个人学习一、我国职务发明创造 《专利法》第条第款规定,职务发明创造,是指发明人或设计人执行本单位任务或者主要是利用本单位地物质技术条件所完成地发明创造为职务发明创造.文档收集自网络,仅用于个人学习 二、我国职务发明创造地专利权归属 根据我国《专利法》地规定,我国在解决职务发明创造专利权归属问题上地三大原则: ()专利权属于发明人或设计人所在地单位()约定原则()发明人或者设计人地权利三、我国职务发明制度存在地主要问题 .职务发明成果归属认定易产生分歧.关于发明人离职后一年内作出地职务发明地规定存在缺陷 .职务发明和非职务发明地分类不尽合理 四、由以上我国职务发明制度存在地主要问题可以看出,一方面,在我国不仅职务发明专利归雇主所有,而且职务发明地范围太宽,限制了科技人员地研发积极性和灵活性;另一方面如发明人所完成地发明创造是在退职、退休或者调动工作后不到一年地时间内作出地,在自己离职一年以后再提出专利申请,或者直接将发明成果授意给第三人申请专利;发明人也可能会在一定时间内多次转职,以上情况按现行法是难以确定发明创造地归属地.因此可能对企业地投资是不利地.所以需要对现有地职务发明制度进行改革.文档收集自网络,仅用于个人学习 简述知识产权地性质 知识产权是一种新型地民事权利,在传统物权、债权、人身权上发展起来,是一种有别于财产所有权地无形财产权.文档收集自网络,仅用于个人学习 性质知识产权是一种无形财产权,客体地非物质性是知识产权地本质属性,其具体表现为:()不发生有形控制地占有;()不发生有形损耗地使用;()不发生消灭智力成果地事实处分与有形交付地法律处分. 文档收集自网络,仅用于个人学习 特征知识产权基于其无形财产权地属性,具有以下基本特征:()知识产权是一种专有性地民事权利(专有性);()知识产权地效力受到地域地限制(地域性);()知识产权在法律规定地期间内受到保护(时间性).文档收集自网络,仅用于个人学习 著作人身权与一般人身权地关系 著作人身权,又称著作精神权利,指作者对其作品所享有地各种与人身相联系或者密不可分而又无直接财产内容地权利,是作者通过创作表现个人风格地作品而依法享有获得名誉、声望和维护作品完整性地权利.该权利由作者终身享有,不可转让、剥夺和限制.作者死后,一般由其继承人或者法定机构予以保护.文档收集自网络,仅用于个人学习 人身权,又称非财产权利.指不直接具有财产地内容,与主体人身不可分离地权利. 人身权包括人格权和身份权两大类. (一)人身权与民事主体地人身不可分离,因此,人身权同时具有不可转让地法律属性.(二)人身权没有直接地财产内容,不能以金钱地价值尺度衡量人身利益. (三)人身权是一种绝对权.又称为对世权. 相同点()不可被替代,不能被扣押、被执行或被剥夺; ()既不得转让也不能放弃; ()也不能被继承、遗赠; ()具有非经济属性.即使著作人身权产生间接经济效果,例如因为作品及其创作者姓名地
物质的分类 一、选择题 1.下列物质的名称、化学式和所属的类别都正确的是( ) A.甲烷、CH4、有机物 B.锰、MN、金属单质 C.氯酸钾、KCl03、金属氧化物 D.氧化汞、HgO、非金属氧化物 2.目前,科学家打算合成一种“二重构造”的球形分子,方法是把足球型的C60分子融进足球型的Si60分子中,使外面的Si原子与里面的C原子结合。下列与这种物质有关的一些说法中,错误的是()。 A.是由两种单质组成的混合物 B.是一种新型化合物 C.其相对分子质量为2400 D.Si60分子的体积比C60分子大 3.现有①液态氧;②铁锈,③食盐水;④小苏打;⑤氢氧化钾;⑥石油。对上述物质的分类全部正确的是( ) A.盐——③④ B.纯净物——④⑤⑥ C.碱——①⑤ D.混合物——②③⑥ 4.许多物质的名称中含有“水”。“水”通常有三种含义:①表示水这种物质;②表示物质处于液态;③表示水溶液。下列物质名称中的“水”不属于以上三种含义的是 ( ) A. 重水 B. 氨水 C. 水银 D. 水晶 5.欲将粗盐提纯并用所得精盐配制一定质量分数的氯化钠溶液。下列说法正确的是( ) A.粗盐过滤时,用玻璃棒搅拌加快过滤的速度 B.蒸发滤液时,待蒸发皿中滤液蒸干时停止加热 C.配制溶液需要经过计算、称量、溶解、装瓶贴标签等步骤 D.配制溶液时必须使用的仪器有托盘天平、酒精灯、量筒、烧杯、玻璃棒等 6.右图表示的是纯净物、单质、化合物、含氧化合物、氧化物、碱之间的包含、不包含关系,若整个大圆圈代表纯净物,则在下列选项中,能正确指出①、②、③、④、⑤所属物质 类别的是( ) A.①单质、③化合物 B.②碱、⑤氧化物 C.④碱、⑤含氧化合物 D.④含氧化合物、③氧化物
必修2 Unit 1 Cultural relics 1. in search of…寻找… Search sb 搜身search for 寻找 search sb. / a place for sth. 搜身/搜查某个地方找某事物 2. could not/never have done 不可能做过某事 3. be used to do sth. 被用来做…The wood will be used to make tables and chairs. be used to doing sth. 习惯于做…He is used to living with the farmers now. used to do sth. 过去常常做…She used to come a lot, but now we seldom see her. 4. make it 达到目的,取得成功 5. in the fancy style 以一种奇特的风格 in style 流行out of style 过时 6. decorate. v. 装饰decoration. n. 装饰decorate sth. with sth. be decorated with sth. 7. survive: v. 生存,存活,经历(事故、灾难后)还活着,幸存,比…长寿 survival: n. 生存,幸存survivor: n. 幸存者 8. by design = on purpose 故意地by chance = by accident 偶然地 9. belong to 属于,是…其中的一员或一部分(无被动,无进行时) In our country, land doesn’t belong to any individual. Belonging to the developing countries, China faces many difficulties. 10. in return 作为报答in return for…作为对…的报答 11. Serve v. 服务service n. 服务serve as 担任,充当 He serves as a waiter here. The box can serve as a table. 12. reception desk 接待处give a warm reception to…热情地接待… 13. have/get sth. done 使…被做 I must have/get my homework finished before going out to play. 14. light: v. 点燃,照亮light up 点(烟),照亮,(使)变亮,(脸等)放光彩 Her eyes lit up with joy. light的过去式和过去分词有两种:lit和lighted,作为动词时二者可通用,但作定语时,只能用lighted. He lit/lighted a candle and handed the lighted candle to me. 15. consider doing sth. 考虑做…. be considered to be…被认为… 16. wonder: v. 想知道,感到惊奇,疑惑n. 奇迹,奇人/事 (It’s) no wonder (that)…难怪…He hasn’t slept at all for three days. No wonder (that) he is worn out. 17. at war 处于战争状态 18. remove:v. ①搬开,拿开,移动②去掉,消除③脱掉④搬家,迁移 His name was removed from the list. 19. furniture: n. 家具(不可数) a piece of furniture = an article of furniture They didn’t buy much furniture before they got married. 20. doubt: v. n. 怀疑,疑惑
一、第二章知识结构梳理 1、物质的分类 (1) 以分散质粒子大小对分散系分类 (2) 以组成为标准对物质进行分类 2、物质的化学变化
二、本章重难点概括 1、电解质和非电解质 (1)电解质应该是化合物; (2)电解质的导电条件:水溶液或熔融状态 (3)电解质导电必须是化合物本身能电离出自由移动的离子,而不是发生化学反应的生成物(如CO2、SO2、SO3、NH3溶于水形成的水溶液可以导电,但是本身为非电解质)。【注意】 (1)单质和混合物既不是电解质也不是非电解质。{电解质和非电解质都是化合物} (2)(纯净的)酸碱盐都是电解质。 电解质包括:酸碱盐、大多金属氧化物、水; 非电解质包括:大多数有机物、非金属氧化物、氨。 (3)电解质本身不一定能导电{NaCl晶体}, 能导电的不一定是电解质{石墨、金属单质、混合物}。 (4)熔融状态下,一般的盐和强碱能导电,酸不能导电{分子构成}。 (5)液氨、液态HCl、HCl、酒精是纯净物,氨水、盐酸是混合物。 2、离子方程式的书写 (1)可拆:强酸、强碱、可溶盐; 不可拆:弱酸、弱碱、不溶盐、单质、气体、氧化物。
(2)HCO 3-不可拆、HSO 4-要拆开。 3、H + + OH -= H 2O 虽然能表明酸碱中和反应的实质,但只能表示强酸和强碱反应生 成可溶性盐的酸碱中和反应。 4、离子方程式正误判断 (1)得失电子不守恒、电荷不守恒、原子个数不守恒。 (2)弱酸、弱碱、难溶盐、气体、氧化物没写成化学式。 (3)反应不符合客观事实。 5、离子共存 (1)无色溶液中不能大量存在有颜色离子:Cu 2+(蓝色)、Fe 3+(棕黄色)、Fe 2+(浅绿色)、MnO 4-(紫 色),但有颜色离子可大量存在于澄清透明溶液中。 (2)强酸性溶液中不能大量存在以下离子:OH -、CO 32-、HCO 3-。 (3)强碱性溶液中不能大量存在以下离子:H +、NH 4+、Al 3+、Fe 3+、Mg 2+。 (4)能发生复分解反应的离子不能大量共存。 6、氧化还原反应 (1)概念:化学反应过程中元素化合价发生变化的反应叫做氧化还原反应。 (2)特征:化合价发生变化。 (3)本质:电子发生转移。 (4)失去电子的物质是还原剂,化合价升高,发生氧化反应,得到氧化产物。 (5)得到电子的物质是氧化剂,化合价降低,发生还原反应,得到还原产物。 (6)氧化剂表现出氧化性。 (7)还原剂表现出还原性。 注意点:氧化剂与还原剂都是指反应物。 (2)单、双线桥表示电子转移的方向和数目(失电子总数=得电子总数) C+2CuO △2Cu+CO 2 化合价升高,失电子,被氧化,发生氧化反应 化合价降低,得电子,被还原,发生还原反应
贯标工作总结 一、企业基本情况 1、企业简介 江苏德长医疗科技有限公司是一家中美合资高科技医疗器械公司,2010年由政府从美国波士顿重点引进,致力于高科技智能化神经康复设备和技术的研究、推广,目前已拥有5项国家发明和15项实用新型专利,是国家高新技术企业和ISO:13485国际医疗器械质量体系标准企业。 德长医疗自创立以来始终坚持“创新、优质、诚信、专业”的精神,在康复领域树立了良好的品牌。产品DC-L-500系列佩戴式足下垂康复仪(智能助行仪),RealGait全身三维步态与运动分析系统,ViR全身情景互动康复训练与评估系统等高科技产品,主要用于中枢神经损伤患者的康复训练和评估,以其创新的性能和高性价比等显著优点迅速进入全国数百家医院使用。 2、企业研发情况 科技研发是企业持续发展,永葆活力的关键。公司高度重视研发工作,由企业总经理统抓研发工作,围绕研发已经指定了严格的管理流程,研发人员激励机制和培养机制。公司内部已形成人人重视研发、人人尊敬研发的良好风气。 公司目前有拥有研发人员6名,有EMG、盆底、压力鞋垫等多项在研项目, 研发团队刻苦专研,不断突破技术难关,为企业奠定良好的技术基础。在研过程更是注重知识产权的保护,目前,企业已经获得国家授权专利25项,正在申请专利12项。 3、企业专利拥有情况一览表 公司目前拥有专利25项,其中,发明专利5项,实用新型15项,所有专利皆已投入实施。
序号种类专利(申请)号名称状态 1 发明ZL201110305663.0 一种足下垂矫正器步态检测装置已授权 2 发明ZL201210065042.4 一种电刺激助行装置及其输出控制方法已授权 3 发明ZL201210065990.8 一种柔性贴电刺激器已授权 4 发明201310354589.00 康复治疗系统已授权 5 发明201310459856.00 网络化康复治疗系统已授权 6 实用新型 ZL201020606684. 7 一种智能足下垂矫正和偏瘫康复装置已授权 7 实用新型 ZL200920303301.6 一种神经网络重建装置已授权 8 实用新型 201120383620.X 一种足下垂矫正器编程装置已授权 9 实用新型 ZL201320217580.0 一种电极座已授权 10 实用新型 ZL201320217579.8 一种绑带装置已授权 11 实用新型 201220518111.80 一种步态检测装置已授权 12 实用新型 201220549585.90 一种双相波电刺激助行装置已授权 13 实用新型 201220723601.10 一种下肢康复治疗装置已授权 14 实用新型201620488831.2 穿戴式全身动作检测传感器系统已授权 15 实用新型201620554023.10 一片式腿部电刺激输出电极已授权 16 实用新型201720001048.3 便于穿戴的电疗用上衣已授权 17 实用新型201720001049.8 刺激器内置行动传感器的校准工装已授权 18 实用新型201720001047.9 组合式神经肌肉电刺激康复设备的 收纳装置 已授权 19 实用新型201720001030.3 便于穿戴的电疗用裤子已授权 20 实用新型201720330653.5 电刺激用液体电极已授权 21 外观201130475790.60 步态检测鞋垫已授权 22 外观201130475804.40 电刺激器已授权 23 外观201230320490.50 编程器已授权 24 外观ZL201230650594.2 步态检测鞋垫已授权 25 外观ZL201330003016.4 刺激器已授权
高中化学物质的分类知识点总结 高中化学物质的分类知识点总结 一、物质的组成、性质和分类: (一)掌握基本概念 1.分子 分子是能够独立存在并保持物质化学性质的一种微粒。 (1)分子同原子、离子一样是构成物质的基本微粒。 (2)按组成分子的原子个数可分为: 单原子分子:Ne 、C、He 、Kr…… 双原子分子:H2 、O2、HCl、No…… 多原子分子:H2O、P4 、C6H12O6…… 2.原子 原子是化学变化中的最小微粒,确切的说,化学反应中原子核不变,只有核外电子发生变化。(1)原子是组成某些物质(如金刚石、晶体硅、二氧化硅等原子晶体)和分子的基本微粒。 (2)原子是由原子核(中子、质子)和核外电子组成的。 3.离子 离子是指带电荷的原子或原子团。 (1)离子可分为阳离子和阴离子 阳离子:Li+、Na+、H+、NH4+…… 阴离子:Cl-、O2-、OH-、SO4-…… (2)存在离子的物质: ①离子化合物中:NaCl、CaCl2、CaSo4…… ②电解质溶液中:盐酸、氯化钠溶液中…… ③金属晶体中:钠、铁、钾、铜…… 4.元素 元素是具有相同核电荷数的(即质子数)的同一类原子的总称。 (1)元素与物质、分子、原子的区别与联系;物质是由元素组成的(宏观看);物质是由原子、分子、或离子构成的(微观看)。 (2)某些元素可以形成不同的单质(性质、结构不同)同素异形体。 (3)各元素在地壳中质量分数各不相同,占前五位的是:O、Si、Al、Fe、Ga。 5.同位素 同位素指同一元素不同核素之间互称同位素,即具有相同质子数不同中子数的同一类原子互称为同位素。如氢(H)有三种同位素:11H、21H、31H(氕、氘、氚)。 6.核素 核素是具有特定质量数、原子序数和核能态,而且其寿命足以被观察的一类原子。 (1)同种元素,可以有若干种不同的核素—同位素。 (2)同一种元素的各种核素尽管中子数不同,但他们质子数与电子数相同。核外电子排布相同,因而他们的化学性质几乎相同。 7.原子团 原子团是指多个原子结合成的集体,在许多反应中,原子团作为一个集体参加反应。原子团有以下几种类型:根(如SO42-、OH-、CH3COO-等)、官能团(有机物分子中能反应物质特殊性质的原子团,如-OH、-NO2、-COOH等)、游离基(又称自由基、具有不成价电子的原子